Трудность диагностики аденомиоза связана со значительной вариабельностью его клинической картины: от малосимптомного проявления до выраженной симптоматики при отсутствии критериев прогнозирования и выбора рациональной тактики лечения [4,9,11]. Не удивительно, что многие авторы высказываются в пользу проведения комплексных исследований вместе клиницистов и морфологов для понимания отдельных звеньев патогенеза аденомиоза на молекулярном уровне [2].
Особенно перспективным представляются сведения о возможном участии в развитие аденомиоза «переходной зоны» [4,7]. По современным представлениям синдром аденомиоз/эндометриоз имеет общий патогенетический фактор, который связывают с абнормальной функцией внутреннего слоя миометрия и, следовательно, с изменениями архитектуры «переходной зоны». Считают, что превалирование фактора гипертрофии гладкомышечных клеток переходной зоны приводит к развитию аденомиоза, а увеличение глубины проникновения эндометрия в переходную зону- к развитию эндометриоза.
Вместе с тем данные о структурной организации переходной зоны в литературе весьма скудны и ограничиваются прежде всего эффектом наличия в ее составе гипертрофированных гладких миоцитов [5].
Настоящее исследование посвящено характеристике компонентов переходной зоны у женщин с аденомиозом.
Материалы и методы
Материалом для исследования послужили образцы маток, удаленных во время операции по поводу аденомиоза (47 женщин, средний возраст 52,03±0,51 года). В качестве контроля использован аутопсийный материал- это матки от условно здоровых женщин. Материал фиксировали в 10% формалине с последующей заливкой в парафин. Срезы окрашивали гематоксилином и эозином, по Ван-Гизону, Маллори, Массону, а также пикросириусом красным с последующим использованием поляризационной микроскопии. Иммуноцитохимическое исследование осуществляли по стандартному протоколу с использованием моноклональных антител. Для выявления коллагена I типа использовали антитела (ab 34710, Abcam, Англия), для коллагена III типа-(ab 778, Abcam, Англия), для коллагена IV типа-(ab 6586, Abcam, Англия). Обнаружение α-SMA проведено с помощью антител фирмы Dako (1:50 VK). Выявление коллагена I и III типов проводили таакже с помощью окраски пикросириусом красным с последующей поляризационной микроскопией. Для характеристики ядер цитогенной стромы эндометрия и миометрия использовали реакцию Фельгена. Полученные с помощью цифровой камеры для микроскопии DCM 310 микрофотографии в формате TIF подвергали компьютерное морфометрии. Измерение диаметров ядер проводили в условных единицах равных одному пикселю при разрешении монитора 640х480. Оптическую плотность ядер измеряли виртуальным зондом постоянных размеров с использованием параметра «Optical denseti» программы Scion Corporation. В микропрепаратах, окрашенных по Ван-Гизону, измеряли объем ядерной массы. Для оценки степени организованности изученных структурных компонентов использовали показатель энтропии [1]. Все цифровые данные подвергались статистической обработке с использованием программы Microsoft Excel (2010).
Согласно данным литературы в составе стенки матки имеется переходная зона, она выявляется с помощью МРТ и трансвагинального ультразвукового исследования и имеет в норме ширину от 2,0 до 5,0 мм [10], увеличиваясь при аденомиозе до 10-12 мм [6].
Предпринятое нами морфологическое изучение этой зоны требует исследования ее в нескольких полях зрения. При этом первое поле это эндометриальная порция переходной зоны,
представленная пограничным с внутренним миометрием участком цитогенной стромы, внеклеточным матриксом и донными частями маточных желез. Второе- это участок внутреннего миометрия с гладкомышечными клетками и элементами окружающей их цитогенной стромы и внеклеточным матриксом. Поэтому при описании переходной зоны матки нами будут использованы термины эндометриальная и миометриальная (внутренний миометрий) порции.
Результаты исследования
При морфологическом изучении стенки матки комплекс стандартных гистологических реакций: окраска гематоксилином-эозином, окраска по Маллори, Массону и Ван-Гизону не привели к выявлению переходной зоны в норме. Так изучение срезов, окрашенных по Маллори и Массону, показало, что на участке эндометрия, прилежащего к внутреннему миометрию, выявляется достаточно большое количество коллагеновых волокон, которые после окраски пикросириусом красным были типированы как коллаген I и III типов (рис.1).

Рис 1. Выявление коллагена I и III типов.
Окраска пикросириусом красным. Поляризационная микроскопия. Об.40х; Ок.10х
Количественно превалирует коллаген I типа. Коллаген III типа выявляется в виде тонких волокон, обнаруживающих зеленое свечение. При окраске по Маллори на участке переходной зоны отчетливо типируются темно-синие коллагеновые волокна, окружающие пучки ГМК, изредка местами видны красные эластические волокна и эпителиоциты маточных желез, заполненные слизью.
При иммуногистохимическом обнаружении коллагена I типа установлена его локализация преимущественно вокруг отдельных мышечных групп.
Интенсивность реакции от слабой до умеренной. Описанная локализация подтверждена окрашиванием срезов пикросириусом красным с последующей поляризационной микроскопией.
Компьютерная морфометрия эндометриальной порции переходной зоны в норме показала, что объем ядерной массы ее в среднем составляет 19,05±1,29, при этом объем гиперхромных и гипохромных ядер совпадает (табл.1), что позволяет установить общность этих
показателей для эутопического эндометрия и переходной зоны. Такая общность выявлена и при расчете фибриллярного и аморфного компонентов экстрацеллюлярного матрикса эутопического эндометрия и переходной зоны. Различия были выявлены при расчете коэффициента энтропии, отражающем степень характера взаимодействия упомянутых компонентов эндометрия. Оказалось, что в эндометриальной порции переходной зоны коэффициент энтропии составляет 2,80±0,14 и отличается с высокой степенью достоверности от коэффициента, присущего эутопическому эндометрию (1,7±0,5).
Таблица 1
Сравнительная характеристика морфометрических параметров эндометриальной порции переходной зон
|
Гиперхромность |
Гипохромность |
ОЯМ |
ВК |
АК |
Энтропия |
|
|
КОНТРОЛЬ |
9,23±0,74 σ=1,49 CV=16,1% |
9,82±0,69 σ=1,39 CV=14% |
19,05±1,29 σ=2,59 CV=13,58% |
22±0,19 σ=0,37 CV=1,7% |
31,45±1,17 σ=2,34 CV=7,4% |
2,80±0,14 σ=0,27 CV=9,7% |
|
АДЕНОМИОЗ |
10,77±0,48 σ=1,51 CV=14,03% |
9,12±0,61 σ=1,93 CV=21,13% |
19,89±0,44 σ=1,4 CV=7,04% |
14,03±0,83 σ=2,63 CV=18,76% |
38,27±1,02 σ=3,22 CV=8,42% |
3,17±0,01 σ=0,04 CV=1,24% |
Примечание:
ОЯМ- объем ядерной массы
ВК- волокнистый компонент
АК-аморфный компонент
При изучении миометриальной порции переходной зоны показатели объема ядерной массы, соотношение гипохромных и гиперхромных ядер (табл.2) и фибриллярного компонента при сопоставлении с наружным эутопическим миометрием совпадали. Различия выявлены для коэффициента энтропии участка миометриальной порции переходной зоны, который оказался равным 2,80±0,16 вместо 0,98±0,22 эутопического миометрия (табл.2).
Таблица 2
Сравнительная характеристика морфометрических параметров миометриальной порции переходной зоны
|
Гиперхромность |
Гипохромность |
ОЯМ |
МТ |
МВ |
Энтропия |
|
|
КОНТРОЛЬ |
8,70±0,68 σ =1,36 CV=15,6% |
9,50±0,25 σ =0,5 CV=5,2% |
18,2±0,6 σ =1,2 CV=6,6% |
39,4±0,6 σ =1,27 CV=3,2% |
14,98±0,43 σ =0,86 CV=5,73% |
2,80±0,16 σ =0,32 CV=11,29% |
|
АДЕНОМИОЗ |
10,33±0,75 σ=2,38 CV=23% |
9,39±0,72 σ=2,28 CV=24,32% |
19,52±0,42 σ=1,33 CV=6,84% |
39,48±0,79 σ=2,5 CV=6,34% |
13,91±0,69 σ=2,17 CV=15,59% |
3,15±0,01 σ=0,04 CV=1,18% |
Примечание:
ОЯМ- объем ядерной массы
МТ-мышечная ткань
МВ-межклеточное вещество
Изучение переходной зоны миометрия у больных с аденомиозом в срезах, окрашенных гематоксилином и эозином показало, что эта зона может быть типирована как граница эндометрия и миометрия, но с достаточно глубоким погружением первого в миометрий. По направлению от поверхности эндометрия к зоне миометрия отчетливо видно, что донные части маточных желез окружены стромой с большим количеством клеток, что указывает на активацию цитогенного компонента эндометрия.
Гладкомышечные клетки окрашены оксифильно и гомогенно, ориентированы преимущественно циркулярно и формируют компактные группы. На участках с поперечно
срезанными ГМК удается отметить рыхлый тип их упаковки, клетки неплотно прилежат друг к другу, при этом цитоплазма отдельных клеток негомогенна и имеет пенистый вид. При выявлении коллагена пикросириусом красным с последующей поляризационной микроскопией отчетливо видно, что волокна экстрацеллюлярного матрикса обнаруживают свечение от светло-зеленого к темно-зеленому, на этом фоне выявляется небольшое количество волокон желтого и красного цветов. Названные окраски позволяют считать, что превалирующим компонентом экстрацеллюлярного матрикса переходной зоны является коллаген III типа. Соединительнотканная строма, прилежащая на участке переходной зоны к концевым отделам маточных желез, обнаруживает красное свечение, соответствующее локализации коллагена I типа. На участке переходной зоны с внутренним миометрием соединительнотканный остов формируется преимущественно за счет коллагена III типа и в условиях поляризационной микроскопии отчетливо видно, что эти волокна обнаруживают свечение от зеленого спектра к насыщенному темно-зеленому.
При проведении иммуногистохимических реакций оказалось, что коллаген I типа локализуется преимущественно вокруг очагов аденомиоза в прослойках соединительной ткани, сопровождающей кровеносные сосуды (рис.2).
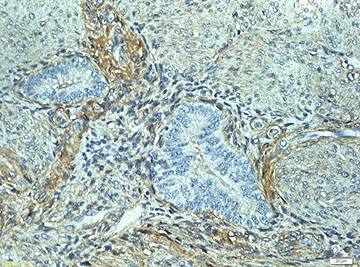
Рис. 2. Выявление коллагена I типа. Об.40х; Ок.10х
При этом интенсивность реакции отдельных коллагеновых волокон высокая. В гладкомышечных клетках окрашивается зона их периферии, соответствующая локализации базальной мембраны, а также аморфный матрикс, последний обнаруживает реакцию слабой интенсивности.
На участке переходной зоны, принадлежащей эндометрию, положительную иммуногистохимическую реакцию на коллаген I типа обнаруживают лишь волокна, базальной мембраны, на которой располагаются эпителиоциты маточных желез, а также коллагеновые фибриллы, окружающие пучки ГМК. В последнем случае местами положительную реакцию умеренной интенсивности обнаруживает экстрацеллюлярный матрикс. Здесь появляются клетки, цитоплазма которых содержит проколлаген. Не исключено, что это миофибробласты, они чаще всего располагаются вокруг донных частей маточных желез.
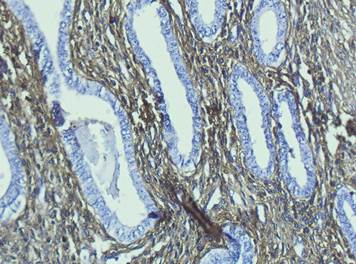
При иммуногистохимической реакции на коллаген III типа реакцию слабой интенсивности обнаруживают экстрацеллюлярный матрикс и отдельные коллагеновые фибриллы, типируемые в матриксе, который чаще всего располагается вокруг мелких кровеносных сосудов типа артериол (рис.3).
 .
.
Рис. 3. Выявление коллагена III типа. Эктопический эндометрий. Об 40х; Ок.10х
На участке эндометрия, принадлежащего переходной зоне, коллаген III типа выявляется в экстрацеллюлярном матриксе цитогенной стромы, окружающей гипертрофированные маточные железы. Интенсивность реакции от слабой до умеренной. В зоне внутреннего миометрия, принадлежащего переходной зоне, положительную реакцию на коллаген III типа обнаруживают волокна, окружающие ГМК, и волокна, прилежащие к стенке капилляров и артериол. Интенсивность их окраски варьирует от слабой до умеренной. В цитогенной строме появляются активные фибробласты, накопившие коллаген, но еще не приступивших к процессу его внеклеточного фибриллогенеза.
Иммуноцитохимическое выявление коллагена IV типа показало присутствие его вдоль стенок кровеносных сосудов. На участке внутреннего миометрия, принадлежащего переходной зоне, окрашиваются слабо и умеренно мембраны, окружающие гладкие миоциты. При наличии поперечно срезанных ГМК видна окраска их мембран, интенсивность реакции умеренная.
Цитоплазма ГМК не окрашивается, а ее периферическая часть дает положительную реакцию за счет окружающих клетку мембран, и такие участки выглядят как зоны «вакуолизации». На участке эндометрия, принадлежащего переходной зоне, положительную реакцию на коллаген IV типа обнаруживают тонкие фибриллы цитогенной стромы, а также базальная мембрана эпителиоцитов эндометриальных желез(рис.4).
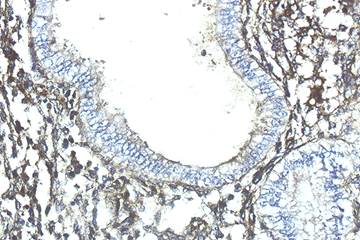
Рис. 4. Выявление коллагена IV типа. Базальная мембрана эндометриальных желез. Об.40х; Ок.10х
В условиях использования иммуногистохимической реакции на α-SMA в переходной зоне положительную реакцию обнаруживают гладкомышечные клетки, интенсивность реакции которых от умеренной до интенсивной (рис.5).
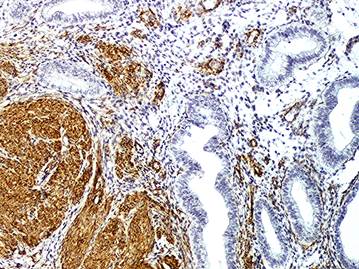
Рис. 5. Выявление актина в гладких миоцитах (SMA). Переходная зона. Об.10х; Ок.10х
При этом в ГМК, ориентированных циркулярно, интенсивность реакции от слабой до умеренной, а в ГМК в поперечном их сечении-интенсивная. В последнем случае удается увидеть, что среди группы ГМК интенсивность их окрашивания варьирует: одни клетки окрашены интенсивно, другие-умеренно, третьи слабо. С одной стороны это может быть показателем различного уровня содержания в ГМК актина. С другой стороны – это может быть результат среза, полученного на различном уровне гладкомышечной клетки, а, следовательно на участке с различным содержанием актина.
Описанные нами иммуногистохимический статус компонентов переходной зоны при аденомиозе мы сочетали с компьютерной морфометрией ядер клеток, формирующих эту зону. Оказалось, что на участке эндометрия объем ядерной массы составляет в среднем 19,89±0,44 усл.ед., при коэффициенте вариации 7,04%. При этом соотношение объема гиперхромных и гипохромных ядер представляется одинаковым, и в среднем составляет 10,77±0,48 и 9,12±0,61 соответственно. Характерным для этой зоны является увеличение объема аморфного компонента, что составляет 38,27±1,02 и по сравнению с объёмом волокнистого компонента 14,03±0,83, увеличен более, чем в 2 раза.
На участке переходной зоны, сформированной внутренним миометрием, объем ядерной массы в среднем составил 19,52±0,42. Соотношение гиперхромных и гипохромных ядер совпадает. Соотношение объема мышечной ткани и стромы было в пределе 3:1 с наличием высокого уровня энтропии, составившим 3,15±0,01.
Заключение
Таким образом, проведенные исследования показали, что иммуногистохимический профиль стромы участка эндометрия, принадлежащего переходной зоне при наличии аденомиоза, характеризуется присутствием преимущественно коллагена III типа, а в зоне экстрацеллюлярного матрикса, вокруг эндометриальных желез и коллагена I типа. Последний встречается и вокруг очагов аденомиоза, и в прослойках соединительной ткани, сопровождающей кровеносные сосуды. Коллаген IV типа выявляется в виде тонких фибрилл в цитогенной строме эндометрия и в базальной мембране эндометриальных желез. Соотношение фибриллярного и аморфного компонентов на эндометриальном участке переходной зоны свидетельствует о превалировании объема аморфного компонента. Изучение коэффициента энтропии со всей очевидностью показало наличие различий между эндометриальной порцией переходной зоны в норме и при аденомиозе, статистически эти различия оказались достоверными, этот феномен был повторен и в случае миометриального участка, что указывает на дезорганизацию структурной целостности и миометрия.
ГМК участка внутреннего миометрия характеризуются высоким содержанием гладкомышечного актина. Различия уровня его содержания выявляются не столько по топографическому признаку, сколько по характеру клеток, формирующих пучки , в составе которых выделяются клетки от слабого до высокого уровня содержания актина, не исключено, что распределение SMA для ГМК может служить показателем деления этих клеток на контрактильные и секреторные. Это согласуется с данными литературы о том, что при аденомиозе происходит гиперплазия и гипертрофия миометрия, что в последующем может привести к дисфункции контрактильности [8]. Приведенные нами данные о тканевой гетерогенности переходной зоны матки согласуется с мнением Brosens I., Benagiano G. [3], которые считают, что в условиях развивающего аденомиоза его клинический статус определяется как эндометриальный и внутренний миометриальный дисфункциональный синдром (в аббревиатуре EJMDS).
Библиографическая ссылка
Могильная Г.М., Куценко И.И., Симовоник А.Н. КОМПОНЕНТЫ ПЕРЕХОДНОЙ ЗОНЫ СТЕНКИ МАТКИ ПРИ АДЕНОМИОЗЕ // Современные проблемы науки и образования. 2016. № 6. ;URL: https://science-education.ru/ru/article/view?id=25621 (дата обращения: 17.05.2026).



