На современном этапе развития хирургии перитонит остается одним из наиболее тяжелых осложнений абдоминальной хирургии, сохраняя высокие показатели летальности, которые, по данным разных исследований, достигают 20–35% при вторичном перитоните, 60% и выше при третичном перитоните [3, 4, 2].
Несмотря на совершенствование методов диагностики и хирургической тактики, достижения анестезиологии и реаниматологии, расширение возможностей антибактериальной терапии, перитонит осложняет течение хирургических вмешательств в 0,5–8% случаев [3, 4, 2].
По материалам Красноярского краевого гнойно-септического центра (ККГСЦ), от острых хирургических заболеваний в 2015 г. погибли 350 человек. Из них у 18 пациентов причиной летального исхода были кровотечения, у 105 пациентов — острый панкреатит, у 227 пациентов причиной смерти стали перитонит и абдоминальный сепсис. Таким образом, проблема распространенного гнойного перитонита не теряет своей актуальности и представляет собой сложную задачу, требуя комплексного подхода к лечению, поиска хирургической тактики и путей ее модификации.
Оперативное лечение распространенного гнойного перитонита направлено на ликвидацию источника, санацию и адекватное дренирование брюшной полости [4, 5]. При тяжелом перитоните, как правило, необходимо выполнение нескольких санирующих операций по «программе» или «по требованию» [4, 5]. В последнее десятилетие частота релапаротомий возросла до 7–10% [5, 6]. В настоящее время существует несколько технических вариантов закрытия лапаростомы [1, 4, 5, 6]. Одним из наиболее активно развивающихся и перспективных направлений для решения этой задачи является применение методов локального отрицательного давления [5, 6].
Применение вакуум-ассистированной лапаростомии представляется нам многообещающим методом, позволяющим решить многие задачи в лечении разлитого гнойного перитонита. На сегодняшний день существует много различных систем локального отрицательного давления, таких как Renasys Go, PICO, Vivano и др. В своем клиническом наблюдении мы использовали технологию VivanoTec® S 042 NPWT фирмы Hartmann.
Пациент П., 41 года, поступил в приемно-диагностическое отделение КГБУЗ «Краевая клиническая больница» в тяжелом состоянии. Из анамнеза известно, что болен в течение двух недель. Основные жалобы: гипертермия, боли в животе, слабость.
Диагностический этап для объективизации состояния больного включал: развернутый анализ крови, биохимический анализ крови, общий анализ мочи, обзорную рентгенографию брюшной полости и грудной клетки, мультиспиральную компьютерную томографию (МСКТ) брюшной полости с внутривенным болюсным контрастным усилением.
По результатам лабораторных исследований отмечались нейтрофильный лейкоцитоз до 25,29*10*9/л, повышение СОЭ до 58 мм/ч, повышение уровня активности трасаминаз, щелочной фосфотазы, увеличение уровня фибриногена, септические изменения.
По данным УЗИ в брюшной полости и малом тазу определялась свободная жидкость.
На обзорной рентгенограмме брюшной полости определялись единичные горизонтальные уровни жидкости (рис. 1).
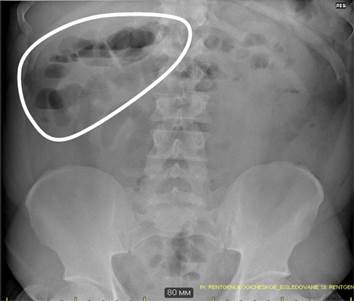
Рис. 1. Обзорная рентгенография органов брюшной полости (отмечаются расширенные петли кишечника в верхнем этаже брюшной полости с горизонтальными уровнями жидкости — чаши Клойбера)
По результатам МСКТ брюшной полости на уровне входа в малый таз, межпетельно, определялось ограниченное скопление содержимого высокой плотности, порядка 35 ед.Н (гной?), с большим содержанием газа, отграниченное от петель кишки тяжистыми уплотнениями (соединительнотканные тяжи), интимно прилежащее к сигмовидной кишке (рис. 2), общим размером 81х25х25 мм, что позволило заподозрить межпетельный абсцесс.
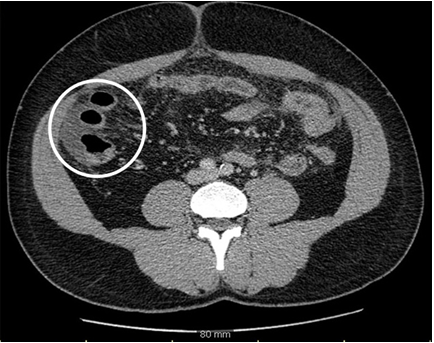
Рис. 2. МСКТ брюшной полости с внутривенным болюсным контрастным усилением (определяется ограниченное скопление содержимого высокой плотности, интимно прилежащее к сигмовидной кишке, — межпетельный абсцесс)
Таким образом, проведенные диагностические мероприятия позволили выявить острую хирургическую патологию органов брюшной полости, осложненную перитонитом. После минимальной предоперационной подготовки, в экстренном порядке пациент был оперирован. Выполнены лапаротомия, ревизия брюшной полости. Интраоперационно: в брюшной полости до 1000 мл фибринозно-гнойного экссудата, петли тонкой кишки делатированы до 4–4,5 см, перистальтика крайне вялая, париетальная и висцеральная брюшины инъецированы, с единичными нитями фибрина. Источник перитонита — перфорация дивертикула сигмовидной кишки. Мангеймский индекс перитонита (МИП) составил 28 баллов, индекс брюшной полости (ИБП) = 19 баллов. При оценке интегральных шкал тяжести степень полиорганной недостаточности (SOFA) составила 2 балла, тяжесть состояния (SAPS) — 11 баллов.
Выполнена обструктивная резекция сигмовидной кишки с последующим выведением сигмостомы на переднюю брюшную стенку. Брюшная полость санирована водным раствором антисептика, физиологическим раствором, осушена. Выполнена назоинтестинальная интубация тонкой кишки. Учитывая тяжесть перитонита и выраженность эндотоксикоза, было принято решение о завершении операции с наложением лапаростомы по традиционной методике.
В послеоперационном периоде пациент проходил лечение в условиях отделения реанимации ККГСЦ. На третьи сутки была выполнена программируемая санационная релапаротомия, в брюшную полость установлена вакуум-ассистированная лапаростома с использованием абдоминального набора VivanoMed® Abdominal Kit и аппарата отрицательного давления VivanoTec® (рис. 3).
В последующем, для купирования явлений перитонита, пациенту выполнялись санирующие операции по программе, с периодом между операциями в среднем 70 +/– 8 ч. При выполнении релапаротомий выполнялись санация брюшной полости с применением аппарата «Гейзер» (рис. 4), лапаростомия с применением проточно-аспирационной системы по оригинальной методике с использованием антисептика Лавасепт (рис. 5). Спустя 10 ч после пятой санирующей операции, на 10-е сутки после первичной операции, пациенту потребовалось экстренное оперативное вмешательство по поводу возникновения системного осложнения — стрессовой перфорации тонкой кишки. Были выполнены ревизия брюшной полости, ушивание стрессовой перфорации тонкой кишки. Учитывая экстренный порядок выполнения операции, лапаростома была наложена по традиционной методике. В ходе релапаротомии по поводу стрессовой перфорации отмечались явления панцирного перитонита на фоне прогрессирования показателей полиорганной недостаточности (динамика показателей интегральной шкалы оценки тяжести SOFA представлена на рисунке 6).
На фоне многократно проводимых санирующих операций у пациента наблюдалась демедиализация мышц передней брюшной стенки с диастазом до 15 см. Во избежание формирования гигантской послеоперационной вентральной грыжи, значительно снижающей качество жизни пациента и приводящей к инвалидизации, потребовалось закрытие брюшной полости с помощью спиц Киршнера (рис. 7).
Регулярно производился посев перитонеального выпота с коррекцией антибактериальной терапии. На 7-й санации у пациента был установлен диагноз третичного перитонита. Из экссудата брюшной полости были высеяны Enterococcus faecalis ++, Proteus mirabilis ++. ++). Из инфицированной лапаротомной раны передней брюшной стенки был высеян Citrobacter species. Также были диагностированы выраженные нарушения иммунной системы. Для коррекции иммунного статуса был проведен курс иммунотропной терапии иммуноглобулином человека нормальным [IgG+ IgM+ IgA] в течение 3 суток.
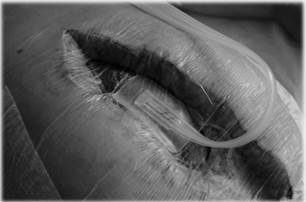
Рис. 3. Вакуум-ассистированная лапаростома
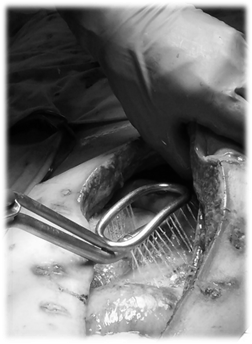
Рис. 4. Санация брюшной полости аппаратом «Гейзер»
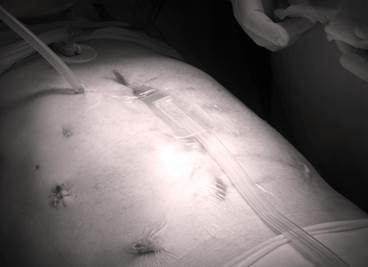
Рис. 5. Лапаростомия с применением проточно-аспирационной системы по оригинальной методике
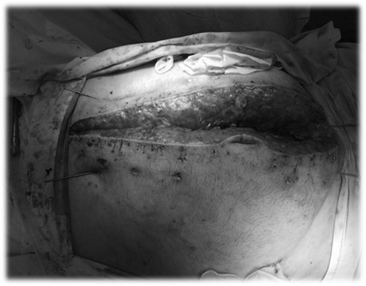
Рис. 6. Закрытие брюшной полости при помощи спиц Киршнера
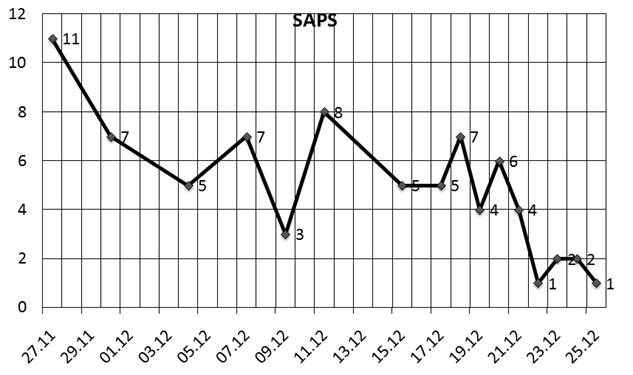
Рис. 7. Динамика изменения показателей интегральной шкалы оценки степени тяжести полиорганной недостаточности – SOFA
В результате комбинированного лечения, включающего в себя хирургические вмешательства с применением вакуум-ассистированной лапаростомы при помощи аппарата локального отрицательного давления VivanoTec®, технологии лапаростомии с применением проточно-аспирационной системы по оригинальной методике с использованием антисептика Лавасепт (рис. 5), массивную инфузионную, антибактериальную (Merexidi 6.0, Ampicillini — sulbactam 1.5 gr, Vancomicini 6,0), дезинтоксикационную терапию, коррекцию эндотоксикоза, у пациента был достигнут положительный результат. На 24-е сутки отмечались нормализация температуры, снижение лейкоцитоза до 10*9*10/л, нормализация уровня трансаминаз, отсутствие азотемии. На 27-е сутки после первичной операции пациент переведен из отделения реанимации в отделение хирургии ГСЦ.
Активизирован на 30-е сутки после первичной операции. Выписан в удовлетворительном состоянии. Общая продолжительность лечения составила 57 дней.
По истечении одного, трех месяцев и полугода после выписки пациент являлся на динамический осмотр в удовлетворительном состоянии.
Подготовлено при поддержке Краевого Государственного автономного учреждения «Красноярский краевой фонд поддержки научной и научно-технической деятельности».
Библиографическая ссылка
Шапкина В.А., Первова О.В., Черданцев Д.В., Трофимович Ю.Г., Дятлов В.Ю., Пирова А.Ш., Тахтобин Е.Г. УСПЕШНОЕ ЛЕЧЕНИЕ ТЯЖЕЛОГО ГНОЙНОГО ПЕРИТОНИТА В КРАСНОЯРСКОМ КРАЕВОМ ГНОЙНО-СЕПТИЧЕСКОМ ЦЕНТРЕ (КЛИНИЧЕСКИЙ СЛУЧАЙ) // Современные проблемы науки и образования. 2016. № 6. ;URL: https://science-education.ru/ru/article/view?id=25619 (дата обращения: 19.05.2026).



