Синдром обструктивного апноэ/гипопноэ сна (СОАГС) – это состояние, характеризующееся наличием храпа, периодическим спадением верхних дыхательных путей на уровне глотки и прекращением легочной вентиляции при сохраняющихся дыхательных усилиях, снижением уровня кислорода крови, грубой фрагментацией сна и избыточной дневной сонливостью [10]. Храп определяют как звуковой феномен, возникающий при биении друг о друга мягких структур глотки на фоне прохождения струи воздуха через суженные дыхательные пути. Дыхательные пути могут спадаться полностью, и тогда развивается апноэ – прекращение воздушного потока (легочной вентиляции) длительностью 10 c и более. Под гипопноэ понимают снижение респираторного потока воздуха не менее чем на 50 %, при длительности эпизода не менее 10 с и снижении кислородного насыщения крови минимум на 3 %. Выделяют 3 степени тяжести СОАГС в зависимости от индекса-апноэ/ гипопноэ (ИАГ), представленные в таблице 1. Количество эпизодов апноэ-гипопноэ в час может колебаться от 5 при лёгких формах СОАГС до 30 и более при тяжёлом варианте синдрома, что играет важную роль в отношении определения лечебной тактики и прогнозирования исхода заболевания [1].
Таблица 1
Характеристика СОАГС по степени тяжести [4,5]
|
Степень тяжести СОАГС |
Индекс апноэ/гипопноэ сна |
Сатурация кислорода |
Дневная сонливость |
|
Легкая |
5 – 15 в час |
Средняя сатурация не менее 90 % Максимальная десатурация не ниже 85 % |
Неконтролируемая сонливость во время нагрузки, не требующей высокой концентрации внимания. ШСЭ* < 12 |
|
Средняя |
16 – 30 в час |
Средняя сатурация не менее 90 % Максимальная десатурация не ниже 70 % |
Неконтролируемая сонливость или задремывания во время деятельности, требующей некоторой концентрации внимания. ШСЭ = 13-17 |
|
Тяжелая |
Более 30 в час |
Средняя сатурация менее 90 % Максимальная десатурация ниже 70 % |
Неконтролируемая сонливость или задремывания во время деятельности, требующей высокой концентрации внимания. ШСЭ = 18-24 |
|
* – шкала дневной сонливости Эпворта |
|||
К возникновению СОАГС предрасполагает любое состояние, приводящее к уменьшению просвета верхних дыхательных путей на уровне глотки и снижению тонуса глоточных мышц во время сна. Основными факторами риска развития СОАГС являются ожирение, пол, возраст, национальность, семейный анамнез и наследственная предрасположенность, черепно-лицевая патология, курение и др. [5,6].
В последние годы был проведен ряд широкомасштабных проспективных исследований, в которых изучали связь эпилепсии с нарушениями дыхания во время сна. Частота встречаемости СОАГС с эпилепсией варьирует от 9 % до 40 % случаев [9,11,12]. В исследовании Маnni и соавт. (2003 г.) выявлено, что коморбидность СОАГС и эпилепсии высока и составляет 10 %, выше у мужчин (15,4 %), чем у женщин (5,4 %). Также исследование продемонстрировало, что у пациентов с эпилепсией и СОАГС течение эпилепсии более тяжёлое, чем при изолированной эпилепсии. Выявлена коморбидность СОАГС с эпилепсией выше при позднем дебюте припадков и их ночном профиле [11].
Эпизоды цикличной десатурации и ночная гипоксемия при СОАГС могут провоцировать гипоксемические генерализованные судорожные припадки, мимикрируя эпилепсию, но таковым не являющиеся. С другой стороны, эпилептические припадки могут осложняться апноэ сна, что является жизнеугрожающим состоянием [2,3]. Особую актуальность имеет проблема СОАГС при фармакорезистентных формах эпилепсии, поскольку ночная гипоксемия при СОАГС является триггером эпилептиформной активности (интериктальной и/или иктальной) в ночное время суток. У пациентов с фармакорезистентной эпилепсией обнаружена высокая распространенность СОАГС (до 30 %) [12].
К тому же, противоэпилептическая терапия может иметь нежелательные последствия на течение СОАГС. Противоэпилептические препараты могут снижать чувствительность дыхательного центра, снижать тонус верхних дыхательных путей и вызывать прибавку массы тела, что способствует формированию СОАГС. По результатам В.А. Malow и соавт. (2005), пациенты с эпилепсией и коморбидным СОАГС имели ожирение различной степени и чаще находились на политерапии, чем пациенты без СОАГС [12]. Из исследований с использованием стимуляции блуждающего нерва стало известно, что VNS-терапия может вызывать апноэ сна в зависимости от частоты стимуляции. В частности, высокочастотная стимуляция приводит к коллапсу верхних дыхательным путей, эпизодам апноэ, способствует пробуждениям из-за респираторных событий [7]. У пациентов с СОАГС после стимуляции блуждающего нерва часто регистрируется увеличение ИАГ. Авторы предлагают проводить скрининг апноэ сна до и после VNS-имплантации [13].
У пациентов с эпилепсией необходимо целенаправленно выявлять симптомы, характерные для СОАГС. Такой весомый маркер СОАГС как дневная сонливость, имеет важное значение, потому что при эпилепсии причиной сонливости могут быть и нежелательные лекарственные явления на фоне приёма противоэпилептических препаратов, так и депривация сна из-за частых ночных эпилептических приступов, тем самым снижая эффективность сна. При наличии высокого риска респираторных расстройств сна, нужно проводить комплексную диагностику нарушений дыхания во сне, включая инструментальные методы обследования, а также необходимо применение различных шкал для качественной или количественной оценки СОАГС [15].
Один из основных методов терапии СОАГС является СИПАП-терапия (метод создания положительного давления воздуха в верхних дыхательных путях), которая эффективно уменьшает интериктальную эпилептиформную активность на ЭЭГ. В исследовании Р. Hollinger и соавт. (2006), показано, что СИПАП терапия уменьшает количество эпилептических припадков и помогает улучшить контроль над ними у 30 % пациентов [8]. По данным сравнительного исследования фармакорезистентных больных эпилепсией и СОАГС, рандомизированных по приему противоэпилептических препаратов и СИПАП терапии, приступы снизились по частоте (на 50 % и более) в группе пациентов с СИПАП терапией у 28 % пациентов, в то время как в группе с субоптимальным ведением СОАГС лишь у 15 % [14].
Цель – исследование частоты встречаемости СОАГС у взрослых больных с эпилепсией и оценка суточного характера эпилептических приступов в зависимости от степени тяжести СОАГС.
Материал и методы. Нами проанализировано 331 амбулаторная карта пациентов, обращавшихся за помощью в неврологический центр эпилептологии, нейрогенетики и исследования мозга Университетской клиники КрасГМУ им. проф. В.Ф. Войно-Ясенецкого в период с 2013 по 2015 г., которым проводилось исследование нарушения дыхания во сне. Временной срез проведенного исследования составил 3 года.
Критерии включения: возраст пациентов от 18 лет и старше, мужской и женский пол, верифицированный диагноз эпилепсии, наличие консультации невролога-эпилептолога, сомнолога, оториноларинголога.
Критерии исключения: возраст младше 18 лет, предположительный (неуточненный) диагноз эпилепсии. Согласно критериям включения и исключения рандомизирован 91/331 (27 %) клинический случай.
Объем диагностики: анализ жалоб, анамнеза жизни и анамнеза заболевания; физикальное и инструментальное (эндоскопическое) обследование (челюстно-лицевая дисморфия, оценка аденотонзиллярной патологии); ночной видео-ЭЭГ-мониторинг на компьютерном электроэнцефалографическом комплексе «Энцефалан-131-03» («Медиком МТД», Таганрог, Россия); магнитно-резонансная томография (МРТ) головного мозга по программе эпилепсии, высокопольная с шагом сканирования 0,8–1 мм (Siemens Symfhoy); ночной респираторный мониториторинг с пульсоксиметрией (Somnochek micro Weinman, Германия; ApneaLink ResMed, Австралия); ночной кардиореспираторный мониторинг – КРМ (Энцефалан, Медиком МТД, Россия); полисомнография – ПСГ (Embla N7000, ResMed, Исландия); консультация невролога-эпилептолога, сомнолога, оториноларинголога. Статистическая обработка базы данных проводилась согласно требованиям, предъявляемым к статистическому анализу биомедицинских данных и осуществлялась с использованием пакета прикладных программ STATISTICA v. 7.0 (StatSoft, USA), SPSS 22.0. Описательная статистика для качественных учетных признаков представлена в виде абсолютных значений, процентных долей и их стандартной ошибки. Вид распределения определялся с помощью критерия Шапиро – Уилка. Данные для вариационных рядов с непараметрическим распределением представлены в виде медианы и процентилей (Ме [Q25;Q75]). Для сравнения долей использовали двухсторонний критерий Фишера, при уровне значимости p ≤ 0,05.
Результаты и обсуждение. Общая выборка пациентов составила 91 человек в возрасте от 18 до 73 лет, медиана возраста – 30 [25 ; 43] лет, в том числе: 61 (67 ± 4,9 %) мужчин и 30 (37 ± 4,9 %) женщин (рис.1) .
р>0,05
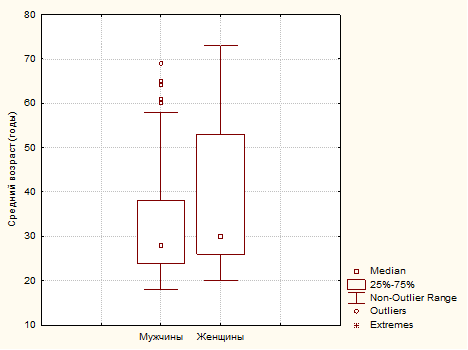
Рис. 1. Средний возраст наблюдаемых пациентов с эпилепсией в зависимости от пола
Распределение пациентов в зависимости от нозологической формы эпилепсии было следующим: 68/91 (74,7±4,55 %) человек с симптоматическими формами эпилепсии, включая 15/91 (16,5 ± 3,88 %) с лобно-долевой эпилепсией, 23/91 (25,3 ± 4,55 %) – с височно-долевой эпилепсией; 1/91 (1,1 ± 1,09 %) – с теменно-долевой эпилепсией; 26/91 (28,6 ± 4,74 %) с полифокальная эпилепсией; 12/91 (13 ± 3,5 %) с идиопатическими формами эпилепсии, включая 2/91 (2,2 ± 1,5 %) – с юношеской абсансной эпилепсией; 10/91 (11 ± 3 ,3 %) – с юношеской миоклонической эпилепсией; 13/91 (14,3 ± 3,66 %) человек с криптогенными формами эпилепсии. Таким образом, преобладали пациенты с симптоматическими височно-долевой и полифокальными формами эпилепсии.
Суточный профиль эпилептических приступов был следующим: у 5/91 (5,5 ± 2,38 %) человек зарегистрированы дневные приступы; ночные приступы – у 16/91 (17,6 ± 3,99 %) человек; смешанные приступы (преимущественно ночные) – у 32/91 (35,2± 5 %) ; у 39/91 (42,9±5,18 %) приступы не зарегистрированы (фармакоиндуцированная клиническая ремиссия). Таким образом, ночные и преимущественные ночные припадки зарегистрированы в целом у 52,8 % пациентов.
Ронхопатию (храп во время сна) имели 25/91 (27,5 ± 4,61 %) взрослых. СОАГС верифицирован у 40/91 (43,96 ± 5,2 %) человек, из них: легкой степени тяжести – у 19/40 (47,5 ± 7,8 %) и средней степени тяжести – у 15/40 (37,5 ± 7,6 %) человек, тяжёлой степени – у 6/40 (15± 5,6 %). Синдром центрального апноэ регистрировался – лишь у 4/91 (4,4 ± 2,1 %) (рис. 2). Осложненное течение СОАГС с лёгкой ночной гипоксемией во время респираторных событий имели 30/91 (33±4,92 %) человек, у 2/91 (2,2 ± 1,53 %) регистрировалась умеренная ночная гипоксемия. Таким образом, частота встречаемости СОАГС статистически значимо превышала частоту встречаемости центрального апноэ (43,9 % против 4,4 %) соответственно составила 9:1. Более чем в трети случаев СОАГС сопровождался ночной гипоксемией.
ИАГ в общей выборке варьировал от 0 до 35 в час (медиана – 2,5 [1; 7]). Индекс десатурации варьировал от 0 до 39 (медиана – 1 [0,4; 3]). Минимальная сатурация составила 61 %.
Осмотрены оториноларингологом 48/91 (52,8±5,23 %) пациентов. Хроническую патологию ЛОР-органов (искривление носовой перегородки, гипертрофия глоточной, нёбных миндалин, хронический гиперпластический синусит) имел 41/48 (85,4 ± 5,09 %) человек, в том числе: искривление носовой перегородки – 26/48 (54,2 ± 7,19 %), хронический тонзиллит – 5/48 (10,4 ± 4,4 %), гипертрофия глоточной миндалины 2–3 степени – 10/48 (20,8 ± 5,86 %), гипертрофия небных миндалин – 11/48 (22,9 ± 6,06 %), синусит – 10/48 (20,8 ± 5,86 %) человек.
Ожирением 1 степени страдали 11/91 (12,09 ± 3,41 %) человек , 2 степени – 3/91 (3,3 ± 1,87 %), 3 степени – 2/91 (2,20 ± 1,53 %), но в выборке преобладали пациенты с нормальным весом 75/91 (82,42 ± 3,99 %).
Средняя частота сердечных сокращений (ЧСС) варьировала от 42 до 91 ударов в минуту (медиана – 60 [55; 66] ударов в минуту).
Нарушения ритма сердца и проводимости во время респираторных событий выявлены в 18/91 (19,8 ± 4,17 %) случаях, включая 7/18 (38,9 ± 11,49 %) случаев синусовой аритмии, 5/18 (27,8 ± 10,55 %) экстрасистоли. У 1/18 (5,6± 5,39 %) пациента регистрировалась атрио-вентрикулярная блокада 2 степени, у 1/18 (5,6± 5,39 %) – фибрилляция предсердий.
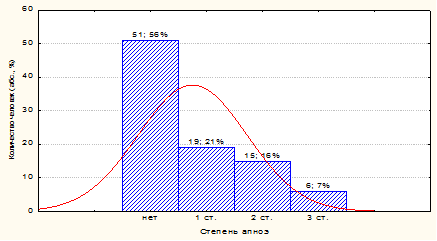
Рис. 2. Распределение пациентов с эпилепсией по степени тяжести СОАГС (N = 91)
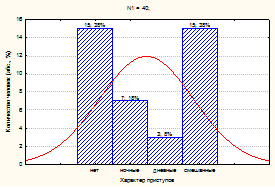
Для уточнения коморбидности СОАГС и эпилептических приступов у наблюдаемых взрослых общая выборка была разделена на две группы сравнения: 1 группа (сопоставимая) – 40 взрослых с эпилепсией и СОАГС; 2 группа (контрольная) – 51 взрослых с эпилепсией без СОАГС. У пациентов с СОАГС и эпилепсией чаще встречались смешанные эпилептические приступы (дневные и ночные) – 15/40 (37,5 ± 7,65 %), у 7/40 (17,5 ± 6,0 %) пациентов регистрировались только ночные эпилептические приступы, у 3/40 (7,5 ± 4,16 %) пациентов только дневные эпилептические приступы и у 15/40(37,5 ± 7,65 %) взрослых эпилептические приступы не регистрировались в связи с фармакоиндуцированной клинической ремиссией.
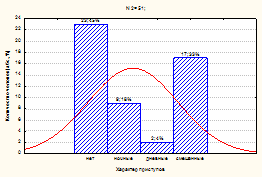
У взрослых контрольной группы с эпилепсией без СОАГС преобладали смешанные эпилептические приступы (дневные и ночные) – 17/51 (33,3 ± 6,6 %), у 9/51(17,6 ±5,3 %) взрослых регистрировались ночные приступы, у 2/51(3,92 ± 2,71 %) – дневные эпилептические приступы и у 23/51 (45,0 ± 6,8 %) взрослых отмечалась фармакоиндуцированная клиническая ремиссия без регистрации эпилептических приступов.
Частота достижения фармакоиндуцированной ремиссии у пациентов без СОАГС (группа контроля) по сравнению с пациентами с СОАГС (сопоставимая группа) – 45 % против 38 % соответственно (р<0,05).
а)
б)
Рис. 3. Коморбидность СОАГС и эпилептических приступов у наблюдаемых пациентов:
а) в 1 группе (сопоставимой); б) во 2 группе (контрольной)
Таким образом, частота преимущественно ночных и ночных эпилептических припадков у пациентов с СОАГС была выше, чем в группе контроля без СОАГС (55,0 % против 50,9 % соответственно), но межгрупповые различия не достигали статистической значимости (р>0,05), что побудило нас провести внутригрупповой и межгрупповой анализ в зависимости от степени тяжести СОАГС.
У пациентов с лёгкой степенью СОАГС одинаково часто встречались ночные и преимущественно ночные приступы – 5/19 (26 ± 10 %) и дневные эпилептические приступы – 4/19 (21 ± 9 %), а более чем в половине случаев достигнута фармакоиндуцированная ремиссия – 10/19 (52 ± 11 %).
У пациентов со средней степенью СОАГС чаще встречались ночные и преимущественно ночные приступы – 7/15 (46 ± 12 %), у 5/15 (33 ± 12 %) пациентов – только дневные эпилептические приступы. Фармакоиндуцированная ремиссия достигнута лишь у 2/15 (13 ± 8 %) человек.
У пациентов с тяжёлой степенью СОАГС изолированные дневные приступы не встречались, доминировали ночные приступы – 3/6 (50±20 %) и смешанные – преимущественно ночные приступы регистрировались у 3/6 (50 ± 20 %). Таким образом, выявлена статистически значимая прямая корреляция зависимости между степенью тяжести СОАГС и частотой ночных эпилептических приступов (р<0,01). Характер эпилептических приступов коррелирует с ИАГ: при лёгкой степени СОАГС дневные и ночные приступы встречаются одинаково часто, с увеличением ИАГ регистрируются преимущественно ночные приступы. Фармакоиндуцированная клиническая ремиссия у пациентов с эпилепсией в сочетании с СОАГС лёгкой степени регистрируется чаще (52 %), чем при средней степени СОАГС (13 %) в соотношении 4:1. Ремиссия эпилептических припадков не достигнута у всех пациентов с эпилепсией в сочетании с СОАГС тяжёлой степени.
Таблица 2
Характер эпилептических приступов в зависимости от степени тяжести СОАГС
|
Характер эпилептических приступов |
Степень тяжести СОАГС |
||
|
1 ст. абс. (%) |
2 ст. абс. (%) |
3 ст. абс. (%) |
|
|
Дневные |
4 (21,9 %) |
2 (13 %) |
0 (0,0 %) |
|
Ночные и преимущественно ночные |
5 (26 %) |
7 (46 %) |
6 (100 %) |
|
Фармакоиндуцированная ремиссия |
10 (52 %) |
2 (13 %) |
0 (0,0 %) |
Выводы
Симптоматическая фокальная (височно-долевая и полифокальная) эпилепсия у взрослых характеризуется высокой степенью коморбидности с СОАГС. Соотношение СОАГС и синдрома центрального апноэ у взрослых больных с эпилепсией составляет 9:1. Степень тяжести СОАГС статистически значимо негативно влияет на характер и частоту эпилептических припадков и снижает прогноз достижения фармакоиндуцированной ремиссии эпилепсии на фоне приёма противоэпилептических препаратов. Обоснован междисциплинарный подход к ведению (лечению и диспансерному наблюдению) взрослых больных с эпилепсией с участием не только невролога-эпилептолога, клинического нейрофизиолога, но и сомнолога и оториноларинголога. Пациентам с эпилепсией и СОАГС 2–3 степени тяжести показана респираторная поддержка во время ночного сна (СИПАП терапия) как один из методов болезнь-модифицирующей терапии.
Библиографическая ссылка
Шнайдер Н.А., Алексеева О.В., Артюхов И.П., Демко И.В., Петрова М.М., Сидоренко Д.Р. КОМОРБИДНОСТЬ СИНДРОМА ОБСТРУКТИВНОГО АПНОЭ/ГИПОПНОЭ СНА КАК ВАЖНЫЙ АСПЕКТ МЕНЕДЖМЕНТА ЭПИЛЕПСИИ У ВЗРОСЛЫХ // Современные проблемы науки и образования. 2016. № 6. ;URL: https://science-education.ru/ru/article/view?id=25472 (дата обращения: 07.05.2026).



