Постнекротические кисты поджелудочной железы (ПКПЖ) являются наиболее частым осложнением деструктивного панкреатита и травм поджелудочной железы. По данным разных авторов, частота их формирования составляет 18–92% [1-4].
В настоящее время на высоком уровне сохраняется частота осложнений и летальности при ПКПЖ, таких как инфицирование содержимого кист (28–67%), аррозивные кровотечения (1,6–20%), перфорация кист (20%), прорыв кисты в брюшную полость с развитием перитонита (5–15%), сдавление различных отделов желудочно-кишечного тракта (3–4%) [2; 5; 9; 10].
Проблема выбора тактики лечения ПКПЖ остаётся актуальной до настоящего времени. Традиционные методы лечения ПКПЖ – операции внутреннего (ВД) и наружного дренирования (НД) путём лапаротомии - имеют массу недостатков, связанных с травматичностью операции, высоким риском возникновения интра- и послеоперационных осложнений, продолжительным периодом стационарного и поликлинического периодов лечения, а также формированием наружного панкреатического свища [2; 3; 5; 7; 8].
Ряд авторов считают наружное дренирование кист ПЖ только вынужденной мерой, когда внутреннее дренирование не представляется возможным. Другие авторы применяют пункционные и дренирующие методы под контролем УЗИ как первый этап лечения, направленный на санацию нагноившейся кисты для создания оптимальных условий для последующей радикальной операции [4; 6].
В настоящее время все большую актуальность приобретают методы малоинвазивных вмешательств при ПКПЖ: транскутанные пункционно-дренирующие вмешательства под ультразвуковым контролем, а также выполнение внутреннего эндоскопического транслюминального дренирования.
Материал и методы. В период с 2013 по 2015 г. в Краевой клинический больнице было выполнено 19 малоинвазивных вмешательств – эндоскопическое транслюминальное дренирование по поводу постнекротических кист поджелудочной железы. Большинство из пациентов были мужчины – 68,4% (n=13), женщин – 31,6% (n=6), средний возраст составил 49,5 ± 14,6 года. Диагноз устанавливался на основании данных анамнеза, общеклинических и инструментальных методов исследования: УЗИ, МСКТ брюшной полости, при необходимости выполняли диагностические пункции жидкостных образований с исследованием их содержимого, эндо-УЗИ и пункции кисты под ЭУС-наведением. Наиболее частые жалобы пациентов при поступлении были: болевой синдром, чувство «тяжести» в эпигастрии, периодические подъемы температуры тела до субфебрильных цифр, слабость, тошнота.
Среди причин острого панкреатита и панкреонекроза у 26,3% (n=5) установлена желчнокаменная болезнь, у 42,1% (n=8) – злоупотребление алкоголем, у 26,4% (n=6) – погрешность в диете, 5,2 % (n=1) – посттравматическая.
Для распределения по размеру псевдокист, который устанавливался по данным УЗИ и МСКТ, мы использовали следующую классификацию: гигантские (более 15 см) – 3, большие (от 10 до 15 см) - 8, средние (от 5 до 10 см) – 8. У 2 пациентов с гигантскими псевдокистами имело мест сдавление окружающих органов и тканей (желудок, ДПК, гепатодуоденальная связка), при этом явлений механической желтухи и признаков стеноза выходного отдела желудка не отмечалось.
По характеру содержимого кисты: у 52,6% (n=10) пациентов кисты были инфицированными (в полости гной, у нескольких пациентов с элементами секвестрации ПЖ), у 47,4% (n=9) пациентов - неинфицированными.
По локализации псевдокист: в головке поджелудочной железы – 26,3% (n=5), тело – 31,5% (n=6), хвост – 42,2% (n=8). При наличии нескольких кист учитывалась локализация наибольшей из них. Также мы оценивали связь полости псевдокисты с вирсунговым протоком, используя данные МСКТ и клиническое течение: у 5 пациентов такая связь имелась, причем у 80% из них (n=4) локализация кисты была в головке поджелудочной железы. Явления внутрипротоковой гипертензии (вирсунгоэктазия) отмечена у 4 пациентов.
Выбор метода стентирования постнекротических кист определялся непосредственно при эндоскопическом исследовании и зависел от расположения кистозного образования, строения стенок, взаимоотношения с соседними органами и характера содержимого кисты. Показанием к выбору пластиковых стентов было гомогенное содержимое кисты. Для выбора металлических саморасправляющихся стентов показаниями служили: отсутствие четкой стенки образования, наличие секвестров, инфицирование образования, киста более 5 см в диаметре, толщина ткани между стенкой ЖКТ и образованием не более 1 см, наличие бессосудистой зоны.
Для транслюминального дренирования использовали стандартное оборудование марки для проведения эндоскопической ретроградной холангиопанкретографии (ЭРХПГ), эндоскопической папиллосфинктеротомии (ЭПСТ), билиарного эндопротезирования: гастроскоп и дуоденоскоп фирмы Olympus, C-дуга Dixion Cyberbloc, пластиковые стенты Olympus и металлические саморасправлющиеся стенты MTW.
Первым этапом в условиях общей внутривенной анестезии проводили осмотр стенок желудка и ДПК, выявляли выбухание стенки желудка, к которой предположительно предлежит кистозное образование, окончательная верификация кисты выполнялась с помощью эндоскопической ультрасонографии (эндо-УЗИ).
Эндо-УЗИ позволяет точно лоцировать псевдокисту, определить расстояние между стенками псевдокисты и верхних отделов ЖКТ, характер содержимого кисты, выявить бессосудистую область для безопасной установки стента (рис. 1). Затем через бессосудистую зону стенки желудка в полость кисты вводили струну-проводник. С помощью С-дуги производили рентген-контроль введения проводника в полость кисты (рис. 2). Выполняли контрастирование полости кисты для установления разгерметизации протоков поджелудочной железы.
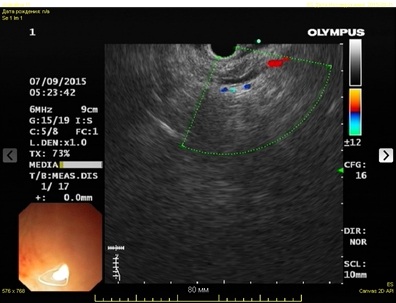
Рис. 1. Эндо-ультрасонография с доплерографией для выявления бессосудистой области стенки желудка
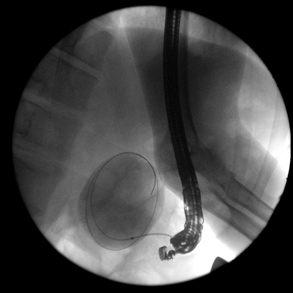
Рис. 2. Рентген-контроль введения струны-проводника в полость кисты
По струне-проводнику в полость кисты устанавливали пластиковый или металлический стент. Инструменты извлекали и проводили визуальный осмотр стента.
Для оценки уменьшения объема псевдокисты рассчитывали исходный объем (при поступлении), конечный объем (при выписке), а также их соотношение для оценки степени уменьшения объема, используя стереометрическую формулу: V = (π × D1 × D2 × D3) / 6; где V – объем жидкостного образования; π – 3,14; D1, D2, D3 – взаимно перпендикулярные размеры жидкостного образования, вычисленные по данным МСКТ. При этом клинически значимым признавалось уменьшение объема псевдокисты более чем на 80% от исходного объема.
Эффективность дренирования оценивали по следующим критериям.
1. Хороший результат: жидкостное образование не выявлено при УЗИ на момент выписки больного из стационара.
2. Удовлетворительный результат: уменьшение размеров жидкостного образования на момент выписки больного из стационара.
3. Неудовлетворительный результат: размеры жидкостного образования не уменьшились на момент выписки больного из стационара.
Таким образом, эффективность лечения оценивали по улучшению общего состояния, уменьшению полости кисты и наличию осложнений, продолжительности стационарного лечения.
Статистическая обработка результатов проводилась с использованием программ Exсel-2016 и Statistica 10. StatSoft. Для проверки нормальности распределения использовали критерий Шапиро-Уилка. Статистическую равнозначность сравниваемых групп пациентов мы проверяли с помощью непараметрического критерия Манна-Уитни. При p>0,05 статистически значимого отклонения не выявлялось. А при p≤0,05 выявляемые отклонения считались статистически значимыми. Это соответствует общепринятым стандартам анализа в медико-биологических исследованиях. Далее исследуемые группы пациентов сравнивались по соотношению летальности и риску развития осложнений, а также по среднему койко-дню, проведённому в стационаре.
Результаты и обсуждение
Всем пациентам проводилась системная антибактериальная, инфузионная, антисекреторная и симптоматическая терапия.
В послеоперационном периоде 6 пациентам в дополнении к трансгастральному дренированию выполнено наружное дренирование кисты под ультразвуковым контролем: у 3 псевдокист имелась связь полости кисты с вирсунговым протоком; 3 псевдокисты с инфицированным содержимым. Клиническое течение не осложнялось, к 6-7-му дню послеоперационного периода отсутствовали жалобы на боли, температура тела и лабораторные показатели (лейкоцитоз менее 10 тысяч, амилаземия менее 200 Ед/л) нормализовались, наружный дренаж был удален в разные сроки (5-10-е сутки после дренирования) при уменьшении объема кисты на 80% и более. В дальнейшем клинически значимое уменьшение объема кисты перед выпиской установлено у всех 6 пациентов (p<0.05). Продолжительность лечения составила 22,8±13,2 койко-дня. Хороший и удовлетворительный результат лечения также достигнут у всех 6 пациентов.
3 пациента после трансгастрального дренирования были оперированы открыто в связи с прорывом содержимого псевдокисты в сальниковую сумку, дислокацией стента в полость кисты (повторное стентирование также привело к дислокации стента) и в связи с прогрессированием панкреонекроза.
Одному пациенту с псевдокистой после резекции хвоста ПЖ – выполнено ЭРХПГ, ЭПСТ, стентирование вирсунгового протока. Перед выпиской объем кисты уменьшился на 96,4%, благодаря чему достигнут удовлетворительный результат лечения.
У 10 пациентов, которым было выполнено только эндоскопическое транслюминальное дренирование, клиническое течение протекало без осложнений. К 3-4-му дню послеоперационного периода нормализовалась температура тела и лабораторные показатели у 7 пациентов с инфицированными псевдокистами. В дальнейшем перед выпиской клинически значимое уменьшение объема кисты установлено у 8 пациентов (p<0,05). У 2 пациентов уменьшение объема составило 77,6% и 73,5%, при этом у этих пациентов имелись признаки внутрипротоковой гипертензии (вирсунгоэктазия, установленная по данным МСКТ). Продолжительность лечения составила 15,6±6,2 койко-дня (р<0,05). Хороший и удовлетворительный результат лечения достигнут у всех 10 пациентов.
Заключение. На основании результатов представленного первого клинического опыта можно сделать следующие выводы.
1. Выполнение трансгастрального дренирования псевдокист ПЖ под ЭУС-наведением является малоинвазивным методом лечения, с минимальным риском развития таких грозных послеоперационных осложнений, как кровотечение, перфорация, перитонит.
2. Эндоскопическая методика лечения позволяет достичь хороших результатов, не прибегая к хирургическим методами лечения: клинически значимое уменьшение объема псевдокисты достигнуто у 73,6% пациентов (p<0.05), хороший и удовлетворительный результат лечения достигнут в 84,2% случаев (p<0.05).
3. Средняя продолжительность пребывания больных в стационаре составила 18,7±3,1 койко-дня.
4. Комбинированное дренирование (эндоскопическое трансгастральное и наружное дренирование под ультразвуковым контролем) дает хорошие клинические результаты при наличии связи полости кисты с вирсунговым протоком и/или инфицированности содержимого псевдокисты. У всех пациентов этой группы уменьшение объема кисты было клинически значимым (p<0.05), хорошие и удовлетворительные результаты достигнуты у 100% пациентов этой группы (p<0.05). У пациентов (n=2) с диагностированной внутрипротоковой гипертензией, котором было выполнено изолированное эндоскопическое транслюминальное дренирование, уменьшение объема кисты было клинически незначимо, при этом хороший и удовлетворительный результат лечения был достигнут.
Таким образом, индивидуальный подход к выбору способа дренирования постнекротических псевдокист поджелудочной железы и/или их комбинации позволяет избежать многоэтапных хирургических вмешательств, избавить пациентов от последующих рецидивов и осложнений, повысить эффективность оказания медицинской помощи больным с острым панкреатитом и панкреонекрозом.
Библиографическая ссылка
Черданцев Д.В., Первова О.В., Жегалов П.С., Носков И.Г., Курбанов Д.Ш. ВОЗМОЖНОСТИ ТРАНСЛЮМИНАЛЬНОГО ДРЕНИРОВАНИЯ ПОСТНЕКРОТИЧЕСКИХ КИСТ ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ ПОД ЭУС-НАВЕДЕНИЕМ // Современные проблемы науки и образования. 2016. № 5. ;URL: https://science-education.ru/ru/article/view?id=25416 (дата обращения: 15.05.2026).



