Несмотря на современное усовершенствование перинатальной помощи, не наблюдается тенденция к снижению частоты перинатальных поражений ЦНС. По статистическим данным по Воронежской области на 2012 год было зарегистрировано 4943 случая, а на 2015 – 5929 случаев перинатальных поражений ЦНС [4]. На сегодняшний день на диспансерном учете состоит 1112 детей с последствиями перинатального поражения ЦНС [1].
Перинатальная гипоксия – наиболее распространенное осложнение беременности и родов, важная причина повреждения ЦНС у новорожденных детей, приводящая к жизненно важным долгосрочным неврологическим осложнениям [2]. Неврологический дефицит, как следствие перинатального повреждения, колеблется от легких поведенческих расстройств до детского церебрального паралича, эпилепсии, умственной отсталости и т.д. Кроме того, врач не всегда по клиническим проявлениям и лабораторно-инструментальным данным может достоверно определить исход заболевания, что в свою очередь ведет к неблагоприятным последствиям в будущем в связи с отсутствием своевременной и адекватной терапии [5].
Поэтому помимо функциональной активности нервных клеток важна оценка трофического обеспечения их жизнедеятельности, реализующаяся посредством нейротрофинов (НФ) [8].
НФ представляют собой регуляторные белки нервной ткани, образующиеся в нейронах и глии. Главной функцией НФ является реализация регенераторных процессов восстановления и активации компенсаторных возможностей нейроглиального окружения, что актуально при изучении перинатальной энцефалопатии и ее исходов [6].NGF (фактор роста нервов) представляет наибольший интерес среди нейротрофинов в качестве маркера для оценки неврологического дефицита [3]. Он широко экспрессируется в различных тканях, может оказывать нейротрофический эффект на поврежденные нейроны и содействовать нейрогенезу. Кроме того, очень важно, что глиальные клетки стимулируют нейротрофиновые рецепторы, и определенный уровень NGF в крови является показателем нормальной функцией глии [7,9].
Все вышесказанное определяет актуальность изучения NGF в качестве диагностического маркера при оценке степени выраженности неврологического дефицита у детей первого года жизни.
Целью настоящего исследования явилось провести анализ зависимости уровня NGF от степени тяжести неврологического дефицита у детей первого года жизни.
Материалы и методы
В ходе исследования было обследовано 419 пациентов в возрасте от 0 до 6 месяцев, из них мальчики составили 52 %, девочки – 48 %. В основную группу вошли 336 пациентов первого года жизни, находившихся на стационарном лечение по поводу последствий перинатального поражения нервной системы различной степени тяжести, контрольную группу – 83 условно здоровых ребенка. Дети контрольной группы проходили осмотр педиатра в рамках стандартного обследования в регламентированные периоды наблюдения на этапе поликлинического обслуживания. Обязательным условием включения пациентов контрольной группы явилось отсутствие неврологической симптоматики, постановки на учет у невролога и получения медикаментозной терапии по поводу неврологических отклонений на первом году жизни.
Все дети были разделены на две подгруппы пациентов с учетом возрастного показателя: основная группа – 163 ребенка (48 %) в возрасте от 1 до 3 мес. и 173 пациента (52 %) в возрасте 4–6 мес., контрольная группа – в возрасте от 1 до 3 мес. – 43 (52 %) ребенка и 40 (48 %) детей в возрасте 4-6 мес. (таблица 1).
Таблица 1
Количественная характеристика обследуемых детей
|
возраст |
Основная группа |
Контрольная группа |
||
|
легкая степень тяжести |
средняя степень тяжести |
тяжелая степень тяжести |
||
|
1-3 мес. |
60 |
58 |
45 |
43 |
|
4-6 мес. |
62 |
60 |
51 |
40 |
|
всего |
336 |
83 |
||
Первый возрастной период характеризуется снижением нейрональных потерь и уменьшением выраженности неврологических расстройств, что особенно важно для своевременной диагностики неврологического дефицита ребенка. Во второй возрастной период происходит рост дистрофически изменённых нейронов, разрыв синаптических связей, нарушение взаимодействия различных областей мозга, что определяет более широкую клиническую картину неврологических симптомов на данном этапе с одной стороны при отсутствии адекватной терапии или закрепление положительного результата, полученного на более раннем этапе.
В структуре подгрупп основной группы детей нами было произведено разделение еще на 3 подгруппы в зависимости от степени тяжести патологического процесса вследствие перенесенного перинатального поражения ЦНС: 1 группа (легкая степень тяжести) – 122 человек (36 %), 2 группа (средняя степень тяжести) – 118 (35 %) человек, 3 группа (тяжелое течение) – 96 человек (29 %) (рисунок).
Всем детям, независимо от группы, проводился анализ паспортов новорожденных, тщательный сбор анамнеза, оценка соматического и неврологического статуса с привлечением осмотра узких специалистов, лабораторно-инструментальных методов обследования. Для оценки поражения нервной системы использовали классификацию Ю.А. Якунина (1979). Неврологический дефицит ребенка оценивался количественным методом, исходя из 3 баллов по степени тяжести (0 – норма, 1 – легкое отклонение, 2 – отклонение средней степени тяжести, 3 – тяжелая степень).
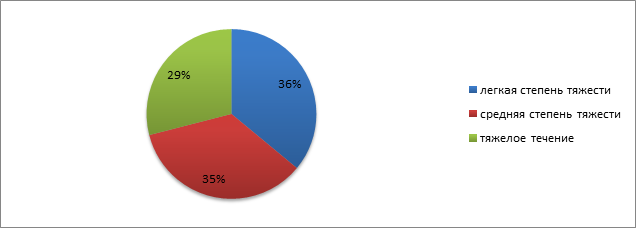
Распределение на подгруппы в зависимости от степени тяжести патологического процесса вследствие перенесенного перинатального поражения ЦНС
Для определения бета субъединицы человеческого фактора роста нервов применяли иммуноферментный набор (Beta-NGF; каталожный номер ELH-BNGF-001 – 96 определений, фирма производитель «RayBio», фирма поставщик – «БиоХимМак», Россия).
Статистическая обработка результатов исследования проводилась на ПЭВМ Реntium III-500, с помощью пакетов программ Ехсеl 2003, Statistica, SPSS for Windows. Включала в себя использование стандартных методов вариационной статистики (расчет средних значений (М), ошибки средних значений (m)). При нормальном распределении различия между группами определялись с помощью t-критерия Стьюдента (достоверные различия при p< 0,05). Для оценки корреляционных связей между параметрами использовался критерий Пирсона. Слабая связь по критерию Пирсона определялась при r ≤ 0,25, умеренная – при r< 0,75, сильная – при r ≥ 0,75.
Результаты исследования и их обсуждение
Анализ паспорта новорожденного основной группы выявил, что гипоксическое поражение нервной системы доминирует в структуре последствий перинатального поражения нервной системы и составило 59,8 %. В удовлетворительном состоянии родилось в основной группе – 211 пациентов и все дети контрольной группы. Среднетяжелое состояние при рождении имели 85 человек, тяжелое – 40 детей. Реанимационным мероприятиям с последующим пребыванием на ИВЛ от 2 до 7 суток были в анамнезе у 6 детей. Доношенными родилось 285 детей основной группы и 59 контрольной, недоношенность I степени составила 35 и 24 ребенка соответственно, недоношенность II степени – 12 детей и недоношенность III степени – 4 человека были установлены только в контрольной группе.
Оценка анамнестических данных выявила, что ведущим фактором риска гипоксически-ишемического поражения ЦНС у детей можно отнести наличие у женщин в анамнезе курения, хронических и острых соматических и/или гинекологических заболеваний, ранний токсикоз (в срок до 12 недель беременности), гестоз второй половины беременности, угрозу прерывания в I триместре, хроническую гипоксию плода и родоразрешение путем кесарева сечения. Все вышеописанные факторы риска встречались чаще в 2–3 раза у детей основной группы, в структуре подгрупп: достоверно чаще в 3-ей группе по сравнению с другими, по сравнению с 1 группой (ρ<0,05). Данные факторы потенцируют диффузную ишемию с каскадом биохимических реакций, приводящих в конечном итоге к двум вариантам развития событий: пикнозу и/или апоптозу, которые собственно и обуславливают последствия перинатального поражения нервной системы.
Анализируя частоту клинических неврологических проявлений в основной группе, можно отметить, что у детей доминантными неврологическими синдромами были: синдром внутричерепной гипертензии (91 %), двусторонняя пирамидная недостаточность (89 %), вегето-висцеральная дизрегуляция (54 %), синдром двигательных расстройств (43 %), различные пароксизмальные состояния (17 %), ликвородинамические нарушения (28 %), органическое поражение ЦНС (21 %).
Структура тяжести неврологического дефицита детей основной группы была представлена следующим образом:
· возраст 1–3 месяца (n=163/49 %): первая (легкая) степень тяжести клинических проявлений была установлена у 60 (18,6 %) пациентов; средняя (вторая) степень тяжести зафиксирована у 58 (17,2 %) обследуемых; третья (тяжелая) степень клинических проявлений выявлена у 45 (13,4 %) детей;
· возраст 4–6 месяцев (n=173/51 %): первая (легкая) степень тяжести клинических проявлений была установлена у 62 (19 %) пациентов; средняя (вторая) степень тяжести – 60 (18,6 %) обследуемых; третья (тяжелая) степень клинических проявлений выявлена у 51 (15,2 %) детей;
· контрольная группа (n=83): в каждой возрастной выборке методом аккумулированных средних определялись свои контрольные значения исследуемых показателей, но их значения достоверно совпадали между собой, поэтому исходные показатели для сравнения были выбраны едиными для всех групп объектов изучения.
Итогом проведенного корреляционного анализа изучаемых факторов как клинического, так и нейротрофического состояния пациентов стало выявление прямой достоверной высоко положительной связи динамичных значений NGF от клинического состояния ребенка во всех группах исследования: симптом Грефе (r=-0,67, p<0,05), снижением мышечного тонуса (r=0,84, p<0,05), снижением сухожильных рефлексов (r=0,77, p<0,05), асимметричностью складок (r=-0,83, p<0,05), наличием пирамидных знаков (r=0,89, p<0,05).
В группе 1–3 мес. при легкой степени тяжести клинических проявлений поражения нервной системы NGF практически не изменялся, либо достоверно (p<0,01) повышался, но не более 7–8 % в сравнении с данными контрольной группы. При средней степени тяжести клинических проявлений поражения нервной системы было установлено, что NGF достоверно снижался на 12–15 %. Для тяжелой степени тяжести клинических проявлений поражения нервной системы установлено, что достоверно (p<0.01) снижался по сравнению с контрольными данными NGF на 44–48 % (таблица 2). Полученные результаты отражают зависимость уровня NGF от степени тяжести. Отсутствие динамических изменений в подгруппе с легкой степенью тяжести может свидетельствовать об отсутствии выраженных клинических проявлений неврологического дефицита, а поэтому важно учитывать целевой уровень значения NGF в сыворотке крови.
Таблица 2
Динамика фактора NGF в исследовании
|
группы / исходный уровень (пг/мл) |
легкая степень тяжести(пг/мл) |
средняя степень тяжести(пг/мл) |
тяжелая степень тяжести(пг/мл) |
|||
|
1-3 мес 243±168,62 |
NGF |
342,1±92,37 |
NGF |
201,9±72,79 |
NGF |
166,8±75,57 |
|
4-6 мес 243±168,62 |
NGF |
339,4±97,61 |
NGF |
190,7±61,29 |
NGF |
145,7±69,49 |
В группе 4–6 месяцев при легкой степени тяжести клинических проявлений поражения нервной системы NGF практически не изменялся, либо достоверно (p<0.01) повышался, но не более 10–12 % в сравнении с данными контрольной группы, что отражает напряжение компенсаторных функций ЦНС и, как следствие, улучшение клинической симптоматики. Для средней степени тяжести клинических проявлений поражения нервной системы установлено, что NGF достоверно снижался на 20–25 %. При тяжелой степени тяжести клинических проявлений поражения нервной системы установлено, что достоверно (p<0.01) NGFснижался по сравнению с контрольными данными на 45–50 % соответственно. Полученные результаты являются прогностически неблагоприятными, отражают более тяжелое поражении тканей головного мозга в данной группе детей и необходимость в массивной нейропротекторной терапии.
Выводы.
Во-первых, полученные результаты позволяют рассматривать NGF в качестве диагностического маркера неврологического дефицита у детей раннего возраста.
Во-вторых, открывают новые возможности в патогенетически обоснованном подборе медикаментозной терапии и оценке ее эффективности.
Библиографическая ссылка
Красноруцкая О.Н., Бугримов Д.Ю., Зуйкова А.А., Котова Ю.А., Добрынина И.С., Страхова Н.В., Ханина Е.А. ФАКТОР РОСТА НЕРВОВ – ДИАГНОСТИЧЕСКИЙ МАРКЕР СТЕПЕНИ ВЫРАЖЕННОСТИ НЕВРОЛОГИЧЕСКОГО ДЕФИЦИТА У ДЕТЕЙ // Современные проблемы науки и образования. 2016. № 5. ;URL: https://science-education.ru/ru/article/view?id=25199 (дата обращения: 22.03.2026).



