Актуальной проблемой в современном эндопротезировании коленного сустава является разработка и усовершенствование технологии оперативного вмешательства, которая позволила бы более прецизионно восстановить биологическую ось конечности, более точно выполнить позиционирование компонентов эндопротеза и уменьшить количество асептических расшатываний имплантатов, составляющих от 38,8 до 56,5% среди всех причин ревизий [1; 3; 4; 30]. Использование только стандартных экстрамедуллярных и интрамедуллярных направителей не позволяет достигнуть решения данной проблемы [13; 23; 28]. С целью повышения точности восстановления биологической оси конечности, позиционирования компонентов эндопротеза наиболее часто в мире применяются две технологии: использование индивидуальных направителей и компьютерной навигации, которая, по данным различных авторов, зачастую приводит к неудовлетворительным результатам операции [11; 30]. Одним из инновационных решений данной проблемы является разработка прецизионных персонифицированных направителей (ППН), которые включают в себя как индивидуальные кондукторы для проведения пинов, так и резекционные блоки. Очевидным преимуществом данной технологии является возможность более точной реконструкции биологической оси конечности с уменьшением времени оперативного вмешательства, его упрощением [24]. При терминальных стадиях гонартроза имеются многоплоскостные деформации как проксимального отдела большеберцовой кости, так и дистального отдела бедренной кости. Выполнение оперативного вмешательства в данном случае сопряжено с высоким риском развития неудовлетворительных результатов эндопротезирования. Решением данной проблемы является тщательное предоперационное планирование. Однако применение только данных рентгенологического обследования и даже телерентгенограмм (FLFS) не позволяет достоверно отобразить трехплоскостную деформацию. Таким образом, необходимым в подобных случаях является использование технологий 3D-моделирования с последующим созданием ППН [1-4; 13].
Несмотря на большое количество исследований по данной теме, их результаты противоречивы, а научных работ, в которых были бы представлены данные сравнительного анализа различных публикаций со сформулированными показаниями к применению индивидуальных направителей, нами не обнаружено.
Разнообразие персонифицированных прецизионных направителей. В современный период происходит увеличение количества выполняемых операций с использованием ППН, появляются новые технологии их создания, расширяются показания к применению. Наиболее часто используемыми индивидуальными направителями являются: TruMatch (DePuy), PSI (Zimmer), GMK MyKnee (Medacta), VISIONAIRE Patient Match Technology (Smith & Nephew), PROPHECY® Preoperative Navigation Guides (Microport Orthopaedics), Signature (Biomet Victoria Tasmania).
Опыт применения персонифицированного направителя TruMatch, DePuy (рис. 1) описан в исследовании Collins, где автор показал отличные, как клинические, так и рентгенологические, результаты более чем 600 выполненных операций. Использование ППН позволило добиться более точного позиционирования компонентов эндопротеза по сравнению со стандартным инструментарием, уменьшить роль ассистента в ходе оперативного вмешательства [12].

Рис. 1. Персонифицированный направитель TruMatch, DePuy [15]
Использование PSI, Zimmer (рис. 2) при эндопротезировании коленного сустава приводит к несоответствию расположения бедренного и большеберцового компонентов эндопротеза более чем на 3 градуса в 3-17% случаях по сравнению с предоперационным планированием [31]. Однако в исследовании Köster с соавторами представлены данные о том, что применение данного персонифицированного направителя позволило добиться более точного позиционирования компонентов эндопротеза по сравнению с традиционной техникой эндопротезирования [20].

Рис. 2. Персонифицированный направитель PSI, Zimmer [39]
Применение направителей GMK MyKnee привело в 12,4% случаях к отклонению расположения компонентов эндопротеза более чем на 3 градуса от запланированного. Также авторы исследования указывают на отсутствие различий в результатах эндопротезирования коленного сустава с использованием ППН и компьютерной навигации [37].
Применение VISIONAIRE Patient Match Technology при эндопротезировании коленного сустава привело к несоответствию более чем на 2 мм по сравнению с предоперационным планированием уровня резекции дистального отдела бедренной кости в 90% случаях и более чем в 70% случаях проксимального отдела большеберцовой кости [33].
При сравнении индивидуальных направителей различных производителей Huijbregts с соавторами показали наименьший риск смещения расположения компонентов эндопротеза от запланированного при использовании PSI, Zimmer [19]. Однако в данной научной работе не были учтены результаты многих крупных исследований: Köster 2016 [20], Scholes 2014 [31], Tibesku 2016 [33], Zambianchi 2015 [37], в которых показатели отклонения установленных компонентов эндопротеза коленного сустава значительно меньше. Таким образом, несмотря на многочисленные исследования, результаты у разных авторов по использованию ППН одного и того же производителя отличаются. По нашему мнению, это связано со сравнением показателей после эндопротезирования коленного сустава по поводу гонартроза с различной степенью выраженности деформации, различным опытом хирургов по использованию индивидуальных направителей, неоднородными группами пациентов.
Предоперационное планирование и хирургическая техника. Основным показанием к применению ППН для эндопротезирования коленного сустава является деформирующий гонартроз III-IV стадии [по классификации Kellgren и Lawrence] с невозможностью использования компьютерных навигационных систем и стандартных направителей (рис. 3).
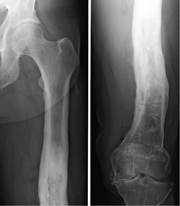
Рис. 3. Посттравматическая деформация бедренной кости, затрудняющая использование интрамедуллярного направителя [24]
Создание ППН по методике, описанной в работах Mattei, Barrett, Ajwani, Lustig, включает в себя несколько этапов [5; 9; 22; 24]. Первоначально, по данным КТ или МРТ, производится создание компьютерной 3D-модели коленного сустава конкретного пациента. На втором этапе с помощью методик программного моделирования хирург осуществляет резекцию бедренной и большеберцовой костей под определенными углами в различных плоскостях с целью реконструкции биологической оси конечности.
Контроль ротации бедренного компонента эндопротеза осуществляется относительно чрезнадмыщелковой оси бедра, тибиального – относительно бугристости большеберцовой кости. Затем с помощью методик топологической оптимизации и гибридного параметрического моделирования создается ППН в виде направителя для проведения пинов или резекционного блока. На компьютерной модели коленного сустава определяются необходимые размеры компонентов эндопротеза. Третий этап включает в себя 3D-печать ППН. Для этого может быть использован FDM, SLS, SLA и другие 3D-принтеры. Бедренный ППН используется для установки вальгуса, уровня резекции и необходимой ротации феморального компонента эндопротеза. Большеберцовый ППН применяется для позиционирования тибиального компонента эндопротеза, определения уровня резекции, слопа (наклона) и ротации. Средний срок создания ППН составляет 3-4 недели [5; 9; 22; 24; 26; 34]. Другие методики создания индивидуальных направителей отличаются только используемыми инструментами программного моделирования [12; 20; 28; 31; 33; 37].
Во время оперативного вмешательства ППН используются с целью позиционирования пинов для стандартных резекционных блоков (рис. 4) или в качестве непосредственно резекционных блоков. Остальная часть операции выполняется по стандартной методике. Если не удается достигнуть необходимого восстановления оси конечности при использовании ППН, хирург может перейти к применению стандартных резекционных блоков [9; 22; 24; 34].
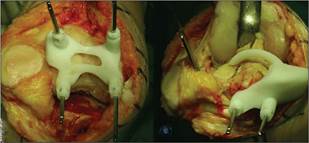
Рис. 4. Персонифицированные направители для прецизионного введения пинов [21]
Создание ППН на основе данных МРТ, по мнению ряда авторов, позволяет учитывать хрящевую ткань сустава, мениски, которые могут быть использованы в качестве дополнительных ориентиров. Однако данная технология не получила распространения ввиду более точного позиционирования индивидуальных направителей, созданных по данным КТ [5; 20; 22; 24; 31; 37].
Клинические и рентгенологические результаты. Несмотря на многочисленные исследования, единого мнения по поводу улучшения рентгенологических и клинических результатов при использовании ППН по сравнению со стандартными направителями и применением компьютерной навигации до сих пор нет.
Ряд авторов показали в своих исследованиях отсутствие целесообразности применения ППН при эндопротезировании коленного сустава.
В сравнении с компьютерной навигацией, Conteduca с соавторами доказали, что ППН не способны достичь удовлетворительного позиционирования компонентов эндопротеза [14]. В исследовании Sassoon с соавторами представлены данные о том, что ППН не имеют преимуществ по сравнению со стандартными направителями в более точном восстановлении оси конечности [30]. Также не было обнаружено разницы в восстановлении оси конечности при сравнении традиционной техники и ППН в исследовании Rho с соавторами. Однако они сообщают о 12% случаях наружной ротации бедренного компонента протеза при применении индивидуальных направителей [29]. В исследовании Barrett с соавторами представлена информация о том, что применение компьютерной навигации позволяет более точно позиционировать компоненты эндопротеза по сравнению с индивидуальными направителями [9]. В научной работе Boonen представлена информация о 29% случаев отклонений от механической оси нижней конечности (более 3°) во фронтальной плоскости при использовании ППН [10]. В исследовании Nunley с соавторами представлены данные о худших результатах, в виде смещения биологической оси конечности от нормы у 37% пациентов при использовании ППН [26].
Тем не менее, несмотря на представленные результаты исследований, некоторые авторы сообщают о более высокой точности позиционирования компонентов эндопротеза и восстановления биологической оси нижней конечности при использовании ППН, связывая это с более тщательным предоперационным планированием.
Anderl с соавторами представили результаты, которые показывают значительно высокую точность восстановления механической оси и позиционирования компонентов эндопротеза по сравнению со стандартными направителями. В данном проспективном исследовании среднее отклонение от целевого положения компонента протеза во всех плоскостях составило менее 2° [6]. В своих исследованиях Heyse с соавторами доказали, используя различные методы томографии, что ППН позволяет достичь более высокую частоту ротационной стабильности компонентов эндопротеза по сравнению с традиционной технологией эндопротезирования [17; 18].
При сравнении клинических результатов после операции мнения разных авторов о целесообразности применения ППН при эндопротезировании коленного сустава также расходятся.
Yaffe с соавторами показали значительное улучшение функционального результата через 6 месяцев после операции с использованием ППН по сравнению со стандартными направителями [36]. С другой стороны, разные авторы продемонстрировали, что никаких существенных клинических преимуществ ППН по сравнению со стандартной технологией эндопротезирования нет. Это было установлено как для тотального, так и одномыщелкового эндопротезирования коленного сустава [27; 38].
Кровопотеря. В исследовании Thienpont с соавторами оценили влияние ППН на кровопотерю, сравнивая со стандартной технологией эндопротезирования. Было доказано, что применение интрамедуллярного направителя для бедра, когда обязательным является вскрытие костномозгового канала, приводит к большей кровопотере, по сравнению с использованием индивидуальных направителей [32]. Спорные данные были найдены в литературе по оценке кровопотери при применении экстрамедуллярного направителя [5; 7; 14; 25]. Однако Voleti с соавторами в своем исследовании отмечают, что использование костной аутопластики для закрытия костномозгового канала бедренной кости приводит к снижению кровопотери при применении интрамедуллярного направителя [35].
Время оперативного вмешательства. Существует мнение о том, что ППН теоретически может сократить время операции, особенно для менее опытных хирургов. В рандомизированном контролируемом исследовании Hamilton с соавторами показали, что ППН не сокращает время эндопротезирования по сравнению с традиционными методиками [16]. Похожие результаты получили в своих исследованиях Nunley [26] и Voleti [35]. Однако Bali с соавторами показали, что ППН позволяет значительно сократить время оперативного вмешательства по сравнению с традиционным эндопротезированием коленного сустава [8].
Заключение. Несмотря на наличие многочисленных исследований в данной области, до сих пор единого мнения относительно ППН у большинства хирургов нет. Имеющиеся неудовлетворительные результаты применения индивидуальных направителей, по нашему мнению, были связаны с недостаточно тщательным проведением предоперационного планирования, отсутствием опыта и навыков компьютерного моделирования у хирургов, созданием ППН лицами, не имеющими опыта выполнения эндопротезирования коленного сустава, использованием не предназначенного для создания ППН программного обеспечения.
В приведенном анализе современных литературных источников нами не было обнаружено данных по оценке экономической эффективности использования индивидуальных направителей, что, по нашему мнению, необходимо учитывать при оценке целесообразности их применения при эндопротезировании коленного сустава.
Обобщая результаты имеющихся исследований, мы считаем, что показания к применению ППН могут быть следующие: наличие деформации бедренной или большеберцовой кости, когда применение интрамедуллярных направителей затруднено, контрактуры коленного сустава, когда технически трудно выполнить эндопротезирование с использованием компьютерной навигации, наличие в анамнезе воспалительного процесса в бедренной кости, эндопротеза тазобедренного сустава ипсилатеральной стороны, когда необходимо избежать вскрытие костномозгового канала.
Библиографическая ссылка
Карякин Н.Н., Горбатов Р.О. ПРЕЦИЗИОННЫЕ ПЕРСОНИФИЦИРОВАННЫЕ НАПРАВИТЕЛИ ДЛЯ ЭНДОПРОТЕЗИРОВАНИЯ КОЛЕННОГО СУСТАВА // Современные проблемы науки и образования. 2016. № 5. ;URL: https://science-education.ru/ru/article/view?id=25134 (дата обращения: 15.05.2026).



