Бронхиальная астма – это заболевание, характеризующееся хроническим воспалением дыхательных путей, определяющееся по наличию в анамнезе симптомов со стороны органов дыхания, таких как свистящие хрипы, одышка, чувство заложенности в груди, навязчивый кашель, вариабельное ограничение скорости воздушного потока на выдохе [1].
Бронхиальная астма (БА) является серьезной глобальной проблемой в области здоровья, затрагивающей все возрастные группы. Во многих странах распространенность БА возрастает, особенно среди детей [1]. Бронхиальная астма – одно из наиболее распространенных заболеваний, в мире около 235 млн человек страдают этим заболеванием – от 1 до 18% населения в различных странах [1; 6]. В России БА страдают более 350 тысяч детей и подростков [6], в структуре аллергических заболеваний её доля составляет 30-40%. Более чем в 70% случаев бронхиальной астме предшествует развитие аллергического ринита [6].
Основными принципами лечения бронхиальной астмы являются:
• устранение контакта с аллергеном;
• фармакотерапия;
• анти Ig E – терапия;
• аллергенспецифическая иммунотерапия (АСИТ) [5; 6].
АСИТ – это метод лечения аллергических заболеваний, воздействующий на все звенья аллергического процесса, в его основе лежит введение в организм пациента возрастающих доз причиннозначимого аллергена [2; 3].
Аллергенспецифическое лечение имеет принципиальные преимущества перед всеми другими методами терапии аллергии, так как является патогенетическим видом лечения, видоизменяет характер реагирования организма на аллерген [2; 4; 8].
Клиническая эффективность АСИТ выражается в торможении внешних проявлений заболевания и уменьшении потребности в лекарственных препаратах. Снижение специфической и неспецифической тканевой гиперреактивности и противовоспалительное действие после завершения АСИТ сохраняются на протяжении длительного (многолетнего) периода наблюдений [2; 5; 7].
Отмечено, что под действием АСИТ происходит перестройка характера иммунного ответа на действие аллергена, состоящая в образовании так называемых блокирующих антител, принадлежащих к IgG и лишенных способности сенсибилизировать ткани, но обладающих аллергенсвязывающей активностью. За счет этого они уменьшают вероятность взаимодействия аллергена с IgE-антителами [2]. В последнее время появились сведения о том, что и образование анти-IgE-антител может иметь значение в лечебном действии АСИТ [10].
Вероятнее всего, образование IgG-антител, анти-IgE-антител и угнетение продукции IgE-антител совместно опосредуют механизм АСИТ [10]. В последние годы было показано, что клинически эффективная иммунотерапия характеризуется угнетением вовлечения в аллергическую реакцию клеток, опосредующих эффекторную стадию аллергии. Так, в результате АСИТ в тканях уменьшается содержание тучных клеток, накопление эозинофилов, нейтрофилов, тормозится высвобождение медиаторов из клеток-мишеней аллергии (тучных клеток, базофилов) при стимуляции их специфическим аллергеном или неспецифическими активаторами [9; 10]. Под действием АСИТ происходит смещение профиля лимфоцитов от Тh2-клеток в сторону Тh1-клеток [2]. Описанные механизмы могут служить объяснением влияния АСИТ не только на раннюю, но и на позднюю фазу аллергического процесса [2; 7].
Итак, АСИТ, в отличие от известных фармакологических препаратов, обладает терапевтическим действием, которое распространяется на все этапы аллергического процесса. Кроме того, у АСИТ есть принципиальное отличие от фармакотерапии: речь идет о длительном сохранении лечебного эффекта после завершения курсов лечения [2].
Цель исследования
Целью исследования являлась оценка эффективности аллергенспецифической иммунотерапии бронхиальной астмы.
Задачи исследования.
- Оценка состояния больных, страдающих бронхиальной астмой в сочетании с аллергическим ринитом, до начала проведения АСИТ.
- Оценка эффективности АСИТ в процессе лечения.
- Сравнительная характеристика течения бронхиальной астмы в сочетании с аллергическим ринитом у детей, получающих АСИТ, и детей, которым АСИТ не проводят.
Материал и методы исследования
В исследование были включены 2 группы детей, страдающих бронхиальной астмой легкой и среднетяжелой степени в сочетании с аллергическим ринитом, которые получали лечение в течение 2-3 лет.
1 группа – дети, получающие АСИТ и базисную терапию.
2 группа (контрольная) – дети, получающие только медикаментозную базисную терапию.
1 и 2 группы включали по 51 пациенту, в каждой из них было 54,9% мальчиков и 45,1% девочек.
Критериями включения в исследуемые группы являлись:
• бронхиальная астма легкой интермиттирующей, легкой и среднетяжелой персистирующей формы в сочетании с аллергическим ринитом;
• возраст от 5 до 18 лет;
• отсутствие тяжелых сопутствующих заболеваний;
• получение информированного согласия на участие в исследовании.
Для статистической обработки данных исследования использован параметрический метод с определением t-критерия.
Результаты исследования
У детей 1-й и 2-й групп в большинстве случаев (47,4 и 42,9% соответственно) была выявлена бытовая сенсибилизация, а также пыльцевая (21,7 и 26,1%), эпидермальная (7,3 и 12,3%), пищевая (3,6 и 5,1%), поливалентная (20 и 13,6%) виды гиперчувствительности.
Для проведения работы были выделены критерии, по которым оценивалось состояние детей до начала АСИТ и в процессе её проведения:
• частота обострений в год;
• потребность в симптоматической терапии (короткодействующие β2-агонисты, деконгестанты);
• пиковая скорость выдоха (ПСВ);
• АСТ-тест (тест по контролю над астмой);
• частота симптомов ринита.
Среднее число обострений заболевания в 1-й и 2-й группах до начала терапии составляло 5,53 и 5,78 (р>0,05), через 1 год после начала лечения – 2,18 и 4,06 (р<0,01), через 2 года – 1,61 и 3,0 (р<0,01) соответственно.
Средняя ежемесячная потребность в β2-агонистах короткого действия в 1-й и 2-й группах до начала лечения составляла 3,06 и 3,41 (р>0,05), через 1 год после начала лечения – 1,14 и 2,88 (р<0,01), через 2 года – 0,29 и 2,12 (р<0,01) соответственно. До начала АСИТ детей с отсутствием потребности в β2-агонистах не было, через 2 года 37 детей (73%) не нуждались в их использовании.
Средняя еженедельная потребность в деконгестантах в исследуемых группах до начала лечения составляла 3,53 и 3,53, через 1 год после начала лечения – 0,53 и 1,69 (р<0,01), через 2 года – 0,04 и 1,37 (р<0,01) соответственно. Через 2 года 96% детей, получавших АСИТ, не нуждались в данном виде симптоматической терапии.
Средний показатель ПСВ в 1-й группе увеличивается с 83,8 до 88,53% (р<0,01), во 2-й группе – с 81,86 до 83,71% (р<0,01).
АСТ-тест содержит 5 вопросов и позволяет на основании количества набранных баллов судить об уровне контроля БА у данного пациента. Максимальное количество баллов (25) означает, что астма полностью контролируется, 20-24 балла – частично контролируется, менее 20 – контролировать не удается.
Результаты АСТ-теста показывают разной степени положительную динамику в обеих группах.
Из таблицы 1 видно, что в 1-й группе дети, испытывающие затруднение дыхания 3-6 раз в неделю, отсутствуют через 2 года после проведения АСИТ, а во 2-й группе на фоне базисной терапии проблема сохраняется у 8 пациентов. Потребность в β2-агонистах уменьшилась в 1 группе в 6 раз, что более значительно, чем во 2 группе, где уменьшилась менее чем на треть. Аналогичная картина наблюдается в отношении ограничения жизнедеятельности: число детей, испытывающих ограничение жизнедеятельности, в 1-й группе уменьшилось значительнее, чем во 2-й группе. В 1-й группе на фоне АСИТ-терапии количество детей, ни разу не просыпающихся ночью, увеличилось на 1/3. Во 2-й группе аналогичная подгруппа детей остается примерно на том же уровне. В 1-й группе 96% детей считают, что они хорошо или полностью контролируют астму. Во 2-й группе существенной динамики контроля заболевания нет.
Таблица 1
Результаты АСТ-теста
|
1 группа (чел.) |
2 группа (чел.) |
||||||
|
Вопросы АСТ-теста (за последние 4 недели) |
До начала терапии |
Через 1 год терапии |
Через 2 года терапии |
До начала терапии |
Через 1 год терапии |
Через 2 года терапии |
|
|
Ограничение жизнедеятельности |
Никогда |
8 |
11 |
13 |
7 |
9 |
10 |
|
Редко |
27 |
29 |
34 |
27 |
30 |
31 |
|
|
Иногда |
13 |
10 |
4 |
13 |
10 |
9 |
|
|
Очень часто |
3 |
1 |
0 |
4 |
2 |
1 |
|
|
Затруднённое дыхание |
< 1 раза в неделю |
15 |
17 |
20 |
12 |
13 |
15 |
|
1-2 раза в неделю |
28 |
30 |
31 |
26 |
27 |
28 |
|
|
3-6 раз в неделю |
8 |
4 |
0 |
13 |
11 |
8 |
|
|
Использование быстродействующего ингалятора |
< 1 раза в неделю |
12 |
15 |
18 |
11 |
12 |
12 |
|
1 раз в неделю или реже |
26 |
29 |
31 |
24 |
26 |
29 |
|
|
2-3 раза в неделю |
10 |
7 |
2 |
12 |
11 |
9 |
|
|
1-2 раза в день |
3 |
0 |
0 |
4 |
2 |
1 |
|
|
Ночные пробуждения из-за астмы |
Ни разу |
22 |
27 |
31 |
18 |
19 |
21 |
|
1-2 раза |
25 |
23 |
20 |
25 |
28 |
27 |
|
|
1 раз в неделю |
4 |
1 |
0 |
6 |
4 |
3 |
|
|
Оценка контроля астмы |
Полный контроль |
15 |
18 |
22 |
14 |
15 |
17 |
|
Хорошо удаётся контролировать |
23 |
26 |
27 |
25 |
26 |
25 |
|
|
В некоторой степени удаётся контролировать |
13 |
7 |
2 |
12 |
10 |
9 |
|
Рисунок наглядно демонстрирует снижение распространенности симптомов ринита на фоне лечения. АСИТ значительно повлияла на симптомы аллергического ринита. Через 2 года жалобы на заложенность носа, зуд, чихание уменьшились в 2 раза, ринорея почти в 3 раза, а нарушение обоняния в 5 раз. Во 2-й группе на фоне базисной терапии произошло менее значительное угасание симптомов: заложенности носа – на 10%, зуда на – 10%, чихания – на 12%, ринореи – на 14%, нарушения обоняния – на 4%.
Общий обзор динамики симптомов бронхиальной астмы и аллергического ринита у детей основной и контрольной групп представлен в таблице 2.
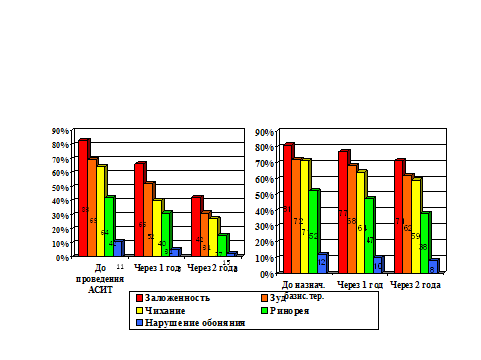
Частота симптомов ринита
Таблица 2
Общий обзор динамики симптомов
|
Показатели |
1-я группа |
2-я группа |
||||
|
До начала терапии |
Через 1 год терапии |
Через 2 года терапии |
До начала терапии |
Через 1 год терапии |
Через 2 года терапии |
|
|
Средняя частота обострений в год |
5,53 |
2,18 |
1,61 |
5,78 |
4,06 |
3,0 |
|
Средняя потребность в симптоматической терапии: β2-агонисты (в мес.) деконгестанты (в нед.) |
3,06 3,53 |
1,14 0,53 |
0,29 0,04 |
3,41 3,53 |
2,88 1,69 |
2,12 1,37 |
|
Среднее значение ПСВ (%) |
83,8 |
86,11 |
88,53 |
81,86 |
83,0 |
83,71 |
|
Средний общий балл АСТ-теста |
20,67 |
21,11 |
22,78 |
20,29 |
20,71 |
21,04 |
|
Частота симптомов ринита (%): Заложенность носа Зуд Чихание Ринорея Нарушение обоняния |
83 69 64 42 11 |
66 52 40 31 5 |
42 31 27 15 2 |
81 72 71 52 12 |
77 68 64 47 10 |
71 62 59 38 8 |
Выводы
В группе детей, получающих АСИТ, через 2 года наблюдения частота обострений уменьшилась в 3,4 раза (р<0,01), потребность в симптоматической терапии, β2-агонистах и деконгестантах уменьшилась в 10,6 (р<0,01) и 88,3 (р<0,01) раза соответственно; ПСВ увеличилась на 4,7%; общий балл АСТ-теста увеличился на 2,11 (р<0,01); частота встречаемости симптомов ринита уменьшилась в 2-5,5 раза.
В группе детей, получающих базисную терапию, через 2 года наблюдения частота обострений уменьшилась в 1,9 (р<0,01) раза; потребность в симптоматической терапии, β2-агонистах и деконгестантах, уменьшилась в 1,4 (р<0,01) и 2,8 (р<0,01) раза соответственно; ПСВ увеличилась на 1,85%; общий балл АСТ-теста увеличился на 0,75 (р<0,01), что достоверно ниже (р<0,01), чем в 1-й группе; частота встречаемости симптомов ринита уменьшилась в 1,1-1,5 раза.
Таким образом, аллергенспецифическая иммунотерапия (АСИТ) является основой патогенетической терапии и приводит к значительному облегчению течения бронхиальной астмы и аллергического ринита у детей. Результаты исследования показали большую эффективность АСИТ по сравнению с медикаментозной противовоспалительной терапией.
Библиографическая ссылка
Краснов М.В., Боровкова М.Г., Николаева Л.А., Сергеева О.Н. ПАТОГЕНЕТИЧЕСКАЯ ТЕРАПИЯ БРОНХИАЛЬНОЙ АСТМЫ У ДЕТЕЙ // Современные проблемы науки и образования. 2016. № 3. ;URL: https://science-education.ru/ru/article/view?id=24842 (дата обращения: 09.04.2026).



