Бремя травматизма в России, как и в странах Европы и Америки, остается высоким, из-за общей интенсификации жизнедеятельности населения [1]. При этом доля травматизма, связанного с употреблением алкоголя, составляет от 20 до 60 %. Алкогольное потребление видоизменяет динамику системного патологического процесса при травматической болезни, затрудняет диагностику, отрицательно влияет на процессы репарации и может приводить к смерти, напрямую не связанной с травматическим повреждением [2]. В этой ситуации возникает настоятельная необходимость разработки алгоритмов лечебной и восстановительной тактики при травме, ассоциированной с алкогольным потреблением.
Ранее нами было показано, что удлинение сроков пребывания в стационаре пострадавших с сочетанной черепно-мозговой и скелетной травмой на фоне алкоголизации связано с подавлением репаративных процессов вследствие дефицита иммунных механизмов в сочетании с окислительно-метаболическими нарушениями, активацией про-воспалительных цитокинов и апоптоза иммунокомпетентных клеток. Выявлено, что частота лёгочных осложнений напрямую коррелирует с предшествующей алкоголизацией и характером адаптивного ответа системы иммунологической защиты, что также способствует удлинению восстановительного периода после травмы. Немаловажную роль в течении травматической болезни играют адаптивные системные реакции микроциркуляторного русла и эндотелия, которые существенно искажаются вследствие предшествующего алкогольного потребления [4, 5, 6, 7].
Сравнительный анализ клинического течения и диагностический мониторинг на всех этапах ведения травмированного пациента, включающий анализ нейрогуморальных сдвигов, эндотелиальных и микроциркуляторных функций, позволил описать патопластические механизмы и обосновать концепцию травматически обусловленной микроциркуляторной и эндотелиальной дисфункции, которая является причиной кризисного состояния и возможного летального исхода при развитии травматической болезни, которая является причиной неблагоприятных исходов или затяжного процесса восстановления [10, 11, 15]. На основе данной концепции и результатов исследования патогенетических механизмов сочетанной черепно-мозговой и скелетной травмы на фоне алкоголизации обоснованы алгоритмы лечебной тактики. Общий алгоритм специализированной экстренной помощи выглядит следующим образом (рисунок).
Диагностика алкогольного потребления проводится на самом раннем этапе, причем по возможности с учетом всех отягчающих факторов: микроциркуляторной и эндотелиальной дисфункции, алкоголь-обусловленной органопатологии: возможных сердечных и печеночных проблем, а также риска психотических осложнений на фоне алкогольного абстинентного синдрома [13, 14]. Следует помнить, что при алкоголизме может иметь место толерантность к целому ряду препаратов в результате ингибирования этанолом некоторых ферментов, и терапевтические дозы могут оказаться недостаточно эффективными; могут развиваться гепатотоксические реакции, например, на парацетамол, остеомаляция, склонность к судорогам в результате дезактивации витамина D метаболитами этанола. Это только малая часть эффектов хронической алкоголизации, которые необходимо учитывать у больного алкоголизмом, получившего травму.
Активная противоалкогольная терапия в травматологическом стационаре, как правило, не проводится, однако купирование алкогольной интоксикации и алкогольного абстинентного синдрома (ААС) и устранение связанных с ними психосоматических расстройств зачастую становятся необходимыми условиями выживания пациента.
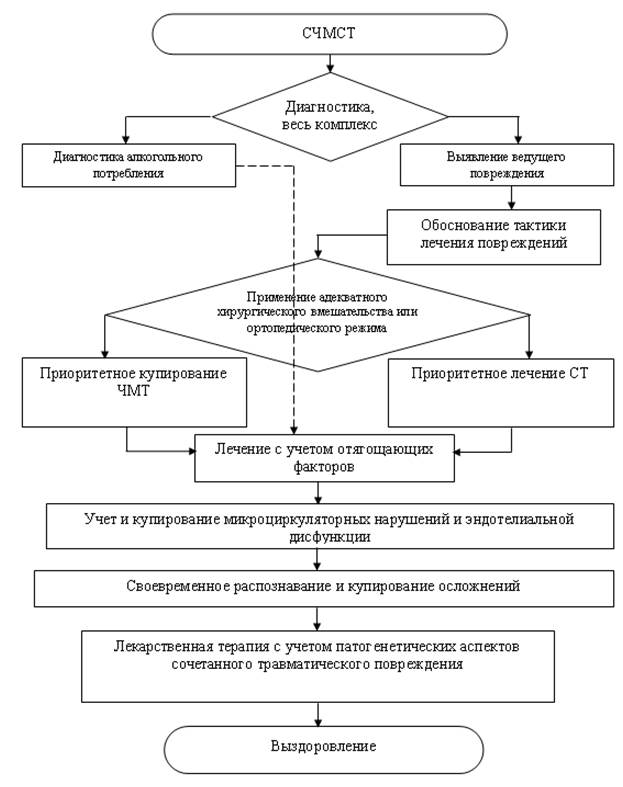
Алгоритм лечения сочетанной черепно-мозговой и скелетной травмы (СЧМСТ) с учетом алкогольного потребления
Нарушения, помимо травматического процесса, имеющиеся в этот период, представляют собой результат системных посталкогольных метаболических изменений, при которых возникают расстройства функции мозга. Функциональные изменения ЦНС в виде преобладания явления раздражения в головном мозгу являются следствием тканевой гипоксии и подтверждаются особенностями динамики вегетативных и гемодинамических показателей, в том числе микроциркуляции, свидетельствующих о снижении адаптивных возможностей и резервов основных регуляторных систем. Как было показано выше, это сочетается со снижением тканевой перфузии в результате травматогенных микроциркуляторных нарушений, обусловленных уменьшением функциональных резервов местной регуляции микрогемоперфузии и угнетением механизмов пассивной регуляции, вовлечением в системный процесс сосудистых и клеточных механизмов гемостаза, связанных с травматогенной эндотелиальной дисфункцией. Все это происходит на фоне усиления окислительных процессов, повышенной генерации свободных радикалов, раннего истощения антиокислительного резерва у больных с тяжелыми травмами и «депрессии» антиоксидантного статуса. Как выявлено, эти процессы при сопутствующей алкоголизации имеют существенно более выраженный характер, поскольку накладываются на уже измененный в результате алкоголизации структурно-метаболический фон.
Структурно-метаболические нарушения, свойственные хроническому алкогольному потреблению, определяют более быстрое прогрессирование гипоксии головного мозга, сердца и печени при сопутствующей травме. Ослабление функции печени приводит к накоплению вторичных эндогенных токсинов, что усиливает системные нарушения. ААС зачастую создает прямую угрозу жизни пациента, при этом известные методы его купирования на фоне травмы являются неэффективными. Часто это становится очевидным только при развитии серьезных осложнений и прямой опасности для жизни. Вместе с тем по внешнему виду больного не всегда можно определить, что в данном случае купирование ААС будет представлять большие трудности. Пациенты часто бывают с сопутствующей терапевтической патологией или с последствиями противоалкогольного лечения (тетурам и др.), на фоне изменения энергетического обмена вследствие приема лекарственных препаратов, например, гипотензивных или сердечных средств, или воздействия экзогенных вредностей. Помимо создания ксенобиотической нагрузки, обусловленной злоупотреблением алкоголем, медикаменты зачастую прямо влияют на энергетический обмен, ингибируя те или иные его звенья. Наиболее часто встречающиеся побочные эффекты – это нарушение деградации углеводов, липидов или белков, угнетение дегидрогеназ и трансаминаз, блокирование либо шунтирование транспорта электронов в дыхательной цепи, разобщение окислительного фосфорилирования [6,16]. Кроме того, оказывая влияние на функциональное состояние систем организма (основной и побочные фармакологические эффекты), лекарственные препараты либо активируют их, что отвлекает энергию на обеспечение гиперактивности, либо угнетают, что создает помимо деэнергизации, десинхроноз между системами организма и дополнительную энергетическую нагрузку на его восстановление. Это особенно важно для хронических алкоголиков, энергетические ресурсы которых на исходе. Довольно часто встречаются случаи общего снижения резистентности таких больных при нарастании объема медикаментозной помощи. Этот процесс мы наблюдали при сопутствующей нозокомиальной пневмонии у травмированных алкоголиков [7]. Фармакологическая регуляция энергетического обмена жизненно важна для пациентов, находящихся в критическом состоянии.
В этой ситуации основной задачей интенсивной терапии становится нормализация гомеостаза и энергетического обмена, а также восстановление функций систем организма, при этом медикаментозная нагрузка должна быть сведена к минимуму.
Коррекция нарушений микроциркуляции должна касаться преимущественно воздействия на центральную гемодинамику и осуществляться с помощью препаратов гемодинамического действия с положительным инотропным влиянием, например, введение коллоидных плазмозаменителей из группы гидроксиэтилкрахмала (ГЭК) в сочетании с дофамином, однако при остаточных явлениях алкогольной интоксикации, особенно при угрозе алкогольного делирия, введение дофамина нежелательно, и следует ограничиться введением дезагрегантов.
Нейропротекция приобретает особую важность при сочетанной черепно-мозговой и скелетной травме, осложненной алкоголизмом. Защита нейронов от ишемии, нейротоксичных субстанций (цитокины, свободные радикалы, продукты распада крови, молекулы средней массы и т.д.), от механического сдавления тканей мозга вследствие отека, связанного не только с травмой черепа, но с метаболическими нарушениями вследствие распада продуктов метаболизма этанола и гидроионными нарушениями имеет первостепенное значение.
При травматической болезни в условиях микроциркуляторного и иммунного дистресса, универсальной эндотелиальной дисфункции, окислительного стресса и энергодефицита закономерно возникает вопрос о качественном составе инфузионной терапии – выборе соответственно клинической задаче оптимального сочетания и соотношения различных инфузионных сред. Помимо препаратов ГЭК, которые обладают доказанным эндотелийпротекторным эффектом, в комплексе интенсивной терапии травматической болезни на фоне алкоголизации для стартовой болюсной инфузионной терапии необходимо использовать субстратный антигипоксант реамберин или мафусол [8].
При лечении острой травмы головного мозга могут быть использованы препараты лития. Одним из наиболее важных нейропротекторных свойств лития является антиапоптозное действие [9]. Последние исследования в естественных и в лабораторных условиях показывают, что литий замедляет этанол-индуцированный нейроапоптоз, поскольку является ингибитором гликоген-синтазы-киназы-3 (GSK3), которая недавно была идентифицирована в качестве медиатора нейротоксичности этанола. Нейропротекция лития обусловлена торможением GSK3. Кроме того, литий влияет на некоторые другие сигнальные белки и пути регуляции восстановления и дифференцировки нейронов [9].
Принципиально важно в условиях иммунодефицита использовать заместительную иммунокоррекцию, особенно у пациентов с алкогольным анамнезом: 1) донорскими иммуноглобулинами для внутривенного введения (ИГВВ), преимущественно препаратом III поколения биовен моно (иммуноглобулин человека нормальный жидкий), донорский иммуноглобулин для внутримышечного введения; 2) рекомбинантными цитокинами rIL2 (биолейкин), rIFNa2b (лаферобион). Не менее эффективно применение других иммуноориентированных препаратов (полиоксидоний, иммунофан, индуктор интерферона – циклоферон), а также лекарственных средств, обладающих антикининовой и неспецифической антицитокиновой активностью, – ингибиторов протеолиза (апротинин), ферментных препаратов, улучшающих доставку кислорода и антибиотиков в очаги инфекции и деструкции. При выборе препаратов, их доз и продолжительности введения следует ориентироваться на стадии иммунного дистресса.
Тяжелейшим синдромом является также и гипоальбуминемия, отражающая снижение белоксинтетической функции печени. Выброс медиаторов воспаления требует огромного числа разнообразных белков. Формируется скрытая системная белковая дистрофия. Альбумин принимает участие в формировании одной из детоксицирующих систем организма, он является регулятором обмена липопротеинов крови. Страдает также транспортная функция альбумина как переносчика многих гормонов, витаминов, микроэлементов. Граница его ниже 35 г/л оказывается абсолютно критической. Гиперактивация катаболизма приводит к субстратному истощению, несмотря на наличие запаса субстратов. Одновременно существует необходимость метаболической детоксикации ацетальдегида.
При травме алкоголезависимых лиц для коррекции энергетического обмена предпочтение следует отдавать аминокислотам как энергетическому субстрату, который непосредственно оказывается вовлеченным в цикл трикарбоновых кислот.
Таким образом, терапевтическая тактика при травме на фоне хронической алкогольной интоксикации должна учитывать наличие дополнительных альтерирующих факторов с целью своевременной и эффективной коррекции их повреждающего действия.
Библиографическая ссылка
Фирсов С.А., Матвеев Р.П., Федотов Е.А. ОСНОВНЫЕ ПРИНЦИПЫ ПАТОГЕНЕТИЧЕСКОЙ ТЕРАПИИ ПРИ ТРАВМАТИЧЕСКОЙ БОЛЕЗНИ, АССОЦИИРОВАННОЙ С АЛКОГОЛЬНЫМ ПОТРЕБЛЕНИЕМ // Современные проблемы науки и образования. 2016. № 3. ;URL: https://science-education.ru/ru/article/view?id=24478 (дата обращения: 17.05.2026).
DOI: https://doi.org/10.17513/spno.24478



