Послеоперационное спайкообразование в ряде случаев выходит за рамки физиологической нормы и приобретает патологические проявления, зачастую порождающие ряд проблем, особенно выраженных в хирургической гинекологии. По данным экспериментальных и клинических наблюдений, после акушерских и гинекологических полостных операций спаечный процесс в полости живота и малого таза наблюдается в 60 –100 % случаев [2,4]. Гинекологические операции сопровождаются наибольшим риском спайкообразования, в том числе вне пределов малого таза [5].
Цель исследования
Дать характеристику спаечного процесса в брюшной полости и его клинических проявлений у женщин, перенесших удаление матки без придатков, и женщин, перенесших удаление матки с придатками.
Материал и методы исследования
В клиническом исследовании приняли участие 160 женщин 30–55лет, разделенных на 2 группы:
1 группа – пациентки, перенесшие лапаротомию, гистерэктомию без придатков (80);
2 группа – пациентки, перенесшие лапаротомию, гистерэктомию с придатками (80).
Критериями включения пациенток в исследование были сохраненная менструальная функция, необходимость произведения гистерэктомии по поводу невоспалительного заболевания гениталий, 1–2 степень чистоты мазка на флору из влагалища на момент операции, неосложненное течение операции и послеоперационного периода. Критериями исключения из исследования были наличие клинических проявлений спаечной болезни или выраженный спаечный процесс, верифицированный интраоперационно, операции на органах брюшной полости, в том числе в связи с воспалительными заболеваниями, перитонитом в анамнезе, воспалительная этиология заболевания пациентки (гистерэктомии по поводу тубоовариальных образований), указание на гормональную недостаточность, эндокринное бесплодие, синдром преждевременного истощения яичников в анамнезе, специфическая инфекция в анамнезе, острая специфическая или неспецифическая инфекция генитального тракта на момент операции, состояние в менопаузе. Все пациентки относились к репродуктивному или перименопаузальному возрасту. В 1 группе средний возраст на момент операции составил 43,5±5,2 года. Средний возраст во 2 группе составил 47,4±3,4 года. Менструальная функция до операции была сохранена у 100 % исследуемых; в большинстве случаев изменена в виде той или иной формы геморрагического синдрома.
Сопутствующая экстрагенитальная патология была достаточно вариабельной в обеих группах. Наиболее часто встречались сердечно-сосудистые заболевания, хроническая анемия. Более чем в 80 % случаев показанием к операции были миома матки или аденомиоз, реже кисты яичников, патология эндометрия и другое. Технически под эндотрахеальным наркозом женщинам обеих групп производилась лапаротомия, классическая надвлагалищная ампутация или экстирпация матки без или с придатками с перитонизацией листками пузырно-маточной, прямокишечной складок и широкой связкой. В послеоперационном периоде в обеих группах проводилось сравнительное исследование, включающее:
- осмотр, бимануальное влагалищное исследование (при повторной явке пациенток через 30–45 дней после выписки из стационара);
- лабораторное исследование концентрации фибриногена крови по методу Клауса (лабораторная норма до 4 г\л) после внутривенного забора натощак на 1–3 сутки после операции (в условиях клинической лаборатории ГУЗ «ВОКБ №1»);
- определение уровня эстрадиола, фолликулостимулирующего гормона в крови после операции. Кровь для исследования содержания гормонов брали из локтевой вены натощак на 6–7-е сутки после операции, чтобы исключить влияние наркоза, операционного стресса, инфузионной и обезболивающей терапии;
- ультразвуковое исследование состояния органов малого таза через 30–60 дней после операции при помощи вагинального датчика аппаратов Siemens «Antares» или Voluson 730. Исследование проводили в первую половину дня, после опорожнения кишечника.
Также, особенности спайкообразования в зависимости от объема операции оценивались нами при проведении повторных лапаротомических или лапароскопических вмешательств 22 пациенткам после субтотальных гистерэктомий из лапаротомического доступа, произведенных 1 мес. – 16 лет назад. В 12 случаях произведены повторные оперативные вмешательства у пациенток после гистерэктомии без придатков в анамнезе (5 лапароскопических и 7 лапаротомических операции) по поводу новообразований яичников. В 10 случаях наблюдения произведены повторные оперативные вмешательства у пациенток после гистерэктомии с придатками в анамнезе (3 лапароскопических операции по поводу спаечного процесса в малом тазу, хронической тазовой боли и 7 лапаротомических операции по поводу заболевания культи шейки матки, послеоперационного пролапса гениталий). Интраоперационно производилась видео и\или фотофиксация цифровой системой камеры эндовидеохирургического копмлекса CarlStorz (telecamSLII) или фотокамерой SonyCyber-shot 8.1 Mgp с обработкой в программах Pinnacle, Iphoto. Оценка спаечного процесса после ранее выполненных оперативных вмешательствах нами производилась в соответствии с принятой терминологией и классификацией внутрибрюшинных адгезий [3], в обеих группах производилось сравнение макроскопических форм и типов спаек, определялась степень интенсивности спайкообразования (по Калугину А. С., 1976). Статистический анализ нами проводился с помощью программы MicrosoftEХСEL для Windows.
Результаты исследования
Жалобы, связанные с перенесенной операцией, предъявляли 86 % женщин 1 группы и 95 % женщин 2 группы. В обеих группах самыми частыми жалобами были вегетативные жалобы: приливы, сердцебиения и потливость. При анализе послеоперационных жалоб обращает на себя значительное преобладание количества обследуемых 2 группы с жалобами на тревогу, депрессивные расстройства и снижение либидо – 32.5 % против 20 % случаев в 1 группе. Во 2 группе обследуемых жалобы на постоянные тянущие боли в нижних отделах живота, в пояснице, в области промежности, после операции отмечали 27.5 % обследуемых, периодический дискомфорт в животе и проекции рубца отмечали более 37 % женщин. Для сравнения 33 % пациенток 1 группы предъявляли жалобы на периодические тянущие ощущения, болезненность в нижних отделах живота, в пояснице, в области промежности в основном при физической активности, что носило скорее характер дискомфорта, нежели боли. Постоянные боли тянущего характера в области нижних отделов живота, пупка, пояснице или промежности беспокоили лишь 11 % обследуемых 1 группы. Метеоризм, дискомфорт в кишечнике, проблемы со стулом, урогенитальные расстройства после операции отмечали практически в одинаковой степени пациентки обеих групп. При проведении динамического влагалищного бимануального исследования у пациенток обеих групп через 30–45 после выписки обращает на себя внимание более высокая частота выявления ограничения подвижности культи, тяжистости в проекции придатков, инфильтрированности и уплотнения тканей (в 37.5 % случаев в 1 группе и в 27.5 % случаев наблюдения во 2 группе), жалобы на болезненность при исследовании также чаще предъявляли пациентки 2 группы. Бимануальная идентификация объемных образований небольших размеров в малом тазу имеет чуть большую частоту в 1 группе обследуемых – 7.5 % случаев против 5 % во 2 группе, что по нашим наблюдениям связано с повышенной частотой образования ретенционных рассасывающихся кист в оставленных яичниках – как адаптивная реакция после операционной травмы и возможной транзиторной гипоэстрогении в указанных случаях.
При лабораторном мониторинге концентрации эстрадиола крови, как наиболее активного эстрогена, содержание его в послеоперационном периоде во 2 группе во всех случаях составило менее 82 пг\мл (минимальная концентрация 13 пг\мл – максимальная концентрация 60 пг\мл, в среднем 27.75 пг\мл), что соответствует и даже ниже содержания гормона на фоне естественной менопаузы. В 1-й группе концентрация эстрадиола составила в среднем 128.88 пг\мл. Нормоэстрогения или незначительное снижение периферической концентрации данного гормона после операции наблюдалось в 86.2 % случаев (таблица).
Концентрация эстрадиола крови у пациенток после гистерэктомии без и с придатками (n – количество пациенток)
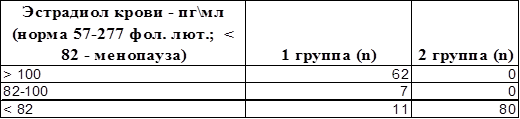
Уровень Фолликулостимулирующего гормона практически не изменился или был повышен незначительно в 1 группе обследуемых (параметры концентрации от 5 – до 36 МЕ\л), а во 2 группе уровень ФСГ значительно повышался (55.5–74.5 МЕ\л) по механизму обратной связи, что соотносится с имеющимися литературными данными.
Показатель содержания в крови фибриногена крови – предшественника фибрина, основного «cклеивающего» вещества послеоперационных сращений, был в пределах нормы у 80 % женщин 1 группы и 43.75 % – 2 группы, в остальных случаях отмечена гиперфибриногенемия. Во всех случаях повышение концентрации фибриногена во 1 группе носило умеренный характер (фибриноген от 4 до 5 г/л), во 2 группе – 33.75 % случаев умеренной гиперфибриногенемии, у 22.5 % обследуемых уровень фибриногена был выше 5 г/л.
В обследуемых группах при ультразвуковом сканировании в послеоперационном периоде на 30-й – 45-й день после выписки из стационара нормальная эхографическая картина, соответствующая состоянию после проведенной операции, наблюдалась у 81.25 % женщин 1 группы и у 72.5 % женщин 2 группы. Атипичное расположение, смещение культи шейки матки / влагалища, изменение положения тазовых органов чаще выявлялись у пациенток 2 группы (18.75 % против 11.25 % в 1 группе), как и идентифицированные сращения в виде линейных структур неправильной формы (в 10 % случаев во 2 группе и в 3.75 % случаев в 1 группе). Объемные образования, как правило, в виде ретенционных кист небольших размеров (до 3.5-4 см) или серозоцеле чаще выявлялись у пациенток 1 группы (в 7.5 % случаев, во 2 группе – в 2.5 % случаев соответственно). Необычная фиксация, изменение контуров, сращения с брюшной стенкой мочевого пузыря визуализировано при ультразвуковом исследовании у 3.75 % пациенток 2 группы. В 1 группе подобных нарушений не встречалось. В структуре спаек в обеих группах преобладали преимущественно сальниковые сращения неплотной структуры с прослойками жировой ткани. Припаивание к париетальной брюшине переднебоковой стенке живота в проекции старого лапаротомного рубца во 2 группе во всех случаях зафиксировано по всему длиннику рубца, в 1 группе локализовано преимущественно в его средней трети. В половине случаев во 2 группе отмечено припаивание петли кишечника к старому рубцу, в 1 группе подобных наблюдений не было. Анализируя особенности спайкообразования в 1 группе, можно отметить выявленные рыхлые спайки полюсов объемного образования с париетальной брюшиной, большим сальником (более чем в 90 % случаев); реже с петлями кишечника (в 50 % случаев). В 16 % случаев в 1 группе выявлено образование серозоцеле, чего не встретилось у пациенток после гистерэктомии с придатками. Во 2 группе чаще выявлялись сальниковые, пленчатые плоскостные спайки с тазовой брюшиной, мочевым пузырем, петлями тонкого кишечника, сигмовидной кишкой, задней поверхностью культи, отмечена склонность к образованию спаечных конгламератов прядей большого сальника с париетальной брюшиной в проекции перитонизации культи, близ культей связочного аппарата, в 7 случаях с вовлечением петель кишечника. Структурно отмечена уплотненность тканей, затрудненная их дифференцировка, во всех случаях затрудненный доступ к культе. В обеих группах в углублении за культей шейки матки обнаружены спайки: сальниковые, пленчатые рыхлые спайки у пациенток 1 группы, сальниковые, тракционные пленчатые плоскостные спайки с тазовой париетальной брюшиной, петлями тонкого кишечника, сигмовидной кишкой, задней поверхностью культи шейки матки у пациенток 2 группы. Также визуализированы рыхлые пленчатые, бессосудистые спайки по боковым карманам брюшной полости у пациенток после гистерэктомии без придатков, подобные же спайки с дополнительным вовлечением и тракцией петель кишечника у пациенток 2 группы. Единичные межпетельные спайки тонкого кишечника отмечались в 30% случаях во 2 группе, в 1 группе подобных сращений не визуализировано.
Таким образом, выраженность спаечного процесса выше у женщин после удаления матки с придатками, как и клинические проявления спайкообразования, что в том числе проявляется в снижении показателей качества жизни у данной группы пациенток по сравнению с женщинами после гистерэктомии с сохранением яичников. Учитывая многочисленные биологические эффекты эстрогенов (в том числе снижение выработки тромбоксана, повышение фибринолитической активности, увеличение секреции простациклина, снижение резистентности сосудистого кровотока, повышение индекса резистентности и индекса пульсации сосудов, реализация эффекта антагониста кальция,
стимуляция выработки релаксирующего фактора эндотелия), логично, что хирургически обусловленная, резко наступающая эстрогенная недостаточность приводит к усугублению микроциркулярных нарушений, в том числе в тканях брюшины, способствует нарастанию ишемии, инициации каскадных реакций, отнюдь не способствующих активации фибринолиза, но инициирующих спайкообразование.
Выводы
Выраженность спаечного процесса и его клинических проявлений выше у женщин после удаления матки с придатками, чем у женщин с аналогичной операцией и сохранением функции яичников, что служит дополнительным аргументом к включению в комплекс ранних послеоперационных профилактических противоспаечных мероприятий заместительной терапии половыми гормонами.
Библиографическая ссылка
Дворецкая Ю.А., Ильина О.В., Кушнерук Н.Э., Селихова М.С. ВЗАИМОСВЯЗЬ ЭСТРОГЕННОЙ НЕДОСТАТОЧНОСТИ И ВНУТРИБРЮШИННОГО СПАЙКООБРАЗОВАНИЯ // Современные проблемы науки и образования. 2016. № 3. ;URL: https://science-education.ru/ru/article/view?id=24399 (дата обращения: 08.04.2026).



