В последние время широко использует ацидофильных микроорганизмов в процессе окисления сульфидных минералов. Объектами исследований являлись аборигенные штаммы хемолитотрофных микроорганизмов, распространенные в растворах после кучного выщелачивания уранового месторождения «Восток». В результате выполненных исследований изучены ареалы и численность Acidithiobacillus ferrooxidans, Thiobacillus thiooxidans, осуществляющих бактериальное выщелачивание окисленных и забалансовых руд месторождения «Восток». Установлено, что численность Аcid. ferrooxidans и Th. thiooxidans – составляет в количестве от 102 кл./мл до 107 кл./мл. Последовательные пассажи аборигенных культур Acidithiobacillus ferrooxidans приводят к активации окислительного процесса. Аcid. ferrooxidans заметно активизировался уже после второго пассажа и окисление закисного железа завершилось на двенадцатые сутки, т.е. на пять суток раньше исходной культуры. Последующие пассажи еще больше активировали эту культуру. Максимальное активирование было достигнуто после третьего пассажа, когда окисление железа завершалось на третьи сутки.
До настоящего времени в условиях кучного выщелачивания урана микробиологическое обследование и изучение участия микроорганизмов в процессах извлечения урана не проводились. Для понимания физиологических и биохимических механизмов приспособляемости определенных видов микроорганизмов и их природных популяций к геохимическим условиям среды необходимо определение основных точек приложения химических элементов среды к процессам метаболизма, установление вызываемых ими изменений обменных процессов и биологических реакций [1, 5]. Такие исследования вскрывают биотехнологическую сущность воздействия химических элементов естественной среды обитания на организмы на популяционном и организменном уровнях [2].
Все это повышает ценность способа бактериально-химического выщелачивания урана из забалансовых и бедных руд, сочетающего высокую эффективность с малым загрязнением окружающей среды.
Большое значение имеют изучение физиологии Acidit hiobacillus ferrooxidansс целью получения наиболее активную культуру для создания биотехнологии извлечения цветных и благородных металлов из руд и продуктов их флотации.
Материалы и методы исследования
Для роста и развития культуры Acid.ferrooxidans применяли среду 9КСильвермана и Лундгрена. Способность бактерий окислять Fe2+ определяли по изменению в среде количества Fe2+ и Fe3+. Количество Fe2+ и Fe3+ определяли комплексонометрическим методом, с использованием в качестве титранта ЭДТА (этилендиаминтетрауксусной кислоты динатриевая соль). Метод основан на реакции образования комплексных соединений ионов металлов с органическими соединениями [3].
Окислительно-восстановительный потенциал и рН среды измеряли на рН- метре ЭВ-74.
Забор материалов для исследования производили по общепринятой методике из растворов под штабелем № 4, 5, 6 и маточного раствора, а также из испарительных карт № 1, 2, 3, 4, 5.
Результаты исследования и их обсуждение
Нами были проведены химико-микробиологические исследования растворов, вытекающих из- под штабеля и испарительных карт с целью лучше представить микробиологическую обстановку, в которой происходят процессы окисления урансодержащих руд.
Было предположение, что урансодержащим рудам на объектах кучного выщелачивания более свойственны микроорганизмы семейства серобактерий, то есть тионовых бактерий, окисляющих серу и соединения серы (сульфиды). Поэтому больше внимание обращали на изучение видового и количественного состава представителей следующих видов хемолитоавтотрофных бактерий: Acidithiobacillus ferrooxidans , Acidithiobacillus thiooxidans в условиях кучного выщелачивания урана. Пробы для исследования отбирали из растворов под штабелями № 4, № 5, № 6 и из испарительных карт № 1–5 участка кучного выщелачивания урана месторождения «Восток» РУ-1 Степногорского горно-химического комбината (рис.1).

Отобранные растворы

Раствориз под штабелями

Раствор из испарительных карт
Рис. 1. Точки отбора проб растворов
Руды месторождения «Восток» относятся к комплексным урано-молибденовым. Кроме основного компонента – урана, практическое значение имеет молибден, содержание которого связано с распределением урана корреляционной зависимостью. Тенденция такова, что доля основного металла в руде уменьшается с понижением глубины отработки рудных залежей месторождения. Содержание молибдена в руде изменяется от тысячных долей процента в рядовых и бедных рудах до десятых в богатых, составляя в среднем 0,038 %.
Забалансовые, бедные и окисленные виды урансодержащих руд месторождения «Восток» складируют штабелями на предварительно подготовленную резиновую подложку. На поверхность созданной таким образом кучу, где проводится кислотное орошение, в качестве окислителя обычно применяется 1,5–2,0 % раствор серной кислоты как технологический раствор. Полученный после орошения технологический раствор с низким содержанием урана как продуктивный раствор, содержащий 0,1 г/л U , поступает на сорбцию. Обычно после адсорбции урана в растворе остается до 0,01 г/л U , и его называют маточным раствором.
Как показали результаты химического анализа (таблица), содержание молибдена (Мо), изучаемого нами в продуктивном растворе, составляет до 0,07 г/л. Во всех исследуемых растворах железо находится в трехвалентной форме, и концентрация его в продуктивном растворе доходит до 6,4 г/л Fe 3+ . Присутствие железа в основном в трехвалентной форме происходит не без участия А cid . ferrooxidans .
Температура раствора под штабелем оказалась ниже (17–18,5 °С), чем у раствора испарительной карты (19–21 °С). Его характерной особенностью оказалось преобладание кислых растворов (рН от 1,17 до 2,18), что создает благоприятные условия для развития хемолитоавтотрофных (А cid . ferrooxidans , Acid . thioxidans ) бактерий, которые играют главную роль в процессе биогеотехнологии металлов из руд.
Анализируя данные о численности хемолитоавтотрофных бактерий – основных показателей степени окислительно-восстановительных процессов, необходимо отметить, что они встречались в растворах в незначительных количествах, кроме А cid . ferrooxidans . Содержание А cid . ferrooxidans было отмечено во всех пробах растворов, имеющих кислую реакцию, а численность его клеток достигала от 102 до 107 кл/мл.
Химический состав и количество Acidithiobacillus ferrooxidans , Acidithiobacillus thiooxidans в растворах на участках кучного выщелачивания урана Рудоуправления № 1
|
Место отбора раствора |
Содержание в растворах, г/л |
кл/мл |
|||||||||||
|
ph |
H2SO4 |
Fe3+ |
Fe2+ |
Feобщ |
U |
Мо |
SiO2 |
SO42- |
Cорг |
NH4+ мг/л |
A.ferroоxidans, |
A.thiоoxidans, |
|
|
Штаб.№ 4(отр.) |
2,18 |
0,48 |
2,58 |
0 |
2,58 |
0,067 |
0,033 |
- |
31,92 |
- |
28 |
107 |
103 |
|
Штаб. № 5 |
1,63 |
2,4 |
6,3 |
0,1 |
6,4 |
0,086 |
0,072 |
0,47 |
62,4 |
0,095 |
26 |
107 |
103 |
|
Штаб. № 6 |
1,56 |
2,9 |
6,3 |
0 |
6,3 |
0,042 |
0,073 |
- |
57,6 |
- |
20 |
107 |
103 |
|
Мато. раств. |
1,77 |
1,3 |
4,48 |
0,35 |
4,83 |
0,017 |
0,016 |
0,062 |
43,6 |
0,095 |
- |
105 |
- |
|
Карта №1 |
1,17 |
5,8 |
9,38 |
0 |
9,38 |
0,042 |
0,033 |
- |
110,4 |
- |
30 |
102 |
- |
|
Карта №2 |
1,96 |
0,92 |
2,52 |
0 |
2,52 |
0,011 |
0,008 |
- |
50,4 |
- |
24 |
103 |
- |
|
Карта №3 |
1,42 |
3,9 |
5,25 |
0 |
5,25 |
0,011 |
0,043 |
- |
50,4 |
- |
24 |
103 |
- |
|
Карта №4 |
1,60 |
2,4 |
1,3 |
0 |
1,3 |
0,016 |
0,028 |
- |
55,2 |
- |
20 |
102 |
- |
|
Карта №5 |
1,74 |
1,5 |
5,6 |
0 |
5,6 |
0,028 |
0,025 |
- |
122,4 |
- |
21 |
103 |
- |
Как видно из таблицы, изучение показало, что в растворах под штабелями встречается численность А cid . ferrooxidans в количестве 107 клеток в 1 мл.
В маточном растворе количество достигает 105кл/мл, тогда как в растворах испарительной карты – всего 102кл/мл. Такая малая численность, по-видимому, была связана с низкой аэрацией раствора испарительной карты. Возможно, что в застойных кислых растворах, скопившихся на испарительных картах, солнечные лучи оказывают ингибирующее или даже стерилизующее действие на клетки бактерий Acid.ferrooxidans.
Для определения численности Acid . thi о oxidans (таблица) в жидкую питательную среду Ваксмана с серой засева ли исследуемый раствор после выщелачивания . После инкубиро вания в термостате при 28–30 °С через 3–4 дня появ илось помутнение среды, а рН ее снизился. Присутствие в растворах под штабелями № 4, 5, 6 незначительного количества (103кл/мл) Acid . thi о oxidans позволяет предположить об их участии в процессах бактериального выщелачивания урана. В маточном растворе и в кислых растворах испарительных карт Acid . thi о oxidans не были обнаружены.
Итак, основная роль в окислении урана на кучном выщелачивании принадлежит тионовым бактериям, и главным образом Acid . ferrooxidans . Факт присутствия железа в кислых выщелачивающих производственных растворах преимущественно в трехвалентной форме еще раз подтверждает высокую активность А cid . ferrooxidans [4], стерильные растворы в подобных условиях содержали бы только железо в закисной форме, образующееся при окислении сульфидов.
Мы сочли необходимым изучить их основные признаки: морфологию клеток, характер роста на твердой питательной среде, окислительную способность на жидкой среде Сильвермана и Лундгрена 9К.
Клетки палочковидной формы, по Граму, окрашиваются отрицательно, подвижны. Acid .ferrooxіdans показано наличие S -слоя (рис. 2). На твердой среде на третьи сутки культивирования формируют мелкие колонии, размером 1–1,2 мм, округлой формы, с гладкой поверхностью. Структура колоний однородная, плотной консистенции. Колонии окрашены в оранжевый цвет, под микроскопом заметны рыжие вкрапления за счет окислов железа.
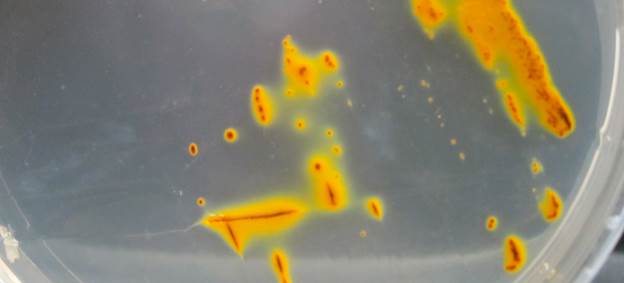
Рис. 2. Характеристика роста Acid .ferrooxіdansна гельевой пластинке пропитанной средой Сильвермана и Лундгрена 9К
Одним из ранних методов поддержания культур в активном состоянии является последовательный периодический пересев культур на свежую питательную среду. Кроме того, этот метод широко использовался для получения адаптированных к металлам культур тионовых бактерий. Нами этот способ был использован для повышения активности аборигенных штаммов А cid . ferrooxidans , так как они являлись слабоактивными. Последовательные пересевы производились следующим образом: культуры выращивали глубинным методом в колбах со 100 мл жидкой среды 9К Сильвермана и Лундгрена (рН 2,0) и ежедневно определяли содержание закисного и окисного железа. При развитии бактерий жидкая среда, сначала прозрачная, постепенно приобретала янтарный оттенок, переходящий в красно-коричневый, что совпадало с наибольшей степенью окисления железа. На этой стадии отбирали 20 мл культуры и помещали вновь в жидкую среду 9К (первый пассаж). В сроки наибольшего накопления окисного железа производили повторный пересев культуры на свежую питательную среду 9К (второй пассаж) и так повторяли несколько раз. Каждый раз инокулят брался в различные сроки роста предыдущей культуры.
Всего проведено три последовательных пассажа. Результаты приведены на рис. 3.
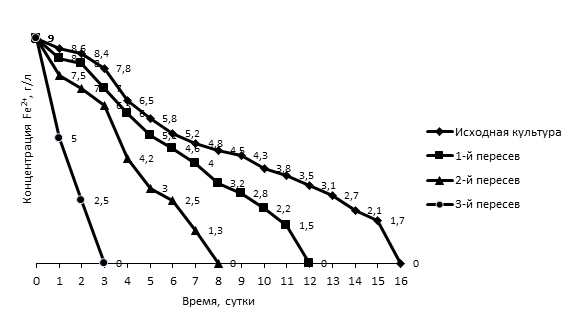
Рис. 3. Динамика окисления закисного железа культурой Acid . ferrooxidans в зависимости от количества кратного пересева
Как следует из графиков, последовательные пассажи приводят к активации окислительного процесса. Так, А cid . ferrooxidans заметно активизировался уже после второго пассажа и окисление закисного железа завершилось на двенадцатые сутки, т.е. на пять суток раньше исходной культуры. Последующие пассажи еще больше активировали эту культуру. Максимальное активирование было достигнуто после третьего пассажа, когда окисление железа завершалось на третий сутки.
Выводы
Итак, для активирования выделенных аборигенных культур Acid . ferrooxidans из природного субстрата в лабораторных условиях достаточно трехкратного пересева.
Таким образом, культура отличается по скорости окисления Fe2+ , и об их активности можно судить по конечному результату, срокам завершения окисления закисного железа.
Библиографическая ссылка
Канаев А.Т., Канаева З.К., Сейдахмет З.С., Аманбаева У.И. ИЗУЧЕНИЕ КУЛЬТУРЫ ACIDITHIOBACILLUS FERROOXІDANS МЕСТОРОЖДЕНИЯ «ВОСТОК» И АКТИВИРОВАНИЕ МЕТОДОМ ПОСЛЕДОВАТЕЛЬНОГО ПЕРЕСЕВА // Современные проблемы науки и образования. 2016. № 1. ;URL: https://science-education.ru/ru/article/view?id=24093 (дата обращения: 22.05.2026).



