В настоящее время проведение химиотерапии больным с ГИСТ считается нецелесообразным по причине имеющейся точки зрения о химиорезистентности данных злокачественных новообразований [1]. Поэтому основным нехирургическим методом лечения больных с неоперабельными, рецидивирующими и/или метастатическими формами ГИСТ является проведение им таргетной терапии иматинибом (Гливеком), воздействующей на активирующую мутацию тирозинкиназного рецептора с-KIТ в опухолевых клетках ГИСТ, следствием которой является усиление пролиферации и митотической активности опухолевых клеток ГИСТ. Однако, несмотря на высокую изначальную эффективность применения таргетных препаратов (в том числе, иматиниба) в лечении пациентов с ГИСТ с течением времени к ним начинает развиваться резистентность, существенным образом снижающая эффективность их дальнейшего применения. Например, было установлено, что после 2-х лет с момента начала проведения таргетной терапии иматинибом у более чем у половины пациентов с ГИСТ развивается резистентность к данному препарату, обусловленная развитием в клетках ГИСТ вторичных мутаций [2,7]. Несмотря на открытие и внедрение в практическую онкологию таргетных препаратов второго и третьего поколения (Сутент и Регорафениб, соответственно) высокая частота побочных эффектов от их применения, а также развитие к ним вторичной резистентности опухоли, являются стимулом для поиска новых альтернативных решений в терапии больных с неоперабельными, рецидивирующими и метастатическими формами ГИСТ.
Также известно, что существующее в настоящее время мнение о химиорезистености ГИСТ основано на результатах клинических наблюдений, проведенных до внедрения в практическую онкологию точных методов диагностики ГИСТ, позволяющих обнаружить совокупность гистологических и иммуногистохимических признаков, отличающих ГИСТ от других типов гладкомышечных и нейрогенных новообразований (например, лейомиосарком, лейомиом и шванном). Установлено, что данные типы опухолей обладают устойчивостью к большинству современных химиопрепаратов. Следовательно, отсутствие на момент проведения данных исследований точных методов дифференциальной диагностики ГИСТ и других гладкомышечных и нейрогенных злокачественных новообразований могли существенным образом повлиять на достоверность результатов исследований и привести к формированию ошибочного мнения о химиорезистентности ГИСТ.
В соответствии с вышеизложенным, представляло интерес изучение способности химиопрепаратов различных групп оказывать анти-пролиферативный эффект по отношению к клеткам ГИСТ и вызывать их гибель по механизму апоптоза.
Материалы и методы исследования. В качестве объекта исследования была выбрана клеточная линия ГИСТ Т-1, чувствительная к действию таргетного препарата иматиниба. Клетки культивировали в стандартных условиях (37оС, 5%СО2) в культуральной среде RPMI-1640 (ПанЭКО) с добавлением 10% эмбриональной телячьей сыворотки (HyClone), антибиотиков пенициллина-стрептомицина и L-глутамина (все реагенты ПанЭКО). Опухолевые клетки ГИСТ культивировали с доксорубицином, винбластином, нокодазолом, паклитакселом, иматинибом (Sigma), этопозидом, гидроксимочевиной (Calbiochem). Изменение уровня экспрессии белков-маркеров повреждения ДНК и маркеров апоптоза оценивали методом иммуноблоттинга с использованием соответствующих моноклональных антител (мАТ).
Результаты исследований и их обсуждение.
Было обнаружено, что инкубация опухолевых клеток ГИСТ Т-1 с химиопрепаратами индуцирует их гибель по механизму апоптоза. Об этом свидетельствовало значительное повышение уровней экспрессии расщепленных форм ПАРП и каспазы-3 в клетках ГИСТ после их инкубации с большинством из химиопрепаратов (РИС.1А). Наибольший про-апоптогенный эффект был обнаружен у препаратов платины, а также препаратов, влияющих на динамическое состояние микротрубочек веретена деления (в частности, винбластина). Ингибиторы топоизомеразы II типа доксорубицин и этопозид также вызывали гибель клеток ГИСТ по механизму апоптоза, тем не менее их эффект был менее выраженным. Примечательно, что уровень экспрессии одного из расщепленных фрагментов ПАРП (мол. массой 86 кДа) в опухолевых клетках ГИСТ коррелировал с уровнем экспрессии каспазы-3, что согласуется с данными литературы, свидетельствующими о способности каспаз (в том числе каспазы-3) индуцировать расщепление ПАРП на 2 фрагмента молекулярной массой 86 и 24 кДа, соответственно [6]. Важно отметить, что про-апоптогенный эффект ряда химиопрепаратов (этопозида, цисплатины, а также всех препаратов, влияющих на динамическое состояние микротрубочек) был более выраженным по сравнению с действием таргетного препарата иматиниба. Была также выявлена корреляционная зависимость между про-апоптогенным эффектом вышеназванных химиопрепаратов и их способностью индуцировать повышение уровня экспрессии гистона 2А, фосфорилированного по остаткам серина в положении 139 (-H2AX) (РИС.1Б). Известно, что данная форма гистона является общепризнанным маркером двунитевых разрывов ДНК, а также накапливается в М-фазе клеточного цикла, в частности, за счет ATM- или DNA-PKcs/Chk2-опосредованных механизмов фосфорилирования данной формы гистона даже на фоне отсутствия каких-либо повреждений ДНК, в том числе, двунитевых разрывов [4, 5]. В клетках ГИСТ, инкубированных с таргетным препаратом иматинибом, происходило умеренное повышение уровня экспрессии -H2AX, коррелировавшее с уровнем экспрессии расщепленной формы ПАРП, являющейся маркером апоптоза. Эти данные коррелируют с данными литературы, свидетельствующими о способности H2AX индуцировать апоптоз клеток ГИСТ под влиянием иматиниба [3].
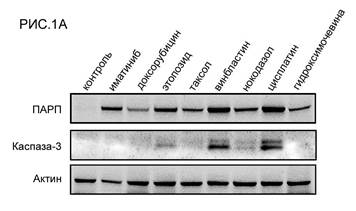
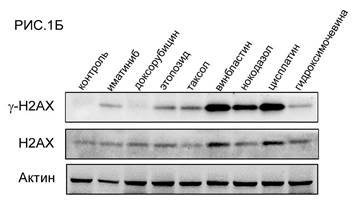
РИС. 1. Способность химиопрепаратов и таргетного препарата иматиниба индуцировать апоптоз (А) и вызывать фосфорилирование гистона H2AХ – -H2AX (Б) в клетках ГИСТ Т-1.
Таким образом, проведенные нами исследования свидетельствуют о способности химиопрепаратов индуцировать гибель клеток ГИСТ по механизму апоптоза. Наибольшим про-апоптогенным эффектом в отношении опухолевых клеток ГИСТ обладают препараты, влияющие на динамическое состояние микротрубочек, а также препараты платины. Полученные нами результаты свидетельствуют о чувствительности опухолевых клеток ГИСТ к некоторым химиопрепаратам, что ставит под сомнение существовавшую в настоящее время точку зрения о химиорезистентности у ГИСТ.
Заключение. Клетки ГИСТ чувствительны к ингибиторам топоизомеразы II типа, индуцирующим образование двунитевых разрывов ДНК и последующую гибель опухолевых клеток по механизму апоптоза. Наиболее эффективными химиопрепаратами в отношении клеток ГИСТ явились препараты, влияющие на динамическое состояние микротрубочек веретена деления – винбластин и паклитаксел. Полученные нами экспериментальные данные о чувствительности клеток ГИСТ к некоторым химиопрепаратам in vitro свидетельствуют о перспективности использования вышеназванных химиопрепаратов в лечении больных с неоперабельными, рецидивирующими и/или метастатическими формами ГИСТ, а также формами рефрактерными к монотерапии таргетным препаратом, в частности, иматинибом.
Работа финансировалась грантом Российского Научного Фонда (РНФ) № 14-15-00342.
Библиографическая ссылка
Галембикова А.Р., Дунаев П.Д., Боичук С.В. ОЦЕНКА ЧУВСТВИТЕЛЬНОСТИ ГАСТРОИНТЕСТИНАЛЬНЫХ СТРОМАЛЬНЫХ ОПУХОЛЕЙ (ГИСТ) К ХИМИОПРЕПАРАТАМ РАЗЛИЧНЫХ ГРУПП. // Современные проблемы науки и образования. 2015. № 6. ;URL: https://science-education.ru/ru/article/view?id=23728 (дата обращения: 16.05.2026).



