Полиморбидность (мультиморбидность, множественность заболеваний у одного человека) – одна из самых сложных проблем, с которой сталкиваются медицинские работники при работе с больными пожилого и старческого возраста [1,3]. В среднем при клиническом обследовании больных пожилого и старческого возраста диагностируется не менее 4—5 болезней, проявлений патологических процессов [5]. В плане развития геронтологии и гериатрии наибольший интерес представляют патогенетические механизмы, задействованные в формировании полиморбидности при социально значимой возраст-ассоциированной патологии[2]. Необходимо отметить, что согласно эпидемиологическим данным, к наиболее распространенным заболеваниям пожилого и старческого возраста относятся сердечно-сосудистые, болезни дыхательной системы, неврологическая патология, а также стресс на фоне проводимых в пожилом и старческом возрасте оперативных вмешательств [4]. В этой связи изучение молекулярных биомаркеров диагностики, прогноза, оценки эффективности терапии наиболее востребовано, прежде всего, при социально значимой возраст-ассоциированной патологии.
Цель работы – изучить формирование полиморбидности путем развития оксидативного дисбаланса при соматической патологии, не имеющей общих патофизиологических механизмов развития и их молекулярные маркеры.
Материал и методы
Исследование включало в себя несколько этапов.
1.1. Сравнительное изучение показателей оксидативного статуса практически здоровых лиц среднего и пожилого возраста с целью выявления возрастных особенностей. На данном этапе проведено обследование 61 человека: 31 человека среднего возраста (от 40 до 49 лет, средний возраст 44,1+2,2 года, мужчин – 17 чел., женщин – 14 чел.) и 30 человек пожилого возраста (от 60 до 69 лет, средний возраст 64,4+2,3 года, мужчин – 14 чел., женщин – 16 чел.). Группы пациентов различного возраста были сопоставимы по возрасту, полу, факторам риска заболеваний.
1.2. Сравнительное изучение оксидативного статуса у практически здоровых пожилых людей с различными факторами риска сердечно-сосудистыми заболеваний. На данном этапе было обследовано 78 пациентов пожилого возраста (от 60 до 69 лет, средний возраст 64,8+2,4 года, мужчин – 42 чел., женщин – 36 чел.), в т.ч. лиц с курением – 17 чел., лиц с гиподинамией – 15 чел., лиц, подверженных хрониострессу – 15 чел., лиц с гиперхолестеринемией – 17 чел.; лиц с отсутствием факторов риска – 14 чел.
1.3. Изучение возрастных особенностей оксидативного статуса при хронической ИБС. На данном этапе проведено обследование 63 пациентов: 31 человека среднего возраста (от 40 до 49 лет, средний возраст 45,2+2,7 года, мужчин – 21 чел., женщин – 10 чел.) и 32 пациентов пожилого возраста (от 60 до 69 лет, средний возраст 65,8+2,2 года, мужчин – 19 чел., женщин – 13 чел.). Все пациенты страдали ИБС в виде стенокардии напряжения I-III ФК, ХСН ФК I-II по классификации NYHA. Группы пациентов различного возраста были сопоставимы по возрасту, полу, характеристикам ИБС. Следует подчеркнуть, что эти пациенты не имели другой, кроме ИБС, клинически значимой патологии, выявляемой рутинными методами, поэтому в нашем исследовании мы трактовали их как «пациентов, страдающих монопатологией в виде ИБС».
1.4. Изучение возрастных особенностей оксидативного статуса при железодефицитной анемии. На данном этапе проведено обследование 61 пациента: 30 человек среднего возраста (от 40 до 49 лет, средний возраст 44,8+3,1 года, мужчин – 11 чел., женщин – 19 чел.) и 31 пациента пожилого возраста (от 60 до 69 лет, средний возраст 64,0+2,7 года, мужчин – 13 чел., женщин – 18 чел.). Все пациенты страдали железодефицитной анемией легкой и средней степени тяжести. Группы пациентов различного возраста были сопоставимы по возрасту, полу, причинам и характеристикам железодефицитной анемии. Эти пациенты не имели другой кроме железодефицитной анемии клинически значимой патологии, выявляемой рутинными методами, а заболевания, явившиеся причиной железодефицитной анемии, находились в стадии выраженной клинической ремиссии, поэтому в нашем исследовании мы трактовали их как «пациентов, страдающих монопатологией в виде железодефицитной анемии», понимая определенную условность этого термина.
1.5. Изучение особенностей оксидативного статуса при сочетанной кардиоваскулярной и гематологической патологии у лиц пожилого возраста.
На данном этапе проведено обследование 32 человек пожилого возраста (от 60 до 69 лет, средний возраст 64,9+1,8 года, мужчин – 17 чел., женщин – 15 чел.). Все пациенты страдали ИБС в виде стенокардии напряжения I-III ФК, ХСН ФК I-II по классификации NYHA, железодефицитной анемией легкой и средней степени тяжести.
Уровень оксидативного стресса по содержании МДА и SH-группы и их соотношения определялся при помощи ферментативного метода с применением стандартных реактивов на биохимических автоанализаторах FP-901 «Labsystem» (Франция), «Harizon» (Канада).
Результаты и обсуждения
Проведя анализ полученных данных мы выявили, что в пожилом возрасте имелась тенденция к увеличению концентрации МДА: в нашем исследовании этот показатель увеличился с 33,2±1,3 мкмоль/л у людей среднего возраста до 39,2±1,1 мкмоль/л у людей пожилого возраста, р<0,05. Это свидетельствовало об увеличении прооксидантного потенциала в пожилом возрасте, по мере старения, несмотря на отсутствие заболеваний (табл. 1). Также была отмечена тенденция к снижению содержания маркеров прооксидантов SH-групп с 318,6±10,6 мкмоль/л у людей среднего возраста до 292,5±7,4 мкмоль/л у людей пожилого возраста, р<0,05. Соответственно, происходило снижение суммарного коэффициента SH/МДА, характеризующего оксидативный статус. Так, у лиц среднего возраста его значение составило 9,91±0,3, у здоровых лиц пожилого возраста – 7,08±0,3, р<0,05. Таким образом, у пожилых пациентов без сердечно-сосудистой патологии наблюдалось достоверное снижение маркеров антиоксидантной защиты в сыворотке крови и увеличение содержания МДА как показателя течения оксидативных процессов.
Таблица 1
Сравнительная характеристика оксидативного статуса у лиц среднего и пожилого возраста
|
Показатель |
Средний возраст (n=31) |
Пожилой возраст (n=30) |
|
МДА (мкмоль/л) |
33,2±1,3 |
39,2±1,1* |
|
SH ( мкмоль/л) |
318,6±10,6 |
292,5±7,4* |
|
SH / МДА |
9,91±0,3 |
7,08±0,3* |
* p<0,05 по сравнению с лицами среднего возраста
Оксидативный статус у практически здоровых людей пожилого возраста с факторами риска сердечно-сосудистой патологии
При изучении влияния управляемых факторов риска было выявлено, что по степени значимости они расположены в порядке убывания следующим образом (согласно значению коэффициента SH/МДА): хронический стресс, гиподинамия, гиперхолестеринемия, курение, р<0,05. Наибольшей активностью в плане стимуляции оксидативного стресса обладало курение, коэффициент SH/МДА был наименьшим среди других факторов риска – 3,58±0,1, при этом значение МДА составило 51,3 ± 1,1 мкмоль/л, SH-групп – 184,1 ± 7,3 мкмоль/л. Значимый вклад в стимуляцию процессов ПОЛ вносила гиперхолестеринемия, коэффициент SH/МДА составил 3,93±0,1, уровень МДА был 51,5±1,1 мкмоль/л, SH-групп – 201,3 ± 8,9 мкмоль/л. Несколько меньшей активностью в отношении оксидативных процессов обладали такие факторы риска как гиподинамия (уровень МДА составил 45,1±1,2 мкмоль/л, SH-групп – 255,2±5,4 мкмоль/л, коэффициент SH/МДА – 5,65±0,3) и хрониостресс (уровень МДА составил 43,1±0,7 мкмоль/л, SH-групп – 259,4±8,2 мкмоль/л, коэффициент SH/МДА – 6,01 ± 0,2). Необходимо отметить, что при сравнении колебаний показателей концентрации МДА, SH-групп, значений коэффициента SH/МДА у лиц с наличием факторов риска и без них выявлены статистически достоверные различия. Так, у людей с отсутствием факторов риска показатель содержания МДА составил 41,5±1,2 мкмоль/л, SH-групп – 292,5±7,1 мкмоль/л, коэффициент SH/МДА соответствовал значению 7,04±0,2. При этом показатель МДА был достоверно ниже (p<0,05), чем у людей, которые имели такие факторы риска как курение и гиперхолестеринемия, показатель SH и отношение SH/МДА – выше, чем у людей со всеми изучаемыми факторами риска (p<0,05). Это свидетельствовало об активации оксидативных процессов и снижении антиоксидантной защиты на фоне факторов риска, значимость оксидативного стресса в формировании патологии сердца и сосудов, артериальной гипертензии. Таким образом, оксидативные процессы характеризовались большей напряженностью у практически здоровых лиц пожилого возраста по сравнению с лицами среднего возраста. Кроме того, наличие факторов риска сердечно-сосудистых заболеваний потенцировало прооксидантные процессы в пожилом возрасте.
Оксидативный статус при хронической ишемической болезни сердца
В среднем возрасте при ИБС имело место более низкое содержание МДА в сыворотке крови, чем в пожилом – 34,5±1,2 мкмоль/л и 43,4±1,5 мкмоль/л соответственно, р<0,05; более высокая концентрация SH-групп – 319,8±9,3 мкмоль/л и 291,5 ± 7,4 мкмоль/л соответственно, р<0,05. Коэффициент SH/МДА также свидетельствовал о росте прооксидантных влияний в пожилом возрасте при ИБС, он составил в среднем возрасте – 9,26 ± 0,1, а в пожилом – 6,7±0,2, р<0,05.
Оксидативный статус при железодефицитной анемии
При железодефицитной анемии показатели оксидативного статуса в пожилом возрасте были менее благоприятными. Так, достоверно более высокими значениями у пожилых характеризовался уровень МДА: у пожилых больных он составил 43,2±1,4 мкмоль/л, у лиц среднего возраста – 32,6±1,1 мкмоль/л, p<0,05. Противоположная картина имела место в отношении уровня сульфгидрильных групп – в пожилом возрасте их содержание соответствовало 292,3±7,1 мкмоль/л, в среднем было достоверно больше – 367,5±8,1 мкмоль/л, p<0,05. Соответственно, у пожилых коэффициент SH/МДА был достоверно меньшим – 6,65±0,3 – против 9,22±0,2 у лиц среднего возраста, p<0,05. Таким образом, железодефицитная анемия у пожилых людей способствовала снижению антиоксидантных защитных механизмов и активации проокислительных процессов в достоверно большей степени, чем у людей среднего возраста.
Оксидативный статус при сочетании ишемической болезни сердца и железодефицитной анемии у людей пожилого возраста
При изолированной ИБС и железодефицитной анемии состояние оксидативного статуса не имело достоверных различий (показатели МДА составили соответственно 43,4±1,5 и 43,2±1,4 мкмоль/л, р>0,05; показатели содержания SH-групп соответственно 291,5±7,4 и 292,3±7,1, р>0,05). При сочетании этих заболеваний имели место достоверно более высокие значения МДА (50,1±1,2 мкмоль/л, p<0,05) и меньшие показатели уровня SH-групп (252,4±4,3 мкмоль/л), значение суммарного коэффициента, характеризующего оксидативный стресс, составляло 6,01±0,1 (p<0,05 по сравнению с практически здоровыми пожилыми людьми и с пациентами с монопатологией) (рис. 1). Соответственно, при сочетании ИБС и железодефицитной анемии в пожилом возрасте отмечались достоверно меньшие значения суммарного коэффициента, характеризующего оксидативный статус: при ИБС значение коэффициента составило 6,71±0,2, при железодефицитной анемии – 6,65±0,3, при их сочетании 5,98±0,3 (p<0,05 по сравнению с практически здоровыми пожилыми людьми и с пациентами с одним ведущим заболеванием).
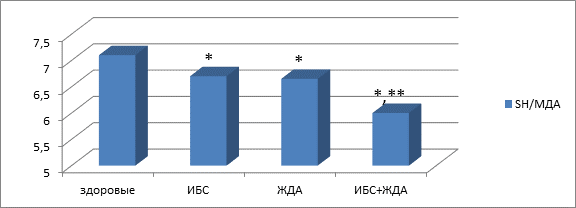
* p<0,05 по сравнению с практически здоровыми пожилыми людьми
** p<0,05 по сравнению с лицами с монопатологией
Рис. 1. Значения коэффициента SH/МДА у пожилых пациентов с ишемической болезнью сердца, железодефицитной анемией и их сочетанием.
Выводы:
1. У пожилых людей без сердечно-сосудистой патологии наблюдается более выраженное снижение маркеров антиоксидантной защиты (по показателю содержания SH-групп в сыворотке крови в среднем на 8,9%) и увеличение содержания малонового диальдегида по сравнению с лицами среднего возраста (в среднем на 18,1%), при этом присоединение управляемых факторов риска развития кардиоваскулярной патологии способствует ухудшению оксидативного статуса.
2. Железодефицитная анемия у пожилых людей способствует снижению антиоксидантных защитных механизмов и активации проокислительных процессов в достоверно большей степени, чем у людей среднего возраста, что проявляется снижением коэффициента SH/МДА в 1,4 раза.
3. Сочетание ишемической болезни сердца и железодефицитной анемии обладает наибольшим прооксидатным влиянием по сравнению со здоровыми пожилыми людьми, а также у больных с монопатологией и сопровождается снижением коэффициента SH/МДА в 1,2 раза.
Рецензенты:
Ильницкий А.Н., д.м.н., профессор, заведующий кафедрой терапии, гериатрии и антивозрастной медицины ФГБОУ ДПО «Институт повышения квалификации Федерального медико-биологического агентства», г. Москва;
Перелыгин К.В., д.м.н., старший научный сотрудник отдела клинической геронтологии Автономной некоммерческой организации «Научно-исследовательский медицинский центр «Геронтология», г. Москва.
Библиографическая ссылка
Мурсалов С.У., Хаммад Е.В., Седова Е.В., Чижова М.А. ФОРМИРОВАНИЕ ПОЛИМОРБИДНОСТИ ПУТЕМ РАЗВИТИЯ ОКСИДАТИВНОГО ДИСБАЛАНСА ПРИ СОМАТИЧЕСКОЙ ПАТОЛОГИИ, НЕ ИМЕЮЩИХ ОБЩИХ ПАТОФИЗИОЛОГИЧЕСКИХ МЕХАНИЗМОВ РАЗВИТИЯ И ИХ МОЛЕКУЛЯРНЫЕ МАРКЕРЫ // Современные проблемы науки и образования. 2015. № 6. ;URL: https://science-education.ru/ru/article/view?id=23171 (дата обращения: 16.05.2026).



