В связи с этим необходима разработка и поиск доступных и, в то же время, эффективных лекарственных средств и подходов к лечению раневой инфекции, отвечающих современным требованиям.
В этом плане в последние годы вызывает интерес и развивается сорбционно-аппликационная терапия, направленная на сокращение сроков очищения ран от микроорганизмов и продуктов их жизнедеятельности, а также некротических тканей [1,4,5,12].
Однако необходимо подчеркнуть, что все существующие на сегодняшний день медицинские сорбенты могут использоваться или в фазе воспаления или в фазах регенерации. Кроме того, многие из них не обладают противомикробными свойствами [7].
В этой связи вызывает интерес медицинский растительный сорбент нового поколения «Целоформ», представляющий собой порошкообразное средство на основе механически размельченного упруго деформационным методом хлопкового волокна до размеров волокон 20-50 мкм.
Ранее были изучены особенности его состава, заключающиеся в наличии в нем большого количества свободных радикалов, образующихся в процессе измельчения сырья — хлопковой целлюлозы. Поэтому была выдвинута предварительная рабочая гипотеза, что свободные радикалы, входящие в состав сорбента «Целоформ», взаимодействуют с бактериями, подавляя их активность [6].
Цель исследования: установить механизм противомикробного действиярастительного сорбента «Целоформ».
Методы исследования:
1. Измерение скорости линейной диффузии;
2. Изучение сорбционной способности «Целоформа»;
3. Измерение парциального давления кислорода в ране.
1. Для оценки влияния «Целоформа» на диффузионные процессы в ране измерялась скорость линейной диффузии по движению красителя метиленового синего [4].
При этом использовались 3 стеклянные трубки с внутренним диаметром 0,42 см (площадь сечения 0,138 см2). Первая трубка (эталонная), запаянная с одного конца была заполнена физиологическим раствором, вторая – на 70 мм медицинской ватой, которая была уплотнена внешним механическим давлением 300 г/см2. Масса ваты – 0,092 г, после насыщения водой – 0,760 г.(воды – 0,674 г.).
Третью трубку заполнили «Целоформом». Высота его слоя составляла 70 мм, масса – 0,344 г. После насыщения водой масса увеличилась до 0,999 г. (воды – 0,655 г).
После этого все три трубки помещались в чашку Петри диаметром 3,5 см, заполненную 0,05% раствором красителя метиленового синего.
Через 87 часов проведены замеры длины окрашенной зоны во всех трубках.
Длина окрашенной зоны оказалась равна для воды 84 мм, для столба ваты – 24 мм и 6 мм – для слоя «Целоформа».
Вывод: диффузионные процессы на поверхности раны при нанесении порошка «Целоформа» замедляются более чем в 12 раз.
2. Изучение сорбционной способности «Целоформа» в условиях динамической сорбции должно осуществляться путем нанесения его порошка на раневую поверхность. Для моделирования этого процесса был проведен эксперимент, схожий с восходящей хроматографией в сухой колонке [4].
Для этого стеклянная трубка заполнялась слоем «Целоформа», после чего на нижний торец наносились 2 капли 0,05% раствора метиленового синего, и трубку опускали в чашку Петри, заполненную физиологическим раствором.
Под воздействием капиллярных сил уровень жидкости в трубке повысился и через 30 минут достиг верхнего уровня слоя сорбента. При этом зона красителя сместилась незначительно – всего на 2,5 мм. Этот эксперимент наглядно демонстрирует высокую сорбционную активность исследуемого порошка «Целоформа» по отношению к полярным органическим соединениям.
Величина хроматографической подвижности Rf, которую в данном случае можно использовать как меру сорбционной способности в динамических условиях, оказалась равной 0,025. (Величина Rf равна отношению путей, пройденных красителем и растворителем. В данном случае Rf = 2,5 мм/100 мм = 0,025).
Вывод: процессы массобмена с участием полярных органических веществ в среде «Целоформа», насыщенного водой значительно замедляются.
3. Оценка влияния «Целоформа» на уровень парциального давления кислорода проводилась на границе раневая поверхность – сорбент «Целоформ».
Как известно, окислительно-восстановительный потенциал водных растворов, находящихся в контакте с газообразным кислородом, определяется полуреакцией:
O2 + 4H+ +4e = 2 H2O E0 = +1.229 V
уравнение Нернста: ![]()
Пользуясь приведенным соотношением, можно оценить изменение уровня парциального давления кислорода при протекании различных химических или микробиологических процессов, не сопровождающихся заметным изменением рН.
Если редокс-потенциал в
начальный момент равен![]() ,
а через заданный промежуток времени
,
а через заданный промежуток времени![]() ,
легко прийти к соотношению, позволяющему оценить изменение парциального
давления за время эксперимента:
,
легко прийти к соотношению, позволяющему оценить изменение парциального
давления за время эксперимента:
![]()
![]()
![]()
Здесь ![]() –
парциальное давление кислорода в начале эксперимента,
–
парциальное давление кислорода в начале эксперимента, ![]() –
в заданный момент времени.
–
в заданный момент времени.
В качестве индикаторного электрода использовалась платиновая проволока диаметром 0,5 мм, впаянная в стеклянную трубку с длиной рабочей области 6 мм. Измерения потенциала проводились относительно хлорид-серебряного электрода[5].
Платиновый электрод прикладывался к раневой поверхности, электрод сравнения – к поверхности неизмененной ткани на расстоянии 2-3 см от края раны.
В течение нескольких минут потенциал электрода стабилизировался на уровне 115 мв. Затем на поверхность раны насыпался порошок «Целоформа», после чего через 65 мин потенциал достигал своего максимального значения ~60 мв, продолжая в дальнейшем оставаться на этом же уровне (рис. 1).
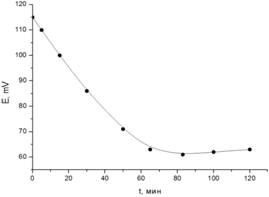
Рис. 1. Динамика изменения уровня парциального давления кислородав ране под влиянием сорбента «Целоформ»
Вывод: уровень редокс-потенциала после нанесения«Целоформа» понижался более чем на 50 мв, что соответствует практически полному удалению кислорода с раневой поверхности:
Заключение. После нанесения сорбента на поверхность раны происходит выраженная сорбция раневого содержимого с удержанием ее как за счет капиллярных сил, так и благодаря образованию гелевых структур на поверхности частиц целлюлозы. При этом резко замедляются процессы массобмена, в том числе и за счет понижения линейной диффузии.
Процесс сорбции «Целоформом» раневой жидкости сопровождается существенным падением уровня парциального давления кислорода на поверхности раны. «Целоформ» в данном случае выступает в роли «пассивного антиоксиданта», сначала удаляя кислород с поверхности раны вместе с сорбируемой жидкостью, а затем (во влажном состоянии), препятствуя его доступу из атмосферного воздуха. Это должно приводить к практически полному прекращению обмена веществ у патогенных микроорганизмов и удалению продуктов их метаболизма.
Таким образом,установленное в ходе исследований существенное падение уровня парциального давления кислорода на покрытой сорбентом «Целоформ» раневой поверхности, приводящее к резкому замедлению процессов массообмена и, следовательно, практически полному прекращению обмена веществ у патогенных микроорганизмов, лежат в основе механизма противомикробного действия «Целоформа».
Рецензенты:Анохина А.В., д.м.н., профессор заведующая кафедрой терапевтической, детской стоматологии и ортодонтии ГБОУ ДПО Казанской государственной медицинской академии, г.Казань;
Фаизов Т.Т., д.м.н., профессор заведующий кафедрой челюстно-лицевой хирургии ГБОУ ВПО Казанского государственного медицинского университета, г.Казань.
Библиографическая ссылка
Нестеров О.В., Ксембаев С.С., Нестерова Е.Е. МЕХАНИЗМ ПРОТИВОМИКРОБНОГО ДЕЙСТВИЯ РАСТИТЕЛЬНОГО СОРБЕНТА «ЦЕЛОФОРМ» // Современные проблемы науки и образования. 2015. № 6. ;URL: https://science-education.ru/ru/article/view?id=23159 (дата обращения: 16.05.2026).



