Цель исследования состояла в изучении ВРСв до и послеоперационном периодах после выполнения радикальной операции на пищеводе с учетом локализации рака.
Материалы и методы исследования
В клиническое исследование было включено 32 пациента с раком пищевода различной локализации, перенесшие операцию типа Льюиса. В зависимости от локализации онкологического процесса пациенты были разделены на две группы. Первую группу из 13 человек составили больные с локализацией рака в верхней и средней трети пищевода (средний возраст 60,3 ± 1,2 лет). Вторую группу, 18 больных, рандомизированную с первой по возрасту и полу, срокам выявления и тяжести онкологического процесса, с локализацией рака в нижней трети пищевода (средний возраст 59,5 ± 1,8 лет). В ходе работы были проанализированы данные ВСР до, через 2 недели и 3 месяца после резекции грудного отдела пищевода с одномоментной аутогастропластикой – операция типа Льюиса. Клинически значимой сопутствующей сердечно-сосудистой патологии у пациентов зафиксировано не было.
Исследование ВСР с определением временных, спектральных показателей и визуальным анализом проводили на аппаратно-программном комплексе компьютерной ритмокардиографии по стандартной методике. Регистрировались 5-минутные записи ритма сердца. Исследованию ВСР предшествовал 5–10 минутный период адаптации к окружающим условиям, в одно и то же время суток (в период с 8-00 до 9-00), натощак, при постоянной температуре 20–22 °С в помещении, в положении лежа на спине. В ходе исследования ВСР пациенту рекомендовалось дышать равномерно и спокойно, не делать глубоких вдохов, не кашлять, не сглатывать слюну [1]. Перед исследованием отменялись физиотерапевтические процедуры, лекарственные препараты с выраженным действием на вегетативную нервную систему. Согласно рекомендациям Европейского общества кардиологов и Североамериканского общества электростимуляции и электрофизиологии (1996) проводили временной и частотный анализ записей RR интервалов с расчетом средней частоты сердечных сокращений (ЧССср), среднеквадратического отклонения интервалов RR от их среднего значения (SDNN, с), триангулярного индекса (TINN, усл. ед.), высокочастотных дыхательных волн (HF, мс²), низкочастотных медленных волн (LF, мс²), очень низкочастотных медленных волн (VLF, мс²) и их отношения (LF/HF), коэффициента корреляции (КК, %) высокочастотных дыхательных волн и пневмограммы. Эпизоды аритмий удалялись автоматизировано подпрограммой.
Статистическая обработка материала проведена непараметрическими методами (критерий знаков, критерийВилкоксона – Манна – Уитни) с помощью пакета прикладных статистических программ EXCEL 7.0 [5].
Полученные результаты
Результаты анализа частотных и спектральных показателей ВСР в исследуемых группах представлены в таблице 1.
Таблица 1
Показатели вариабельности сердечного ритма (М ± m)
|
Показатели |
Са в/т и ср/т |
Са н/т |
|||||
|
исходный |
ч/з 2 недели |
ч/з 3 месяца |
исходный |
ч/з 2 недели |
ч/з 3 месяца |
||
|
TINN, мс2 |
2253,9±11,8 |
977±17,2*# |
1033,6±19,9* |
2791,7±14,9 |
1486,1±23,5* |
1483,1±13,4 |
|
|
VLF, мс2 |
660,4±7,0 |
551,4±8,7 |
528,4±9,0 |
585,2±7,6 |
565,2±15,7* |
523,8±7,0 |
|
|
LF, мс2 |
966,9±9,6 |
557,0±13,8* |
445,1±15,9* |
920,0±11,7 |
460,5±14,2* |
552,1±11,8* |
|
|
HF, мс2 |
906,6±6,9 |
397,4±14,8* |
484,6±11,4* |
1104,5±14,6 |
569,9±18,5* |
612,6±12,6* |
|
|
LF/HF |
0,89±0,3 |
1,28±1,3 |
0,71±0,5 |
0,79±0,2 |
0,85±1,3* |
0,69±0,3 |
|
|
%VLF |
25,1±1,2 |
44,2±3,6 |
33,3±2,8 |
23,1±1,6 |
35,9±2,6* |
28,7±2,4 |
|
|
%LF |
36,5±1,6 |
16,5±1,3* |
19,6±2,0* |
38,3±1,5 |
24,1±2,6* |
29,1±2,5* |
|
|
%HF |
37,7±2,0 |
20,6±3,0* |
24,9±2,5* |
43,6±1,4 |
27,4±2,3* |
25,4±1,9* |
|
|
SДNN, мс2 |
49,7±1,2 |
35,3±1,9*# |
40,3±1,6* |
55,1±1,2 |
48,5±3,5* |
45,1±1,4* |
|
Примечание. * – разница показателей (р< 0,05) внутри групп; # – разница показателей (р < 0,05) между группами.
Среднее значение SDNN в предоперационном периоде в группе пациентов с локализацией рака в верхней и нижней трети пищевода составило 49,7±1,2, в нижней трети пищевода – 55,1±1,2, что значимо не отличалось от показателей нормы. Через 2 недели после операции наблюдалось умеренное снижение SDNN в обеих группах на 29% и 22 % соответственно, что говорит об усилении симпатической регуляции с последующим незначительным подъемом через 3 месяца. Анализ частотной мощности спектра RR выявил значительное снижение TINN на 56,7 % и 46,8 % от исходных значений, в позднем послеоперационном периоде значения TINN оставались по-прежнему низкими.
При анализе соотношения мощности волн различной частоты в спектре ВРС у пациентов с локализацией рака в верхней и средней трети пищевода через 2 недели после оперативного вмешательства отмечено достоверное снижение мощности волн высокой частоты на 56,2 %, в группе с нижней локализацией рака – на 48,5 %, резкое снижение мощности волн барорефлекторной симпатической составляющей спектра на 50 % и 42,4 % соответственно. Пациенты обеих групп имели незначительное снижение в спектре волн очень низкой частоты в раннем послеоперационном периоде и статистически значимое снижение в позднем.
Обсуждение
Как любое заболевание, рак пищевода изменяет процессы адаптации и компенсации в организме больных. Адаптация – процесс поддержания функционального состояния гомеостатических систем и организма в целом, обеспечивающий его сохранение, развитие, работоспособность, максимальную продолжительность жизни в неадекватных условиях среды. Компенсация – один из способов обеспечения приспособления в условиях болезни, когда недостаточность функции пораженных органов или систем восполняется усиленной деятельностью сохранившихся структур организма.
Анализ вариабельности сердечного ритма – это современная методология и технология исследования и оценки состояния регуляторных систем организма, в частности функционального состояния различных отделов вегетативной нервной системы. В последнее время в медицине большое внимание уделяется функциональному состоянию вегетативной нервной системы [2]. Оценка адаптационных резервов больного человека имеет большое значение, поскольку адаптационный потенциал организма во многом влияет на характер течения заболевания, результативность лечебных и реабилитационных процедур. Были выявлены взаимосвязи между изменением функционирования вегетативной нервной системы и смертностью от сердечно-сосудистыхзаболеваний, включая внезапную смерть [6,9,10,11]. Использование ВСР для оценки функционального состояния больных при хирургическом лечении рака пищевода – это возможность прогнозирования ближайших послеоперационных осложнений.
Взаимодействие между ЖКТ и ССС представляет несомненный интерес. Близость расположения с сердцем, общность иннервации способны при переполнении желудка, патологии пищевода по типу висцеро-висцеральных рефлексов провоцировать аритмии, имитировать ИБС. Патология верхнего отдела ЖКТ может приводить к функциональным расстройствам сердечно-сосудистой системы, возникающим опосредованно через ВНС. Большинство клинических проявлений ВСД, включая изменения синусового ритма и отчасти эктопические аритмии, зависит от дисбаланса вегетативных влияний. Проведение хирургического лечения усугубляет ситуацию. Результаты операций на пищеводе далеко не утешительные. Пятилетняя выживаемость по результатам многоцентрового исследования не превышает 5–10 % [7]. Продолжительность жизни данной категории больных зависит от стадии рака и изменений в функциональных системах гомеостатического и поведенческого уровней, регуляторно-адаптивного статуса организма, определяя настоящий и дальнейший ход адаптации, состояние здоровья человека.
Уменьшение значений SDNN (рис. 1)в раннем послеоперационном периоде обычно связывают с усилением симпатической регуляции, подавляющей активность автономного контура.
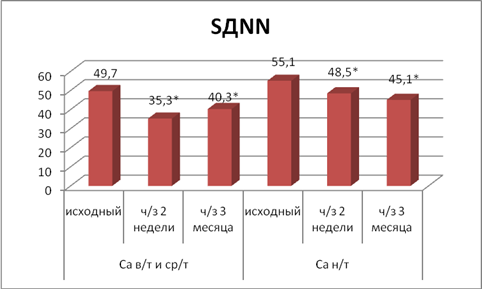
Рис.1.SDNN – среднеквадратическое отклонение интервалов RR от их среднего значения
Снижение SDNN в раннем послеоперационном периоде может быть связано с периоперационной частичной вагуснойденервацией, хирургическим повреждением, с воздействием общего наркоза, с кровопотерей, с увеличением концентрации катехоламинов в крови.
Об этом свидетельствует и резкое падение значений триангулярного индекса через 2 недели после операции, сохраняющееся и через 3 месяца (рис. 2).
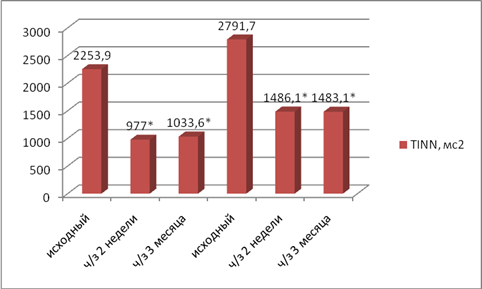
Рис.2.Триангулярный индекс
Снижение SDNN и TINN указывает на падение общего адаптационного резерва организма, включение всех функциональных резервов организма под воздействием центральной регуляции гипоталамо-гипофизарного уровня.
Одним из фундаментальных положений для понимания нервной регуляции синусового ритма является концепция баланса симпатического и парасимпатического отделов вегетативной нервной системы, которая соотносится с тем наблюдением, что в большинстве физиологических условий активация любого из них сопровождается торможением другого отдела иннервации [12].
Статистически значимое уменьшение мощности волн высокой и низкой частоты на фоне увеличения соотношения LF/HF в постоперационном периоде (рис. 3) говорит о переходе в управлении кровообращением на более высокие уровни регуляции центральной нервной системы, централизации механизмов регуляции и напряжении адаптационных механизмов [4].
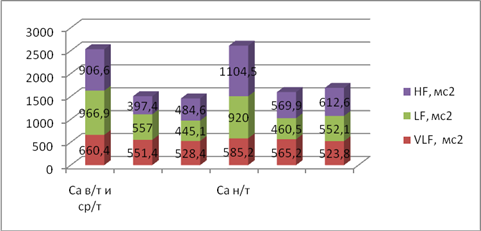
Рис.3. Спектральная составляющая ВСР
Это состояние можно расценить как еще более выраженное напряжение регуляторных механизмов и сдвиг вегетативного баланса в сторону преобладания активности симпатического отдела ВНС с активацией центральных эрготрофных механизмов.
Проведенные исследования демонстрируют, что оперативное лечение является мощным агрессивным фактором.
Состояние вегетативной регуляции сердечного ритма у большинства пациентов, перенесших радикальную операцию по поводу рака пищевода желудка, характеризуется повышением активности симпатического звена автономной нервной системы в покое, что говорит о снижении их адаптационных возможностей.
Степень послеоперационного напряжения автономной нервной системы зависит от локализации рака пищевода. Более высокая степень напряжения регуляторных систем имеет место при локализации рака в верхней и средней трети пищевода.
Рецензенты:Железнов Л.М., д.м.н., профессор, заведующий кафедрой анатомии человекаГБОУ ВПО «Оренбургский государственный медицинский университет» Минздрава России, г. Оренбург;
Чернышева Т.В., д.м.н., профессор кафедры ФППС, ГБОУ ВПО «Оренбургский государственный медицинский университет» Минздрава России,г. Оренбург.
Библиографическая ссылка
Юдаева Ю.А., Иванов К.М., Корнякова А.Р., Юльметова И.Г. ВЕГЕТАТИВНЫЙ СТАТУС БОЛЬНЫХ РАКОМ ПИЩЕВОДА В ПОСЛЕОПЕРАЦИОННОМ ПЕРИОДЕ // Современные проблемы науки и образования. 2015. № 6. ;URL: https://science-education.ru/ru/article/view?id=22919 (дата обращения: 16.05.2026).



