Лецитины (холинфосфоглицериды) в живом организме являются основополагающим веществом для формирования межклеточного пространства, нормального функционирования нервной системы и рабочей деятельности мозговых клеток, служат одним из основных материалов печени. Смесь лецитинов и кефалинов содержится во всех без исключения животных и растительных тканях и почти во всех жидкостях животного организма. Так, из лецитина состоит 50% печени, 1/3 мозговых изолирующих и защитных тканей, окружающих головной и спинной мозг. Лецитины обеспечивает избирательную проницаемость и транспортную функцию клеточных мембран (участвуют в транспорте питательных веществ, витаминов и лекарств к клеткам), являются мощным, естественным для живого организма антиоксидантом и предупреждают образование высокотоксичных свободных радикалов. Транспортная функция лецитинов основана на поверхностно-активных и эмульгирующих свойствах молекул. Функционирование биологических объектов определяется и зависит от молекулярных кооперативных структур [9]. Так, агрегация лецитинов в нормально функционирующем живом организме сопровождается формированием ламеллярных бислоев, внутри которых аккумулируются водорастворимые и жирорастворимые биологически активные вещества и вода (рис. 1).
|
|
|
|
а) |
б) |
Рис. 1. Виды бислоев, сформированных дифильными молекулами лецитина, и включение в них различных биологически активных веществ: а) плоскостная структура бислоя в соответствии с геометрической моделью мицелл;
б) сферическая структура бислоя
Возможно образование не только плоскостных бислоев, но и сферических структур в формате бислоя (рис. 1), в которых водорастворимые биологически активные вещества и вода включаются во внутренний объем сферы, а жирорастворимые биологически активные вещества – в пространство внутри слоя. Именно в такие структуры-каркасы возможно включение различных фармакологически активных веществ и получение современных липосомальных лекарственных форм и ультраэмульсий [2].
Формирование периодических структур, называемых автоволновыми, выявлено для объектов живой и неживой природы. Автоволновые структуры в неживой природе характерны для осадков оксигидратов переходных металлов [5], в живой природе автоволновые образования наблюдаются при дегидратации сыворотки крови или растворов белков [9]. Причем структурная самоорганизация биологических жидкостей имеет свои особенности для нормы и патологических состояний. Лецитин является биологическим объектом, и, как было сказано ранее, в водных растворах могут формироваться коллоидные структуры ламеллярного или сферического строения. Изменение концентрации лецитина или изменение любого другого параметра окружающей среды может привести к периодическому изменению структурных и вязкостных характеристик объекта, содержащего лецитин. Образование ламелей лецитинов в растворе должно определенным образом отражаться на вязкости биологической системы. Если лецитин является компонентом жидкой лекарственной формы, то вязкость данной лекарственной формы при хранении и при попадании в организм человека будет изменяться под воздействием различных температур. При этом возможна перестройка ламеллярных образований. В связи с этим целью данного исследования являлось изучение коллигативных и вязкостных свойств водных растворов лецитина соевого, выявление возможных периодических изменений указанных характеристик и определение границ применимости уравнения Эйнштейна для описания функций вязкости.
Материалы и методы исследования
В качестве объекта исследования использовали водные растворы лецитина соевого (комплекс фосфолипидный гранулированный (лецитин соевый), изготовитель – ООО «Балтик Гранд Сервис», г. Санкт-Петербург). Вязкость растворов определяли при помощи капиллярного вискозиметра серии ВПЖ-2 (диаметр капилляра 0,73 мм, константа капилляра 0,02863 мм2/с2). Термостатирование при различных температурах осуществляли при помощи термостата ТС-1/80 СПУ и холодильной камеры. Определение температуры замерзания проводили на автоматическом криоскопическом осмометре ОМТ–5–02. Предварительно прибор калибровали с помощью серии растворов рабочих стандартных образцов натрия хлорида. Испытуемые растворы лецитина соевого различной концентрации помещали в кювету прибора, погружали в термостат с контролируемой температурой и замораживали. Осмолярность раствора автоматически определяется по фиксированной температуре замерзания.
Результаты и их обсуждение
На рис. 2 представлены графические зависимости динамической
вязкости водных растворов лецитина соевого от концентрации при различных
температурах. Форма кривых кинематической и относительной вязкости аналогична и
на начальных участках (при концентрации лецитина до 2% включительно) может быть
аппроксимирована прямой. Уравнение для аппроксимации изменения относительной
вязкости растворов от концентрации лецитина соевого ![]() аналогично
уравнению Эйнштейна для описания относительной вязкости растворов
высокомолекулярных веществ, не взаимодействующих с молекулами растворителя
(табл. 1).
аналогично
уравнению Эйнштейна для описания относительной вязкости растворов
высокомолекулярных веществ, не взаимодействующих с молекулами растворителя
(табл. 1).
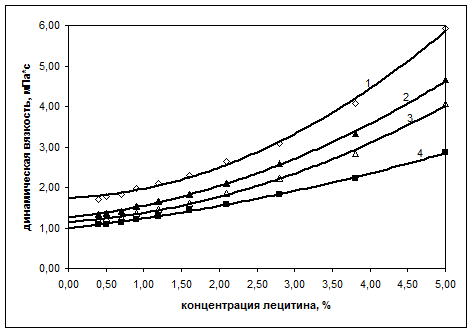
Рис. 2. Зависимость динамической вязкости водных растворов лецитина соевого
от концентрации при различных температурах (1–8 °С; 2–16 °С; 3–25 °С; 4–30 °С)
Близость коэффициента ![]() к
единице свидетельствует о применимости классического уравнения Эйнштейна к
описанию вязкости водных растворов лецитина в данном интервале концентраций.
Указанные прямолинейные участки кривых относительной вязкости лецитина при
различных температурах практически совпадают. Графическое изображение
концентрационных срезов кинематической вязкости водных растворов лецитина (рис.
3) подтверждает вывод о том, что относительная вязкость водных растворов
лецитина практически не зависит от температуры в интервале от 8 до 30 °С
при концентрации лецитина соевого не выше 2%. Угловые коэффициенты
аппроксимирующих линейных зависимостей 1, 2 и 3 (рис. 3) составляют величину
порядка -0,03 – -0,04 с ошибкой определения, сопоставимой со значениями данных
коэффициентов. Это означает, что угловые коэффициенты указанных зависимостей
незначимо отличаются от нуля.
к
единице свидетельствует о применимости классического уравнения Эйнштейна к
описанию вязкости водных растворов лецитина в данном интервале концентраций.
Указанные прямолинейные участки кривых относительной вязкости лецитина при
различных температурах практически совпадают. Графическое изображение
концентрационных срезов кинематической вязкости водных растворов лецитина (рис.
3) подтверждает вывод о том, что относительная вязкость водных растворов
лецитина практически не зависит от температуры в интервале от 8 до 30 °С
при концентрации лецитина соевого не выше 2%. Угловые коэффициенты
аппроксимирующих линейных зависимостей 1, 2 и 3 (рис. 3) составляют величину
порядка -0,03 – -0,04 с ошибкой определения, сопоставимой со значениями данных
коэффициентов. Это означает, что угловые коэффициенты указанных зависимостей
незначимо отличаются от нуля.
Таблица 1
Результаты аналитической аппроксимации значений относительной вязкости водных
растворов
лецитина (С ≤ 2,0%) при различных температурах по уравнению ![]()
|
Температура, °С |
Коэффициент
|
Коэффициент
|
Коэффициент корреляции |
|
30 |
1,078 |
33,346 |
|
|
25 |
1,033 |
38,327 |
|
|
16 |
0,998 |
40,066 |
|
|
8 |
1,069 |
35,391 |
|
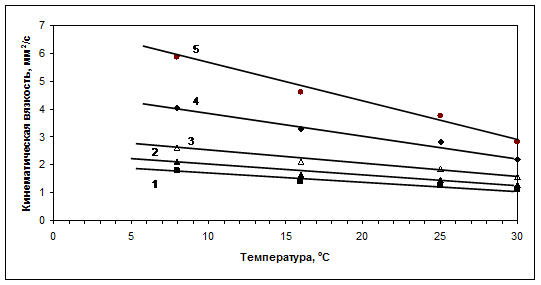
Рис. 3. Концентрационные срезы изменения кинематической вязкости водных растворов лецитина соевого от температуры (1 – 0,5%-ный раствор (R=-0,97); 2 – 1,2%-ный раствор (R=-0,98); 3 – 2%-ный раствор; 4 – 3,8%-ный раствор (R=-0,99); 5 – 5%-ный раствор(R=-0,99))
При концентрациях лецитина выше 2,5% отклонения концентрационных зависимостей относительной вязкости от линейного закона становятся существенными, и экспериментальные данные при различных температурах удовлетворительно аппроксимируются полиномами второй степени (табл. 2). Линия концентрационного среза 5 для концентрации лецитина 5% имеет угловой коэффициент, значимо отличающийся от нуля (-0,13±0,04).
Таблица 2
Значения полиномиальных коэффициентов для зависимостей относительной вязкости
водных растворов лецитина (С ≥ 2,5%) при различных температурах
|
Температура, °С |
Коэффициенты
полинома второй степени |
||
|
a |
b |
c |
|
|
30 |
1,129 |
23,305 |
362,827 |
|
25 |
1,158 |
13,864 |
875,665 |
|
16 |
1,099 |
19,204 |
794,961 |
|
8 |
1,222 |
6,025 |
1042 |
Ламеллярные структурные образования, характерные для
агрегированного лецитина, имеют выраженную анизодиаметричность, что находит
отражение в экспериментально найденных значениях коэффициента ![]() - они на порядок превышают значения,
найденные для белков со сферической глобулярной конформацией молекул [1; 3; 4;
6]. Если для водных растворов альбумина и интерферона лейкоцитарного
человеческого
- они на порядок превышают значения,
найденные для белков со сферической глобулярной конформацией молекул [1; 3; 4;
6]. Если для водных растворов альбумина и интерферона лейкоцитарного
человеческого ![]() , то для водных растворов
лецитина соевого
, то для водных растворов
лецитина соевого ![]() находится в интервале от 30 до
40. Причем величина коэффициента
находится в интервале от 30 до
40. Причем величина коэффициента ![]() претерпевает
некоторые изменения в изученном интервале температур 8–30 °С:
найденные значения
претерпевает
некоторые изменения в изученном интервале температур 8–30 °С:
найденные значения ![]() образуют полупериод
периодической кривой (рис. 4). Поскольку изучен небольшой интервал температур,
данный вопрос по периодическому изменению свойств требует дальнейших
исследований.
образуют полупериод
периодической кривой (рис. 4). Поскольку изучен небольшой интервал температур,
данный вопрос по периодическому изменению свойств требует дальнейших
исследований.
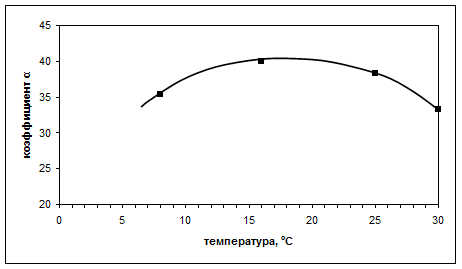
Рис. 4. Влияние температуры на коэффициент α, входящий в уравнение Эйнштейна
Выводы
1. Определены границы применимости уравнения Эйнштейна для описания концентрационных и температурных зависимостей вязкости растворов лецитина соевого. Статистически установлена линейная зависимость между относительной вязкостью раствора и массовой долей лецитина соевого при концентрации менее 2,5%.
2. Полиномиальная зависимость относительной вязкости от концентрации найдена для диапазона концентраций лецитина соевого 2,5–5%.
3. Подтвержден вывод о том, что в биологических системах, включающих молекулы белков и лецитина, в значения коэффициентов в уравнении Эйнштейна заложена не только форма частиц вещества в растворе, но и способность молекул к агрегации, ассоциации и сольватации.
Рецензенты:Смолко В.А., д.т.н., профессор, ФГБОУ ВПО «Южно-Уральский государственный университет» (национальный исследовательский университет), г. Челябинск;
Колесников О.Л., д.м.н., профессор, ГБОУ ВПО «Южно-Уральский государственный медицинский университет», г. Челябинск.
Библиографическая ссылка
Миняева О.А., Зацепина М.Н., Сидорченко А.С. О КОЛЛИГАТИВНЫХ И ВЯЗКОСТНЫХ СВОЙСТВАХ ВОДНЫХ РАСТВОРОВ ЛЕЦИТИНА // Современные проблемы науки и образования. 2015. № 1-2. ;URL: https://science-education.ru/ru/article/view?id=19873 (дата обращения: 16.05.2026).





