Репарация костной ткани является одной из важнейших проблем регенеративной медицины, особенно травматологии, реконструктивной хирургии, стоматологии [3]. Ежегодно в мире травматизм, связанный с переломами костей, постоянно растет. При этом большой проблемой является высокая степень инвалидизации, закономерно увеличивающаяся с возрастом пострадавших [2]. В связи с этим перед современной медициной возникает задача стимуляции посттравматической регенерации костной ткани, особенно при ограничении собственных компенсаторных реакций организма, обусловленном различными этиологическими факторами. Решение данной задачи может осуществляться в двух направлениях. Во-первых, путем активации защитно-приспособительных резервов организма в целом, что достигается использованием витаминов, анаболических гормонов и ряда других препаратов. Однако при этом может возникнуть проблема недостаточной величины самих компенсаторных резервов, превысить которую в этом случае невозможно [1]. Другой путь – местная активация репаративной регенерации путем использования стимуляторов регенерации – репарантов, к которым относятся факторы роста, в частности фактор роста фибробластов (ФРФ) [5].
В 2011 г. на кафедре травматологии и ортопедии Оренбургской государственной медицинской академии разработан препарат «Винфар», содержащий ФРФ (Патент № 2427644 от 27.08.2011), выделенный из метаболитов штамма бактерий Bacillus subtilis 804.
Цель исследования – изучение особенностей репаративного гистогенеза костной ткани в условиях открытого диафизарного перелома длинной трубчатой кости крыс при использовании препарата «Винфар».
Материал и методы исследования. Экспериментальное исследование проведено на 70 половозрелых крысах самцах линии «Вистар». Все исследования на животных были выполнены в соответствии с «Правилами проведения работ с использованием экспериментальных животных» (приказ Минвуза СССР от 13.11.1984 г. № 724). Животным под ингаляционным наркозом формировали открытый поперечный перелом средней трети диафиза левой большеберцовой кости. В опытной группе (ОГ) животным в область перелома на 1-е и 2-е сутки эксперимента вводили по 0,5 мл препарата «Винфар», в контрольной группе (КГ) – 0,5 мл физраствора. Осуществлена естественная иммобилизация посредством сохранившей целостность малоберцовой кости. Животных выводили из опыта на 3-и, 7-е, 14-е, 21-е, 44-е и 61-е сутки. Фрагменты отломков костей с костной мозолью фиксировали в 10%-ном нейтральном формалине (на фосфатном буфере) с последующей декальцинацией смесью: Трилон Б + 40% NaOH + Н20(дист.), обезвоживанием в спиртах возрастающей крепости, заливкой кусочков парафином — целлоидином и изготовлением гистосрезов толщиной 5,0 мкм. Исследования проводили с использованием гистологических, иммуногистохимических методов и морфометрии. Гистологическое исследование включало окраску гематоксилином Майера и эозином. При проведении иммуногистохимических методов исследования для выявления экспрессии CD34 (маркер эндотелиоцитов), CD68 (маркер макрофагов, хондро- и остеокластов) и collagen I использовались соответственно антитела anti-CD34 и anti-CD68 («SPRING Bioscience», США), anti-Collagene I Type («GeneTex», США). Используемая система детекции — Reveal Polyvalent HRP – DAB Detection System («SPRING Bioscience», США). Подсчет клеток производился в абсолютных значениях (абсолютная численная плотность — АЧП) при общем увеличении х300 на площади соответствующего среза (поля зрения – п.з.), равной 0,077 мм² минимум в 5 полях зрения для каждого показателя. Подсчет площади коллагеновых волокон производился в относительных значениях (относительная объёмная плотность - ООП), как отношение площади коллагена I типа к общей площади тканевых элементов в пределах исследуемого гистосреза на 1 микрофотографии (равной 1 полю зрения) при увеличении х300 минимум в 5 полях зрения (микрофотографий) для каждого показателя. При проведении статистической обработки результатов вычисляли средние значения абсолютных и относительных величин (M), ошибки средних величин (m) и t-критерий Стьюдента. Различия считали достоверно значимыми при уровне вероятности р<0,05.
Результаты исследования и их обсуждение. На 3-и сутки у животных контрольной группы (КГ) в интермедиарной зоне перелома выражена воспалительная реакция: отек, лейкоцитарная инфильтрация, появление грануляционной ткани, отсутствие остеокластов. Пролиферирующие клетки надкостницы начинают дифференцироваться в хондробласты (АЧП 101,0±8,0/п.з.), формируя тонкий слой периостальной костной мозоли толщиной 0,26±0,015 мм. Признаки формирования эндостальной костной мозоли отсутствуют.
На 3-и сутки у животных опытной группы (ОГ) в области интермедиарной мозоли воспалительная реакция нивелирована, имеется обилие волокнистого матрикса, появившиеся остеокласты формируют лакуны резорбции в интермедиарной зоне костных отломков. На фоне развитой грануляционной ткани заметна выраженная пролиферация клеток мезенхимы с началом дифференцировки фибробластоподобных клеток предшественников в хондробласты и остеобласты. Сформирована толстая периостальная костная мозоль (толщина 0,79±0,020 мм), хрящ которой в центральных отделах состоит преимущественно из хондроцитов (АЧП 31,0±4/п.з.), часть которых в состоянии вакуолярной дистрофии и лизиса (деградация хряща). В периферических отделах формирующейся периостальной мозоли число остеобластов достигает 66,0±5,0/п.з., а остеоцитов – 10,0±2,0/п.з., т.е. преобладают процессы остеогенной дифференцировки фибробластоподобных клеток-предшественников. В эндостальной зоне перелома признаки пролиферации клеток эндоста с миграцией в интермедиарную зону, на границе с которой формируется тонкая прослойка хряща. Заметна реакция остеокластов (АЧП 3,0±1,0/п.з.). Эндостальная костная мозоль в центральных отделах представлена значительным числом пролиферирующих фибробластоподобных клеток-предшественников (АЧП 411,0±25,0/п.з.) с отсутствием признаков хондро- и/или остеогенной дифференцировки. Число эндотелиоцитов (АЧП 25,0±3,0/п.з.) двукратно превосходит этот же показатель в группе контроля (АЧП 13,0±2,0/п.з.). Важными отличиями гистоархитектоники места перелома в ОГ на 3-и сутки являются более выраженная реакция фибробластов в зоне перелома, появление в периферических частях хрящевой манжетки участков остеоидной ткани. Характерно, что в ОГ в костных отломках остеоциты сохранены в большей степени, чем в КГ, где большинство костных лакун запустевшие.
На 7-е сутки в контроле в интермедиарной зоне перелома на фоне развитой грануляционной ткани заметна пролиферация клеток мезенхимы (АЧП 195,0±13,0/п.з.), в небольшом количестве появляется волокнистый матрикс (ООП коллагена I типа 4,83±1,02%) и небольшие группы остеогенных клеток (АЧП остеобластов и остеоцитов 33,0±5,0/п.з.). Остеокласты единичны (АЧП 1-2/п.з.), резорбция костных отломков не выражена. Толстый хрящ периостальной костной мозоли (толщина 1,25±0,14 мм) состоит из хондробластов и хондроцитов (АЧП хондробластов и хондроцитов 165,0±15,0/п.з.), незначительная часть которых в состоянии вакуолярной дистрофии и лизиса. В эндостальной зоне перелома признаки пролиферации клеток эндоста с дифференцировкой преимущественно в остеобласты (АЧП остеобластов 33,0±4,0/п.з.) и формированием незрелой ретикулофиброзной костной ткани, частично заполняющей костномозговой канал в области костных отломков.
На 7-е сутки в опыте со стороны периостальных зон перелома начинает формироваться интермедиарная мозоль, состоящая из хряща, клеточный состав которого представлен небольшим числом хондроцитов (АЧП 25,0±3,0/п.з.). Центральные же отделы интермедиарной зоны содержат редуцирующуюся грануляционную ткань с обилием волокнистого матрикса и пролиферирующих остеогенных клеток (АЧП остеобластов 173,0±17,0/п.з.). Периостальная костная мозоль деградирует за счет лизиса хондроцитов и формирования хондрокластами очагов резорбции с замещением хряща на хорошо васкуляризованную волокнистую соединительную ткань (АЧП эндотелиоцитов 25,0±3,0/п.з.) с формированием остеогенных островков ретикулофиброзной кости. Эндостальная костная мозоль представлена деградирующим хрящом с формированием костных балок, состоящих из остеобластов и незрелого внеклеточного остеоидного матрикса. Остеокласты (АЧП 5,0±2,0/п.з.) формируют многочисленные лакуны резорбции.
На 14-е сутки в контроле в интермедиарной зоне перелома на фоне остатков редуцирующейся грануляционной ткани увеличивается ООП волокнистого матрикса (ООП коллагена I типа 9,24±2,14%) с группами пролиферирующих остеогенных клеток (АЧП остеобластов 93,0±8,0/п.з.). Остеокласты (АЧП 3,0±1,0/п.з.) активно участвуют в резорбции костных отломков. Периостальная костная мозоль деградирует за счет лизиса хондроцитов (АЧП 44,0±5,0/п.з.) и формирования хондрокластами очагов резорбции с замещением хряща на волокнистую соединительную ткань. Небольшие тяжи хряща периостальной костной мозоли проникают в интермедиарную зону, таким способом образуя хрящевой компонент интермедиарной костной мозоли. На данном сроке в КГ отмечаем и наибольшую активность хондрокластов (в ОГ она наблюдалась уже на 7-е сутки), обеспечивающих резорбцию хрящевой ткани периостальной мозоли. Эндостальная костная мозоль представлена деградирующим хрящом и формирующимися костными балками, состоящими преимущественно из остеобластов (АЧП 79,0±6,0/п.з.) и незрелого внеклеточного остеоидного матрикса (ООП коллагена I типа 3,33±1,01%). Эндостальная костная мозоль глубоко заполняет весь просвет костномозгового канала и переходит в интермедиарную мозоль.
На 14-е сутки в опытной группе интермедиарная костная мозоль представлена остатками деградирующего хряща и очагами формирования ретикулофиброзной кости, состоящими преимущественно из остеобластов (АЧП 108,0±9,0/п.з.), а также значительного числа остеоцитов (АЧП 91,0±6,0/п.з.) и незрелого внеклеточного остеоидного матрикса (ООП коллагена I типа 15,61±2,89%). Периостальная костная мозоль, так же как и периферические отделы интермедиарной, состоит из остатков деградирующего хряща и очагов формирующейся незрелой ретикулофиброзной кости, достигая на этом сроке максимальной толщины 1,82±0,54 мм. Эндостальная костная мозоль представлена сформированными костными балками, состоящими из остеобластов (АЧП 95,0±7,0/п.з.) и уже значительного числа остеоцитов (АЧП 55,0±4,0/п.з.). ООП коллагена I типа внеклеточного остеоидного матрикса составляет 6,97±1,52%. При этом новообразованные балки эндостальной мозоли активно разрушаются многочисленными остеокластами (АЧП 7,0±2,0/п.з.) за счет формирования лакун резорбции, т.е. уже на этом сроке инициируется процесс формирования костномозгового канала с появлением пока еще единичных гемопоэтических островков клеток красного костного мозга (АЧП 25,0±7,0/п.з.).
На 21-е сутки в группе контроля интермедиарная костная мозоль по-прежнему представлена очагами редуцирующейся грануляционной ткани и широкими участками волокнистого матрикса (ООП коллагена I типа 11,25±2,12%) с группами пролиферирующих клеток преимущественно фибробластического дифферона (АЧП 27,0±4,0/п.з.). Периостальная костная мозоль, так же как и периферические отделы интермедиарной, представлена остатками деградирующего хряща (АЧП хондробластов и хондроцитов 65,0±7,0/п.з.) и очагами формирования незрелой ретикулофиброзной кости (АЧП остеобластов и остеоцитов 140,0±11,0/п.з.). При этом хрящ дистальных отделов периостальной мозоли практически полностью замещен трабекулами ретикулофиброзной кости. Толщина периостальной мозоли продолжает увеличиваться, достигая на этом сроке 2,48±0,61 мм, что объясняется отсутствием стабильной мобилизирующей функции костной мозоли. Широкую эндостальную костную мозоль формируют костные балки, состоящие преимущественно из остеобластов (АЧП 83,0±7,0/п.з.) и небольшого числа остеоцитов (АЧП 9,0±2,0/п.з.), замурованных в остеоидный матрикс (ООП коллагена I типа 8,47±1,63%). На этом инициируется процесс формирования костномозгового канала с появлением немногочисленных гемопоэтических островков клеток красного костного мозга (АЧП 47,0±9,0/п.з.).
На 21-е сутки у животных ОГ вся площадь (периферические и центральные отделы) интермедиарной костной мозоли представлена остатками деградирующего хряща и очагами формирования ретикулофиброзной кости, состоящими преимущественно из остеобластов (АЧП 155,0±12,0/п.з.) и незрелого внеклеточного остеоидного матрикса (ООП коллагена I типа 20,7±3,71%). Периостальная костная мозоль представлена широкими полями ретикулофиброзной кости и лишь небольшими очагами деградирующего хряща (АЧП хондроцитов 4,0±1,0/п.з.). Толщина периостальной мозоли (1,802±0,25 мм) сохраняет значения, сопоставимые с предыдущим сроком, что означает стабильную мобилизирующую функцию костной мозоли при данной толщине уже на этом сроке. Эндостальная костная мозоль представлена узкой полоской сформированной костными балками грубоволокнистой кости (ООП коллагена I типа 19,24±3,25%) на границе с интермедиарной зоной. При этом новообразованные балки эндостальной мозоли активно разрушаются остеокластами (АЧП 5,0±2,0/п.з.), за счет формирования лакун резорбции, т.е. прогрессирует процесс формирования костномозгового канала с появлением уже многочисленных гемопоэтических островков клеток красного костного мозга (АЧП 147,0±18,0/п.з.).
На 44-е сутки у крыс КГ интермедиарная костная мозоль все еще включает небольшие очаги деградирующего хряща (АЧП хондробластов и хондроцитов 40,0±5,0/п.з.) на фоне формирующихся балок ретикулофиброзной кости, состоящих из остеобластов (АЧП 85,0±8,0/п.з.) и остеоцитов (АЧП 105,0±11,0/п.з.), замурованных в остеоидный матрикс (ООП коллагена I типа 21,23±4,13%). Периостальная костная мозоль истончена (толщина 0,27±0,08 мм) и представлена узкими полями немногочисленных балок грубоволокнистой кости, активно подвергающихся резорбции остеокластами (АЧП 4,0±1,0/п.з.) и лишь небольшим участком деградирующего хряща в центре консолидированного перелома. Эндостальная костная мозоль представлена подвергающимися резорбции все еще многочисленными широкими костными балками ретикулофиброзной кости, глубоко пронизывающими костномозговой канал в дистальном направлении.
На 44-е сутки в опытной группе намечается ремоделирование интермедиарной костной мозоли в диафиз трубчатой кости: из хаотично расположенных на более ранних сроках балок грубоволокнистой кости начинает формироваться компактное и губчатое вещество. Периостальная костная мозоль (толщина 0,102±0,05 мм), сохранившись небольшим участком на границе с интермедиарной костной мозолью, на остальном протяжении уже преобразована в надкостницу (рис. 1) и состоит из хорошо различимых внутреннего (остеогенного) и наружного (фиброзного) (АЧП фибробластов 78,0±6,0/п.з.) слоев. Эндостальная костная мозоль значительной частью редуцирована и представлена немногочисленными узкими костными балками ретикулофиброзной кости лишь на границе с интермедиарной зоной преимущественно у эндоста и формирующимся костномозговым каналом, представленным значительным числом клеток красного костного мозга (АЧП 210,0±16,0/п.з.) в составе гемопоэтических островков (рис. 2).
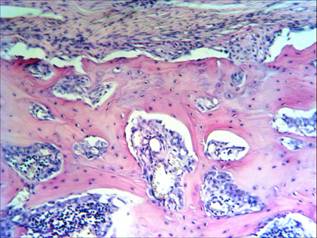
Рис. 1. Опытная группа. Область перелома большеберцовой кости (интермедиарная костная мозоль), 44-е сутки. Окраска гематоксилин-эозин. Об. ув. х150
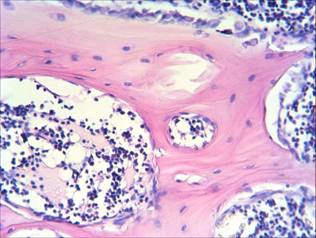
Рис. 2. Опытная группа. Область перелома большеберцовой кости (эндостальная костная мозоль), 44-е сутки. Окраска гематоксилин-эозин. Об. ув. х300
На 61-е сутки в группе контроля интермедиарная костная мозоль представлена разросшейся ретикулофиброзной костной тканью, местами с еще сохраненными мелкими очагами деградирующего гиалинового хряща (АЧП хондроцитов 14,0±3,0/п.з.) и немногочисленными костномозговыми полостями без признаков формирования костномозгового канала. Эндостальная костная мозоль представлена немногочисленными, но широкими костными балками грубоволокнистой кости преимущественно на границе с интермедиарной зоной и у эндоста. На месте редуцирующейся эндостальной мозоли формируется костномозговой канал с АЧП 251,0±19,0/п.з. клеток красного костного мозга.
На 61-е сутки у животных опытной группы наблюдается полная консолидация перелома с полноценной перестройкой костной мозоли в диафиз трубчатой кости с органотипичным строением периоста, эндоста, а также преимущественно пластинчатого строения кости с разделением на компактное и губчатое вещество. Губчатое вещество восстановленного костномозгового канала на месте бывшей эндостальной костной мозоли отличается от губчатого вещества диафиза кости вне зоны перелома лишь большим числом и большей толщиной костных балок (АЧП остеобластов и остеоцитов 42,0±5,0/п.з.).
Заключение. Применение препарата «Винфар» лимитирует выраженность воспалительного процесса (вероятно, в связи с наличием антимикробных веществ в составе метаболитов Bacillus subtilis 804), сокращая фазу ранних посттравматических изменений. В обеих сравниваемых группах сращение отломков кости проходит хрящевую стадию, но в ОГ наряду с формированием более массивной хрящевой манжетки уже к 3-м суткам наблюдаем и раннюю резорбцию хряща (14-е сутки). Благодаря своевременной и надежной фиксации отломков периостальной мозолью в ОГ интермедиарная мозоль начинает формироваться на 7-е сутки (в КГ – на 14-е сутки), а образование костномозгового канала в ОГ отмечаем с 14-х суток (в КГ – с 21-х суток). В ОГ уже на 3-и сутки наблюдается значительная активация неоангиогенеза (АЧП эндотелиоцитов 42,0±6,0/п.з., а КГ – 7±2,0/п.з.), что обеспечивает не только более ранние сроки образования костной мозоли, но и преобладание остеобластического типа дивергентной дифференцировки в междифферонной гетероморфии за счет создания лучших условий оксигенации по сравнению с контролем [4].
Таким образом, консолидация перелома диафиза большеберцовой кости при применении препарата «Винфар» происходит в более ранние сроки, что, вероятно, обусловлено мощным ангиогенным воздействием входящего в его состав ФРФ, а также влиянием на пролиферативную активность хондрогенных и остеогенных элементов.
Рецензенты:
Шевлюк Н. Н., д.б.н., профессор, профессор кафедры гистологии, цитологии и эмбриологии Оренбургского государственного медицинского университета, г. Оренбург;
Сафронов А.А., д.м.н., профессор, заведующий кафедрой травматологии и ортопедии Оренбургского государственного медицинского университета, г. Оренбург.
Библиографическая ссылка
Миханов В.А., Полякова В.С., Копылов В.А., Мхитарян Е.Е., Мещеряков К.Н., Бакаева Н.Р., Шурыгина Е.И. РЕПАРАТИВНЫЙ ГИСТОГЕНЕЗ КОСТНОЙ ТКАНИ В УСЛОВИЯХ ОТКРЫТОГО ПЕРЕЛОМА ДИАФИЗА ДЛИННОЙ ТРУБЧАТОЙ КОСТИ У КРЫС ПРИ ИСПОЛЬЗОВАНИИ ПРЕПАРАТА «ВИНФАР» // Современные проблемы науки и образования. 2015. № 3. ;URL: https://science-education.ru/ru/article/view?id=19689 (дата обращения: 04.04.2026).



