Проблема коморбидности при сердечно-сосудистых заболеваниях в настоящее время особенно актуальна. В частности, по литературным данным, частота сочетания ишемической болезни сердца (ИБС) и хронической обструктивной болезни легких (ХОБЛ) составляет от 12,6 до 61,7%, а летальность при их сочетании составляет более 50% [2,4]. В основе тесных взаимосвязей ИБС и ХОБЛ предполагается общность факторов риска: табакокурение, избыточный вес, обструктивное апноэ сна и др. и общность патогенетических механизмов, таких как оксидантный стресс, гипоксемия, эндотелиальная дисфункция, цитокиновый дисбаланс[1].
Коморбидность формирует особенности клинических проявлений заболеваний, может снижать эффективность терапии, ухудшать прогноз, что требует новых подходов к лечебной тактике таких больных. Результаты многочисленных клинических исследований показали органопротективное действие и влияние на прогноз ингибиторов ангиотензин-превращающего фермента (ИАПФ) при АГ, ИБС, ХСН.У больных ИБС, АГ в сочетании с ХОБЛ препаратами выбора рассматриваются антагонисты кальциевых каналов (АКК), которые также обладают значимыми органопротективными эффектами и не оказывают отрицательного влияния на бронхиальную проходимость. В литературе имеются разноречивые мнения относительно применения АКК у больных ХСН. Установлено, что использование АКК может уменьшать выраженность симптомов декомпенсации ХСН, но с другой стороны, может привести к негативным эффектам, связанным с гиперактивацией нейрогормонов и задержкой жидкости. При этом результаты исследований V-HeFTIII (1997) и PRAISEI и II (1998) показали, что применение АКК у больных ХСН в комплексной терапии не ухудшает прогноз [3]. Поиск наиболее оптимальных лекарственных комбинаций при сочетании ИБС, АГ, ХСН и ХОБЛ, оценка их влияния на метаболический профиль, функциональное состояние почек представляет важную задачу, что и явилось целью нашей работы.
Цель исследования: сравнить влияние фиксированной комбинации периндоприла и амлодипина со свободной комбинацией эналаприла и амлодипинана течение ХОБЛ, метаболический профиль, функциональное состояние почек у больных ИБС и АГ, осложненной ХСН.
Материал и методы: обследовано 60 больных ИБС в сочетании с АГ и ХОБЛ, из них – 28 (46,6%) мужчин и 32 (53,3%) женщины. Критериями включения в исследование явились: возраст пациента от 30 до 65 лет; подтвержденная стабильная ИБС по данным клинической картины, анамнеза, амбулаторных карт, нагрузочных тестов и/или суточного мониторирования ЭКГ; подтвержденная гипертоническая болезнь III стадии; подтвержденная стабильная ХСН II-IIIфункционального класса (ФК) по клиническим симптомам/признакам, наличию дисфункции сердца при проведении ЭхоКГ и/или увеличению уровня N-терминального фрагмента натрийуретического пептида (NT-proBNP); подтвержденная ХОБЛ средней и тяжелой степени, подписанное информированное согласие больного на участие в исследовании. Критериями исключения из исследования явились: вторичные формы артериальной гипертонии; вторичная стенокардия; острый коронарный синдром; ХСН выше IIБ стадии и III ФК; ХСН другой этиологии; фибрилляция предсердий; желудочковые нарушения ритма III и выше градации по Lown и Wolf; бронхиальная астма; хроническое легочное сердце; онкологические заболевания; острые воспалительные и инфекционные заболевания; противопоказания к назначению ИАПФ, дигидропиридиновых АКК; психические заболевания, препятствующие подписанию информированного согласия и дальнейшему адекватному контакту с больным в период наблюдения.
Средний возраст обследованных больных составил 55,3±7,8 лет. Продолжительность ИБС в среднем была 5,8±3,5 лет, средний ФКстенокардии – 2,69±0,59. 7 (11,7%) пациентов перенесли инфаркт миокарда, у 3 (5,0%) было проведено коронарное шунтирование. Анамнестическая длительность ХСН составила в среднем 4,8±2,2 лет, средний ФК ХСН - 2,64±0,48. Анамнестическая длительность ХОБЛ составила 6,0±2,3 лет. Средняя степень тяжести ХОБЛ была зарегистрирована у 42 (70,0%), тяжелая – у 18 (30%) больных, степень тяжести ХОБЛ в среднем составила 2,38±0,49. 35 (58,3%) человек из обследованных были курильщиками. Среднее отношение объема форсированного выдоха в первую секунду (ОФВ1) к форсированной жизненной емкости легких (ФЖЕЛ) составило 0,61+0,11. Средний постбронходилатационный ОФВ1 был равен 68,7+17,5%. У 7 (11,7%)обследованных больных имелся сахарный диабет 2 типа, 7 пациентов (3,3%) перенесли инсульт или транзиторную ишемическую атаку.
До включения в исследование 36 (60,0%) больных постоянно принимали ИАПФ, 3 (5,0%) пациента – антагонисты рецепторов ангиотензинаII (АРА), 24 (40,0%) – тиазидовые или петлевые диуретики, 14 (23,3%) – спиронолактон, 31 (51,6%) – антиагреганты, 18 (30,0%) – статины, 41 (68,3%) – антиангинальные препараты (нитраты, триметазидин), 20 (33,3%) – АКК, 2 (3,3%) пациента получалисахароснижающие препараты, 17 (28,3%) – ингаляционные глюкокортикоиды, 22 (36,7%) – ипратропия бромид, 36 (60,0%) – тиотропия бромид.
В зависимости от выбранного варианта антигипертензивной терапии в комплексном лечении методом простой рандомизации было выделено 2 группы больных по 30 человек: больным первой группы были назначены периндоприл и амлодипин в фиксированной комбинации, пациентам второй группы – эналаприл в свободной комбинации с амлодипином. Препараты исследования назначались после отмены исходных ИАПФ, АРА, АКК без отмывочного периода. Доза препаратов определялась индивидуально в зависимости от их переносимости и динамики артериального давления (АД). Длительность терапии составила 6 месяцев. При недостижении целевого уровня АД через 4 недели в обеих группах добавляли или увеличивали дозу третьего препарата – тиазидового или тиазидоподобного диуретика.
Исходно группы были сопоставимы по полу, возрасту, тяжести стенокардии и ХСН, исходному уровню АД, структуре и тяжести коморбидных заболеваний (табл.1), лабораторно-инструментальным показателям (табл.2), структуре сопутствующей терапии (табл.3).
Таблица 1
Сравнительная характеристика клинико-анамнестических показателей по группам обследуемых (n=60)
|
Показатель |
Первая группа (фиксированная комбинация П+А, n=30) |
Вторая группа (нефиксированная комбинация Э+А, n=30) |
р |
|
Пол, абс.%, ж/м |
17/56,7; 13/43,3 |
15/50,0; 15/50,0 |
0,947/0,934 |
|
Возраст, лет |
55,50±7,97 |
54,24±8,02 |
0,547 |
|
Курение, абс./% |
16/53,3 |
19/63,3 |
0,849 |
|
ИМТ, кг/м2 |
29,27±4,10 |
26,96±4,71 |
0,152 |
|
ИМ в анамнезе, абс./% |
2/6,7 |
5/16,7 |
0,500 |
|
КШ в анамнезе, абс./% |
1/3,3 |
2/6,7 |
0,978 |
|
СД 2 типа, абс./% |
0/0 |
2/6,7 |
0,501 |
|
Инсульт/ТИА в анамнезе, абс./% |
3/9,8 |
4/13,3 |
0,967 |
|
Длительность АГ, лет |
10,52+4,86 |
11,23+5,14 |
0,916 |
|
Длительность ХСН, лет |
6,58±3,23 |
6,67±3,3 |
0,915 |
|
Длительность ИБС, лет |
6,20+3,21 |
7,32+4,92 |
0,301 |
|
Длительность ХОБЛ, лет |
6,87±2,75 |
5,93±2,32 |
0,894 |
|
Офисное САД, мм рт.ст. |
162,3+18,4 |
168,1+14,6 |
0,993 |
|
Офисное ДАД, мм рт.ст. |
100,5+12,8 |
98,6+9,7 |
0,635 |
|
САД среднесут., мм рт.ст. |
139,1±7,64 |
135,8±13,6 |
0,330 |
|
ДАД среднесут.,мм рт.ст. |
89,9±8,0 |
86,2±8,5 |
0,139 |
|
ЧСС офисная, уд/мин |
82,11±12,65 |
86,32±11,40 |
0,135 |
Таблица 2
Сравнительная характеристика исходных лабораторно-инструментальных показателей по группам обследуемых (n=60)
|
Показатель |
Первая группа (фиксированная комбинация П+А, n=30) |
Вторая группа (нефиксированная комбинация Э+А, n=30) |
р |
|
ФВ ЛЖ, % |
63,02±5,29 |
64,21±7,64 |
0,474 |
|
Е/А |
0,89[0,41;1,13] |
0,94[0,51;1,62] |
0,525 |
|
NT-proBNP, фмоль/л |
8,67[0,11;15,15] |
6,89[0,19;28,73] |
0,840 |
|
БронходилатационныйОФВ1, % |
63,41±11,53 |
64,54±9,82 |
0,684 |
|
Бронходилатационноеотношение ОФВ1/ФЖЕЛ |
68,6±8,40 |
64,23±9,66 |
|
|
Креатинин сыворотки, мкмоль/л |
88,65±15,21 |
94,07±19,16 |
0,230 |
|
СКФ (MDRD), мл/мин/1,73м2 |
68,72+12,63 |
74,03+14,35 |
0,086 |
|
СКФ (MDRD)<60 мл/мин/1,73м2, абс./% |
9(30,0) |
7(23,3) |
0,157 |
|
Глюкоза плазмы крови натощак, ммоль/л |
5,24±1,20 |
4,82±0,63 |
0,890 |
|
ОХС натощак, ммоль/л |
5,72±1,22 |
5,45±0,97 |
0,276 |
|
ХС ЛПНП натощак, ммоль/л |
3,85±1,12 |
3,45±0,97 |
0,141 |
|
Калий, ммоль/л |
4,76±0,45 |
4,57±0,34 |
0,071 |
Таблица 3
Сравнительная характеристика структуры терапии при включении в исследование групп обследуемых больных (n=60)
|
Показатель, абс./% |
Первая группа (фиксированная комбинация П+А, n=30) |
Вторая группа (нефиксированная комбинация Э+А, n=30) |
p |
|
ИАПФ |
20/66,6 |
16/53,3 |
0,752 |
|
АРА |
1/3,3 |
2/6,67 |
0,978 |
|
β-адреноблокаторы |
8/26,6 |
8/26,6 |
0,778 |
|
Диуретики |
10/33,3 |
14/46,7 |
0,653 |
|
Спиронолактон |
8/26,6 |
6/20,0 |
0,854 |
|
Антиагреганты |
17/56,6 |
14/46,6 |
0,829 |
|
Статины |
8/26,6 |
10/33,3 |
0,885 |
|
Антагонисты кальция |
8/26,6 |
12/40,0 |
0,605 |
|
Антиангинальные средства (нитраты, триметазидин) |
20/66,7 |
21/70,0 |
0,934 |
|
Сахароснижающие препараты |
2/6,7 |
2/6,7 |
0,606 |
|
Ингаляционные глюкокортикоиды |
7/23,3 |
10/33,3 |
0,713 |
|
Ипратропиум бромид |
12/40,0 |
10/33,3 |
0,908 |
|
Тиотропиум бромид |
19/63,3 |
17/56,7 |
0,958 |
До и после лечения оценивали клиническое течение ХОБЛ, исходные и постбронходилатационные ОФВ1, ФЖЕЛ, отношение ОФВ1/ФЖЕЛ методом спирометрии (прибор MicroLab, MICROMEDICALLTD,UK);показатели суточного мониторирования АД (СМАД) (прибор АВРМ-04, Meditech, Венгрия);состояние фильтрационной функции почек по уровню сывороточного креатинина и скорости клубочковой фильтрации (СКФ, MDRD);показатели липидного спектра; уровни глюкозы и калия. Оценка приверженности пациентов к лечению проводилась по данным индивидуальных дневников ежедневного самоконтроля АД. Для количественной оценки приверженности пациентов к лечению всем больным через 4 недели и в конце лечения было проведено анонимное анкетирование по опроснику Мориски-Грина[7].
Статистическую обработку полученных результатов осуществляли при помощи программы STATISTICA 6.0.Для количественных признаков были рассчитаны среднеарифметическое значение (M) ± и среднеквадратичное отклонение среднего (sdd); медианы, нижнего и верхнего квартилей (Ме[LQ;UQ]). Для качественных признаков были рассчитаны абсолютная частота проявления признака (количество обследованных), частота проявления признака в процентах. Анализ вида распределения осуществлен с использованием критерия Шапиро-Уилка. Для ряда данных гипотеза о нормальности распределения была отвергнута. Для статистического анализа данных при нормальном распределении использовали параметрические методы: для количественных показателей – критерий Стьюдента, для качественных показателей – критерий χ2. При сравнении показателей двух групп при ненормальном распределении статистическая обработка была проведена с использованием непараметрических критериев: для количественных показателей – критерий Манна-Уитни; для качественных показателей – критерий χ2 с поправкой Йетса или точный критерий Фишера. Кpитическийуpовеньдостовеpности нулевой статистической гипотезы, свидетельствующей об отсутствии значимых pазличий, пpинималиpавнымр<0,05. Исследование взаимосвязи между признаками проводили на основе ранговых коэффициентов корреляции Спирмена. За критический уровень достоверности нулевых гипотез при исследовании взаимосвязи был принят уровень p<0,05.
Результаты. Анализ приверженности пациентов к лечению по опроснику Мориски-Грина показал, что большинство больных – 90,0% (54) были комплаентны (p<0,001) и набрали по опроснику Мориски-Грина 4 балла без достоверных различий между группами: 93,3% (28 пациентов в первой группе и 86,7% (26) – во второй группе л (p=0,992).
К концу исследованияв первой группе больных средняя доза периндоприла в фиксированной комбинации составила 7,33+2,53 мг в сутки, амлодипина – 7,50+2,54 мг, во второй группе средняя доза эналаприла составила 12,74+6,30 мг в сутки, амлодипина – 7,50+2,61 мг в сутки. В назначении тиазидового или тиазидоподобного диуретика в первой группе нуждались 13,3% (4) больных, во второй – 6,7% (2) больных (р=0,726).
В ходе лечения отмены исследуемых препаратов в связи с побочными эффектами в первой группе больных не было. Во второй группе у 1 пациента на 7 день лечения развился кашель, потребовавший отмены эналаприла и исключения его из исследования. У 16,7% (5) больных при назначении нефиксированной комбинации эналаприла и амлодипинаотмечались эпизоды головокружения, связанные с избыточным снижением систолического АД (САД), что потребовало уменьшения дозы эналаприла (p=0,029).
В процессе шестимесячной антигипертензивной терапии целевой уровень САД в первой группе был достигнут у 83,3% (25) больных, диастолического АД (ДАД) – у 76,7% (23) пациентов; во второй группе – у 86,7 % (26) и 83,3% (25) больных соответственно (p =0,930; p =0,983).
За период лечения в обеих группах не было зарегистрировано обострений ХОБЛ, субъективно у всех больных отмечено увеличение толерантности к физической нагрузке. Оценка динамики показателей спирометрии после лечения между группами показала, что ОФВ1 и ФЖЕЛ, как исходные, так и после бронходилатационного теста, в первой группе увеличились достоверно больше, чем во второй группе (для исходного ОФВ1 p=0,047; для постбронходилятационного ОФВ1 p=0,005; для исходной ФЖЕЛ p=0,019; для постбронходилятационной ФЖЕЛ p=0,002). На фоне приема фиксированной комбинации периндоприла и амлодипина и свободной комбинации эналаприла и амлодипина динамика отношения ОФВ1/ФЖЕЛ достоверно не отличалась, как исходно, так и после бронходилатационного теста (табл. 4).
Таблица 4
Динамика показателей спирометрии на фоне лечения по группам обследуемых (n=60)
|
Показатель, ∆% |
Первая группа (фиксированная комбинация П+А, n=30) |
Вторая группа (нефиксированная комбинация Э+А, n=30) |
p |
|
ОФВ1 |
9,72[-5,53;15,78] |
1,35[-0,12;5,63] |
0,047 |
|
ФЖЕЛ |
8,54[0;24,12,73] |
1,95[-2,71;10,78] |
0,019 |
|
ОФВ1/ФЖЕЛ |
2,50[-11,61;8,13] |
3,73[-8,79;11,24] |
0,894 |
|
Постбронходилятационный ОФВ1 |
10,24[-0,56;18,72] |
2,41[-3,11;6,74] |
0,005 |
|
Постбронходилятационный ФЖЕЛ |
7,12[0;11,11,48] |
2,76[-2,77;10,74] |
0,002 |
|
Постбронходилятационный показатель ОФВ1/ФЖЕЛ |
2,85[-12,92;10,15] |
4,54[-8,13;14,03] |
0,624 |
После лечения отмечена положительная динамика ФК ХСН в обеих группах обследуемых при отсутствии значимых различий между группами (р=0,121) (табл.5). Средняя дистанция в тесте 6-минутной ходьбы после лечения увеличилась в обеих группах недостоверно (р=0,098). Однако среднее количество баллов по шкале ШОКС достоверно снизилось в первой группе - на 7,3[-16,1;0,7]%, а во второй группе, наоборот, увеличилось на 1,7[-6,1;19,0]% (p=0,016).
Таблица 5
Динамика клинического состояния больных ХСН на фоне лечения по группам обследуемых (n=60)
|
Показатель, ∆% |
Первая группа (фиксированная комбинация П+А, n=30) |
Вторая группа (нефиксированная комбинация Э+А, n=30) |
p |
|
ФК ХСН |
-6,4[-12,6;2,2] |
-5,5[-2,1;16,7] |
0,121 |
|
ШОКС |
-7,3[-16,1;0,7] |
1,7[-6,1;19,0] |
0,016 |
|
Тест 6-минутной ходьбы |
26,9[12,5;52,0] |
18,2[-2,6;33,5] |
0,098 |
При оценке изменений метаболического профиля после лечения в обеих группах отмечена сопоставимая положительная динамика некоторых показателей липидного спектра без достоверных различий между группами, обусловленная рекомендациями приема или коррекции дозы статинов. Динамика уровня глюкозы плазмы крови натощак и калия на фоне лечения не имела достоверных различий, как внутри групп, так и при межгрупповом сравнении (табл.6).
Таблица 6
Динамика показателей липидного спектра, глюкозы и калия на фоне различных вариантов антигипертензивной терапии по группам обследуемых (n=60)
|
Показатель, ∆% |
Первая группа (фиксированная комбинация П+А, n=30) |
Вторая группа (нефиксированная комбинацияЭ+А, n=30) |
p |
|
|
ОХС |
-33,34[-41,95;-9,02] |
-37,18[-46,39;-10,74] |
0,289 |
|
|
ТГ |
-15,02[-27,38;-4,15] |
-18,13[-30,45;-1,59] |
0,385 |
|
|
ХС ЛПВП |
3,27[-0,08;5,22] |
2,98[-0,26;7,13] |
0,362 |
|
|
ХС ЛПНП |
-22,31[-38,62;-5,61] |
-26,72[-41,56;-8,82] |
0,571 |
|
|
Глюкоза плазмы крови натощак |
-8,22[-14,05;-2,61] |
-6,75[-12,49;1,49] |
0,382 |
|
|
Калий |
5,18[-0,14;7,30] |
7,98[-0,63;10,01] |
0,126 |
|
После лечения в обеих группах выявлена достоверная положительная динамика СКФ, более выраженная в первой группе, чем во второй (рис.1). СКФ в первой группе увеличилась на 4,74[-4,90;19,38]%, во второй группе – на 2,62[-11,17;13,25] (p=0,041).Анализ динамики уровня сывороточного креатинина показал достоверные различия между группами при незначимых изменениях его уровня внутри группы: снижение креатинина в первой группе составило - 7,93 [-13,78; 2,21]%, во второй группе - 1,50[-8,56;3,9]% (p=0,041).
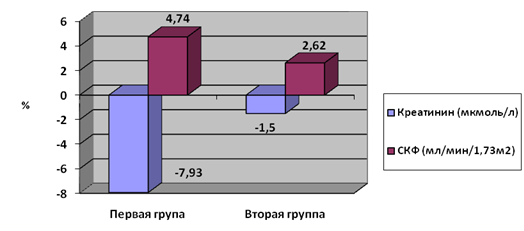
Рис.1. Динамика показателей, отражающих функциональное состояние почек, на фоне лечения по группам обследуемых (n=60)
Обсуждение. В настоящее время ХОБЛ занимает третье лидирующее место в структуре летальности в популяции, поэтому оценка коморбидности у больных сердечно-сосудистыми заболеваниями и ХОБЛ является важной составляющей их прогноза. Метаанализ недавних крупных популяционных исследований продемонстрировал значение снижения ОФВ1 как независимого фактора риска сердечно-сосудистых заболеваний и кардиальной смерти у больных ХОБЛ [9]. Значимое снижение ОФВ1 даже у никогда не куривших пациентов ассоциируется с 5-10-кратным ростом риска кардиальной смерти [5].Результаты нашей работы показали достоверную позитивную динамику ОФВ1, ФЖЕЛ в сочетании с клиническим улучшением течения ХОБЛ на фоне 6-месячной терапии фиксированной комбинацией периндоприла и амлодипина по сравнению со свободной комбинацией эналаприла и амлодипина у обследованных больных.
В комплексной терапии больных с кардиреспираторной патологией важное значение приобретает влияние лекарственных препаратов на показатели углеводного обмена. Инсулинорезистентность у больных ХОБЛ рассматривается как потенциальный механизм формирования сердечно-сосудистой патологии: гипоксия, влияя на периферическую чувствительность к инсулину, может изменять метаболизм глюкозы у больных ХОБЛ. [8]. А развитие инсулинорезистентности при ИБС и ХСН связывают с нарушенной инсулин-стимулированной утилизацией глюкозы в скелетных мышцах [6]. В нашей работе в обеих группах больных после лечения отмечена тенденция к снижению уровня глюкозы натощак, также отмечено отсутствие негативного влияния исследуемых препаратов на липидный профиль и электролитный баланс, оцененный по уровню калия в сыворотке крови, что позволяет рассматривать комбинацию ИАПФ и АКК как метаболически нейтральную у больных с сочетанной кардиореспираторной патологией.
Установлено, что почечная дисфункция является негативным прогностическим фактором у больных ХОБЛ и ХСН и ассоциируется с активацией нейрогуморальных систем, гипоксией, воспалением,оксидантным стрессом,дисфункцией миокарда [3,10]. В нашем исследовании назначение фиксированной комбинациипериндоприла и амлодипина обеспечило более достоверно выраженный прирост СКФ у обследованных больных в сравнении со свободной комбинацией эналаприла и амлодипина.
Выводы. Таким образом, тактика выбора антигипертензивной терапии в виде фиксированной комбинации периндоприла и амлодипина в сравнении со свободной комбинацией эналаприла и амлодипина более предпочтительна у больных ИБС и АГ, осложненной ХСН, в сочетании с ХОБЛ. Такой подход на фоне достоверно высокого антигипертензивного эффекта обеспечивает более благоприятное влияние на течение ХОБЛ, ХСН, фильтрационную функцию почек. Применение обеих стратегий антигипертензивной терапии не оказывает негативного влияния на метаболический профиль пациентов. Использование ИАПФ в комбинации с амлодипином в обеих группах больных не приводи к увеличению частоты кашля или ангионевротического отека, однако прием эналаприла и амлодипина в свободной комбинации демонстрирует достоверно более высокий процент побочных эффектов, преимущественно связанных с избыточным снижением САД.
Рецензенты:
Владимирский Е.В., д.м.н., профессор заведующий кафедрой факультетской терапии №1 с курсом физиотерапии ФДПОГБОУ ВПО ПГМУ им. ак. Е.А.Вагнера МИНЗДРАВА России, г. Пермь;
Ховаева Я.Б., д.м.н., профессор, заведующая кафедрой терапии и семейной медицины ФДПО ГБОУ ВПО ПГМУ им. ак. Е.А.Вагнера МИНЗДРАВА России, г. Пермь.
Библиографическая ссылка
Козлова Е.В., Масалкина О.В. ВЛИЯНИЕ РАЗЛИЧНЫХ ВАРИАНТОВ АНТИГИПЕРТЕНЗИВНОЙ ТЕРАПИИ НА ТЕЧЕНИЕ КОМОРБИДНОЙ ПАТОЛОГИИ У БОЛЬНЫХ ИШЕМИЧЕСКОЙ БОЛЕЗНЬЮ СЕРДЦА И АРТЕРИАЛЬНОЙ ГИПЕРТЕНЗИЕЙ, ОСЛОЖНЕННОЙ ХРОНИЧЕСКОЙ СЕРДЕЧНОЙ НЕДОСТАТОЧНОСТЬЮ // Современные проблемы науки и образования. 2015. № 3. ;URL: https://science-education.ru/ru/article/view?id=18792 (дата обращения: 04.04.2026).



