Согласно литературным данным, производные на основе N-замещенных 2-амино-4-арил-4-оксобут-2-еновых кислот являются перспективными с точки зрения поиска веществ с анальгетической активностью [4,6,7]. Так, в работе [1] в результате биологических испытаний установлено, что введение в структуру амидов 4-арил-2-ариламино-4-оксобут-2-еновых кислот фрагмента пиперазина обеспечивает проявление анальгетического действия выше препаратов сравнения. Кроме того, определенный интерес представляет химическая модификация соединений с включением фармакофорных фрагментов морфолина и адамантана с последующим фармакологическим скринингом полученных веществ.
Целью исследования является изучение анальгетической активности новых соединений в ряду производных N-замещенных амидов 2-ариламино-4-арил-4-оксобут-2-еновых кислот, содержащих фрагменты морфолина и пиперазина, иариламидов 2-адамантаноилметиленгидразино-4-арил-4-оксобут-2-еновых кислот.
Материалы и методы
Структура новых соединений I–III доказана методами ИК-, ЯМР 1Н-спектроскопии и масс-спектрометрии, а также данными элементного анализа. ИК-спектры записаны на приборе ФСМ-1201 в виде пасты в вазелиновом масле. Спектры ЯМР¹-Н записаны на приборе ЯМР BS-567А (100МГц),VarianMercuryplus (300 МГц), внутренний стандарт – ГМДС, растворитель ДМСО-d6. Масс-спектры соединений сняты на хромато-масс-спектрометре Hewlett Packard 5973/6890. Химическую чистоту соединений и протекание реакции контролировали методом ТСХ на пластинках «Sorbfil» тип ПТСХ-АФ-УФ в системе эфир-бензол-ацетон, 10:9:1, пятна детектировали парами йода. Данные элементного анализа, полученные на приборе LECO–CNH(S)932, соответствуют вычисленным значениям.
Острую токсичность соединений Ib,IIb,IIIb изучали на белых нелинейных мышах (самцах) массой 18–22 г с определением LD50. Каждое соединение испытывали на 6 животных. Соединения вводили внутрибрюшинно в виде взвеси в 2 % крахмальном растворе из расчета 0,1 мл/10 г однократно, после чего животные находились под наблюдением в течение 14 дней. Контрольным животным вводили эквиобъемное количество 2 % крахмального раствора [3].
Анальгетическую активность соединений I–III определяли по методу оценки термической соматической боли – тесту горячей пластины на белых нелинейных мышах (самцах) массой 18-22 г [3]. Исследуемые вещества вводили внутрибрюшинно в дозе 50 мг/кг в виде взвеси в 2 % крахмальном растворе до помещения животных на нагретую до 53,5 °С металлическую пластинку. Показателем изменения болевой чувствительности служила длительность пребывания животного на горячей пластине до появления поведенческого ответа на ноцицептивную стимуляцию (облизывания задних лап, прыжков, отдергивания задних лап), измеряемая в секундах. Эффект оценивали через 2 ч после введения соединений. Каждое соединение испытывали на 6 животных. Результаты оценивали по увеличению времени наступления оборонительного рефлекса по сравнению с исходными данными. Контрольной группе животных вводили 2 % крахмальный раствор, в качестве препаратов сравнения использовали коммерчески доступную субстанцию натриевой соли диклофенака Sigma® в дозе 10 мг/кг (ЕД50) и коммерчески доступную субстанцию метамизола натрия ООО «Фармхимкомплект» в дозе 93 мг/кг (ЕД50). Результаты фармакологических испытаний обработаны статистически с помощью программ Windows XP (Excel) с использование t критерия Стьюдента и представлены в таблице.
Результаты исследования и их обсуждение
Объекты фармакологического скрининга – N-замещенные амиды 2-ариламино-4-арил-4-оксобут-2-еновых кислот (Ia-d,IIa-c) синтезированы дециклизацией 5-арил-3-арилимино-3Н-фуран-2-онов под действием пиперазина и морфолина соответственно. Реакция протекает в среде безводного толуола при нагревании в течение 0,5–1 ч, давая продукты с хорошим выходом. Ранее аналогичный процесс раскрытия фуранового цикла был проведен на примере близких по структуре 5-арил-3-гетариламино(3-гидразоно)-3Н-фуран-2-онов [5]. Адамантансодержащие производные получены первоначально реакцией диаза-Виттига с последующей циклизацией в соответствующие фуран-2-оны [7]. При их взаимодействии с ароматическими аминами в среде безводного толуола при нагревании реакционной смеси в течение 0,5 ч. образуются с хорошими выходами ариламиды2-адамантаноилметиленгидразино-4-арил-4-оксобут-2-еновых кислот (IIIa,b). Строение производных I–III хорошо согласуется с характеристиками родственных соединений [5,6,7] и представлено ниже:
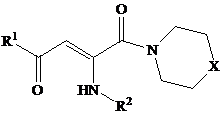
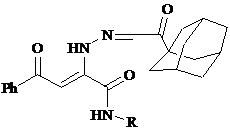
|
I: X=NH, R1=C6H5, R2=4-ClC6H4 (a), 4-CH3OC6H4 (b), R1=4-ClC6H4, R2=3-NO2C6H4 (c), R1=2,4-CH3OC6H3, R2=4-BrC6H4 (d). II: X=O, R1=C6H5, R2=4-ClC6H4 (a), R2=3-NO2C6H4 (b),R1=4-ClC6H4,R2=4-CH3OC6H4 (c). |
III: R= C6H5(a), 4-CH3OC6H4(b). |
Исследование острой токсичности производных Ib,IIb и IIIb показало, что LD50 составляет 1350, 1500 и 1500 мг/кг, соответственно. Таким образом, данные вещества можно отнести к практически нетоксичным соединениям, и они имеют определенные преимущества по безопасности перед препаратом сравнения [2]. По-видимому, низкая токсичность объясняется их структурным сходством с естественными метаболитами организма.
Анальгетическая активность соединений I–III по тесту горячей пластины
|
Соединение |
Латентный период оборонительного рефлекса, с |
Соединение |
Латентный период оборонительного рефлекса, с |
|
Ia |
19,80±0,55***1 |
IIc |
19,82±1,10***1 |
|
Ib |
23,72±1,12***1*2 |
IIIa |
21,40±0,88***1*2 |
|
Ic |
20,72±0,88***1 |
IIIb |
22,40±0,70***1*2 |
|
Id |
21,60±1,50**1 |
Контроль |
10,20±0,37 |
|
IIa |
19,30±1,10**1 |
Метамизол натрия |
18,33±1,02 |
|
IIb |
22,80±0,73***1*2 |
* = p < 0,05, ** = p< 0,01, *** = p < 0,001 |
|
1− по сравнению с контролем; 2 – по сравнению с метамизолом натрия.
Как видно из таблицы, при изучении анальгетической активности соединений Ia-d, содержащих фрагмент пиперазина, выявлено, что все производные проявляют действие на уровне или превышающее эффект метамизола натрия. Так, введение в ариламинный фрагмент электронодонорной группы (OMe) приводит к усилению фармакологического действия (у вещества Ib). В то же время введение электроноакцепторного заместителя (Cl, Br или NO2), а также одновременное введение любых заместителей, независимо от их природы, в ариламинный и/или арильный фрагменты молекул не приводит к усилению анальгетических свойств (у соединений Ia,c,d). Наибольшую активность проявляет 2-(4-метоксифениламино)-1-(пиперазин-1-ил)-4-фенилбут-2-ен-1,4-дион (Ib). В ряду производных IIa-c, содержащих фрагмент морфолина, установлено, что введение в ариламинный заместитель электроноакцепторной группы (NO2) дает наиболее выраженный анальгетический эффект. Наличие электронодонорных групп в арильном и ариламинномфрагментах молекул не приводит к усилению анальгетического действия (у соединения IIc). Таким образом, наибольшую анальгетическую активность проявляет 2-(3-нитрофениламино)-1-(морфолин-1-ил)-4-фенилбут-2-ен-1,4-дион (IIb). Среди адамантансодержащих производных III выявлено, что при введении электронодонорной группы (OMe) в ариламидный фрагмент приводит к увеличению анальгетического действия (у соединения IIIb).
Таким образом, дальнейший поиск веществ с анальгетической активностью среди гетарилариламидов 4-арил-2-ариламино-4-оксобут-2-еновых кислот и 2-адамантаноилметиленгидразино-4-арил-4-оксобут-2-еновых кислот является целесообразным.
Выводы
1. Исследованные соединения обладают низкой токсичностью, что делает их перспективными для дальнейшего изучения.
2. В ряду производных, содержащих фрагмент пиперазина, введение электронодонорной группы, а у соединений, содержащих фрагмент морфолина, введение электроноакцепторной группы в ариламинный заместитель приводит к наиболее выраженному анальгетическому действию.
3. У адамантансодержащих соединений наиболее выраженным анальгетическим эффектом обладает 4-метоксифениламид 2-адамантаноилметиленгидразино-4-арил-4-оксобут-2-еновой кислоты.
Работа выполнена при финансовой поддержке РФФИ (проект № 14-03-96016 р_урал_а).
Рецензенты:Вихарева Е.В., д.ф.н., профессор, заведующая кафедрой аналитической химии «Пермской государственной фармацевтической академии», г. Пермь;
Юшкова Т.А., д.м.н., профессор кафедры фармакологии «Пермской государственной фармацевтической академии», г. Пермь.
Библиографическая ссылка
Кожухарь В.Ю., Кузнецов А.С., Пулина Н.А., Махмудов Р.Р., Рубцов А.Е. ИССЛЕДОВАНИЕ АНАЛЬГЕТИЧЕСКОЙ АКТИВНОСТИ НОВЫХ СОЕДИНЕНИЙ, СОДЕРЖАЩИХ ФРАГМЕНТЫ МОРФОЛИНА, ПИПЕРАЗИНА И АДАМАНТАНА // Современные проблемы науки и образования. 2015. № 3. ;URL: https://science-education.ru/ru/article/view?id=17523 (дата обращения: 16.05.2026).



