На сегодняшний день неотъемлемой частью номенклатуры лекарственных средств назначаемых в комплексной терапии воспалительных заболеваний мочевого пузыря и мочевыводящих путей (циститы, уретриты) является лекарственное растительное сырье, основные из которых это брусники листья (Vitis – idaeae folia) и толокнянки листья (Uvae ursi folia). Мочегонные и уроантисептические свойства данных растительных объектов связаны в первую очередь с фенольными гликозидами арбутином и метиларбутином, а также с гидрохиноном и его метиловым эфиром [1].
Согласно нормативной документации на данные виды сырья, содержание арбутина в них должно быть не менее 6 % (толокнянки листья) и 4,5 % (брусники листья).
Следует сказать, что все нормативные документы на указанные виды сырья в качестве методики количественного определения арбутина предлагают использовать окислительно-восстановительное титрование йодом. Важно также отметить, что методика обременена сложными процедурами пробоподготовки и очистки, занимающими длительное время и невольно приводящими к возрастанию случайной погрешности. Кроме того, в итоге осуществляется титрование не только арбутина, а некоего комплекса, близких по химическим свойствам, веществ, что также не позволяет оценить истинное содержание арбутина.
Решение указанных вопросов возможно с использованием сепарационных методов анализа (ВЭЖХ, капиллярного электрофореза (КЭ)). И на сегодняшний день известно ряд ВЭЖХ-методик количественного определения арбутина в сырье [2-4]. В то же время использование КЭ может быть более оправданным, поскольку не требуется дорогостоящих растворителей и колонок. Кроме того, наличие более высоких параметров эффективности является ключевым преимуществом при анализе сложных растительных объектов, содержащих десятки, а порой и сотни соединений.
Цель работы
Разработка и валидация методики количественного определения арбутина в толокнянки листьях и брусники листьях с применением капиллярного электрофореза.
Материалы и методы исследования
Для исследования использовали стандартный образец (СО) арбутина (Sigma, с содержанием не менее 98%), а так же образцы сырья толокнянки листья (ОАО «Красногорсклексредства», серия 80714) и брусники листья (ОАО «Красногорсклексредства», серия 80614).
Работу проводили с использованием системы капиллярного электрофореза Капель 103 Р (группа компаний Люмэкс, Россия) с кварцевым капилляром диаметром 50 мкм, общей длинной 75 см и эффективной длинной 65 см. Детектирование осуществляли спектрофотометрически при 254 нм в катодной области капилляра. Напряжение составляло 20 кВ (блок положительной полярности). Для подготовки капилляра и восстановления его поверхности проводили его последовательную промывку водой, 0,5 М раствором кислоты хлористоводородной, водой, 0,5 М раствором натрия гидроксида, водой и затем ведущим электролитом.
В работе реализовывался вариант зонного электрофореза, где в качестве ведущего электролита использовали 0,01М боратный буферный раствор с рН 9,0. Выбор электролита связан с тем, что при данном значении рН, арбутин ионизируется по фенольному гидроксилу (Рисунок 1), являясь при этом заряженной частицей.
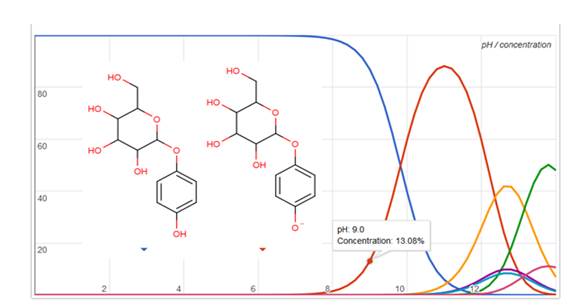
Рисунок 1. Зависимость степени ионизации арбутина от рН среды (по данным http://www.chemicalize.org).
Важно отметить, что при данном значении рН электролита арбутин ионизирован всего на 13 %, однако даже в этих условиях он обладает, хоть и незначительной, эффективной электрофоретической подвижностью.
Извлечение арбутина из сырья проводили в соответствии с методикой, приведенной в нормативной документации на анализируемое лекарственное растительное сырье. Для этого точную навеску (около 0,5 г) сырья помещали в коническую колбу вместимостью 100мл, заливали 50 мл воды и присоединяли к обратному холодильнику. Нагревание вели на плитке, поддерживая слабое кипение, в течение 30 минут. Горячее извлечение фильтровали в мерную колбу вместимостью 100 мл через бумажный фильтр диаметром 7 см. В колбу с сырьем повторно прибавляли 25 мл воды и кипятили в течение 20 минут. Повторное горячее извлечение фильтровали, объединяя извлечения. Остаток на фильтре промывали 20 мл горячей воды, также объединяя все извлечения. После охлаждения раствор доводили до метки водой и перемешивали. Далее 1 мл полученного раствора центрифугировали 5 мин при 8000 мин-1 и подвергали его анализу.
Результаты исследования и их обсуждение
На рисунках 2-4 представлены электрофореграммы раствора СО арбутина, а также извлечений брусники листьев и толокнянки листьев.
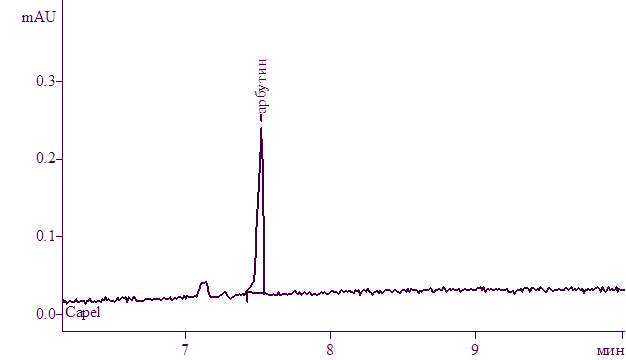
Рисунок 2. Электрофореграмма раствора СО арбутина
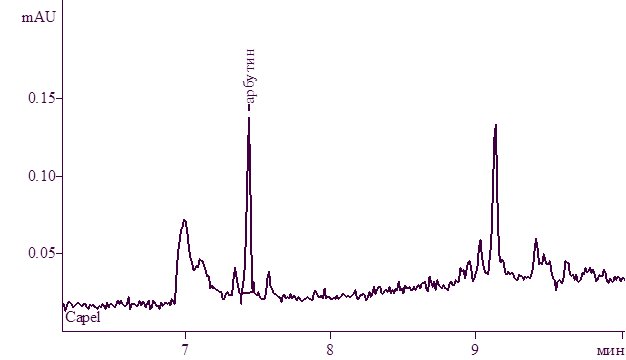
Рисунок 3. Электрофореграмма извлечения брусники листьев
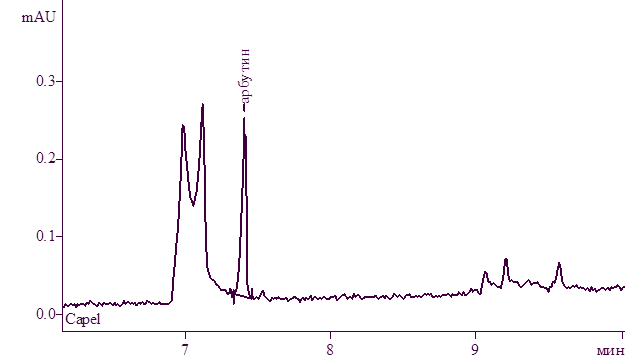
Рисунок 4. Электрофореграмма извлечения толокнянки листьев
В результате в обоих видах сырья было установлено наличие арбутина. При этом коэффициент его разделения с сопутствующими компонентами пробы был достаточным для его количественного определения.
Следующим этапом исследований была валидационная оценка разработанной методики по показателям: линейность, прецизионность и правильность.
Линейность методики определялась по итогам анализа серии растворов СО арбутина различной концентрации (от 0,0051 до 0,0816 г/100мл). На рисунке 5 представлен градуировочный график зависимости площади пика арбутина от его концентрации в растворе. Полученная зависимость имеет линейный характер и описывается следующим уравнением: y=6,1873x-0,002. При этом коэффициент корреляции (r) был равен 0,999995, что позволяет использовать данное уравнение для количественного определения арбутина в указанном диапазоне концентраций.
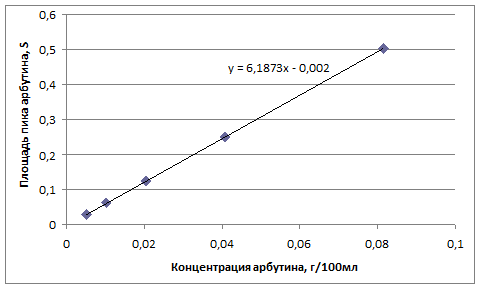
Рисунок 5. Градуировочный график зависимости площади пика от концентрации арбутина в растворе
Для установления прецизионности (воспроизводимости) проводили 6 параллельных определений для каждого образца сырья. Расчет содержания (%) проводили по уравнению градуировочного графика арбутина, в пересчете на воздушно сухое сырье. Результаты оценки прецизионности методики количественного определения арбутина в брусники листьях и толокнянки листьях приведены в таблице 1-2.
Таблица 1
Результаты оценки прецизионности методики количественного определения арбутина в брусники листьях
|
Навеска, г |
Площадь пика, S |
Содержание, % |
Характеристики |
|
0,4999 |
0,167 |
6,28 |
Хср = 6,21 % SD= 0,27 RSD= 4,26% |
|
0,5013 |
0,173 |
6,47 |
|
|
0,5069 |
0,165 |
6,12 |
|
|
0,5222 |
0,162 |
5,83 |
|
|
0,5119 |
0,165 |
6,04 |
|
|
0,5017 |
0,174 |
6,52 |
Таблица 2
Результаты оценки прецизионности методики количественного определения арбутина в толокнянки листьях
|
Навеска, г |
Площадь пика, S |
Содержание, % |
Характеристики |
|
0,5106 |
0,416 |
15,21 |
Хср = 14,49 % SD = 0,54 RSD= 3,73 % |
|
0,5102 |
0,403 |
14,75 |
|
|
0,5030 |
0,389 |
14,44 |
|
|
0,5041 |
0,3715 |
13,76 |
|
|
0,5006 |
0,396 |
14,77 |
|
|
0,5101 |
0,382 |
13,98 |
Полученные результаты свидетельствуют о приемлемых значениях случайной погрешности, что свидетельствует о валидности методики по данному показателю.
Изучение правильности методики проводили путем анализа 9 образцов каждого сырья на трех уровнях концентраций. Оценку правильности методики проводили по открываемости (R, %). Результаты данной оценки представлены в таблице 3-4.
Таблица 3
Результаты оценки правильности методики количественного определения арбутина в брусники листьях
|
№ п/п |
Уровень |
Навеска, г |
Теоретическое содержание арбутина в навеске сырья, мг |
Найденное содержание арбутина в навеске сырья, мг |
Открываемость (R), % |
Характеристики |
|
1 |
1 |
0,3527 |
21,90 |
21,55 |
98,40 |
Rср = 100,57% SD = 3,26 RSD = 3,24% |
|
2 |
1 |
0,3502 |
21,75 |
21,75 |
100,00 |
|
|
3 |
1 |
0,3720 |
23,10 |
24,70 |
106,93 |
|
|
4 |
2 |
0,4999 |
31,04 |
31,39 |
101,13 |
|
|
5 |
2 |
0,5013 |
31,13 |
32,43 |
104,18 |
|
|
6 |
2 |
0,5069 |
31,48 |
31,02 |
98,54 |
|
|
7 |
3 |
0,6510 |
40,43 |
39,91 |
98,71 |
|
|
8 |
3 |
0,6572 |
40,81 |
41,21 |
100,98 |
|
|
9 |
3 |
0,6520 |
40,49 |
38,99 |
96,30 |
Таблица 4
Результаты оценки правильности методики количественного определения арбутина в толокнянки листьях
|
№ п/п |
Уровень |
Навеска, г |
Теоретическое содержание арбутина в навеске сырья, мг |
Найденное содержание арбутина в навеске сырья, мг |
Открываемость (R), % |
Характеристики |
|
1 |
1 |
0,3528 |
51,12 |
51,31 |
100,37 |
Rср = 100,17% SD = 3,71 RSD = 3,71% |
|
2 |
1 |
0,3580 |
51,87 |
50,83 |
98,00 |
|
|
3 |
1 |
0,3679 |
53,31 |
51,21 |
96,06 |
|
|
4 |
2 |
0,5041 |
73,04 |
70,09 |
95,96 |
|
|
5 |
2 |
0,5006 |
72,54 |
73,94 |
101,93 |
|
|
6 |
2 |
0,5101 |
73,91 |
71,31 |
96,48 |
|
|
7 |
3 |
0,6597 |
98,59 |
101,08 |
102,53 |
|
|
8 |
3 |
0,6555 |
94,98 |
99,96 |
105,24 |
|
|
9 |
3 |
0,6548 |
94,88 |
99,59 |
104,96 |
Полученные результаты свидетельствуют, что значения открываемости для обоих веществ находятся в пределах 98 – 102%, что согласно общепринятым рекомендациям [5] свидетельствует о валидности методики по данному показателю.
С использованием разработанной и валидированной методики были получены следующие результаты количественного содержания арбутина в изучаемых образцах. Результаты представлены в таблице 5.
Таблица 5
Результаты количественного определения арбутина в брусники листьях и в толокнянки листьях
|
Образец |
Содержание арбутина, % ±SD |
|
Толокнянки листья (ОАО «Красногорсклексредства», серия 80714) |
14,49±0,54 |
|
Брусники листья (ОАО «Красногорсклексредства», серия 80614) |
6,21±0,27 |
Полученные данные свидетельствуют о значительном содержании арбутина в изучаемых образцах. Кроме того, имеет место явное занижение нормативных показателей по содержанию арбутина в сырье, особенно в случае с толокнянки листьями.
Выводы
Разработана методика количественного определения арбутина в толокнянки листьях и брусники листьях с использованием капиллярного электрофореза. Разработанная методика была валидирована по основным показателям, что подтверждает возможность ее использования для количественного определения арбутина в указанном сырье.
Рецензенты:
Компанцева Е.В., д.фарм.н., профессор кафедры фармацевтической и токсикологической химии ПМФИ – филиала ГБОУ ВПО ВолгГМУ Минздрава России, г. Пятигорск.
Оганесян Э.Т., д.фарм.н., профессор, зав. кафедрой органической химии ПМФИ – филиала ГБОУ ВПО ВолгГМУ Минздрава России, г. Пятигорск.
Библиографическая ссылка
Рознятовская А.А., Сенченко С.П., Харахашян А.А. РАЗРАБОТКА И ВАЛИДАЦИЯ МЕТОДИКИ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ АРБУТИНА В БРУСНИКИ ЛИСТЬЯХ И ТОЛОКНЯНКИ ЛИСТЬЯХ МЕТОДОМ КАПИЛЛЯРНОГО ЭЛЕКТРОФОРЕЗА // Современные проблемы науки и образования. 2014. № 6. ;URL: https://science-education.ru/ru/article/view?id=16982 (дата обращения: 19.05.2026).



