История понятия «экзема», происходящее от греческого слова «eczeo», что означает «вскипать», сопровождает человечество, наверное, с момента появления самого человека.
Термин «экзема» упоминается в трудах Аэция, жившего середине VI века нашей эры, однако Рихтер утверждает, что экзема была известна ещё Дискуридесу из Аназарбы в I столетии нашей эры, а И.Блох (I. Bloch) пишет, что данный термин был известен ещё александрийскому врачу Бакшейосу, умершему за 200 лет до нашей эры. Однако под этим понятием объединялись и другие кожные заболевания, к примеру, такие как фурункул или карбункул (Lorry 1877), по современным представлениям никак не относящиеся к экземе. Большая заслуга в выделении экземы как самостоятельного заболевания принадлежит английскому дерматологу R. Willan (1798, 1808) и его ученику T. Bateman (1824), которые впервые описали клинику этого заболевания. Значительный вклад в уточнение понятия экземы и её клинику внесли A. Devergie (1854), P. Bazin (1861), М.Г. Мгебров (1941), П.С. Григорьев(1946).
Экзема – одно из наиболее распространенных заболеваний, имеющее хроническое рецидивирующее течение и полиморфность клинической симптоматики. Этот дерматоз составляет 30-40% всех кожных заболеваний. По данным разных авторов, заболеваемость колеблется от 6,0 до 15,0 на 1000 населения, а пик заболеваемости отмечают в возрасте 40 лет [7, 9]. Экзему регистрируют во всех странах и у представителей всех рас с одинаковой частотой у мужчин и женщин. По разным данным указанная патология занимает одно из первых мест по причинам обращаемости пациентов в поликлинику дерматологического профиля [10]. Среди случаев патологии кожи, по поводу которых больных направляют в дерматологический стационар до 30-40% приходится на экзему. Учитывая хроническое, часто рецидивирующее течение, выраженный зуд, локализацию на открытых участках тела, данное заболевание значительно снижает качество жизни и приводит к социальной дезадаптации пациентов. Крайне важное значение имеет и то, что экзема чаще развивается у лиц трудоспособного возраста, что соответственно приводит к снижению эффективности труда, а также к длительной потери трудоспособности, а профессиональная экзема нередко становится причиной инвалидности [3, 6].
В настоящее время в мировой и отечественной дерматологии не существует единой универсальной классификации экземы [5, 7]. При всей частоте использования и смысловой однозначности термин «экзема» ассоциируется в первую очередь с мокнутием при самых разнообразных воспалительных процессах в коже и как диагноз обозначает весьма гетерогенную группу заболеваний, по-разному классифицируемую в различных дерматологических школах (истинная, профессиональная, себорейная, детская, микробная, микотическая, контактная, солнечная и пр.). В нашей стране наиболее часто используют классификацию академика Скрипкина Ю.К [7], в которой рассматривается экзема истинная (пруригинозная и дисгидротическая, микробная) и относящаяся к ней нуммулярная, варикозная, паратравматическая, детская, себорейная, экзема сосков, сикозиформная, микотическая, тилотическая и профессиональная экзема. По срокам течения выделяют экзему острую (до 3 месяцев), подострую (от 3 до 6 месяцев) и хроническую (более 6 месяцев).
Поражение кожи при истинной экземе обычно начинается и заканчивается областью кистей и/или стоп, поэтому, говоря о термине «хроническая экзема», дерматологи чаще всего подразумевают длительное, торпидное поражение кистей. Постепенный переход острого течения в хроническое клинически определяют по нарастанию инфильтрации, лихенизации, застойной эритеме и шелушению. Далее процесс при хронической экземе тянется месяцами и даже годами, и нередко это течение нарушается острыми вспышками процесса, поэтому как острая, так и хроническая экзема дают периодические обострения и затихания процесса.
Гистологическая картина в коже при экземе зависит от стадии процесса, разновидностей по локализации и этиологическому признаку [4]. Гистопатологические изменения наблюдаются в основном в виде спонгиоза, паракератоза, акантоза, расширения кровеносных и лимфатических сосудов верхних слоёв дермы. Характерными для хронической экземы является относительно мощная клеточная инфильтрация кожи, удлинённые сосочки дермы, значительно выраженный акантоз, паракератоз и в отдельных случаях – гиперкератоз.
Наиболее распространенными среди существующих принятых концепций этиологии и патогенеза экземы являются: нейроиммунная, вегетодистоническая, инфекционно-аллергическая, метаболических механизмов, генетической отягощенности, иммунного дисбаланса. Проведенные клинико-генетические и иммунологические исследования позволяют отнести дерматоз к заболеваниям наследственно-конституциональной природы, причем доля генетических и средовых факторов при различных формах экземы различна. Многие исследователи, особенно в последнее время, склоняются к роли иммунных нарушений в патогенезе экземы, но значимость и механизмы этих иммунных нарушений, приводящие к хроническому течению до сих пор не ясны [8].
Несмотря на многочисленные отечественные и зарубежные исследования, вопрос этиологии и патогенеза остаётся открытым. Этим объясняется продолжающийся поиск и совершенствование всех существующих способов лечения и профилактики рецидивов.
Лечение экземы проводят с учётом полиэтиологических факторов, особенностей клинической картины, распространённости процесса, стадии заболевания, а также сопутствующей патологии. Терапия данного заболевания, как правило, комплексная с включением глюкокортикостероидов, антигистаминных препаратов, гипосенсибилизирующих, психотропных и иммуномодулирующих средств. Важным является наружное лечение в зависимости от стадии процесса. Наряду с медикаментозными методами используются физические факторы, такие как различные варианты узкополосного и широкополосного ультрафиолетового излучения, общая и локальная ПУВА-терапия. Методы фототерапии при экземе привлекают внимание исследователей, являются предметом диссертационных работ, имеющих практическое применение.
Больные с хронической экземой с явлениями гиперкератоза, кератодермии представляют особую группу пациентов, порой упорно не поддающихся никаким видам лечения. При такой выраженной торпидности к проводимой терапии некоторые авторы рекомендуют назначение ретиноидов (ацитретина) в дозе 10-30 мг в сутки.
Ретиноиды – это группа препаратов, представляющих синтетические аналоги витамина А, имеющих свою эффективность в терапии многих кожных заболеваний, в том числе состояний, связанных с гиперкератозом ладоней и подошв. ПУВА (аббревиатура п- псорален, УВА – ультрафиолет спектра А), т.е. сочетанное применение длинноволнового ультрафиолетового облучения (УФА) с фотосенсибилизаторами. Действие ПУВА-терапии на кожу многогранно (влияние на репрессию генов, апоптоз клеток, вовлечённых в патогенез заболевания, экспрессию молекул клеточной поверхности, усиление проницаемости клеточных мембран, увеличение продукции свободных радикалов и синглетного кислорода, а также различного рода иммуномодулирующие эффекты) и до конца не изучено [2].
Комбинация ретиноидов с ПУВА-терапией получило своё название ре-ПУВА-терапия и при некоторых заболеваниях, связанных с нарушением дифференцировки и пролиферации кератиноцитов, например, псориазе, признано одним из наиболее эффективных методов лечения.
Однако ни один из существующих методов терапии больных с хронической экземой не является специфическим и не способствует формированию стойкой и длительной ремиссии. Более того, нет единого, унифицированного подхода к терапии у разных групп пациентов. Таким образом, разработка эффективных способов лечения больных с хронической истинной экземой, дающих длительную ремиссию или позволяющих контролировать заболевание является актуальной задачей.
Цель исследования:
Изучение эффективности лечения хронической истинной экземы ладоней и подошв методом ре-ПУВА-терапии.
Материалы и методы исследования:
Исследование выполнено с участием 43 пациентов, которые соответствовали следующим критериям отбора: наличие идиопатической экземы ладоней и подошв в хронической стадии, гистологическая верификация диагноза, возраст больных от 18 до 65 лет, давность заболевания не менее 2 лет, появление рецидивов не менее 2-3 раз в год, отсутствие другой соматической патологии, требующей на момент проведения исследования медикаментозной или какой-либо другой коррекции. Все больные были разделены на 2-е группы, стандартизированные по полу, возрасту, течению, давности заболевания, наличие сопутствующей патологии. Пациенты первой группы (22 человека) получали локальную ПУВА-терапию, а пациенты второй группы (21 человек) ре-ПУВА-терапию (локальную ПУВА-терапию с ежедневным приёмом внутрь изотретиноина в дозе 0,5 мг/кг). Также в обеих группах местно использовались глюкокортикостероиды (мометазон фуроат) 3-4 недели с постепенным переходом на индифферентные наружные средства. Общая продолжительность терапии составляла в целом 12- 15 недель.
Пациентам проводилась локальная ПУВА – терапия 3-и раза в неделю до 30 процедур с дальнейшим уменьшением количества сеансов до 1-2 в неделю. Для проведения данной методики использовались аппараты фирмы Waldmann UV 181 AL, UV 200 AL c набором ламп для УФА – спектра (длина волны 320- 410 нм с максимальным пиком эмиссии на 351нм). В качестве фотосенсибилизаторов использовался аммифурин в таблетках (сумма фурокумаринов выделенных из плодов амми большой – Ammi majus семейства сельдерейные – Apiaceae) в дозе 0,8 мг/кг, но не более 80мг (4 таблетки) на приём или оксорален (метоксален) в капсулах в дозе 0,6мг/кг, но не более 70 мг (7 капсул) на приём. Указанные препараты принимались внутрь с приёмом пищи за 1,5-2 часа до УФА-облучения. Начальная доза излучения и дальнейшее её наращивание определялась фототипом пациента. При I, II фототипе кожи начальная доза излучения составляет – 0,5 Дж/см2. Дальнейшее наращивание дозы происходит на 0,5 Дж/см2 на каждую последующую процедуру до получения положительной клинической динамики. Максимальная разовая доза составляет до 7-9 Дж/см2, количество процедур до 30-35 на курс лечения. При III, IV, V фототипе кожи начальная доза излучения составляет – 1,0 Дж/см2. Дальнейшее наращивание дозы происходит на 1 Дж/см2 на каждую последующую процедуру также до получения положительной клинической динамики. Затем дозу излучения сохраняют на прежнем уровне. Максимальная разовая доза составляет до 15-20 Дж/см2, количество процедур до 30-35 на курс лечения. Пациенты с VI фототипом участия в исследовании не принимали.
Оценку эффективности данного комбинированного метода лечения проводили с использованием индекса, определяющего распространенность и тяжесть экземы (EASI – Eczema Area and Severity Index), который включает в себя объективную оценку 4-х признаков (количество везикул, эритема, шелушение, зуд). Каждый признак при этом оценивается от 0 до 3 баллов (выраженность признака: О – отсутствует, 1- слабо, 2 – умеренно, 3 – сильно выражен). Площадь поражения оценивалась по 6-и бальной системе между: от 0 – отсутствие поражения, 1 (площадь от 1-20%), до 5 - 100% поражение кожного покрова. Общий индекс EASI вычисляется как сумма баллов за степень тяжести каждого из 4 параметров (V – везикул, E – эритемы, S – шелушения, I – зуда), умноженная на бальную оценку пораженной поверхности (А): EASI=(Pv+Pe+Ps+Pi)хPa.
Максимально возможная сумма баллов 60 [1]. Дерматологический индекс шкалы симптомов (ДИШС) определяется суммой баллов, определяющих выраженность следующих симптомов: эритема, отёк, экскориации, лихенификация, папулы, сухость, шелушение, трещины, зуд. Степень выраженности симптомов в баллах: от О – отсутствие до 3 – сильно выражены. Также определялся дерматологический индекс качества жизни (ДИКЖ), который является субъективным индексом оценки степени негативного влияния хронической экземы на различные аспекты жизни больного, характеризующие в целом качество его жизни (быт, отношения в социальной сфере, работа, семья). Данный опросник заполняется больными самостоятельно и имеет максимальное суммарное значение – 30 баллов. Достоверность различий исследованных показателей определяли с использованием парного и непарного t-критерия Стьюдента.
Результаты и их обсуждение:
Сравнивая динамику дерматологических индексов через 6 недель от начала терапии были установлены существенные различия в полученных результатах (таблица 1).Так на фоне ре-ПУВА-терапии индекс EASI снизился на 57% (р<0,001), ДИШС на 60% (р<0,001), ДИКЖ на 53% (р<0,001), тогда как на фоне ПУВА терапии без системных ретиноидов их значения уменьшились соответственно EASI на 40% (р<0,001), ДИШС на 43% (р<0,001), ДИКЖ на 32% (р<0,001). Сравнение данных показателей между группами показало достоверное снижение дерматологических индексов у пациентов, получавших ре-ПУВА-терапию; этим объясняется более быстрое регрессирование симптоматики в этой группе, скорейшее наступление ремиссии.
Таблица 1
Сравнительная характеристика изменения индексов EASI, ДИШС, ДИКЖ через 6 недель на фоне лечения ПУВА и ре-ПУВА-терапии (M±m)
|
Индексы |
EASI |
ДИШС |
ДИКЖ |
|||
|
Пациенты получающие |
До лечения |
после 6 нед. леч. |
До лечения |
после 6 нед. леч. |
До лечения |
после 6 нед. леч. |
|
ПУВА-терапию |
19,93±1,7 |
11,58±1,07 |
18,01±0,84 |
10,15±0,75 |
15,45±1,5 |
10,51±1,01 |
|
Ре-ПУВА-терапию |
17,52±2,4 |
7,43±1,58 |
19,65±0,58 |
7,83±0,54 |
15,83±1,82 |
7,35±0,75 |
Дальнейшее наблюдение за пациентами после окончания курса лечения в течение 12 месяцев выявило увеличение длительности ремиссии в группе больных, получивших ре-ПУВА-терапию (рисунок 1). Средние сроки появления рецидивов после ПУВА-терапии отмечались через 3-4 месяца, тогда как в группе пациентов, находящихся на ре-ПУВА-терапии первые обострения симптомов наблюдались через 5-6 месяцев.
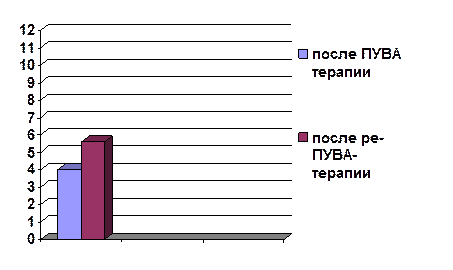
Рисунок 1. График сроков наступления рецидива после ПУВА и ре-ПУВА-терапии
Трудно описать различными индексами и шкалами страдания пациентов, и невозможно выразить их радость при отсутствии симптомов проявлении болезни (рисунок 2, 3)
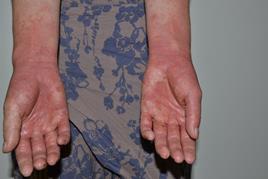 Рисунок 2. До проведения ре-Пува-терапии
Рисунок 2. До проведения ре-Пува-терапии
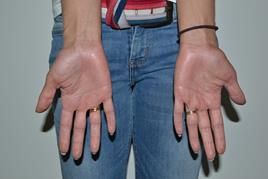 Рисунок 3. После проведения ре-ПУВА-терапии (отдалённые наблюдения)
Рисунок 3. После проведения ре-ПУВА-терапии (отдалённые наблюдения)
Выводы:
1. Данный метод подходит для лечения больных с различными формами, длительностью и тяжестью течения хронической истинной экземы.
2. Описанный способ достоверно превышает по клинической эффективности метод ПУВА-терапии.
3. Важно отметить увеличение сроков ремиссии заболевания после проведенного курса лечения по указанному способу в сравнении с ПУВА-терапией.
4. Данный метод удобен для применения в амбулаторной практике и не требует госпитализации больных.
Рецензенты:
Позднякова В.В., д.м.н., профессор, ведущий научный сотрудник ФГБУ «Ростовский научно-исследовательский онкологический институт» Минздрава России, г. Ростов-на-Дону;
Геворкян Ю.А., д.м.н., профессор, зав. отделением общей онкологии ФГБУ «Ростовский научно-исследовательский онкологический институт» Минздрава России, г. Ростов-на-Дону.
Библиографическая ссылка
Сустретов В.А., Сидоренко О.А., Старостенко В.В. ЭФФЕКТИВНОСТЬ МЕТОДИКИ РЕ-ПУВА-ТЕРАПИИ БОЛЬНЫХ С ХРОНИЧЕСКОЙ ЭКЗЕМОЙ ЛАДОНЕЙ И ПОДОШВ // Современные проблемы науки и образования. 2014. № 6. ;URL: https://science-education.ru/ru/article/view?id=15484 (дата обращения: 29.05.2026).



