Ранее нами приводились данные компьютерного прогнозирования целенаправленно синтезированных гетерилзамещённых 2,3-дигидро-1H-хиназолин-4-онов. Были подтверждены и обоснованы расчеты молекулярного моделирование лиганд-белковых мишеней (ферментов циклооксигеназа-1 и циклооксигеназа-2) представленного ряда соединений. На модели «ватной гранулемы» доказано противовоспалительное действие гетерилзамещённых 2,3-дигидро-1H-хиназолин-4-онов. Полученные результаты фармакологического исследования выявили 3 соединения-лидера противовоспалительной активности, превосходящие по действию препарат сравнения-диклофенак. Молекулярное моделирование гетерилзамещённых 2,3-дигидро-1H-хиназолин-4-онов показало, что, вероятнее всего, исследуемые соединения в большей степени ингибируют ЦОГ-2 и в меньшей мере ЦОГ-1.
Компьютерное прогнозирование целевых структур программой PASS выявило у них вероятный анксиолитический эффект. В продолжение исследований мы сочли целесообразным провести молекулярный докинг лигандов с бензодиазепиновым сайтом связывания ГАМКА рецептора и изучить анксиолитическое действие данного ряда соединений [2-5].
Целью нашего исследования является молекулярный докинг лиганд-рецепторного комплекса в бензодиазепиновом участке связывания и изучение анксиолитической активности гетерилзамещённых 2,3-дигидро-1H-хиназолин-4-онов.
Материалы и методы исследования
Энергии взаимодействия в лиганд-рецепторном комплексе рассчитаны при помощи молекулярного докинга программой Molegro Virtual Docker (вер. 5.5).
В фармакологическом тесте «открытое поле» оценена анксиолитическая активность исследуемых соединений. Помещение животного (крысы) в новые условия приводит к появлению исследовательского поведения, которому препятствует новое окружение, вызывающие страх, тревогу. Две противоположные тенденции поведения характеризуются различным временным ходом. Поэтому, несмотря на уменьшение страха, активность животного к концу опыта снижается. Наилучшим критерием, по которому можно судить об уменьшении страха у животных, является исследование пересечения ими внутренних секторов, которое от опыта к опыту постепенно становится более выраженным. Данный тест достаточен для первичного скрининга, а также является адекватным для выявления токсичности препарата [1; 6].
Результаты исследования и их обсуждение
Молекулярное моделирование
Несомненно, одним из важных факторов, влияющих на уровень фармакологического эффекта, является устойчивая конформация лиганд-рецепторного комплекса: чем ниже энергия связывания, тем прочнее лиганд связан с рецептором, и тем выше вероятность фармакологического эффекта.
При помощи программы Molegro Virtual Docker был осуществлен расчет энергии взаимодействия исследуемых лигандов с ГАМКА рецептором в бензодиазепиновом участке связывания. Данные об энергии лиганд-рецепторного комплекса представлены в таблице 1.
Таблица 1
Энергии взаимодействия гетерилзамещённых 2,3-дигидро-1H-хиназолин-4-онов в бензодиазепиновом участке связывания ГАМКА рецептора
|
Лиганд |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
Диазепам |
|
Энергия |
- 70,67 |
- 71,36 |
- 74,05 |
- 95,53 |
- 80,06 |
- 98,59 |
- 118,07 |
- 87,13 |
Как видно из таблицы 1, наименьшей энергией связывания с бензодиазепиновым сайтом обладает соединение 7, превосходящее по степени сродства препарат-диазепам. На рисунке 1 изображено наиболее оптимальное расположение соединения-лидера (7) в активном центре рецептора.
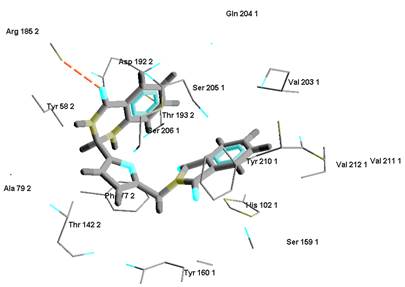
Рис. 1. Расположение QFurIsoInd (соединение 7) в активном центре бензодиазепинового сайта связывания.
Соединение-лидер имеет участки связывания с остатками следующих аминокислот: His 102, Ser 159, Ser 205, Ser 206, Tyr 160, Tyr 210, Val 203, Val 211, Val 212, Ala 79, Arg 185, Asp 192, Phe 77, Thr 142, Thr 193, Tyr 58.
Фармакологические исследования
Для проведения эксперимента были взяты 49 крыс-самок линии Wistar весом 160-180 г (на момент начала эксперимента), содержащихся в стандартных условиях вивария при свободном доступе к воде и пище. С целью изучения нейропсихического статуса крыс (исследования психоэмоциональной, двигательной и исследовательской активности животных) на фоне введения исследуемых веществ использовали тест «открытое поле». Установка представляет собой круглую площадку (около 2 м2), ограниченную непрозрачными бортами высотой 30 см [2].
Репрезентативный ряд из 7 соединений вводили соответствующим группам животных однократно в дозе 10 мг/кг в виде мелкодисперсной суспензии, солюбилизированной твином-80, что было обусловлено плохой растворимостью. Контрольная группа животных получала физиологический раствор в эквивалентном объеме. Вещества вводили перорально с помощью принудительного зондирования за 30-45 минут до проведения эксперимента.
В каждой группе животных проводилось тестирование психоневрологического статуса. В течение 3 минут пребывания крысы в «открытом поле» регистрировали двигательную активность (число пересечённых секторов), эмоциональный статус (количество стереотипных движений – груминг, фекальных болюсов) и ориентировочно-исследовательскую активность (вставание на задние лапы). В каждой экспериментальной группе использовали по 6 животных. Для изучения психоневрологического статуса в динамике исследование проводили в первые, затем на 4-е и 7-е сутки после введения исследуемых веществ.
Тест «открытое поле» показал увеличение двигательной активности животных на фоне исследуемых соединений. Об усилении двигательной активности, а следовательно, активирующем эффекте веществ свидетельствовало и учащение вертикальных стоек, отражая рост исследовательской активности. Заметно увеличивалась подвижность крыс, что приводило к достоверному росту числа пересеченных периферических сегментов.
Методика «открытое поле» выявила повышение вертикальной активности при введении целевых соединений (2, 3, 6 и 7). Необходимо отметить, что соединения в тесте увеличивают вертикальную активность животных более чем в 3 раза. Большинство исследуемых веществ повышали число «стоек» на 26-97%. Наибольшим анксиолитическим влиянием на ЦНС среди гетерилзамещённых 2,3-дигидро-1H-хиназолин-4-онов по результатам оценки двигательной и поисково-исследовательской активности обладают соединения (2, 3, 6 и 7). Интересно отметить, что данные соединения проявляют анксиолитическое действие, без седативного компонента со слабым психостимулирующим эффектом, по типу фенибута. Полученные экспериментальные данные статически обработаны и представлены в таблице 2.
Таблица 2
Результаты фармакологического исследования анксиолитической активности гетерилпроизводных 2,3-дигидро-1H-хиназолин-4-онов
|
Образец |
Кол-во пройденных секторов, Δ% |
Кол-во вертикальных стоек, Δ% |
Болюсы дефекаций, Δ%
|
Число уринаций, Δ% |
Груминг, Δ% |
Кол-во пройденных центральных секторов, Δ% |
|
Контр. |
9,8± 0,6 100% 11,6 ± 0,4 100% |
3,0± 0,2 100% 5,6± 0,4 100% |
0,3± 0,2 100% 1,1 ± 0,3 100% |
0,0± 0,0 100% 0,3± 0,2 100% |
2,0± 0,36 100% 0,1± 0,1 100% |
0,5± 0,2 100% 1,5 ± 0,4 100% |
|
1 |
19,8 ± 1,8 +70,6%* |
10,6 ±1,0 +89,3%* |
1,6 ± 0,3 +50,1%* |
0,1± 0,1 -66,6%* |
7,5 ± 0,4 +750%* |
11,5 ± 1,1 +766,6%* |
|
2 |
28,5 ± 2,0 +245,6%* |
19,0 ± 1,7 +339%* |
1,3 ± 0,21 +118,1%* |
0,0 ± 0,0 -30,0% |
6,3± 0,6 +630%* |
1,3 ± 0,2 +86,6%* |
|
3 |
34,6 ± 2,1 298,2%* |
24,0 ± 1,3 233,0%* |
0,66 ± 0,21 -40% |
0,1± 0,1 +53,3%* |
3,1± 0,4 +310%* |
2,8 ± 0,3 +233,3%* |
|
4 |
14,8 ± 1,1 +127,5%* |
6,6 ± 0,8 +11,7% |
0,8 ± 0,1 +72,7%* |
0,0 ± 0,0 -30% |
1,8± 0,3 +180%* |
1,3 ± 0,2 -13,3% |
|
5 |
19,8 ± 3,0 +70,6%* |
7,0 ± 0,7 +12,5% |
0,16 ± 0,1 +14,5% |
0,16± 0,1 +53,3% |
1,1± 0,6 +110%* |
1,3 ± 0,2 -13,3% |
|
6 |
29,5 ± 1,8 +254%* |
15,1 ± 2,4 +269%* |
1,3 ± 0,2 +18% |
0,0 ± 0,0 -30% |
7,0 ± 0,3 +700%* |
3,8 ± 0,6 +253%* |
|
7 |
36,0 ± 2,5 +310%* |
14,8 ± 0,6 +264%* |
0,1 ± 0,1 +9,1% |
0,1± 0,1 +33,3% |
7,8 ± 0,6 +780%* |
3,3 ± 0,4 +220%* |
|
Примечание - достоверность различий по сравнению с контролем: *- р <0,05 |
||||||
Из данных таблицы 2 видно, что максимальную активность проявляет соединение 7, что подтверждает данные молекулярного моделирования. Это может объясняться присутствием в целевой структуре фрагмента изоиндола.
Выводы
-
Данные, полученные в ходе молекулярного моделирования гетерилзамещённых 2,3-дигидро-1H-хиназолин-4-онов в бензодиазепиновом участке связывания ГАМКА рецептора, позволяют сделать вывод о том, что большинство соединений представленного ряда имеют высокую степень сродства с рецептором.
-
Фармакологические исследования в тесте «открытое поле» выявили, что соединение 7 является лидером анксиолитической активности, что подтверждает обоснованность молекулярного моделирования.
Рецензенты:
Оганесян Э.Т., д.фарм.н., профессор, заведующий кафедрой органической химии, Пятигорский медико-фармацевтический институт-филиал ГБОУ ВПО «ВолгГМУ» Минздрава России, г. Пятигорск.
Кодониди И.П., д.фарм.н., доцент кафедры органической химии, Пятигорский медико-фармацевтический институт-филиал ГБОУ ВПО «ВолгГМУ» Минздрава России, г.Пятигорск.
Библиографическая ссылка
Бандура А.Ф., Арльт А.В., Воронков А.В., Сочнев В.С., Кодониди М.И., Золотых Д.С., Луговой И.С., Базганов А.Ю. МОЛЕКУЛЯРНОЕ МОДЕЛИРОВАНИЕ И АНКСИОЛИТИЧЕСКАЯ АКТИВНОСТЬ ГЕТЕРИЛЗАМЕЩЕННЫХ 2,3-ДИГИДРО-1H-ХИНАЗОЛИН-4-ОНА // Современные проблемы науки и образования. 2014. № 4. ;URL: https://science-education.ru/ru/article/view?id=14147 (дата обращения: 07.06.2026).



