Введение. Вопросы гистогенеза тканей, несмотря на кажущуюся, оставляют ряд неразрешенных вопросов для исследователей [1, 3, 6]. Наличие современных методов исследования позволяет выявить особенности ультраструктурной организации и ее органоспецифичность в ходе гистогенеза. Расшифровка тканевых, цитологических и молекулярных механизмов гистофизиологии тканей чрезвычайно важна для разработки новых эффективных методов профилактики и лечения различных заболеваний [2, 7, 8]. Мышечные ткани входят в состав практически всех полых органов. Сочетание гладкой и поперечно-полосатой мышечной тканей уникально для ряда органов, например пищевода, замыкательного аппарата прямой кишки [1, 4]. Влагалище в своем дистальном отделе содержит волокна исчерченной ткани, которые постепенно заменяются на гладкую мышечную ткань.
Цель работы – изучить ультраструктурные особенности постнатального гистогенеза мышечных тканей влагалища млекопитающих.
Материалы и методы исследования. В работе использован материал от белых беспородных крыс женского пола разных периодов постнатального развития в соответствии с «Правилами проведения работ с использованием экспериментальных животных». Для проведения светового исследования использовали фиксацию материала в 10% нейтральном формалине на фосфатном буфере (рН-7,4), заливку в парафин. Для электронной микроскопии использовали префиксацию в 2,5% глутаральдегиде на 0,2 М какодилатном буфере (рН 7,4), фиксацию в 1% ОsО4 и заливали в аралдит. Для обеспечения прицельного электронно-микроскопического анализа получали серийные полутонкие срезы толщиной 1-2 мкм, которые окрашивали 1% раствором метиленового синего. Прицельные ультратонкие срезы толщиной 200-500 нм просматривали в электронном микроскопе Hitachi-HU-12.
Результаты исследования и их обсуждение. При рождении женский половой тракт претерпевает региональную морфологическую специализацию, которая дифференцирует яйцеводы, матку, шейку, верхнюю часть влагалища. Но окончательное созревание происходит после рождения, до пубертатного периода. В период новорожденности при ультраструктурном исследовании гладкая мышечная ткань мышечной оболочки представлена гетероморфной популяцией клеток. Сохраняются миобласты вытянутой формы, с небольшими отростками. Большая часть клеток представлена малодифференцированными лейомиоцитами, имеющими овальное или вытянутое ядро, с крупными глыбками гетерохроматина, чаще лежащими пристеночно. Иногда видны одно - два довольно крупных ядрышка, кариолемма с небольшими инвагинациями. В цитоплазме – крупные липидные капли. Пучки миофиламентов лежат в разных направлениях, еще рыхлые по своей организации. Плотные тельца формируются и определяются как в глубине цитоплазмы, так и на плазмолемме (рис. 1).
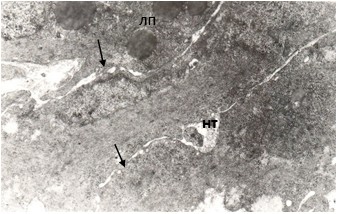
Рис. 1. Ультраструктурная организация малодифференцированных лейомиоцитов. Период новорожденности крысы. лп – липидные капли, нт – нервные терминали, ↑ – мембранные контакты. Ув. 10000.
На первой неделе постнатального развития темп процессов специфической диффференцировки и интеграции повышается. Миоциты отличаются электронной плотностью цитоплазмы, что объясняется, в первую очередь, разными темпами дифференцировки и, соответственно, разным количеством миофиламентов в цитоплазме. Между мышечными клетками обнаруживается большое количество нервных терминалей, которые обладают индуцирующей способностью. Лейомиоциты имеют еще многочисленные отростки, устанавливаются многочисленные и разнохарактерные межклеточные связи. Хорошо развит кавеолярный аппарат, необходимый для обмена веществ. Много рибосом и полисом, которые необходимы для интенсивно протекающего миофиламентогенеза. Профили грЭПС разветвлены, митохондрии активные, с активно формирующимися кристами. Также довольно часто встречаются клетки, находящиеся на разных стадиях апоптоза. На более ранних стадиях они характеризуются электронно-плотным ядром, с крупными глыбками гетерохроматина и глубокими инвагинациями кариолеммы. Перинуклеарное пространство резко расширено, иногда с повреждением ядерной мембраны, также расширены и канальца ЭПС (рис. 2).
С рождением интенсифицируется процесс дифференцировки исчерченных мышечных компонентов. В образовавшихся к концу эмбриогенеза миотубах происходит значительное увеличение объема цитоплазмы. При этом в новообразованных миосимпластах слияние миобластов еще не завершилось, и в их внутренних областях часто можно наблюдать довольно протяженные участки еще нераспавшихся плазмолемм миобластов. Миофибриллы немногочисленны и не всегда параллельны длинной оси симпласта, пока занимают периферическое положение. Некоторые миофибриллы довольно толстые и длинные.
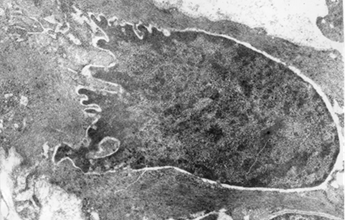
Рис. 2. Ультраструктурная организация апоптотически измененного миоцита. 1 сутки постнатального развития крысы. ↑ – расширение перинуклеарного пространства, ↑↑ – расширение канальцев грЭПС. Ув. 10000.
Начинает формироваться принцип саркомерной организации миофибрилл (рис. 3). К этому периоду развития в миофибриллах можно различить формирующиеся Z- линии.
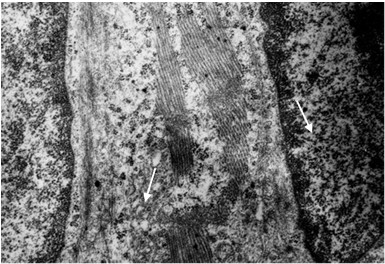
Рис. 3. Ультраструктурная организация встраивания миобластов в миосимпласт. 1 сутки постнатального развития крысы. ↑ – участок слияния плазмолемм миобластов. Ув. 10000.
Наряду с миофибриллами, в цитоплазме можно различить и миофиламенты. Они обычно расположены поодиночке и не ориентированы вдоль оси миосимпласта, часть из них объединены в небольшие пучки.
После рождения, на 7-е сутки постнатального развития при прицельном исследовании нам удалось обнаружить лейомиоциты, обладающие разной электронной плотностью с высоким содержанием миофиламентов. Ряд исследователей (Зашихин А.Л., 1991, Агафонов Ю.В., 1999) трактуют их как «светлые» и «темные» миоциты, которые отличаются своей функциональной активностью (рис. 4). Так же, как и др. исследователи, мы не обнаружили никакой определенной закономерности их расположения в пласте клеток. Формирование хорошо развитого сократительного аппарата свидетельствует о высокой степени дифференцировки клеток и повышении функциональной активности клеток.
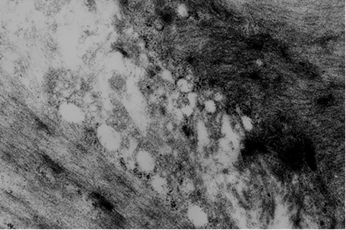
Рис. 4. Ультраструктурная организация фрагментов «светлого» и «темного» лейомиоцитов стенки влагалища. 7 сутки постнатального развития крысы. Ув. 10000.
Следует также отметить увеличение количества и длины щелевидных контактов между миоцитами. Кроме них клетки контактируют и с помощью довольно протяженных простых соединений. В то же время толщина соединительнотканных прослоек между миоцитами становится несколько больше, а ткань в них грубее.
В 1 месяц постнатального развития при электронно-микроскопическом исследовании строение мышечной оболочки во многом подобно зрелому. Миоциты имеют очень вытянутую форму. При этом объем цитоплазмы в центральной околоядерной части клетки увеличивается незначительно. Более заметно удлинение периферических участков миоцитов. Все ядра миоцитов вытянутой, палочковидной формы. Следует отметить уменьшение размеров ядрышек, что свидетельствует о снижении синтетической активности клеток. Цитоплазма миоцитов отличается по электронной плотности, но если на более ранних сроках развития эти различия были обусловлены количеством миофиламентов в клетках, то сейчас и их перераспределением в цитоплазме. В дистальных (по отношению к ядру) участках миоцитов меньшее содержание миофиламентов можно расценивать как следствие распространения миофиламентогенеза от ядросодержащей части клетки к периферии. Зоны активного синтеза сократительных структур, как правило, сопровождает хорошо развитый кавеолярный аппарат. В то же время некоторые клетки содержат скопления митохондрий и свободных рибосом среди которых расположены гранулы гликогена. Это сохраняющийся в популяции синтетический тип лейомиоцитов. Растущие концы клеток образуют с соседними простые контакты и десмосомы. Кроме этих типов соединений в более зрелых центральных участках клеток можно наблюдать и нексусы.
Пубертатный период у крыс начинается в 8 недель постнатального развития. В этот период мы не наблюдали значительных различий в строении как гладкомышечных, так и поперечнополосатых компонентов оболочки по сравнению с четвертой неделей постнального развития.
В 6 месяцев постнатального развития мышечная оболочка имеет зрелое строение. Гладкая мышечная ткань представлена, в основном, дифференцированными миоцитами, среди которых различают, в зависимости от уровня состояния сократительного аппарата, «светлые» и «темные». Эти клетки относятся к сократительному фенотипу. Также встречаются миоциты синтетического типа с развитыми профилями гр ЭПС и скоплениями рибосом и полисом. В популяции дефинитивной гладкой мышечной ткани определяются и единичные миобласты, и дифференцирующиеся миоциты. Ядра гладких миоцитов характеризуются умеренной электронной плотностью. В них, наряду с достаточно большим количеством пристеночного гетерохроматина, содержится и довольно много эухроматина. Ядрышки отличаются небольшими размерами. Эти черты строения ядер могут объясняться предположением, что в этом возрасте интенсивность белок-синтетических процессов, вероятно, стабилизируется и поддерживается на определенном не высоком уровне.
Цитоплазма миоцитов почти полностью «забита» миофиламентами. Причем, если на первом месяце постнатального развития миоциты отличались разной электронной плотностью цитоплазмы, то сейчас этот показатель выравнивается, свидетельствует о приобретении подавляющим большинством клеток дефинитивного строения. Миофиламентов становится так много, что границы между миофибриллами почти не определяются и часто миофиламенты имеют вид одной большой миофибриллы. В то же время, как и ранее, митохондрии остаются не многочисленными, однако, характеризуются развитыми кристами. Количество гликогена относительно не велико.
Часть миоцитов, наряду с развитым сократительным аппаратом, содержат скопления рибосом и канальцев ЭПС. Это клетки синтетического типа. У половозрелых животных мы не смогли обнаружить миоциты в состоянии апоптоза.
Поперечно-полосатая мышечная ткань образована сформированными мышечными волокнами, имеющими хорошо развитые миофибриллы с саркомерным принципом организации. Ядра миосимпластов располагаются на периферии. Сарколемма представляет собой типичную мембрану и прилегает к саркоплазме. Базальная пластинка повторяет контуры сарколеммы. Она отличается меньшей электронной плотностью, содержит в своем составе аморфное вещество и фибриллярные компоненты. Саркоплазма заполнена миофибриллами, имеющими четкий саркомерный принцип организации. В пределах саркомера хорошо определяются А - , I – диски, Z – линии, Н – зона; достаточно отчетливо контурируются М – линии. Отдельные миофибриллы отделены друг от друга участками саркоплазмы, в которой на уровне Z – линий располагаются митохондрии, округлой или овальной формы. Кристы располагаются компактно, матрикс имеет умеренную плотность. Саркоплазматическая сеть в мышечных волокнах развита умеренно, канальцы расположены между миофибриллами. Скопления рибосом и гликогена, липидные включения (чаще округлой или овальной формы) определяются между миофибриллами и под сарколеммой. Миосателлитоциты являются постоянным компонентом исчерченной мышечной ткани стенки влагалища. Они отделены от миосимпласта собственной плазмалеммой, а со стороны межклеточного вещества покрыты базальной мембраной; имеют плотное, богатое гетерохроматином ядро.
Таким образом, популяция лейомиоцитов дефинитивной гладкой мышечной ткани мышечной оболочки влагалища представлена дифференцированными клетками. Тем не менее, популяция не является однородной и в ней присутствуют малодифференцированные и бластные элементы. В процессе специфической дифференцировки в постнатальный период происходит усложнение ультраструктурной организации, интенсивное развитие сократительного аппарата (миофиламенты, плотные тельца, прикрепительные полоски, кортикальные везикулы). Исчерченная мышечная ткань в процессе постнатального развития также характеризуется продолжением активной дифференцировки и образованием мышечных волокон, усложнением их ультраструктурной организации. В дефинитивной ткани они имеет классический саркомерный принцип организации, образования молодых мышечных волокон мы не обнаружили. Наличия контактов между гладкой и поперечно-полосатой мышечной тканью на всем протяжении постнатального гистогенеза и в зрелой ткани не установлено.
Рецензенты:
Суворова Г.Н., д.м.н., профессор, заведующая кафедрой анатомии человека, ГБОУ ВПО «Самарский государственный медицинский университет» Минздрава России, г.Самара.
Колсанов А.В., д.м.н., профессор, заведующий кафедрой заведующий кафедрой оперативной хирургии и клинической анатомии человека с курсом инновационных технологий ГБОУ ВПО «Самарский государственный медицинский университет» Минздрава России, г.Самара.
Библиографическая ссылка
Шурыгина О.В., Ямщиков Н.В., Абрамов В.Н., Балашов В.П. УЛЬТРАСТРУКТУРНЫЕ АСПЕКТЫ ГИСТОГЕНЕЗА МЫШЕЧНЫХ ТКАНЕЙ СТЕНКИ ВЛАГАЛИЩА МЛЕКОПИТАЮЩИХ В ПОСТНАТАЛЬНЫЙ ПЕРИОД РАЗВИТИЯ // Современные проблемы науки и образования. 2014. № 3. ;URL: https://science-education.ru/ru/article/view?id=13787 (дата обращения: 13.05.2026).



