Введение
Необратимые повреждения плечевого сустава различной этиологии приводят к выраженному нарушению функции верхней конечности, восстановление которой является сложной задачей. Повреждение конечности приводит к неспособности самообслуживания, снижается качество жизни. Поэтому лечение тяжелых повреждений плечевого сустава продолжает оставаться одной из значимых проблем современной ортопедии. Развитие эндопротезирования плечевого сустава как варианта решения проблемы уходит своими корнями к 1893 году, когда французский хирург Жюль Эмиль Пеан впервые имплантировал искусственный сустав пациенту с туберкулезным поражением плечевого сустава. При этом он констатировал восстановление функции и мышечной силы [2]. Дальнейшее развитие эндопротезирования сопровождалось появлением новых типов имплантатов (в том числе и реверсивного с 1970 года) и их модифицированием с целью улучшения выживаемости эндопротеза. При этом отмечено, что использование реверсивного типа эндопротеза является наиболее функционально выгодным у больных с повреждением манжеты ротаторов [3]. Анализ литературы показывает, что основное количество публикаций касательно этой темы отражено в иностранной литературе, а число отечественных публикаций чрезвычайно мало. Отмечается неудовлетворенность хирургов функциональным восстановлением плечевого сустава после его артропластики [1]. Таким образом, поиск путей улучшения функциональных результатов актуален и обоснован.
Целью нашей работы было изучение функционального восстановления плечевого сустава после эндопротезирования, в зависимости от заболевания, сохранности коротких ротаторов плеча, состояния дельтовидной мышцы и n. axillaris, который ее иннервирует. Выявление технических моментов и факторов, препятствующих или осложняющих функциональное восстановление.
Материалы и методы
В исследование были включены 38 больных с заболеваниями плечевого сустава, которые проходили лечение в травматолого-ортопедическом отделении №8 РНЦ «ВТО» им. акад. Г.А. Илизарова в период с 2010 по 2013 г. Средний возраст составил 65 лет (от 26 до 81 года). Больных женского пола было 25, мужского – 13. С учетом характерных различий в клинической картине заболеваний, данные больные были разделены на две группы.
Первую группу (29 человек) составили пациенты с застарелой посттравматической патологией плечевого сустава, сопровождающейся утратой целостности ротаторной манжеты (ложный сустав хирургической шейки плеча – 4 пациента, застарелый переломовывих проксимального отдела плечевой кости – 5 пациентов, дефект проксимального отдела плечевой кости – 6 пациентов, неправильно консолидированный перелом в проксимальном отделе плечевой кости – 12 пациентов, несостоятельность вращающей манжеты после однополюсного эндопротезирования – 2 пациента). Из них 11 человек были ранее оперированы.
Во вторую группу вошли 9 пациентов, которые имели заболевания плечевого сустава нетравматического генеза (артроз III стадии – 3 пациента, аваскулярный некроз головки плечевой кости – 2 пациента, rotator cuff tear arthropaty – 4 пациента).
Учитывая наличие признаков необратимого повреждения манжеты ротаторов, всем 38 пациентам было выполнено тотальное гибридное (цементная ножка протеза) эндопротезирование плечевого сустава с использованием реверсивного эндопротеза (Delta Xtend, DePuy, Франция). Давность заболевания до операции колебалась от 1 до 25 лет (в среднем 4 года).
Функция плечевого сустава (в сравнении с контрлатеральным) была изучена у всех пациентов до операции и спустя три месяца после нее с использованием оценочной шкалы CONSTANT [4]. Клиническое обследование производилось в стандартизированной форме, сидя на стуле с равномерным распределением веса тела на седалищные бугры. Техника измерений выполнялась согласно рекомендациям Европейского Общества Хирургии Плечевого и Локтевого суставов (ESSES) [5]. Для измерения углов отведения и сгибания в плечевом суставе использовался стандартный угломер. Силу отведения и сгибания в плечевом суставе измеряли при помощи пружинного ручного динамометра (измерение в кг).
Шестнадцати больным (5 – мужского и 11 – женского пола) в возрасте от 32 до 76 лет проведено комплексное электрофизиологическое обследование пораженной и интактной конечностей. Использованы методы глобальной и стимуляционной электромиографии. Объект исследования: m. deltoideus. М-ответы: форма раздражающих стимулов – прямоугольная, длительность – 1 мс, интенсивность – супрамаксимальная; способ отведения - униполярный; анализируемый показатель - амплитуда "от пика до пика". Глобальная ЭМГ: функциональная проба – "произвольное максимальное напряжение"; тип отведения – биполярный; диаметр электродов – 8 мм, межэлектродное расстояние – 10 мм; анализируемые параметры при использовании теста «произвольное максимальное напряжение» – частота следования колебаний и средняя амплитуда суммарной ЭМГ, программно рассчитываемые по фрагментам экранных копий MVA-теста. Аппаратурное обеспечение: 4-канальная цифровая система ЭМГ и ВП "Viking IV" (Nicolet Biomedical, США). Обследуемые больные распределены на 2 группы: первая – пациенты, имеющие посттравматическую патологию плечевого сустава (10 пациентов), вторая – пациенты, с заболеваниями плечевого сустава нетравматического генеза (6 человек). В качестве контроля использованы показатели ЭМГ показатели интактной конечности. Статистическая обработка исходных данных выполнялась с использованием табличного редактора Exсel.
Результаты исследования
Результаты обследования пациентов согласно оценочной шкале Constant для плечевого сустава представлены в таблице 1.
Из таблицы следует, что общее количество баллов по шкале для первой группы пациентов (имеющих посттравматические изменения) до операции составило 23. Среди них на болевой синдром пришлось в среднем 5 баллов (15 баллов означает отсутствие болей). Величина активного сгибания у данных пациентов до операции составила в среднем 38°, а активное отведение – 32°. Общее количество баллов по Constant score для пациентов 2 группы в среднем составило 36,8 баллов, из них на болевой синдром пришлось 1,1 балл, средний угол активного сгибания в плечевом суставе – 60,5°, отведения – 52°.
Таким образом, балльные показатели у пациентов первой группы по шкале Constant были хуже на 37,5 %, нежели у пациентов 2 группы с заболеваниями плечевого сустава нетравматического генеза. Функциональные показатели у пациентов 1 группы были хуже на 37,2% при сгибании и на 38,4% при отведении. Это обусловлено характером патологии. Однако болевой синдром на 78% был выраженнее у пациентов 2 группы.
Усредненные результаты суммарной ЭМГ m. deltoideus у пациентов первой и второй групп до и через год после операции сведены в таблице 2.
Из таблицы видно, что амплитуда суммарной ЭМГ m. deltoideus ниже в группе пациентов с посттравматической патологией (11,6% – 1 группа, 38,2% – 2 группа в сравнении с интактной). Значимых различий в частоте следования колебаний не выявлено. При стимуляционной ЭМГ у пациентов 1 группы выявлено наибольшее снижение М-ответа: на интактной стороне амплитуда М-ответа была 7,66±0,9мВ, а на поврежденной стороне – 4,2± 0,4 мВ, то есть аксонопатия n.axillaris составила 45%. Это обусловлено грубой травмой плечевого сустава, имеющейся у этих пациентов в анамнезе.
Таблица 1. Клиническая характеристика обеих групп пациентов
|
Параметр |
Баллы |
Посттравматическая патология (n-29) |
Дегенеративное заболевание (n-9) |
|||
|
До операции |
После операции |
До операции |
После операции |
|||
|
1 |
2 |
3 |
4 |
5 |
6 |
|
|
1. Болевой синдром |
|
|
|
|
|
|
|
Выраженный |
0 |
9 |
- |
7 |
- |
|
|
Умеренный |
5 |
12 |
6 |
2 |
1 |
|
|
Слабый |
10 |
7 |
12 |
- |
5 |
|
|
Отсутствует |
15 |
1 |
11 |
- |
3 |
|
|
2. Уровень жизненной активности |
|
|
|
|
|
|
|
Беспокойный сон |
да |
0 |
7 |
3 |
5 |
1 |
|
иногда |
1 |
16 |
10 |
2 |
3 |
|
|
нет |
2 |
6 |
16 |
2 |
5 |
|
|
Ограничение в досуге/спорте |
да |
0 |
24 |
12 |
6 |
1 |
|
умеренное |
2 |
5 |
10 |
4 |
6 |
|
|
нет |
4 |
- |
7 |
- |
2 |
|
|
Ограничение повседневной активности |
да |
0 |
23 |
7 |
6 |
1 |
|
умеренное |
2 |
4 |
14 |
4 |
5 |
|
|
нет |
4 |
2 |
8 |
- |
3 |
|
|
3. Возможное поднятие руки |
|
|
|
|
|
|
|
До талии |
2 |
1 |
- |
- |
- |
|
|
До мечевидного отростка |
4 |
18 |
- |
- |
- |
|
|
До шеи |
6 |
5 |
3 |
5 |
1 |
|
|
До макушки |
8 |
4 |
12 |
3 |
1 |
|
|
Над головой |
10 |
1 |
14 |
1 |
7 |
|
|
1 |
2 |
3 |
4 |
5 |
6 |
|
|
4.Сила мышц при отведении (кг) |
|
|
|
|
|
|
|
0 - 0,4 |
0 |
20 |
3 |
- |
- |
|
|
0,5 - 1,5 |
2 |
4 |
4 |
1 |
1 |
|
|
1,6 - 3,0 |
5 |
3 |
10 |
3 |
1 |
|
|
3,1 - 4,5 |
8 |
1 |
8 |
- |
- |
|
|
4,6 - 6,0 |
11 |
1 |
- |
2 |
- |
|
|
6,1 - 7,5 |
14 |
- |
2 |
2 |
2 |
|
|
7,6 - 9,0 |
17 |
- |
1 |
1 |
2 |
|
|
9,1 - 10,5 |
20 |
- |
- |
- |
2 |
|
|
10,6 - 12 |
23 |
- |
- |
- |
- |
|
|
более 12 |
25 |
- |
1 |
- |
1 |
|
|
ОБЪЕМ ДВИЖЕНИЙ |
|
|
|
|
|
|
|
5. Переднее сгибание |
|
|
|
|
|
|
|
0-30 град |
0 |
16 |
6 |
- |
- |
|
|
31 - 60 град |
2 |
10 |
8 |
4 |
1 |
|
|
61 - 90 град |
4 |
3 |
3 |
4 |
1 |
|
|
91 - 120 град |
6 |
- |
7 |
1 |
1 |
|
|
121 - 150 град |
8 |
- |
4 |
- |
4 |
|
|
151 - 180 град |
10 |
- |
1 |
- |
2 |
|
|
6. Отведение |
|
|
|
|
|
|
|
0 – 30 град |
0 |
17 |
6 |
- |
- |
|
|
31 - 60 град |
2 |
10 |
7 |
6 |
1 |
|
|
61 - 90 град |
4 |
2 |
7 |
3 |
1 |
|
|
91 - 120 град |
6 |
- |
6 |
1 |
1 |
|
|
121 - 150 град |
8 |
- |
2 |
- |
5 |
|
|
151 - 180 град |
10 |
- |
1 |
- |
1 |
|
|
7. Наружная ротация |
|
|
|
|
|
|
|
Рука за головой, локоть вперед |
2 |
19 |
27 |
8 |
9 |
|
|
Рука за головой, локоть назад |
2 |
4 |
21 |
4 |
8 |
|
|
Рука на макушке, локоть вперед |
2 |
15 |
25 |
7 |
8 |
|
|
Рука на макушке, локоть назад |
2 |
1 |
17 |
3 |
6 |
|
|
Полное поднятие |
2 |
- |
3 |
- |
4 |
|
|
8. Внутренняя ротация |
|
|
|
|
|
|
|
Задняя поверхность бедра |
0 |
3 |
- |
- |
- |
|
|
Ягодица |
2 |
5 |
8 |
2 |
2 |
|
|
Пояснично-крестцовая область |
4 |
13 |
10 |
2 |
2 |
|
|
Талия (L-3) |
6 |
4 |
5 |
2 |
2 |
|
|
Т-12 позвонок |
8 |
2 |
3 |
3 |
2 |
|
|
Межлопаточная область (Т-7) |
10 |
2 |
3 |
- |
1 |
|
У пациентов 2 группы на интактной стороне амплитуда М-ответа была 8,43±0,64мВ, а на поврежденной стороне – 7,6± 0,12 мВ, то есть аксонопатия n.axillaris у данных больных составила 9,8 %, что гораздо меньше, чем у пациентов с посттравматической патологией.
После операции в 1 группе пациентов усредненный показатель по Constant score увеличился до 50,1 баллов. При этом отмечается купирование болевого синдрома – 10,8 баллов, увеличение углов активного сгибания в плечевом суставе в среднем до 75° и отведения 81°. Послеоперационные показатели для пациентов 2 группы: общий показатель по Constant score составил 68,7 баллов, уменьшение болевого синдрома (11,1 баллов), сгибание в среднем 128°, отведение 131°.
Таким образом, общий показатель по Constant score после эндопротезирования у пациентов 1 группы улучшился на 54%, болевой синдром снизился на 53%, а углы сгибания и отведения увеличились в среднем на 49% и 60% соответственно. Во второй группе пациентов также отмечается улучшение суммарных показателей после эндопротезирования. Общий показатель по Constant score увеличился на 46,4%, уменьшение болевого синдрома на 90%, угол сгибания в плечевом суставе после операции увеличился на 52,7%, отведения на 60,3%. Следует отметить, что пациенты с заболеваниями нетравматического генеза (2 группа) имели лучшие результаты после эндопротезирования.
Из таблицы 2 видно, что на контроле минимум через год после эндопротезирования, амплитуда суммарной ЭМГ m. deltoideus в первой группе увеличилась до 0,98±0,28мВ, а во второй группе до 1,4±0,16мВ. Таким образом, пациенты 1 группы имели более выраженное улучшение (на 82% против 47% у пациентов 2 группы) при глобальном ЭМГ исследовании. Однако изучение состояния n.axillaris при стимуляционной ЭМГ показало, что через год после операции у всех обследованных больных была отмечена несущественная положительная динамика. Так, увеличение М-ответа n.axillaris составило в среднем: пациенты 1 группы – только на 12,5% (4,8±0,4мВ), 2 группы – на 3,4% (7,9±0,3мВ). Данный факт свидетельствует о сохранении дисфункции n.axillaris и через год после операции.
Таблица 2. Амплитуда (А) и частота следования колебаний (F) суммарной ЭМГ (M±m) m. deltoideus, полученные при глобальной электромиографии
|
Показатели |
Конечность |
1 группа (n - 10) |
2 группа (n - 6) |
||
|
m. deltoideus |
m.deltoideus |
||||
|
До операции |
После операции |
До операции |
После операции |
||
|
А (мВ)
|
пораженная |
0,17 ± 0,13 |
0,98 ± 0,28 |
0,73 ± 0,1 |
1,4± 0,16 |
|
интактная |
1,46 ± 0,18 |
1,51± 0,35 |
1,91 ± 0,3 |
1,8± 0,35 |
|
|
% от интактной конечности |
11,6 |
64,9 |
38,2 |
77,7 |
|
|
F (кол./с) |
пораженная |
129 ± 45,8 |
136 ± 35, 3 |
145 ± 13,5 |
158± 0,16 |
|
интактной |
154 ± 9,36 |
151± 10,4 |
147 ± 12,1 |
170± 0,35 |
|
С целью выявления причин неудач после эндопротезирования нами детально проанализированы пациенты с плохими результатами лечения (менее 16 баллов по Constant score). Всего их было 7 человек, шестеро из 1 группы и один из второй.
Пациент К., 37 л. из второй группы поступил на лечение с диагнозом аваскулярного некроза головки плечевой кости в сочетании с массивным дефектом вращающей манжеты плеча. Относительно легкий в плане курации клинический случай показал плохой результат из-за нарушения техники имплантации эндопротеза. А именно, лопаточный компонент был установлен слишком низко на гленоид, а плечевой компонент в нормопозицию (Рис. 1). Все это привело к избыточному усилию при редукции эндопротеза с чрезмерным натяжением мягких тканей. Впоследствии у пациента сохранялся болевой синдром, как в самом суставе, так и в средней трети плеча (месте прикрепления дельтовидной мышцы), а также отсутствие увеличения объема движений.
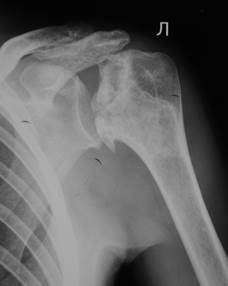
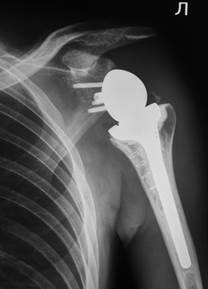
Рис. 1. Рентгенограммы пациента К., 37 л. до и после лечения.
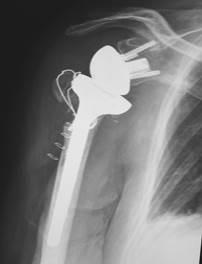
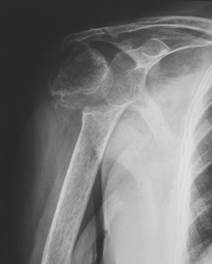
Рис. 2. Рентгенограммы до и после лечения с использование проволочного шва.
Остальные 6 пациентов с неудовлетворительными результатами были из первой группы и имели посттравматическую патологию: постинфекционный дефект проксимального отдела плечевой кости с наличием спейсера – 2 пациента, последствие оскольчатого перелома проксимального отдела плечевой кости после неудачного остеосинтеза – 3 пациента, застарелый переломо-вывих проксимального отдела плеча – 1 пациент. Непосредственными причинами развития плохого результат явились: нейропатия n.axillaris, атрофия дельтовидной мышцы, невосстановленное прикрепление коротких наружных ротаторов (либо несостоятельный остеосинтез бугорков в одном случае). При этом у трех из этих пациентов в раннем послеоперационнм периоде отмечались вывихи в эндопротезе. Учитывая данные литературы [6, 7, 8] и собственные наблюдения, важным моментом при имплантации эндопротеза у таких пациентов является выделение, мобилизация и рефиксация наружных коротких ротаторов. При этом фиксация фрагмента большого бугорка с мышцами при помощи нитей в застарелых случаях не всегда стабильна. В таких случаях оправдано использование проволочного шва (Рис. 2). Также следует отметить, что те пациенты, которым была выполнена стабильная реинсерция малой круглой мышцы, после эндопротезирования показывали сравнительно лучшие функциональные результаты. У всех пациентов с посттравматической патологией, перенесших технически сложное эндопротезирование, обосновано применение иммобилизации конечности в отводящем ортезе сроком на 5-6 недель.
Выводы
Изучение результатов эндопротезирования плечевого сустава показало существенное клиническое и функциональное улучшение, наблюдаемое во всех группах. Однако пациенты с заболеваниями плечевого сустава нетравматической этиологии (первичный остеоартроз плечевого сустава, аваскулярный некроз головки плечевой кости, артропатии, связанные с повреждением ротаторной манжеты) показали относительно лучшие результаты. Залогом хорошего функционального исхода у этих больных в первую очередь является правильное позиционирование компонентов эндопротеза и создание оптимального натяжения мягких тканей. У больных, имеющих посттравматические артриты, деформации, костные дефекты и состояния, требующие ревизионного вмешательства, в среднем были выявлены относительно худшие результаты лечения. Это обусловлено характером патологии: ретракцией мышц, повреждением нервов, рубцовым и жировым перерождением тканей, дефицитом ткани капсулы плечевого сустава и ротаторной манжеты, проблемами дельтовидной мышцы, а также техническими трудностями во время операции. Поэтому залогом хорошего функционального результата у данных пациентов в первую очередь является строгий отбор пациентов, адекватная оценка состояния дельтовидной мышцы и положительный прогноз в плане восстановления коротких ротаторов, соблюдение иммобилизации в послеоперационном периоде. Атрофия дельтовидной мышцы (невозможность активного отведения), нейропатия подкрыльцового нерва, невозможность восстановления коротких ротаторов при отсутствии суставных болей, являются весомыми аргументами для отказа от использования реверсивного эндопротеза.
Рецензенты:
Солдатов Ю.П., д.м.н., профессор, заведующий кафедрой травматологии и ортопедии, детской вертебрологии усовершенствования врачей ТюмГМА, ФГБУ РНЦ «ВТО» им. ак. Г.А. Илизарова Минздрава России, г. Курган.
Чегуров О.К., д.м.н., заведующий лабораторией реконструктивного эндопротезирования и артроскопии, ФГБУ РНЦ «ВТО» им. ак. Г.А. Илизарова Минздрава России, г. Курган.
Атманский И.А., д.м.н., профессор, заведующий кафедрой травматологии и ортопедии ГБОУ ВПО «ЮУГМУ» Минздрава России, г. Челябинск.
Библиографическая ссылка
Чирков Н.Н., Каминский А.В., Поздняков А.В. СРЕДНЕСРОЧНЫЕ ФУНКЦИОНАЛЬНЫЕ ИСХОДЫ ТОТАЛЬНОГО ЭНДОПРОТЕЗИРОВАНИЯ ПЛЕЧЕВОГО СУСТАВА С ИСПОЛЬЗОВАНИЕМ РЕВЕРСИВНОГО ЭНДОПРОТЕЗА // Современные проблемы науки и образования. 2014. № 3. ;URL: https://science-education.ru/ru/article/view?id=13339 (дата обращения: 08.04.2026).



