Введение
Нестероидные противовоспалительные препараты (НПВП) являются одним из наиболее широко применяемых классов лекарственных средств. Их несомненными достоинствами является хорошо доказанная эффективность, простота использования и финансовая доступность [4, 8]. Однако применение НПВП связано с возможностью развития серьезных побочных эффектов, наиболее частым из которых является поражение желудочно-кишечного тракта, характеризующееся развитием эрозий, язв и опасных осложнений – кровотечения и перфорации [6, 9, 10] Это обуславливает целесообразность дальнейшего поиска эффективных методов профилактики подобных осложнений. Перспективным в этом направлении является применение лекарственных препаратов антиоксидантного действия [2, 7].
Работа выполнялась в рамках Приоритетного направления развития Национального исследовательского Мордовского государственного университета им. Н.П. Огарёва «Энергосбережение и новые материалы» (утверждено приказом №757 Министерства образования и науки Российской Федерации 9 июня 2010 г.).
Целью работы явилось исследование противоязвенного профилактического эффекта этоксидола и некоторых производных аминогексановой и ацетилглютаминовой кислот при индукции поражения слизистой оболочки желудка введением диклофенака.
Материалы и методы. Эксперименты выполнены на базе центральной научно-исследовательской лаборатории Медицинского института ФГБОУ ВПО «МГУ им. Н.П.Огарева» в соответствии со статьей 11 Хельсинской декларации Всемирной медицинской ассоциации (1964 г.), «Международными рекомендациями по проведению медико-биологических исследований с использованием животных» (1985 г.) и «Правилами лабораторной практики в Российской Федерации» (приказ МЗ и СР РФ № 708н от 23.08.2010 г.) на 84 белых нелинейных половозрелых крысах обоего пола массой 200-250 г., содержащихся в стандартных условиях вивария.
Индукцирование язвенного поражения желудка осуществлялось путем внутримышечного введения диклофенака в дозе 50 мг/кг один раз в сутки в течение двух дней.
В работе исследовались 3-оксипиридина малат - (2-этил-6-метил-3-гидроксипиридина гидроксибутандиоат) – синтезированный на базе ВНЦ БАВ, запатентованный под названием «этоксидол», проявляющий мембранопротекторное, антигипоксическое, анксиолитическое, ноотропное, антиаритмическое и проитвоишемическое действие [1, 3]. В работе использовалась субстанция препарата, синтезированная во Всероссийском научном центре по безопасности биологически активных веществ (ВНЦ БАВ) (Старая Купавна, Россия) (директор Н.М. Митрохин).
В работе также исследовались отечественные оригинальные органические соединения, впервые синтезированные в ВНЦ БАВ под руководством заведующей отделом химии и технологии лекарственных средств, лауреата Государственной премии РФ, доктора химических наук, профессора С.Я. Скачиловой (в виде порошкообразных субстанций). ЛХТ-1-09 (производное N-ацетил-6-аминогексановой кислоты и 3-оксипиридина); ЛХТ-1-06 (производное N-ацетил-6-аминогексановой кислоты и этилтиодиазола); ЛХТ-2-09 (производное N-ацетилглютаминовой кислоты и 3-оксипиридина); ЛХТ-3-09 (цинковая соль N-ацетил-6-аминогексановой кислоты); ЛХТ-1-05 (производное N-ацетил-6-аминогексановой кислоты и лидокаина).
Животные, составившие контрольную группу (п=12), не получали какой-либо фармакологической коррекции. Животные всех опытных групп с 1 по 5 сутки эксперимента получали внутримышечно один раз в день какой-либо из исследованных препаратов или соединений в изомолярных дозах. На 5 и 6 сутки опыта проводились в/м инъекции диклофенака в дозе 50 мг/кг. Животные в опытной группе №1 (п=12) получали в/м этоксидол в дозе 25 мг/кг, в опытной группе №2 (п=12) – соединение с лабораторным шифром ЛХТ-1-09 в дозе 31 мг/кг, в 3-й опытной группе (п=12) – соединение ЛХТ-3-09 в дозе 41,2 мг/кг, в 4-й опытной группе (п=12) – соединение ЛХТ-1-06 в дозе 30,2 мг/кг, в 5-й опытной группе (п=12) – соединение ЛХТ-2-09 в дозе 32,6 мг/кг, в 6-й опытной группе (п=12) – соединение ЛХТ-1-05 в дозе 41 мг/кг в/м.
Выведение животных из эксперимента осуществлялось после внутрибрюшинного введения тиопентала натрия в дозе 50 мг/кг гильотинным методом. Непосредственно после вскрытия проводилась визуальная оценка язвенного поражения слизистой оболочки желудка с использованием методики Н.Е. Чернеховской с соавт. (2006). Оценивалось количество язв и общая площадь язвенного поражения, количество и площадь поверхностных и глубоких язв, количество и площадь язв с гемосидерином, оценивалась доля глубоких язв и язв с гемосидерином от общего количества язв и общей площади язвенного поражения желудка. Оценивалась доля животных с признаками кровотечения, летальность животных в группе.
Полученные данные обработаны методами вариационной статистики на на ПЭВМ с использованием программ StatPlus 2009 Professional и Microcal Origin 8.0. Для выборок вычисляли среднее арифметическое (М) и среднюю квадратическую ошибку (m), представляя данные в виде M±m. Для оценки значимости различий двух выборок применяли параметрический (t-критерий Стьюдента) и непараметрические (критерий χ2, критерий Фишера) критерии.
Результаты исследования и их обсуждение. В контрольной группе наблюдалась гибель 25% животных. Общее количество язв в желудке составило 5,75±0,80 общей площадью 29,69±2,01мм2. При этом регистрировалось 4,63±0,53 глубоких язв, площадь которых составила 28,4±2,2 мм2, то есть, доля глубоких язв по количеству составила 80,4%, по площади – 95,7%. При этом у всех животных наблюдались признаки желудочного кровотечения. Регистрировалось 4,50±0,46 язв с гемосидерином, площадь которых составила 27,49±2,48 мм2. Доля язв с гемосидерином по количеству и по площади среди данных общего язвенного поражения желудка составила 78% и 92,6%
В опытной серии №1 на фоне профилактического введения этоксидола (25 мг/кг) не регистрировалось гибели животных. Наблюдалось уменьшение общей площади язвенного поражения на 73% (до 8,084±0,624 мм2, р<0,001). Площадь глубоких язв сокращалась на 78% (до 6,309±1,018 мм2, р<0,001), а их количество – на 51% (до 2,25±0,313, р<0,05) (рис. 1). Количество и площадь поверхностных язв на фоне предварительного введения этоксидола в изученной дозе достоверно не менялись. При этом доля глубоких язв по количеству уменьшилась с 80,4% в контроле до 41%, а по площади – с 95,7% до 78%.
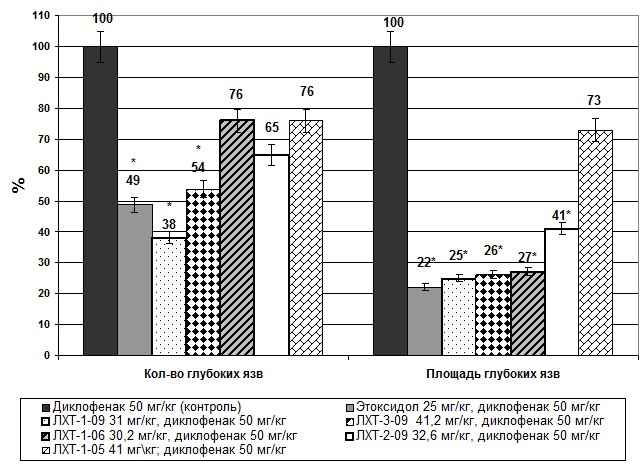
Рис. 1. Влияние этоксидола и производных аминогексановой и ацетилглютаминовой кислот на количество и площадь глубоких язв в слизистой оболочке желудка, индуцированных введением диклофенака 50 мг/кг (в % к данным контроля); * - достоверность различия р<0,05 по отношению к данным контрольной группы.
Признаки внутрижелудочного кровотечения наблюдались у 3-х животных из группы (25%). Количество язв с гемосидерином уменьшилось на 94,4% (до 0,25±0,164, р<0,001), а их площадь – на 98,6% (до 0,375±0,263 мм2, р<0,001) (рис. 2). При этом доля язв с гемосидерином по количеству уменьшилась до 4,5%, а по площади – до 4,6%.
Во 2-й опытной группе с предварительным введением соединения ЛХТ-1-09 летальность животных на фоне индукции язвенного поражения диклофенаком отсутствовала. Выявленный антиульцерогенный эффект ЛХТ-1-09 был сравним с действием этоксидола в изученных дозах: общая площадь язвенного поражения уменьшилась на 54% (до 13,52±1,53мм2, р<0,001). Количество глубоких язв в этой опытной серии уменьшилось на 62% (до 1,75±0,45, р<0,05), а их площадь сократилась на 75% (до 7,135±1,67 мм2, р<0,001) по сравнению с данными контроля. При этом доля глубоких язв по количеству уменьшилась с 80,4% в контроле до 35%, а доля глубоких язв по площади уменьшилась с 95,7% до 52%. Однако количество поверхностных язв при этом возросло на 189% (с 1,125±0,479 в контрольной группе до 3,25±0,37, р<0,05), а их площадь – почти в пять раз (с 1,281±0,499 мм2 в контроле до 6,38±1,04 мм2, р<0,05). Признаки кровотечения наблюдались только у одного животного (8,3%) во 2-й опытной группе (r=4,184, р=0,041 по χ2, р=0,020 по критерию Фишера). Количество язв с гемосидерином в желудке уменьшилось на 94,4% (до 0,25±0,25, р<0,01), а их площадь – на 98% (до 0,56±0,56 мм2, р<0,001). При этом доля язв с гемосидерином по количеству уменьшилась до 5%, по площади – до 4,1%.
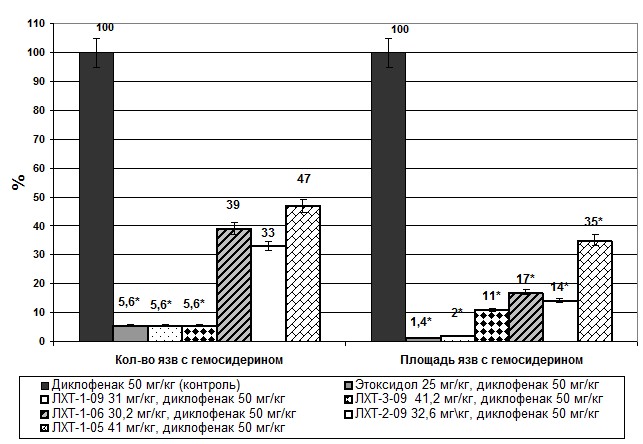
Рис. 2. Влияние этоксидола и производных аминогексановой и ацетилглютаминовой кислот на количество и площадь язв с гемосидерином в слизистой оболочке желудка на фоне внутримышечного введения диклофенака 50 мг/кг (в % к данным контроля); * - достоверность различия р<0,05 по отношению к данным контрольной группы.
В 3-й опытной группе также регистрировалось выраженное гастропротекторное действие изученного соединения ЛХТ-3-09. Общее количество язв составило 74% от данных контроля, но не носило статистически достоверного отличия. Однако общая площадь язвенного поражения желудка снижалась на 52% (до 14,145±2,57 мм2, р<0,05). Количество и площадь глубоких язв уменьшились по сравнению с данными контроля на 46% (с 4,625±0,532 до 2,5±0,61, р<0,05) и 74% (до 7,33±2,11 мм2, р<0,001) соответственно. Хотя количество и площадь поверхностных язв, напротив, возросли в 3,33 и 3,36 раза (р<0,05). При этом доля глубоких язв по количеству от общего язвенного поражения желудка снижалась с 80,4% в контроле до 58,1%, по площади – с 95,7 % в контроле до 51%.
Признаки внутрижелудочного кровотечения в 3-й опытной группе на фоне профилактического введения соединения ЛХТ-3-09 после индукции язвенного поражения диклофенаком регистрировались у 3 (25%) животных. Количество язв с гемосидерином снизилось на 94,4% (до 0,25±0,177, р<0,005), а их площадь – на 89,1% (до 3,0±2,12 мм2, р<0,001) по сравнению с соответствующими показателями контрольной группы. Доля язв с гемосидерином среди всех язв в желудке у животных 3-й опытной группы снижалась по количеству до 6% и по площади – до 21,2%. Не наблюдалось гибели подопытных животных.
В 4-й опытной группе, где предварительно вводилось соединение с лабораторным шифром ЛХТ-1-06, противоязвенное действие изучаемого соединения было уже меньше выражено, чем в первых трех опытных сериях. Общее количество язв и количество глубоких язв слизистой оболочки желудка по сравнению с контрольной группой достоверно не менялись. Однако общая площадь язвенного поражения уменьшилась на 43% (до 17,014±1,008 мм2, р<0,05), а площадь глубоких язв - на 63% (до 7,76±0,99 мм2, р<0,001) по сравнению с данными контрольной группы. Количество и площадь поверхностных язв возросли в 4,22 (до 4,75±0,90, рк<0,05) и 7,22 раза (до 9,25±1,71 мм2, р<0,05) соответственно. При этом доля глубоких язв по количеству от общего язвенного поражения желудка уменьшилась до 42%, а по площади - до 45%. Не отмечалось гибели подопытных животных.
Внутрижелудочное кровотечение наблюдалось у 9 из 12 животных (75%) на фоне предварительного введения соединения ЛХТ-1-06. Количество язв с гемосидерином уменьшилось на 61% по сравнению с соответствующим показателем контрольной группы, хотя динамика не была статистически достоверной. Площадь же язв с гемосидерином сократилась достоверно на 83,2% по сравнению с контрольными данными. При этом доля язв с гемосидерином по количеству снизилась до 21,2%, а по площади - до 27,2%.
В 5-й опытной группе на фоне введения соединения с лабораторным шифром ЛХТ-2-09 общее количество язв в желудке в условиях индукции язвенного поражения диклофенаком не менялось, но их площадь уменьшилась на 43% (до 16,904±1,563мм2, р<0,05). Количество глубоких язв составило 65% от показателя контроля, но разница не была статистически достоверна. Однако площадь глубоких язв достоверно сокращалась на 59% (до 11,63±1,62 мм2, р<0,05). Доля глубоких язв по количеству от общего количества язв в желудке уменьшилась до 50%. По площади доля глубоких язв уменьшилась до 68,8%.
Количество поверхностных язв возрастало, но не носило статистически достоверного отличия. А площадь поверхностных язв увеличилась по сравнению с данными контроля в 4,12 раза (до 5,273±0,740 мм2, р<0,05).
Признаки кровотечения регистрировались у 75% (у 9 из 12) животных 5-й опытной группы с профилактическим введением соединения ЛХТ-2-09. По сравнению с контрольной группой количество язв с гемосидерином в желудке сократилось на 67% (до 1,50±0,423, р>0,05), но не носило статистически достоверного отличия от соответствующего показателя контрольной группы. А площадь язв с гемосидерином уменьшилась на 85,9% (до 3,868±1,193 мм2, р<0,001). При этом доля язв с гемосидерином по количеству уменьшилась с 78,3% в контроле до 25%, а по площади – с 92,6% до 22,9%. Отсутствовала летальность подопытных животных.
Наименее выраженное гастропротекторное действие регистрировалось в 6-й опытной группе. В желудке на фоне введения соединения ЛХТ-1-05 общее количество язв и общая площадь язвенного поражения достоверно не менялись. Количество глубоких язв составило 76%, а их площадь – 73% от данных контрльной группы, но не носило статистически достоверного отличия. Количество поверхностных язв при этом увеличилось в 3,33 раза, а их площадь – в 5,41 раза. Однако следует отметить, что в данной опытной группе наблюдалось уменьшение доли глубоких язв по количеству с 80,4% в контроле до 48%. И по площади – с 95,7 в контроле до 74,9%. Не регистрировалось гибели животных.
Признаки внутрижелудочного кровотечения в 6-й опытной группе на фоне введения соединения ЛХТ-1-05 регистрировались у 9 животных из 12 (75%). Количество язв с гемосидерином составило 47,2% от показателя контрольной группы, но также не носило статистически достоверного отличия. Но площадь язв с гемосидерином при этом сократилась на 65,4%. Доля язв с гемосидерином по количеству уменьшилась до 29,3%, а по площади – до 34,5%.
Заключение. Таким образом, наиболее выраженное профилактические гастропротекторное действие в условиях индукции язвенного поражения желудка введением диклофенака оказали этоксидол и соединения с лабораторными шифрами ЛХТ-1-09 и ЛХТ-3-09, достоверно снижавшими общую площадь язвенного поражения желудка на 73%, 54 и 52%, количество глубоких язв на 51%, 62%, 46%, а их площадь на 78%, 75% и 74% соответственно. Достоверно уменьшающими процент животных с желудочным кровотечением, ограничивающими количество и площадь язв с гемосидерином, их долю по площади и количеству среди общего язвенного поражения слизистой оболочки желудка.
Рецензенты:
Инчина В.И., д.м.н., профессор, заведующий кафедрой фармакологии Медицинского института ФГБОУ ВПО «Мордовский государственный университет имени Н.П. Огарева», г. Саранск.
Столярова В.В., д.м.н., профессор, профессор кафедры госпитальной терапии Медицинского института ФГБОУ ВПО «Мордовский государственный университет имени Н.П. Огарева», г. Саранск.
Библиографическая ссылка
Зорькин М.В., Аткарская О.А., Зорькина А.В. СРАВНИТЕЛЬНОЕ ИССЛЕДОВАНИЕ ГАСТРОПРОТЕКТОРНОГО ДЕЙСТВИЯ ЭТОКСИДОЛА И ПРОИЗВОДНЫХ АМИНОГЕКСАНОВОЙ И АЦЕТИЛГЛЮТАМИНОВОЙ КИСЛОТ // Современные проблемы науки и образования. 2014. № 2. ;URL: https://science-education.ru/ru/article/view?id=12796 (дата обращения: 15.05.2026).



