Карбамид представляет собой бесцветные кристаллы, легкорастворимые в воде, спирте, жидком аммиаке, сернистом ангидриде, при нормальных условиях пожаро- и взрывобезопасен, а также не токсичен. Карбамид является первым органическим веществом, полученным синтетическим путем.
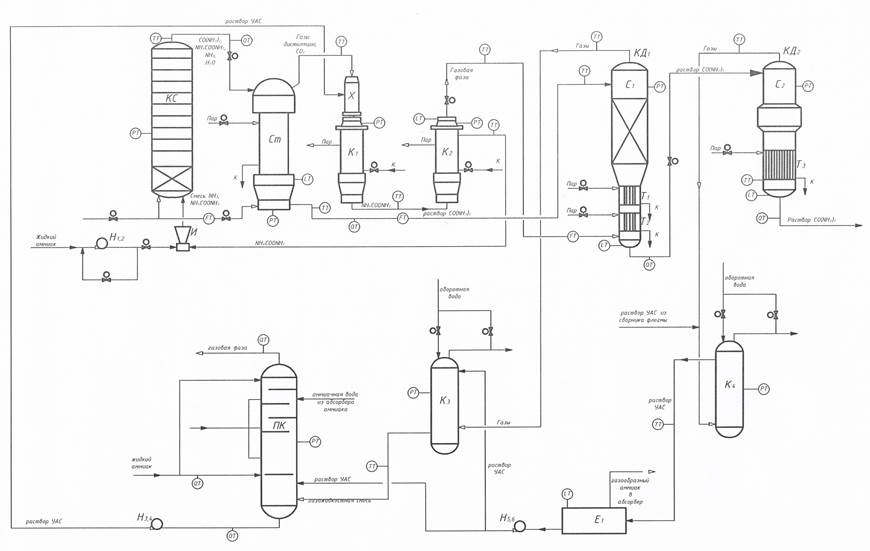
Рис. 1 Функциональная схема производства карбамида (стадия синтеза и дистилляции)
В России выпускают карбамид двух марок – А и Б. Карбамид марки А предназначен для использования в промышленности в производстве пластмасс, смол, клеев. Карбамид марки Б применяется в сельском хозяйстве в качестве минерального азотного удобрения. Карбамид – это вид удобрений, являющийся наиболее концентрированным из азотных удобрений, содержание азота в нем составляет 46,3 %, помимо аммиака. Удельный вес карбамида в производстве азотных удобрений в России составляет 29 – 32 %.
В настоящее время из всех известных способов получения карбамида промышленное значение получил процесс синтеза карбамида из аммиака и диоксида углерода по способу, разработанному в 1868 году русским химиком А.И. Базаровым. Впервые в промышленном масштабе прямой синтез карбамида удалось осуществить лишь в 1920 г. фирмой «И. Г. Фарбениндустри» (Германия).
Технологическая схема производства карбамида, а именно стадия синтеза и дистилляции одного из современных производств, показана на рис. 1.
Основным аппаратом стадии синтеза производства карбамида является колонна синтеза поз. КС, в нижнюю часть которой подается двуокись углерода и смесь аммиака с карбаматом аммония от инжектора поз. И. В качестве рабочего потока в инжектор поз. И подается жидкий аммиак от насосов высокого давления поз. Н1, 2. В колонне синтеза поз. КС при давлении 14,9 ÷ 15,4 МПа и температуре 180 ÷ 189 ºС синтез протекает в две стадии: стадия образования карбамата аммония, описываемая ниже представленным уравнением
2 NH3 + СО2 → NH4СООNH2 + 125,6 кДж
и стадия дегидратации карбамата аммония
NH4СООNH2 → CO(NH2)2 + Н2О – 15,5 кДж
Тепло, выделяющееся на первой стадии образования карбамата аммония, частично используется на второй стадии дегидратации карбамата аммония.
Продукты реакции, содержащие карбамид, карбамат аммония, избыточный аммиак и воду, из верхней части колонны синтеза поз. КС поступают в верхнюю часть стриппера поз. Ст. Расход стриппинг-агента СО2 в стриппер поз. Ст регулируется с помощью клапана по соотношению расходов в колонну синтеза поз. КС и стриппер поз. Ст равному 1,86. Работает стриппер по принципу противотока: двуокись углерода СО2 с температурой не более 140 ºС и давлением 15,1 ÷ 15,4 МПа подается в нижнюю часть стриппера и поднимается вверх навстречу раствору карбамида из колонны синтеза поз. КС, стекающему тонкой пленкой по трубкам вниз. При стекании плава по трубкам за счет массообмена с восходящими газами и тепла насыщенного пара среднего давления 2,0 МПа, подаваемого в межтрубное пространство, при температуре 185 ÷ 190 ºС происходит разложение карбамата аммония в токе свежей двуокиси углерода на аммиак и CO2.
Газы дистилляции, образующиеся при разложении карбамата, из верхней части стриппера совместно со свежей двуокисью углерода, температура которой 185 ÷ 190 ºС, смешиваются в аппарате поз. Х с раствором углеаммониевых солей (РУАС), подаваемым насосами поз. Н3, 4 из промывной колонны поз. ПК.
Из смесителя поз. Х газожидкостная смесь поступает последовательно в трубное пространство конденсаторов карбамата поз. К1, поз. К2. В трубах конденсаторов поз. К1 и поз. К2 происходит абсорбция газов раствором углеаммониевых солей (РУАС) и их конденсация с образованием карбамата аммония. Карбамат аммония из конденсатора поз. К2 с температурой 150 ÷ 160 ºС инжектором поз. И подается в реактор поз. КС. Регулирование уровня в конденсаторе поз. К2 осуществляется автоматически клапаном, установленным на выходе плава из реактора поз. КС за счёт изменения перепада давления между реактором и конденсатором поз. К2. При уменьшении перепада подача карбамата увеличивается и наоборот. Изменение подачи карбамата может быть достигнуто также увеличением давления аммиака перед эжектором поз. И путём прикрытия или открытия проходного сечения иглой эжектора. Предусмотрено автоматическое регулирование давления газов дистилляции на выходе из конденсатора поз. К2 регулирующим клапаном, установленным на трубопроводе выхода газовой фазы в аппарат поз. Т2.
В колонне дистилляции поз. КД1 осуществляется процесс дистилляции раствора карбамида при среднем давлении. Колонна дистилляции среднего давления представляет собой вертикальный аппарат, состоящий из трёх частей:
- верхняя – сепарационная часть поз. С1;
- средняя – подогреватель поз. Т1;
- нижняя – подогреватель поз. Т2;
Раствор из нижней части стриппера поз. Ст отводится в сепарационную (верхнюю) часть колонны дистилляции среднего давления поз. КД1, что обеспечивает регулирование уровня в нижней части стриппера поз. Ст. При этом раствор карбамида, выходящий из стриппера поз. Ст с температурой 125 ÷ 135 ºС, дросселируется до давления 1,5 ÷ 1,8 МПа.
В колонне дистилляции среднего давления КД1 из раствора карбамида отделяются газы, выделившиеся при дросселировании, и раствор вступает в тепло- и массообмен с восходящими газами, распределяясь по трубкам подогревателей поз. Т1, Т2.
При стекании раствора по трубкам при температуре 155 ÷ 170 ºС за счёт тепла пара, подаваемого в межтрубные пространства подогревателей поз. Т1, Т2 колонны дистилляции среднего давления поз. КД1 и массообмена с восходящими газами, происходит разложение карбамата аммония и отгонка аммиака, CO2 и паров воды.
Температура раствора карбамида в подогревателях регулируется клапанами на линиях подачи пара давлением 0,45 МПа в межтрубное пространство подогревателя поз. Т1 и давлением 0,9 МПа – в межтрубное пространство подогревателя поз. Т2.
Регулирование уровня раствора карбамида в нижней части аппарата поз. Т2 предусмотрено дросселированием и отведением раствора карбамида в сепарационную часть поз. С2 колонны дистилляции низкого давления поз. КД2. Газы из верхней части колонны дистилляции среднего давлениям поз. КД1 с температурой 138 ÷ 152 ºС направляются в конденсатор среднего давления поз. К3.
В межтрубном пространстве конденсатора поз. К3 при температуре 70 ÷ 90 оС происходит частичная абсорбция и конденсация аммиака и СО2 в растворе углеаммониевых солей (РУАС), подаваемом из сборника поз. Е1 насосами поз. Н5, 6. В трубное пространство конденсатора поз. К3 на охлаждение подается вода повторного использования с температурой 36 ÷ 38 оС. Предусмотрено регулирование температуры раствора УАС на выходе из конденсатора поз. К3 количеством подаваемой оборотной воды.
Полученная в конденсаторе поз. К3 газожидкостная смесь направляется в нижнюю часть промывной колонны поз. ПК. В растворе, собирающемся в нижней части промывной колонны (в кубе), при температуре 63 ÷ 78 оС завершается абсорбция СО2 из газожидкостной смеси с образованием углеаммониевых солей по реакциям:
СО2 + NH3 + H2O = NH4HCO3
NH4HCO3 + NH3 = (NH4)2CO3
Промывная колонна поз. ПК оборудована барботером в нижней части, тарелками – в верхней части. Уровень раствора УАС в кубе промывной колонны регулируется автоматически изменением числа оборотов двигателей насосов Н3, 4.
Поток газообразного аммиака с остатками двуокиси углерода и инертами из нижней части промывной колонны поз. ПК направляется вверх через колпачковые тарелки. Здесь происходит окончательная отмывка аммиака от двуокиси углерода аммиачной водой, подаваемой из абсорбера аммиака на вторую сверху тарелку.
Процесс дистилляции раствора карбамида при низком давлении осуществляется в колонне дистилляции низкого давления поз. КД2, аналогичной по устройству и принципу работы колонне дистилляции среднего давления поз. КД1, состоящей из двух частей:
- верхняя – сепарационная часть поз. С2;
- нижняя часть – подогреватель поз. Т3.
Раствор карбамида, выходящий из колонны дистилляции среднего давления поз. КД1, дросселируется до давления 0,2 ÷ 0,4 МПа и через распределитель вводится в верхнюю часть поз. С2 колонны дистилляции низкого давления поз. КД2. В сепарационной части поз. С2 из раствора карбамида отделяются газы, выделившиеся при дросселировании, а затем раствор вступает в тепло- и массообмен с восходящими газами распределяется по трубкам подогревателя поз. Т3. При стекании раствора по трубкам подогревателя поз. Т3 при температуре 138 ÷ 140 ºС происходит разложение остатков карбамата аммония и отгонка аммиака, CO2 и воды за счёт подогрева паром давлением 0,45 МПа, подаваемым в кожух подогревателя, и массообмена с восходящими газами. Температура раствора в колонне дистилляции низкого давления регулируется подачей пара в межтрубное пространство подогревателя поз. Т3. Уровень в нижней части подогревателя поз. Т3 регулируется подачей раствора в сепаратор.
Газы из сепаратора поз. С2 колонны дистилляции низкого давления поз. КД2 с температурой 122 ÷ 125 ºС подаются в межтрубное пространство конденсатора низкого давления поз. К4.
На входе в конденсатор поз. К4 в линию газовой фазы подается раствор УАС из сборника флегмы. В конденсаторе поз. К4 при температуре 30 ÷ 45 ºС происходит абсорбция и конденсация газов с образованием раствора углеаммониевых солей (РУАС). Тепло абсорбции и конденсации снимается охлаждающей водой, подаваемой из водооборотного цикла, т. о., температура выходящего из конденсатора поз. К4 раствора углеаммониевых солей (РУАС) регулируется количеством подаваемой оборотной воды в трубное пространство конденсатора. Полученный в конденсаторе раствор УАС сливается в сборник поз. Е1, откуда центробежным насосом поз. Н5, 6 подается в конденсатор среднего давления поз. К3 и в промывную колонну поз. ПК. Газообразный аммиак давлением 0,1÷0,3 МПа и температурой 40÷45 ºС из сборника раствора УАС поз. Е1 поступает в абсорбер.
Со времени создания первых промышленных установок основным направлением в развитии технологии производства карбамида было совершенствование системы рециркуляции NH3 и CO2, поскольку обычно степень превращения NH3 не достигает даже 50 %, а степень превращения CO2 не превышает 70 %. Отметим, что важным показателем производства является степень конверсии CO2 в карбамид. Эта величина зависит от взаимного влияния всех параметров синтеза – температуры, давления, времени пребывания реагирующих веществ в реакционном объеме, чистоты исходных компонентов и соотношения между ними.
Таким образом, помимо стандартных задач поддержания технологических параметров в аппаратах, процесс получения карбамида ставит более сложную задачу, а именно поддержание на заданном уровне таких параметров, как мольное отношение расходов аммиака и диоксида углерода, поступающих в колонну синтеза (W) и процентное отношение диоксида углерода к общему потоку углеаммонийных солей (L). Именно соотношение исходных реагентов имеет большое значение для эффективности синтеза.
Степень превращения диоксида углерода в карбамид определяет количество CO2, которое не вступит в реакцию и вернется в колонну синтеза в составе раствора углеаммонийных солей. Таким образом, меньшему количеству возвратного диоксида углерода будут соответствовать меньшие затраты на электроэнергию.
Избыток аммиака заметно смещает равновесие реакции синтеза в сторону образования карбамида, одновременно уменьшается количество побочных продуктов и коррозия аппаратуры. Это объясняется хорошей растворимостью аммиака в жидкой фазе и связыванием воды, выделяющейся при реакции. Кроме того, при избытке аммиака, процесс синтеза карбамида идет автотермично (без отвода и подвода тепла), несмотря на то что в процессе синтеза выделяется значительное количество тепла. Это тепло расходуется на нагревание подаваемых в колонну синтеза веществ до температуры реакции. Однако увеличение избытка аммиака приводит к росту нагрузки на стадиях выделения целевого продукта из раствора, полученного на стадии синтеза.
Существенное влияние на процесс оказывает наличие воды. В условиях синтеза при высоких температурах и давлении вода в основном находится в жидкой фазе, и именно этим объясняется ее влияние на равновесие реакции (смещается в сторону исходных веществ). Избыток воды заметно тормозит реакцию особенно в начале процесса. В то же время минимальное содержание воды в рециркулируемом растворе углеаммонийных солей лимитируется необходимостью предотвращения выпадения кристаллов солей и нарушения гомогенности раствора.
Оптимальное мольное соотношение компонентов:
NH3 : СО2 : Н2О = (3,2 ÷ 3,6) : 1 : (0,6 ÷ 0,83)
При обеспечении оптимального мольного соотношения компонентов степень конверсии СО2 в карбамид приблизительно 60 %. Наиболее доступный метод контроля состава материальных потоков путем химического анализа обладает существенными недостатками – длительность анализа, возможные погрешности, как при отборе проб, так и в ходе анализа. Использование же промышленной анализаторной техники в данном случае трудноосуществимо, так как РУАС является агрессивной средой и подается под давлением 19 – 20 МПа, кроме того, приборы такого типа обладают высокой стоимостью. Поэтому добиться оптимального мольного соотношения компонентов позволит управление на основе математической модели.
На рис. 2 представлена схема производства карбамида (стадия синтеза) как единый объект управления. Входными параметрами являются три вещественных потока: вода, аммиак и диоксид углерода; выходными – степень конверсии, соотношение аммиака – двуокиси углерода и крепость раствора углеаммонийных солей по CO2. Заданные оператором значения L и W будут вводится в программу в качестве задания, а их поддержание является основной задачей управления.
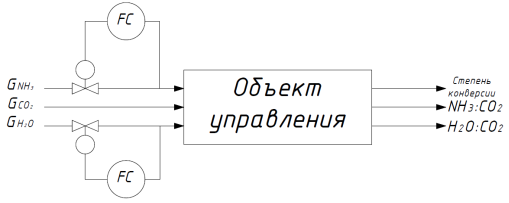
Рис. 2 Представление технологической схемы как объекта управления
Управление выходными параметрами осуществляется регулированием его входных параметров, а именно потоков воды и аммиака. Поток диоксида углерода не подвержен активному регулированию, из-за сложности управления компрессором, с помощью которого диоксид углерода подается в производство. Нецелесообразно управление потоком СО2 и из-за того, что он фактически является отходным продуктом от производства NH3 и его стоимость практически не влияет на себестоимость продукции.
Таким образом, анализ технологического процесса производства карбамида как объекта управления позволил не только установить стандартные задачи поддержания технологических параметров в аппаратах, но и определить основную задачу исследования: стабилизация соотношений аммиак – диоксид углерода и вода – диоксид углерода.
Рецензенты:
Никандров И.С., д.т.н., профессор, профессор кафедры «Автомобильный транспорт и механика» Дзержинского политехнического института (филиал) НГТУ, ФГБО ВПО Нижегородский государственный технический университет им. Р. Е. Алексеева Дзержинский политехнический институт (филиал), Министерство образования РФ, г. Дзержинск.
Сидягин А.А., д.т.н., профессор, должность профессор кафедры «Машины и аппараты химической и пищевой производств» Дзержинского политехнического института (филиал) НГТУ, ФГБО ВПО Нижегородский государственный технический университет им. Р. Е. Алексеева Дзержинский политехнический институт (филиал), Министерство образования РФ, г. Дзержинск.
Библиографическая ссылка
Баранова Н.И. АНАЛИЗ ТЕХНОЛОГИЧЕСКОГО ПРОЦЕССА ПРОИЗВОДСТВА КАРБАМИДА КАК ОБЪЕКТА УПРАВЛЕНИЯ // Современные проблемы науки и образования. 2013. № 6. ;URL: https://science-education.ru/ru/article/view?id=10993 (дата обращения: 02.06.2026).



