Введение
В настоящее время рядом работ показано, что нарушение процессов оральной толерантности и формирование пищевой гиперчувствительности (ПГ) может являться одной из значимых причин формирования хронической гастроэнтерологической патологии, полидефицитных состояний, особенно у детей раннего возраста [1, 7]. Установлено, что развитие гиперчувствительности к пище происходит в результате неспособности организма сформировать эффективную иммунологическую толерантность к пищевым антигенам [1, 6, 7]. Роль иммунной системы, ассоциированной со слизистыми оболочками, состоит в поддержании баланса между развитием иммунных реакций и процессами толерантности на фоне постоянных контактов с потенциально патогенными и непатогенными микроорганизмами и пищевыми антигенами [8, 10]. Существуют данные, что ключевая роль в осуществлении этого баланса может принадлежать дендритным клеткам [5]. Микроокружение дендритной клетки в момент ее встречи с антигеном осуществляет регуляцию экспрессии ко-стимулирующих молекул и продукцию ряда цитокинов. Межклеточные взаимодействия контролируют антиген-специфическую активность Т-клеток, в частности, развитие других эффекторных Т-клеточных популяций (Th1/Th2), что определяет сценарий иммунного ответа [9].
Согласно современным данным, энтеропатия, индуцированная пищевыми белками (белок-индуцированная энтеропатия), является одной из частых проявлений гастроинтестинальной пищевой гиперчувствительности у детей раннего возраста, клинически проявляется симптомами персистирующей диареи, срыгиванием, рвотой, белково-энергетической недостаточностью. До настоящего времени, несмотря на многочисленные исследования механизмов формирования толерантности и пищевой гиперчувствительности, многие вопросы рассматриваются лишь гипотетически, до конца не ясна роль межклеточных взаимодействий в генезе данных процессов [4].
Цель настоящего исследования состояла в изучении состояния межклеточных взаимодействий в слизистой оболочке тонкой кишки у детей с белок-индуцированной энтеропатией.
Материал и методы исследования. Под наблюдением находилось 39 детей с тяжелыми проявлениями аллергической энтеропатии, возникшей на фоне непереносимости белков коровьего молока (белок-индуцированная энтеропатия), в возрасте от 6 до 12 месяцев. Всем детям осуществлено комплексное клинико-иммунологическое, биохимическое и функциональное обследование в динамике. В периоде выраженных клинических проявлений с целью дифференциальной диагностики с другими заболеваниями желудочно-кишечного тракта (целиакия, лактазная недостаточность, синдром мальабсорбции другой этиологии) пациентам была проведена эзофагогастроеюноскопия с энтеробиопсией. Обследуемым пациентам производили забор пристеночной дуоденальной слизи с помощью эндоскопа с щёточной насадкой «Pentax» из двенадцатиперстной кишки (ДПК) для характеристики состояния первого звена локального иммунного барьера слизистой оболочки тонкой кишки и оценки мукозального иммунитета [3]. Из полученного материала готовили мазки для последующего анализа с помощью фазово-контрастной микроскопии при иммерсионном увеличении х1000. Изучение срезов проводили на микроскопе Olympus Вх72 с цифровой фотокамерой и фирменным компьютерным программным обеспечением. Биоптаты слизистой оболочки заливали в парафин по стандартной методике для иммуногистохимических исследований с использованием автоматических систем заливки и получения серийных срезов [2]. Срезы толщиной 3-5 мкм окрашивали с применением автоматизированных систем для иммуногистохимических методов при помощи моноклональных антител. Использованы современные высокочувствительные иммуногистохимические методы EPOS и En Vision [2]. Для выявления CD4, CD8, CD68 использовали маркёры фирмы DAKO. Идентификация иммунокомпетентных клеток проводилась по одинаковой схеме, несмотря на различную локализацию антигена в клеточных структурах: мембраны, лизосомы, ядра, комплекс Гольджи. Демаскировка антигенных детерминант проводилась в стеклянном контейнере, заполненном восстанавливающим раствором, и созданием условий водяной бани в течение 1 часа. Часть препаратов обработана с помощью микроволнового излучения, которое даёт лучший демаскировочный эффект, в течение получаса. Для демаскировки антигенов применяли 10 ммоль/л цитратный буфер, рН 6,0 или DАКО TRS (Target retrieval solution, сode № S 1700). Остывшие препараты промывали в дистиллированной воде. Использовали антитела в разведении 1:50 и 1:100. Окрашивание коричневого цвета свидетельствовало о положительной реакции. Подсчёт клеток производили в 100 полях зрения, при этом определяли общее количество клеток в поле зрения и анализировали степень их окрашивания. Фон и неспецифическое окрашивание исключали, строго соблюдая условия и алгоритм протокола методики – температуру, рН, время. Для блокирования неспецифического окрашивания срезы в течение 20 минут инкубировали с неиммунной сывороткой, а уже затем инкубировали с первичными антителами. Для контроля и исключения артефактов при выполнении исследований часть препаратов обрабатывали дважды только неиммунной сывороткой.
Результаты. Проведенный анализ показал, что при фазовоконтрастной микроскопии в мазках пристеночной слизи ДПК данной категории больных выявляются дендритные клетки, лимфоциты, макрофаги, нейтрофилы и слущенные каёмчатые эпителиальные клетки. Макрофаги имели размеры до 20х25 мкм, большое количество фагосом в цитоплазме и чётко идентифицирующееся ядро, расположенное центрально. Поверхность макрофагов характеризовалась многочисленными инвагинациями, глубиной до 2-х мкм. Выявленные нейтрофилы имели ядра, состоящие из 3-х и более сегментов. В цитоплазме и на клеточной поверхности идентифицировались везикулы. В пристеночной слизи выявлены лимфоциты размерами до 10 мкм. Дендритные клетки достигали размеров 20х40 мкм, на поверхности имели выросты в количестве 4-6, ядро формы с конденсированным гетерохроматином и большое количество везикул в цитоплазме. Обращало на себя внимание наличие в пристеночной слизи ДПК слущенных конусовидных эпителиальных клеток, имеющих хорошо выраженную складчатую поверхность в виде гофре. Размеры клеток достигали 14 мкм в высоту и 5 мкм в основании. Апикальная часть эпителиоцитов была расширена, достигала до 6 мкм. Основание эпителиальных клеток было закруглённо, ниже центрально расположенного ядра идентифицированы многочисленные гранулы.
Иммунногистохимические исследования биоптатов показали наличие интраэпителиальных лимфоцитов в слизистой оболочке ДПК (рис. 1).
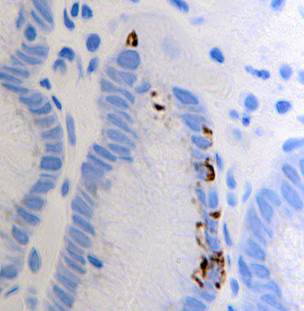
Рис. 1. Интраэпителиальные лимфоциты. Иммунная гистохимия. Микрофото. Ув.х 800.
При этом клетки лимфоцитарного дифферона были идентифицированы не только в эпителиальном пласте, но и в просвете ДПК, что подтверждает наши данные, полученные при изучении пристеночной слизи с помощью фазовоконтрастной микроскопии.
С помощью иммуногистохимического анализа были выявлены ДК - CD68 в слизистой оболочке ДПК (рис. 2).
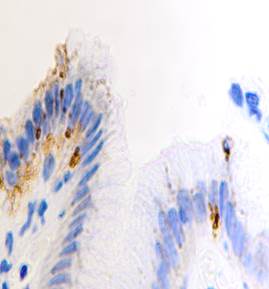
Рис. 2. Дендритные клетки CD68. Иммунная гистохимия. Микрофото. Ув.х 800.
ДК Лангерганса локализовались в базальном слое эпителиальной пластинки в количестве 8–12. Клеточные отростки были разветвленными и имели различное направление. Характерной была их локализация в базальном слое эпителия в виде скоплений клеток, что свидетельствует об усиленной миграции ДК из эпителия. В толще собственной пластинки ДК было меньше, их отростки располагались в основном биполярно и были направлены к поверхности эпителия и к базальной мембране, что свидетельствует об активации их передвижения. В собственной пластинке наблюдалось значительное увеличение количества ДК клеток по сравнению с нормой, отражающее их интенсивный приток. Отростки ДК ориентировались по ходу соединительно-тканных волокон, что также служит признаком движения.
Обсуждение полученных результатов. Полученные в исследовании данные позволяют расширить имеющиеся представления о первом (мукозном) звене местного иммунного гомеостаза слизистой оболочки и роли межклеточных взаимодействий при формировании оральной толерантности. Согласно современным представлениям, в механизмах пищевой толерантности участвуют не только клетки иммунной системы слизистой оболочки тонкой кишки, решающая роль в ее развитии принадлежит процессу межклеточных взаимодействий Т-клеток с АГ-презентирующими клетками (АПК) и присутствию при этом взаимодействии ко-стимулирующих молекул [6]. Одним из уникальных представителей мукозального иммунитета, не зависимого от общей мукозальной системы, является субпопуляция интраэптелиальных Т-лимфоцитов, обнаруженных нами при фазово-контрастной микроскопии и с помощью методов иммунной гистохимии. К настоящему времени сформировалось представление об интраэпителиальных Т-лимфоцитах как о сторожевых клетках эпителиальных тканей (первой линии защиты), способных распознать и разрушить как антиген, в том числе пищевой, так и собственную эпителиальную клетку, стрессовое состояние которой достигло критического уровня, не совместимого с продолжением нормального функционирования [5, 8]. Важная роль в формировании энтеральной толерантности отводится и антиген-презентирующим клеткам, в частности, дендритным клеткам. Дендритные клетки захватывают антиген и после процессинга протеолитическими ферментами связывают антиген молекулами MHC класса I или II. Причем презентация антигена дендритными клетками (поглощение антигена, его внутриклеточный захват и расщепление с последующим транспортом) отличается от презентации другими антиген-презентирующими клетками, что подчеркивает уникальную роль незрелых дендритных клеток в индукции толерантности. Наличие дендритных клеток в пристеночной слизи свидетельствует о том, что антиген-представление происходит не только на уровне внутриэпителиального барьера, а на его поверхности, в зоне действия первого звена иммунной защиты. Обильная миграция этих клеток на поверхность эпителиального пласта, выявленная нами при проведении исследования, их длительная персистенция, может служить ранним маркером пищевой гиперчувствительности.
Таким образом, полученные данные способствуют расширению представлений о роли межклеточных взаимодействий при пищевой гиперчувствительности, могут служить основой для дальнейшей разработки патогенетической терапии. Фазовоконтрастная микроскопия мазков, полученных из пристеночной слизи ДПК, может применяться для мониторинга состояния слизистой оболочки желудочно-кишечного тракта у детей при различных патологических процессах, сопровождающихся пищевой гиперчувствительностью.
Рецензенты:
Шапкина Л.А., д.м.н., профессор, зав. кафедрой педиатрии ФПК и ППС, иммунологии и аллергологии ГБОУ ВПО ВГМУ Минздравсоцразвития России, г. Владивосток.
Ни А.Н, д.м.н., профессор кафедры педиатрии ФПК и ППС, иммунологии и аллергологии ГБОУ ВПО ВГМУ Минздравсоцразвития России, г. Владивосток.
Библиографическая ссылка
Шуматова Т.А., Приходченко Н.Г., Григорян Л.А. АНАЛИЗ МЕЖКЛЕТОЧНЫХ ВЗАИМОДЕЙСТВИЙ В СЛИЗИСТОЙ ОБОЛОЧКЕ ТОНКОЙ КИШКИ У ДЕТЕЙ С БЕЛОК-ИНДУЦИРОВАННОЙ ЭНТЕРОПАТИЕЙ // Современные проблемы науки и образования. 2013. № 5. ;URL: https://science-education.ru/ru/article/view?id=10723 (дата обращения: 01.06.2026).



