Введение
В настоящее время большое внимание исследователями различных стран мира уделяется вопросу создания высокоэффективных устройств удаления сажи выхлопных газов дизельных двигателей [6], требования к чистоте которых ужесточаются. При этом необходимо не только улавливание частиц сажи, но и их каталитическое окисление для регенерации фильтров. К катализаторам, способным решать указанную задачу, относится оксид церия, допированный ионами различных металлов [5, 9]. В ходе очистки газов от углеродсодержащих веществ важным моментом является способность катализатора ускорять как первичную реакцию окисления сажи, в ходе которого может возникать монооксид углерода [1], так и дожигание монооксида до диоксида углерода. На каталитическую активность помимо других факторов при введении допантов решающее влияние оказывает фазовый и химический состав сложнооксидной системы.
Допирующие металлы различаются по своей стоимости, способности негативного воздействия на окружающую среду, влиянию на физико-химические характеристики катализатора, такие как стабильность его удельной поверхности и каталитической активности в ходе эксплуатации [5] и пр. Поэтому для целенаправленного выбора допирующих оксид церия элементов необходимо систематическое изучение влияния допантов на свойства катализаторов вышеназванных реакций. В настоящей работе мы исследовали, как зависит каталитическая активность оксида церия от введения ионов различной природы: щелочного металла (Cs), переходных металлов (Cu и Ag), редкоземельных элементов со стабильной (Sm) и переменной (Pr) степенью окисления. В качестве допирующего металла цезий был выбран, исходя из того, что в реакции окисления сажи активность сложных оксидов возрастает при увеличении ионного радиуса вводимого щелочного металла [1].
Экспериментальная часть
Синтез оксидных образцов Ce1-xMexO2-δ проводили методом пиролиза полимерно-солевых композиций [4]. Готовили смешанные водные растворы нитратов церия и соответствующих металлов в заданных стехиометрических соотношениях. Для этого использовали реактивы квалификации «ч.д.а.»: нитрат церия (III) шестиводный Ce(NO3)3*6H2O, нитрат цезия CsNO3, нитрат меди (II) четырехводный Cu(NO3)2*4H2O, карбонат празеодима (III) Pr2(CO3)3*xH2O, оксид самария (III) Sm2O3. Оксидные и карбонатные формы переводили в нитратный раствор путем растворения в азотной кислоте HNO3 квалификации «о.с.ч. 18-4». Для синтеза также был взят нитрат серебра AgNO3 квалификации «х.ч.». В качестве полимерного компонента применяли поливиниловый спирт ПВС марки 11/2 (по ГОСТ 10779-78). Полимер после получения отдельно его 5 %-го водного раствора добавляли к растворам солевых компонентов. Полученный рабочий раствор нагревали в фарфоровых чашках до начала самопроизвольного пиролиза и подвергали окончательной термообработке при температуре 650 ºС в течение 48 часов. Идентификацию синтезированных допированных оксидов и контроль фазового состава образцов осуществляли методом порошкового рентгенофазового анализа, выполненного с помощью рентгеновского автоматизированного дифрактометра ДРОН-6. Рентгенограммы снимались в CuКa-излучении в интервале углов 2Θ=15-70 градусов со скоростью 2 градуса в минуту. Параметры элементарных ячеек рассчитывали с помощью программных пакетов «FPeaK», «Celref». Идентификация фаз проведена с использованием картотеки ICDD.
Удельную поверхность полученных оксидных образцов измеряли на приборе Sorbi N41, Meta, предназначенном для измерения удельной поверхности дисперсных и пористых материалов. В основу измерения удельной поверхности положен метод БЭТ. Удельная поверхность рассчитывается по изотерме низкотемпературной сорбции паров азота. Анализатор Sorbi N41, Meta работает под управлением специализированной программы в среде Windows.
Исследование морфологии и структурных свойств полученных материалов с нанометровым пространственным разрешением проводили методом сканирующей электронной микроскопии, с использованием рабочей станции AURIGA (CrossBeam, Carl Zeiss NTS). Управление, анализ полученных данных осуществляли с использованием программного пакета Analysis Station, AURIGA series, Version 3.7.
Измерения каталитической активности по окислению сажи проводили на воздухе в изотермическом режиме в открытом реакторе, контролируя массу образца гравиметрически. Заданную температуру в зоне реакции поддерживали при помощи измерителя-регулятора «Овен» и термопары типа ХА. В качестве образцов использовали «реальную» сажу, образующуюся при сгорании керосина в авиационных турбинах на обкаточном стенде [4]. Навеску сажи предварительно тщательно смешивали с 4-кратным количеством катализатора в агатовой ступке в течение 10-15 минут для создания тесного контакта между частицами сажи и катализатора.
Оценку каталитической активности в реакции окисления сажи проводили также политермическим методом, что обеспечивало экспрессный отбор наиболее эффективных каталитических составов. При этом механическую смесь катализатора и сажи помещали в специальный тигель и проводили термический анализ на воздухе с использованием термоанализатора Mettler Toledo STARe SW 8.10 с соответствующим программным обеспечением. При этом получали кривые дифференциального термического (ДТА), гравиметрического анализа в интегральной (ТГ) и дифференциальной форме (ДТГ). Скорость нагрева образцов составляла 8 град/мин. Из политермических зависимостей получали такие параметры каталитической активности, как, температура начала реакции окисления сажи, интервал ее интенсивного протекания, полнота выгорания сажи и пр.
Изучение каталитической активности в отдельной реакции окисления монооксида углерода катализаторами окисления сажи проводили в реакторе проточного типа, где обеспечивался режим, близкий к режиму идеального вытеснения [2]. Для исследований образцы готовили в форме гранул: формовали в таблетки (давление при прессовании составляло 60 кгс/см2), а затем дробили и просеивали через сита, отбирая фракцию 1,4-1,6 мм. Содержание СО в рабочей газовой смеси составляло не более 0,2 об. %, кислорода - 3,5 об. %, скорость газового потока - 1 литр в минуту, нагрузка на катализатор - 1700 мин-1. Для создания рабочей смеси необходимого состава использовали газовые баллоны поверочных газовых смесей N2-CO (содержание СО - 0,2 %). Для контроля содержания кислорода и монооксида углерода в исходной и конечной смесях использовали электронный газоанализатор Testo-350 XL. Экспериментальные данные получали при ступенчатом нагревании реакционной зоны.
Результаты и обсуждение
Образцы Ce1-xMexO2-δ (Me= Sm, Pr, Cu, Cs, Ag) были синтезированы методом пиролиза полимерно-солевых композиций, следуя методике, описанной выше. Фазовый состав получаемых оксидных образцов контролировали методом РФА. Образцы Ce1-xSmxO2-δ,
Ce1-xCsxO2-δ (х = 0.1; 0.2) по данным проведенного анализа однофазны (примесные фазы не обнаружены), и, следовательно, образуют твердые растворы со структурой флюорита на основе диоксида церия. Образцы Ce1-xCuxO2-δ, Ce1-xAgxO2-δ неоднофазны и содержат в качестве примесных фаз CuO (оксид меди) и Ag (металлическое серебро), соответственно. Значение удельной поверхности всех образцов находилось в пределах 15-20 м2/г.
В результате изучения каталитической активности были получены временные зависимости степени превращения в реакции окисления сажи на образцах, содержащих 0,1 и 0,2 моля каждого из допантов, на рис. 1 приведены такие данные для температуры 400 °С. При всех изученных температурах в интервале 300-400 ºС каталитическая активность образцов, включающих серебро или цезий, была более высокой. Остальные допанты расположились по убыванию каталитической активности в ряд Ag≈Cs>Cu>Pr>Sm. Высокая каталитическая активность цезий-содержащих оксидов в реакции окисления сажи была нами прогнозируема, так как в целом присутствие щелочных металлов положительно влияет на каталитические свойства сложнооксидных материалов в реакциях с твердыми углеродистыми веществами [3, 1]. Наиболее низкой каталитической активностью обладали оксиды, содержащие самарий. Полученные данные еще раз могут свидетельствовать о том, что на каталитические свойства в изучаемой реакции положительное влияние оказывают металлы 1 группы, или металлы, способные менять свою степень окисления. Празеодим, как и медь, имеет несколько устойчивых степеней окисления, которые реализуются в сложнооксидных и оксидных соединениях, однако празеодимсодержащий диоксид церия уступает по своим каталитическим свойствам в данной реакции медьсодержащим образцам, что, по-видимому, связано с тем, что последние образцы являются неоднофазными и содержат оксид меди в качестве примесной фазы. Оксид меди в свою очередь проявляет высокую каталитическую активность в реакциях окисления углеродсодержащих веществ, однако при использовании его в чистом виде происходит его восстановление до чистой меди.
Высокая каталитическая активность в окислительно-восстановительных реакциях сложных оксидов в целом, содержащих серебро, как в кристаллической решетке, так и свободном состоянии, очень характерна, о чем свидетельствуют полученные ранее данные, в частности [1]. Как отмечено выше, образцы, включающие серебро и медь, были неоднофазными, они содержали помимо основной фазы со структурой типа флюорита также металлическое серебро и оксид меди CuO (в том числе и после проведения каталитических реакций). На наличие металлического серебра в высокоэффективных оксидных катализаторах указывалось также в работе [7]. По-видимому, оно и обеспечивало вкупе с синергетическим действием оксида церия максимальную активность катализатора. Серебро было достаточно однородно распределено в образце, на что указывают результаты анализа образцов при помощи электронного микроскопа с использованием больших увеличений (рис. 2). Имеющиеся в образце фазы находились в наноразмерном состоянии (агрегированные наночастицы). Отдельные крупные частицы серебра, образование которых характерно в ряде случаев, нами не обнаружены. По-видимому, наличие наноразмерных оксидных частиц в изучаемой системе стабилизирует ультрадисперсное состояние металлического серебра. В системе, содержащей медь, также проявляется эффект стабилизации примесной фазы оксида меди, которая оказывает очень существенное влияние на повышение каталитической активности. В данном случае при воздействии восстановительной реакционной среды не происходило возникновения ощутимых количеств металлической меди, что подтверждалось методом рентгенофазового анализа. Полученные рентгенограммы исходных медьсодержащих образцов и после проведения каталитического окисления сажи были идентичны друг другу. Указанный стабилизационный эффект подтверждается и другими исследователями, например, результатами работы [8].
а) б)
б)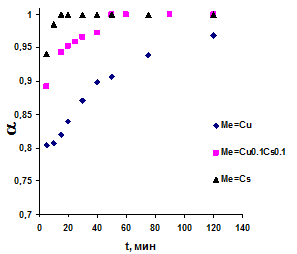
Рис. 1. Степень конверсии сажи в присутствии оксидных образцов а) - Ce0.9Me0.1O2-δ (400 °С); б) - Ce0.8Me0.2O2-δ (400 ºС)
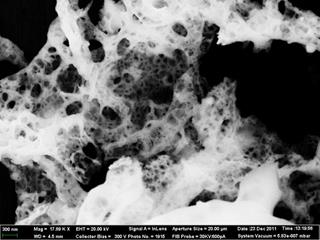
Рис. 2. Электронная микрофотография исходного образца Ce0.9Ag0.1O2, полученного в виде порошка (увеличение 18000, напряжение 20 кВ, апертура 20 мкм)
Интересно было выяснить, как влияет на свойства катализаторов двойное допирование (рис. 1б). При одновременном введении по 0,1 молей цезия и меди каталитическая активность возрастала по сравнению с Ce0.8Cu0.2O2-δ, однако для образца с 0,2 молями цезия она была, тем не менее, еще выше. Таким образом, можно полагать, что на каталитическую активность при окислении сажи серьезно влияет наличие переходного металла, способного в ходе реакции обратимо изменять степень окисления. Однако не менее сильное (и даже определяющее) влияние оказывает наличие щелочного металла, образующего неустойчивые карбонатные комплексы [3], существование которых облегчает первоначальное окисление сажи.
Результаты проведенного политермического анализа каталитического окисления сажи на разных составах композиций сведены в табл. 1.
Таблица 1
Результаты обработки термогравиметрических кривых, полученных при нагревании образцов
|
Валовый состав |
Tig, °C |
Tp, °C |
Tf, °С |
ΔTr, °С |
δm, % |
|
Ce0.9Cs0.1O2-δ |
345 |
390 |
530 |
185 |
77 |
|
Ce0.9Cu0.1O2-δ |
428 |
530 |
690 |
262 |
79 |
|
Ce0.9Pr0.1O2-δ |
415 |
510 |
570 |
155 |
100 |
|
Ce0.9Sm0.1O2-δ |
482 |
619 |
660 |
178 |
100 |
|
Ce0.9Ag0.1O2-δ |
214/391* |
294/440** |
600 |
386 |
95 |
В таблице обозначено:
Tig, °C - температура начала реакции (температура зажигания),
Tp, °C - температура наибольшей скорости горения сажи,
Tf, °С - температура достижения практически полного выгорания сажи,
ΔTr, °С - температурный интервал интенсивного протекания реакции,
δm, % - степень превращения сажи.
* - для процесса, протекающего в несколько стадий, приведены температуры начала каждого пика; ** - приведена температура окончания процесса для пика при максимальной температуре для многостадийного процесса; *** - приведена суммарная степень превращения.
Наименьшей температурой начала реакции окисления сажи обладал диоксид церия, допированный серебром (Ce0.9Ag0.1O2-δ) или цезием (Ce1-xCsxO2-δ), а наибольшей - самарием (табл. 1). Полученные данные согласуются с результатами, полученными в изотермических условиях. Конечная убыль массы сажи в среднем очень близка для всех сравниваемых образцов. При этом результаты, полученные по двум методикам, хорошо коррелируют. Таким образом, по результатам двух экспериментов можно сделать вывод, что на каталитические свойства в реакции окисления сажи оказывает сильное влияние природа допирующего иона, при этом наибольшей каталитической активностью обладают диоксиды церия, допированные элементами 1 группы (щелочной металл или серебро).
В реакции окисления монооксида углерода высокую активность проявлял оксид церия, допированный серебром, как и в реакции окисления сажи. Образцы при всех изученных температурах (50-700 °С) располагались следующим образом по убыванию активности Ag≈Cu>>Pr≈Sm≈Cs (рис.3). Относительна невысокая активность составов, содержащих цезий, подтверждает его более существенное влияние на первый этап окисления сажи. Двойное допирование не привело к повышению каталитической активности по сравнению с образцами, содержащими один допант (рисунок 3, таблица 2). Так, каталитическая активность медьсодержащих (Ce0.9Cu0.1O2-δ) образцов была выше, чем у образца, содержащего одновременно цезий и медь (Ce0.8Cs0.1Cu0.1O2-δ), что выглядит вполне логично. Результаты экспериментов указывают на то, что максимальное воздействие на каталитическую активность при окислении монооксида углерода оказывает введение в диоксид церия переходных металлов. Такая ситуация хорошо согласуется с имеющимися представлениями о каталитической активности оксидных систем. Переходные металлы, как известно [10], образуют на поверхности сложного оксида каталитические центры окисления монооксида углерода, например, за счет облегчения диссоциативной сорбции кислорода на поверхности сложного оксида.
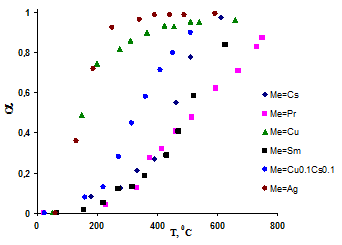
Рис. 3. Степень конверсии монооксида углерода для образцов Ce0.9Me0.1O2-δ в зависимости от температуры
Таблица 2
Параметры каталитической активности оксидов Ce0.9Me0.1O2-δ в реакции окисления монооксида углерода
|
Состав |
Тig, ºС |
T50, ºC |
T90, ºC |
|
CeO2-δ |
300 |
440 |
635* |
|
Ce0.9Pr0.1O2-δ |
250 |
500 |
750 |
|
Ce0.9Sm0.1O2-δ |
200 |
470 |
660 |
|
Ce0.9Cs0.1O2-δ |
120 |
420 |
540 |
|
Ce0.9Cu0.1O2-δ |
-** |
150 |
360 |
|
Ce0.9Ag0.1O2-δ |
- ** |
100 |
220 |
|
Ce0.8Cs0.1Cu0.1O2-δ |
100 |
320 |
500 |
В таблице обозначено:
Тig, ºС - температура начала реакции окисления монооксида углерода,
T50%, ºC - температура достижения 50 % превращения монооксида углерода,
T90%, ºC - температура достижения 90 % превращения монооксида углерода.
* - степень превращения CeO2-δ достигла максимально 86 %,
** - реакция начинается уже при комнатной температуре.
Результаты, полученные в настоящей работе, позволяют выбрать наиболее активные каталитические композиции для дальнейшего изучения, в частности тестирования их устойчивости при более длительном циклическом использовании в средах, моделирующих состав реальных выхлопных газов.
Выводы
Методом пиролиза полимерно-солевых композиций синтезированы образцы состава Ce1-xMexO2-δ (Me= Sm, Pr, Cu, Cs, Ag). Определен их фазовый состав, измерена удельная поверхность. Введение ионов металлов в диоксид церия приводит к увеличению каталитической активности в реакциях окисления сажи и монооксида углерода. Каталитическая активность в обеих указанных реакциях значимо зависит от природы допирующего иона. Наибольшей каталитической активностью в обеих реакциях обладает состав Ce0.9Ag0.1O2-δ. Кроме того, в реакции окисления сажи высокой активностью обладают диоксиды церия, допированные цезием, а в реакции окисления угарного газа - медью. Полученные результаты могут быть использованы в дальнейшем для целенаправленного выбора каталитических систем в практических целях.
Работа выполнена при финансовой поддержке Министерства образования и науки Российской Федерации, соглашения 14.A18.21.1186, 14.132.21.1455; РФФИ (проект № 12-03-31875мол а), и поддержке молодых ученых УрФУ в рамках реализации программы развития УрФУ.
Рецензенты:
Остроушко А. А., д.х.н., профессор, с.н.с., заведующий отделом, ФГАОУ ВПО «УрФУ имени первого Президента России Б. Н. Ельцина», г. Екатеринбург.
Анимица И. Е., д.х.н., профессор, с.н.с., ФГАОУ ВПО «УрФУ имени первого Президента России Б. Н. Ельцина», г. Екатеринбург.
Библиографическая ссылка
Русских О.В., Тонкушина М.О., Гржегоржевский К.В. ВЛИЯНИЕ ДОПИРУЮЩИХ ИОНОВ НА КАТАЛИТИЧЕСКУЮ АКТИВНОСТЬ ОКСИДА ЦЕРИЯ В РЕАКЦИЯХ ОКИСЛЕНИЯ УГЛЕРОДСОДЕРЖАЩИХ ВЕЩЕСТВ // Современные проблемы науки и образования. 2013. № 5. ;URL: https://science-education.ru/ru/article/view?id=10348 (дата обращения: 17.05.2026).



