В последние годы в лечении рака все большее место занимает фотодинамическая терапия, в основе которой лежит использование светочувствительных материалов – сенсибилизаторов, способных выделять «реактивный кислород», уничтожающий раковые клетки. Однако существующие на сегодняшний день сенсибилизаторы разлагаются под воздействием солнечного света, что ограничивает их практическое применение.
Так, на сегодняшний день известны работы по увеличению противораковой активности сенсибилизаторов благодаря использованию специальных полимерных наночастиц, которые доставляют сенсибилизаторы к раковым клеткам, после чего сенсибилизаторы высвобождаются и производят противораковый эффект [23].
Cеленоорганические гетероциклические соединения могут быть использованы в качестве лекарственных препаратов, радиопротекторов, компонентов оптических записывающих сред, фотогальванических элементов, фотоматериалов, инициаторов фотополимеризации, электрофотографии, фотопроводящих материалов в измерительной технике, материалов для быстрореагирующих пассивных затворов лазеров, что отражено в целом ряде статей и патентов [1–5, 7, 9, 11, 24, 28–32].
Актуальность освещаемой в настоящей работе проблемы заключается в поиске новых cенсибилизаторов и методов их cинтеза фотохимическим путем, необходимости установления механизмов фотохимических процессов с участием селеносодержащих гетероциклов ввиду их применения в качестве лекарственных препаратов.
В настоящее время изучены некоторые аспекты механизма протекания фотохимических процессов окисления арилзамещенных селенопиранов, октагидро-селеноксантенов [6, 11, 12, 22, 34].
Из литературных данных известно, что 2,4,6-трифенил-4Н-пиран в среде четыреххлористого углерода способен подвергаться фотохимическому окислению, причем предполагался цепной, свободнорадикальный механизм [20, 21] (схема 1). В качестве инициатора реакции использовали перекись бензоила, причем реакция резко ускоряется при УФ-облучении. Авторы представили следующую схему1 превращений.
В работе [10] показано, что моноарилзамещенные 5,6-полиметилен-селено-пирилиевые соли можно с хорошими выходами получать непосредственно из 1,5-дикетонов. В остальных случаях легкодоступными бициклическими соединениями остаются только 2,4-диарил-5,6-полиметилен-2-гидроселено-2,3-дигидро-4Н-селено-пираны.
Древко [10] было установлено, что в присутствии четырехбромистого углерода под действием полихроматического ультрафиолетового излучения гидроселено-производные дигидроселенопиранов 1, 2, 3 превращаются в соответствующие бромиды селенопирилия 4, 5, 6 с выходами 39–50 % (схема 2).
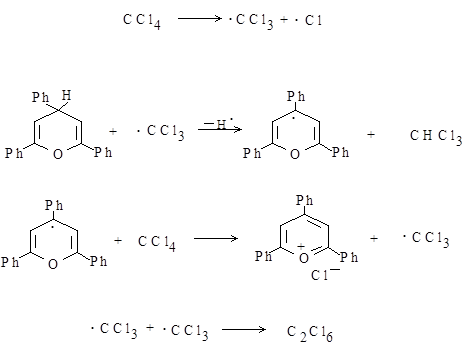
1,4 R = Ph, n = 2 ;
2,5 R = C6H4OCH3-p, n = 2 ;
3,6 R = Ph, n = 1
Схема 1
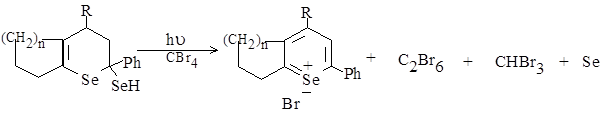
1, 2, 3 4, 5, 6
Схема 2
Авторами [10] было установлено, что основную роль играет сенсибилизированный фотоэффект (схема 3).
На схемах 2, 3 показаны основные пути генерации свободных радикалов в реакционной системе. По аналогии со свободнорадикальными реакциями тиолов в работе [10] предположено, что полученный на основе селенолов радикал будет присоединяться по двойной связи гетероцикла, хотя более вероятным является отщепление атома брома от СBr4 c последующим преобразованием образующегося интермедиата в соответствующую соль селенопирилия.
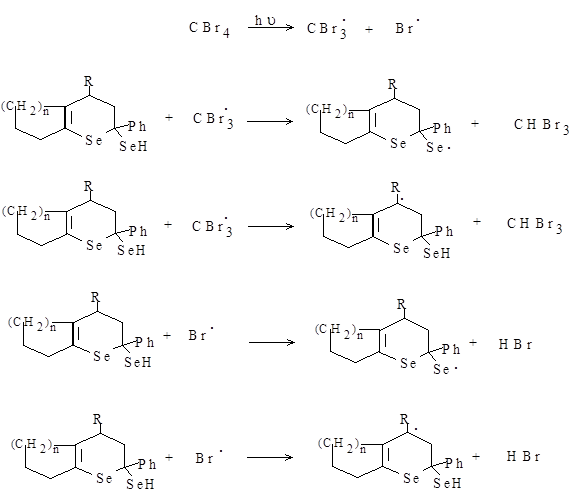
Схема 3
На схемах 2, 3 показаны основные пути генерации свободных радикалов в реакционной системе. По аналогии со свободнорадикальными реакциями тиолов в работе [10] предположено, что полученный на основе селенолов радикал будет присоединяться по двойной связи гетероцикла, хотя более вероятным является отщепление атома брома от СBr4 c последующим преобразованием образующегося интермедиата в соответствующую соль селенопирилия.
Радикал, образовавшийся при отщеплении атома водорода из g- положения гетероцикла, после элиминирования селеноводорода будет преобразовываться, как описано в работах [2, 3, 10, 14], для фотохимических реакций халькогенопиранов.
Гексабромэтан в данной реакции образуется при рекомбинации радикалов CBr3 , как cледует из схемы 4.
Таким образом, показано, что фотохимические реакции являются весьма перспективным методом синтеза солей полиметиленселенопирилия.
Общие вопросы техники эксперимента проведения фотохимических процессов представлены в статьях [13–21, 33, 35].
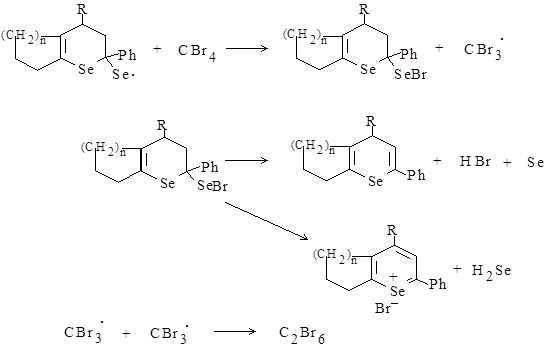
Схема 4
Блинохватовым с сотр. [5] накоплен огромный экспериментальный материал по синтезу и изучению химических превращений 9R-cимм.-нонагидро-10-халькогена-антраценов, которые выгодно отличаются от моно- и бициклических халькогено-пиранов доступностью отечественного сырья для синтеза циклогексанона, простотой методов синтеза, высокими выходами и стабильностью. В работе [6] произведена сравнительная оценка реакционной способности катионов 9 R-симм. – октагидро-10-халькогенанонагидроантраценов и установлено, что их электрохимическое катодное восстановление показало увеличивающуюся в ряду: пирилий-тиопирилий- селенопири-лий, электроноакцепторную способность. Б. И. Древко с сотр. [9, 22, 11, 12] были исследованы реакции фотохимического окисления 4H-cелено-(тио)пиранов и было установлено, что они способны превращаться в соответствующие гетероароматические катионы, причем предполагался свободнорадикальный механизм превращения.
Из литературных данных известно, что 2,4,6-трифенил-4Н-пиран в среде четыреххлористого углерода способен подвергаться фотохимическому окислению, причем предполагался цепной, свободнорадикальный механизм [12]. Фотохимические реакции являются весьма перспективным методом синтеза солей полиметилен-селенопирилия [10].
Нами исследованы процессы фотохимических превращений 2,4,6-трифенил-тиациклогексана, 2,6-диметоксифенил-4-фенилселенациклогексана, 2,4,6-трифенил-селенациклогексана; 2,6-дифенил-4-метоксифенилсе-ленациклогексана и 2,4,6-триметоксифенилселенациклогексана в среде диизопропилового эфира и этилового спирта при инициировании четырехбромистым углеродом [13, 15, 16, 20, 21]. Обнаружено [13–15], что халькогенациклогексаны способны подвергаться фотохимическому окислению в присутствии CCl4 и CBr4 с образованием гетероароматических катионов. Показано, что халькогенациклогексаны могут служить в качестве сенсибилизаторов при фотохимическом окислении халькогенопиранов.
Найдена новая модификация перегруппировки Пуммерера, которая сопро-вождается полным элиминированием реагента с образованием соответствующего непредельного соединения. Фотохимические превращения могут рассматриваться как новый способ получения селено(тио)пиранов и солей селено(тио)пирилия [13–15].
Октагидроселеноксантены проявляют антиоксидантные свойства, являются официально зарегистрированными ветеринарными препаратами и пищевыми добавками, а также аналогами селеноксантенов, обладающими радиопротекторными свойствами.
Цель исследования – синтез новых сенсибилизаторов и установление особенностей механизмов протекания свободнорадикальных реакций в селеноорганических гетероциклических наноструктурированных системах и изучение строения продуктов фотохимического окисления с использованием методов ГХ с МСД, ВЭЖХ и УФ-спектроскопии.
В качестве объектов исследования были выбраны:
9R- Cимм. - октагидрохалькогеноксантены (9-фенил-Симм.-октагидро-селеноксантен; 9-фенил-Симм. -октагидротиоксантен; 9-фенил-Симм.- октагидроксан-тен) и соли октагидрохалькогеноксантилия; халькогенациклогексаны различного строения.
При протекании фотохимических процессов с октагидрохалькогено-ксантеновыми структурами теоретически был возможен механизм, который предполагал первоначальную атаку по гетероатому фотовозбужденной молекулой:
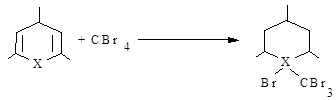
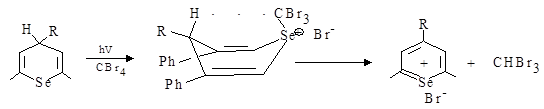
В 9R-симм.-октагидрохалькогеноксантенах заместитель в С9 положении гетероцикла находится в «псевдо»-аксиальном положении (у арилалифатических халькогенопиранов подобный заместитель располагается экваториально), поэтому реакция, которая протекает по гетероатому, вероятно, может заканчиваться отщеплением бромбензола или трибромтолуола, а не бромоформа или бромистого водорода.
Наличие в реакционной смеси бромбензола позволило предположить, что радикальные процессы с халькогенопирановыми структурами протекают по необычному механизму. В классическом варианте это могло бы выглядеть следующим образом:
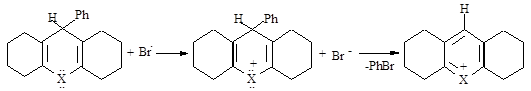
Вероятность протекания реакции по данному механизму меньше, чем по стандартному, так как энергия диссоциации связи С-Ph намного больше энергии диссоциации связи C-H. Наличие в реакционной бромоформа дает основание предполагать, что реакция протекает по «стандартному» механизму:
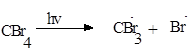
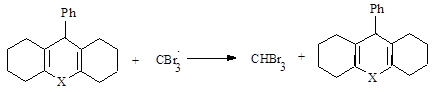
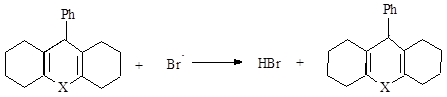
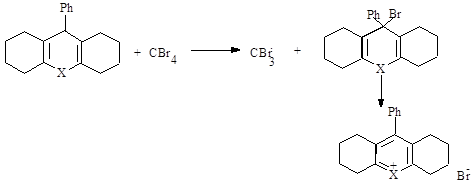
![]()
В реакционной среде значительно больше образуется бромоформа, чем бромбензола, поэтому второй вариант механизма более предпочтителен, так как в данном случае присутствует «цепной механизм». Согласно проведенным исследованиям, в реакционной среде может находиться тетрабромэтилен CBr2 = CBr2 , что указывает на протекание следующего процесса:
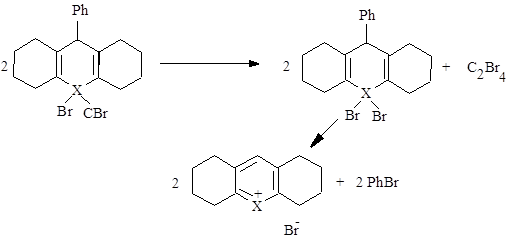
В результате проведенного исследования получены некоторые данные, которые не могут быть однозначно объяснены и которые коррелируют с двумя известными ранее аналогиями, обнаруживаемыми в химии гетероциклических соединений.
Молекула халькогенопирана, сталкиваясь с возбужденной молекулой четырехбромистого углерода, превращается в относительно устойчивую структуру, которая затем диспропорционирует с образованием соли халькогенопирилия, тетрабромэтилена и бромбензола. Это хорошо согласуется с результатами, которые были получены при исследовании радиопротекторных свойств селеноксантенов.
На основании предполагаемого нового механизма можно сделать вывод, что указанные соединения могут блокировать свободнорадикальные реакции, вступая во взаимодействие с фотовозбужденными молекулами и не допускать гомолитического распада связи. Этим могут быть объяснены некоторые аномалии, которые были обнаружены при изучении радиопротекторных свойств селеноксантенов на биологических объектах.
В проведенных нами ранее исследованиях помимо продуктов фотохимического окисления – симм.-октагидрохалькогеноксантенов, не идентифицировались соли октагидроксантилия. Нами была предпринята попытка идентифицировать подобные соединения хроматомасс-спектрометрическим методом. Реакция протекала недостаточно селективно, поэтому достоверно обнаружить в сложной смеси сигналов трибромтолуол не удалось. Следует отметить, что в реакционной среде были обнаружены некоторые количества тетрабромэтилена.
В результате анализа реакционной смеси, кроме бромоформа, было обнаружено присутствие бромбензола, что позволило сделать следующие предположения относительно механизма протекания реакции.
На рис. 1 представлена хроматограмма серосодержащего субстрата – 9 фенил-симм.-oктагидротиоксантена, указывающая на сигналы двух соединений, которые характеризуются УФ-спектрами, представленными на рис. 2–4.
Возможно отщепление атома водорода в С4 положении гетероцикла с последующей ароматизацией и диспропорционированием аддуктов, которые образуются при реакции по гетероатому:
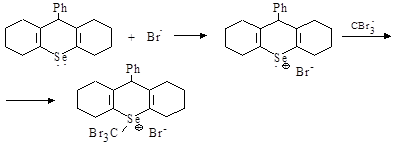
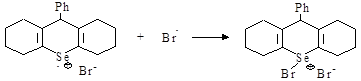
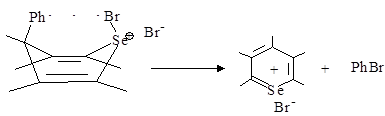
Для проверки предложенной гипотезы нами было принято решение провести аналогичные реакции в растворителях, которые могут выводить полученные интермедиаты из сферы реакции. Реакции проводили в диизопропиловом эфире, который значительно труднее реагирует со свободными радикалами, чем исследуемые нами соединения.
Характеристичные ионы, обнаруженные в масс-спектрах 9-фенил-симм.-октагидрохалькогеноксантенов после их фотохимического окисления, совпадают с характеристическими ионами, проявляющимися в масс-спектрах анализируемых веществ. Наличие данных характеристичных ионов подтверждает предполагаемый нами механизм реакций фото-химического окисления 9-фенил-симм.-октагидрохалькогеноксантенов.
На хроматограмме серусодержащего субстрата обнаружены сигналы двух соединений, УФ-спектры которых имели максимумы поглощения в области 210 нм для соединения с временем удерживания 0,722 минуты и 200, 235 и 255 нм для соединения с временем удерживания 2,427 мин.
Данные спектры не могли принадлежать исходному тиоксантену и соли тиопирилия, УФ- спектр которой (без фенильного заместителя) представлен на рис. 2.
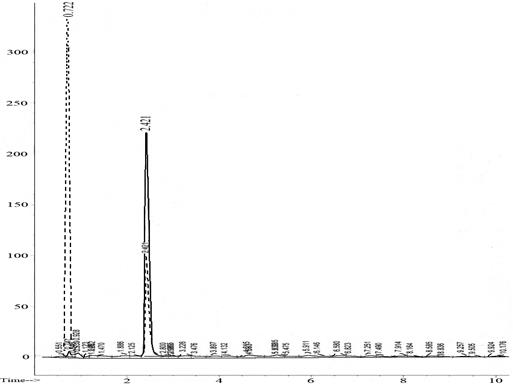
Рис. 1. Хроматограмма 9-фенил-симм.-октагидроселеноксантена в диизопропиловом эфире, полученная на приборе ВЭЖХ при λ=230,4 нм и λ=210,4 нм
Из анализа УФ-спектров следует, что полученные соединения имеют электронные спектры поглощения, характерные для С- Br связи и фенильного заместителя для соединения с временем удерживания 2,427 мин.
Определение структуры вещества со временем удерживания 0,222 минуты весьма проблематично, так как такое время удерживания не характерно для легких галоидпроизводных углеводородов, а структуры, которые образуются при взаимодействии тиоксантена, должны иметь поглощение в области 240–260 нм, т.е. области, характерной для фенильного заместителя.
В результате проведения хроматомасс-спектрометрического анализа 9-фенил-симм.-октагидроcеленоксантена было установлено, что сигналу наибольшей интенсивности соответствует время удерживания 25,068 минуты и молекулярный ион с m/z =330 у.е. для Se80. Пик молекулярного иона представлял собой серию из шести сигналов, соответствующих природному изотопному составу селена, интенсивность которых соответствует содержанию изотопов в природном селене: Se74 (0,87 %), Se76 (9,02 %), Se77 (7,58 %), Se78 (23,52 %), Se80 (49,827 %), Se82 (9,19 %). Первоначальная фрагментация происходила с элиминированием фенильного заместителя и образованием фрагмента с m/z = 253 у.е. Характеристичные ионы, обнаруженные в масс-спектрах 9-фенил-симм.-октагидрохалькогеноксантенов после их фотохимического окисления, совпадают с характеристическими ионами, проявляющимися в масс-спектрах анализируемых веществ. Наличие данных характеристичных ионов подтверждает предполагаемый нами механизм реакций фотохимического окисления 9-фенил-симм.-октагидрохалькогеноксантенов (рис. 9–7).
Экспериментальным путем было показано, что возможно протекание процессов фотохимического окисления халькогенопирановых структур по гетероатому. Впервые получены галогенированные по атому халькогена 9-фенил-симм-октагидрохалькогено-ксантеновые структуры, которые удалось идентифицировать с использованием методов УФ-спектроскопии, ВЖЭХ и ГХ с МСД. Установлено, что галогенированные по гетероатому халькогеноксантеновые структуры могут спонтанно превращаться в соответствующие гетероароматические катионы.
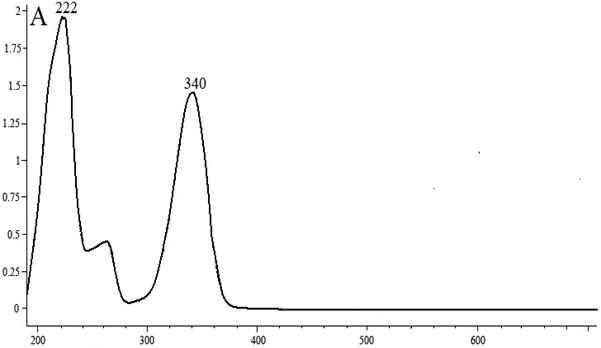
Рис. 2. УФ-спектр соли тиопирилия без фенильного заместителя в ацетонитриле, полученный на УФ-спектрометре
Таким образом, в ходе проведенных исследований нами был предложен наиболее вероятный механизм протекания процессов фотохимического окисления 9- фенил-симм.-октагдрохалькогеноксантенов на основе анализа продуктов исследуемых превращений современными физико-химическими методами анализа.
Показанные на рис. 3–8 УФ-спектры характеризуют процессы образования новых структур в процессах фотохимического окисления.
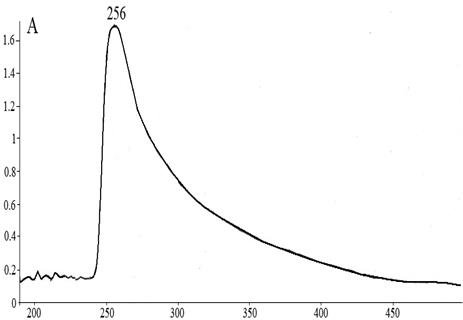
Рис. 3. УФ-спектр 9-фенил-симм.-октагидроселеноксантена в хлороформе, полученная на УФ-спектрометре
Для получения более надежных сведений о структуре исходных синтезированных наноструктурированных материалов использовался метод ВЖЭХ. На рис. 9 приведена хроматограмма исходного селеноксантена, полученная на приборе ВЭЖХ при λ=254,4 нм, λ=224,4 нм, λ=210,4 нм, λ=300,4 нм, указывающая на чистоту исходных препаратов. Анализ хроматограмм рис. 10–16 указывает на механизм, представленный схемами, приведенными выше.
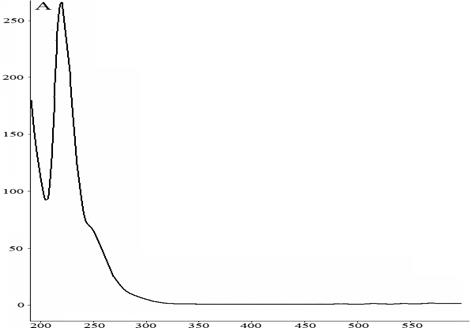
Рис. 4. УФ-спектр реакционной массы после фотохимического окисления 9-фенил-симм.-октагидроселеноксантена, полученная на приборе ВЭЖХ
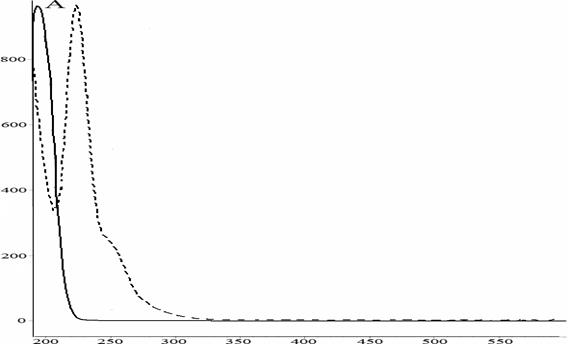
Рис. 5. УФ-спектр реакционной массы после фотохимического окисления 9-фенил-симм.-октагидроселеноксантена, полученная на приборе ВЭЖХ
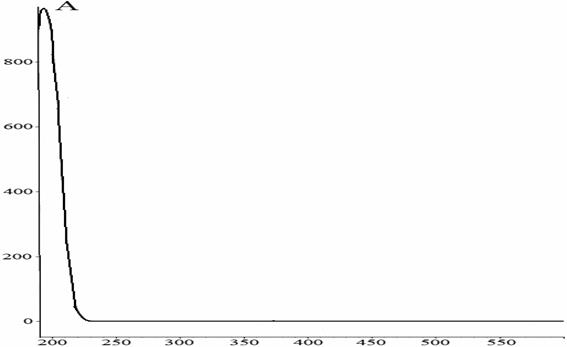
Рис. 6. УФ-спектр реакционной массы после фотохимического окисления 9-фенил-симм.-октагидроселеноксантена, полученная на приборе ВЭЖХ
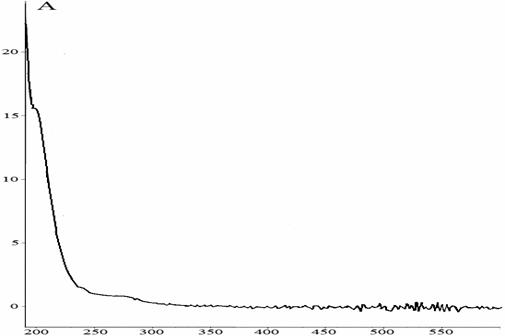
Рис. 7. УФ-спектр 9-фенил-симм.-октагидроселеноксантена после фотохимического, полученный на приборе ВЭЖХ
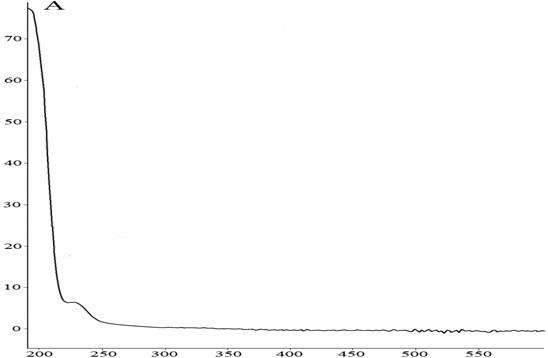
Рис. 8. УФ-спектр 9-фенил-симм.-октагидроселеноксантена после фотохимического, полученный на приборе ВЭЖХ
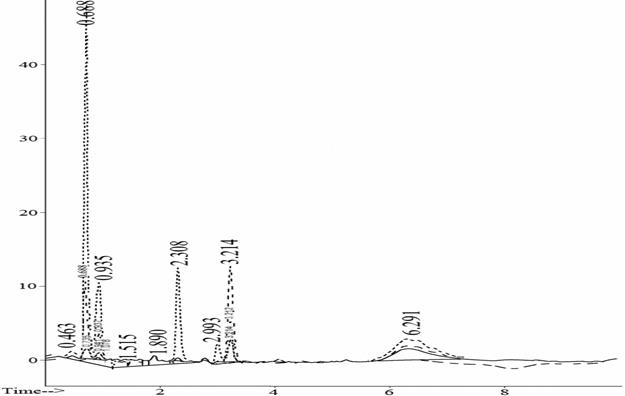
Рис. 9. Хроматограмма исходного селеноксантена, полученная на приборе ВЭЖХ при λ=254,4 нм, λ=224,4 нм, λ=210,4 нм, λ=300,4 нм
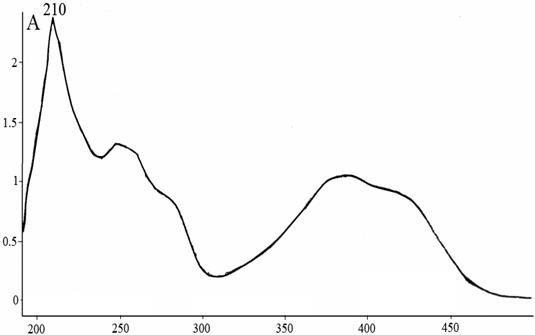
Рис. 10. УФ-спектр исходного селеноксантена
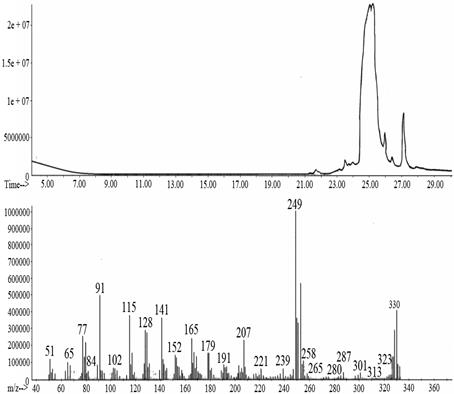
Рис. 11. Хроматограмма и масс-спектр 9-фенил-симм.- октагидроселеноксантена
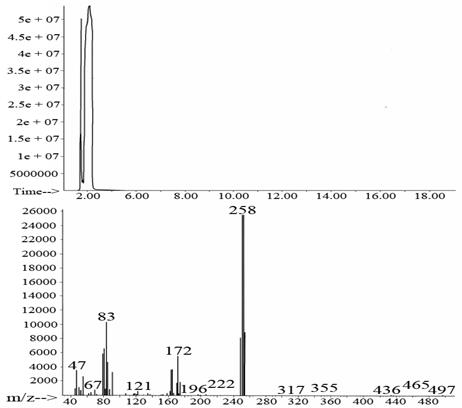
Рис. 12. Масс-спектр фрагмента m/z = 253 у.е., образованного при фрагментации 9-фенил-симм.-октагидроселеноксантена, полученный на ГХ с МСД
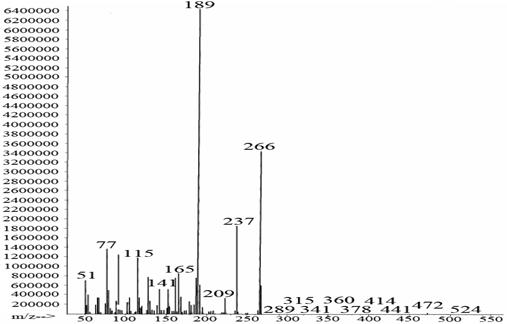
Рис. 13. Масс-спектр реакционной массы после фотохимического окисления 9-фенил-симм.-октагидроселеноксантена, полученный на ГХ с МСД
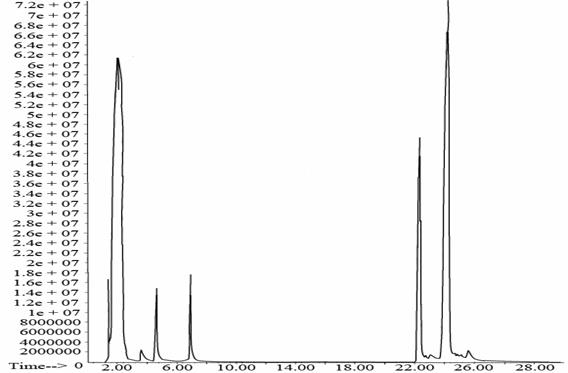
Рис. 14. Хроматограмма 9-фенил-симм.-октагидротиоксантена после фотохимического окисления, полученная на ГХ с МСД
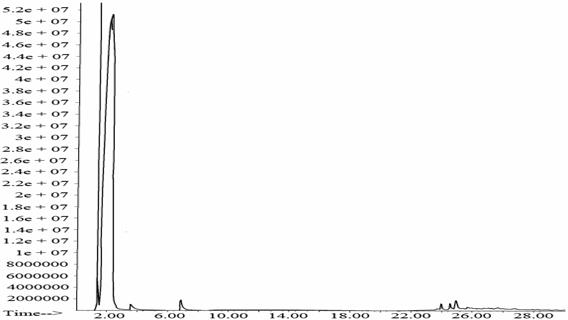
Рис. 15. Хроматограмма 9-фенил-симм.-октагидротиоксантена после фотохимического окисления, полученная на ГХ с МСД
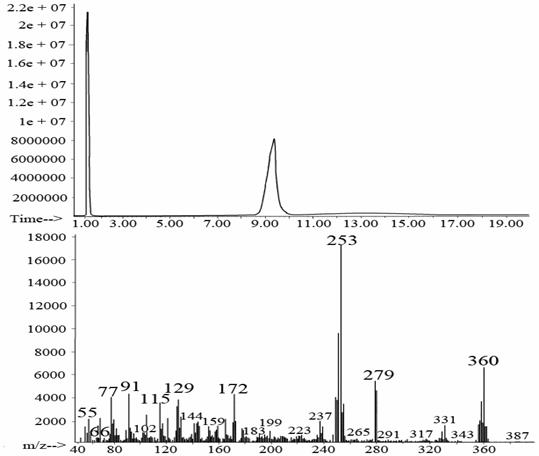
Рис. 16. Хроматограмма и масс-спектр 9-фенил-симм.-октагидротиоксантена
При фотохимическом окислении 2,4,6-трифенилтиациклогексана нами обнаружено образование соответствующих солей тиопирилия, которые были идентифицированы в виде соответствующих перхлоратов.
Теоретически можно было предположить, что фотохимическое окисление 2,4,6-трифенилтиа(селена)циклогексанов в присутствии СBr4 происходит посредством элиминирования галогеноводорода.
Исходя из анализа масс-спектров, мы могли предположить следующую схему 51 превращения:
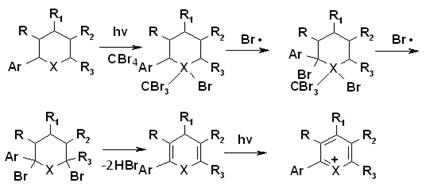
Схема 5. X – S, Se.
Механизм данной реакции может быть представлен соответствующим образом (схема 6):
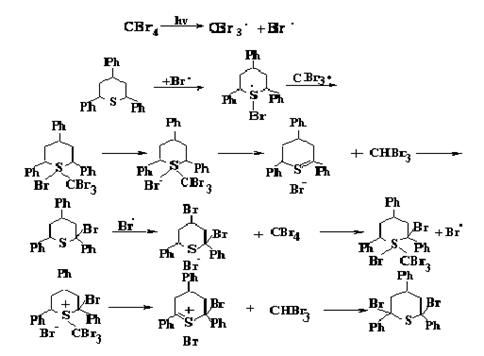
Схема 6
Полученное соединение не может термодинамически существовать в индивидуальном состоянии и претерпевает следующие превращения:
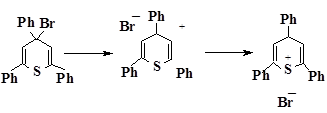
Существование последней структуры термодинамически наиболее выгодно.
Очевидно, соответствующая соль халькогенопирилия поглощает квант света в видимой области спектра, переходя при этом в возбужденное состояние, и передает энергию комплексу халькогенопирана (НР) с CВr4, который разлагается на бромид халько-генопирилия и бромоформ.
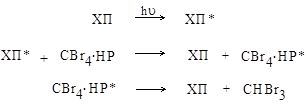
Вероятно, что в роли сенсибилизатора в этой реакции выступает соль селено-пирилия, так как из всех образующихся солей только она имеет интенсивное поглощение в видимой области спектра.
Аналогичные результаты получались при проведении фотохимической реакции с 2,6-диметоксифенил-4-фенил-селенациклогек-саном в среде четырех-хлористого углерода. При фотохимическом окислении 2,4,6-трифенилтиациклогексана в реакционной смеси при помощи хроматомассспектрометрии были обнаружены следующие продукты реакции:
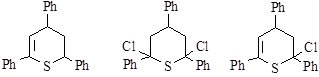
I II III
Соответствующий тиопиран не мог находиться долго в данных условиях, так как легко превращается в соль. В данном случае лимитирующей стадией реакции будет образование дихлор- и дигидропроизводных трифенилтиациклогексанов. В реакционной смеси основными компонентами являлись: 2,4,6-трифенил-2,3-дигидротиа-циклогексан (I) и 2,4,6-трифенил-2,3-дегидро-6-хлортиациклогексан (III). Последний мог возникнуть как в реакционной смеси, так и в результате реакции дегидрохлорирования на адсорбенте при хроматографическом анализе.
В результате из тиа(селена)циклогексанов I, II получена соответствующие соли тио(селено)пирилия III, IV, идентифицированные в виде перхлоратов V:
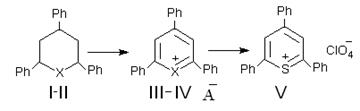
Хроматомасс-спектрометрией зафиксированы промежуточные соединения А, Б и В, что можно представить как механизм реакций:
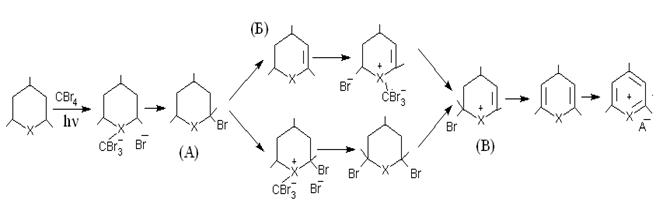
Таким образом, в данном исследовании были впервые получены тио(селено)пираны путем фотохимического окисления тиа(селена)циклогексанов, что представляет определенную практическую ценность; исследованы процессы фотохимических превращений 2,4,6-трифенилтиациклогексана, 2,6-диметоксифенил-4-фенил-селенацикло-гексана, 2,4,6-трифенил-селенациклогексана; 2,6-дифенил-4-метокси-фенилселенациклогексана и 2,4,6-триметоксифенилселенациклогексана в среде диизопропилового эфира и этилового спирта при инициировании четырехбромистым углеродом.
Выводы
Таким образом, в ходе проведенных исследований нами был предложен наиболее вероятный механизм протекания процессов фотохимического окиления 9- фенил-симм.-октагдрохалькогеноксантенов на основе анализа продуктов исследуемых превращений современными физико-химическими методами анализа.
Экспериментальным путем было показано, что возможно протекание процессов фотохимического окисления халькогенопирановых структур по гетероатому. Впервые получены галогенированные по атому халькогена 9-фенил-симм-октагидрохалькогеноксантеновые структуры, которые удалось идентифицировать с использованием методов УФ - спектроскопии, ВЖЭХ и ГХ с МСД. Установлено, что галогенированные по гетероатому халькогеноксантеновые структуры могут спонтанно превращаться в соответствующие гетероароматические катионы.
Обнаружено, что халькогенациклогексаны способны подвергаться фотохимическому окислению в присутствии CCl4 и CBr4 с образованием гетероароматических катионов. Показано, что халькогенациклогексаны могут служить в качестве сенсибилизаторов при фотохимиическом окислении. Установлено образование промежуточных продуктов фотохимического окисления халькогенацикло-гексанов методом газовой хроматографии с масс-селективным детектором, и на основании полученных экспериментальных данных предложен механизм изучаемых реакций. Обнаружено, что при окислении 4Н-селенопиранов термодинамически наиболее стабильными продуктами реакции являются соответствующие производные ароилселенофенов. Установлено, что реакции фотохимического окисления селенопиранов могут протекать как по положению С4 гетероцикла, так и по гетероатому. Найдена новая модификация перегруппировки Пуммерера, которая сопровождается элиминированием реагента с образованием соответствующего непредельного соединения. Процессы фотохимического окисления селена(тиа)-циклогексанов являются новым способом синтеза селено(тио)пиранов и солей селено(тио)пирилия.
Полученные нами в процессе фотохимического синтеза наноструктурированные материалы могут оказать наилучших наилучший пролонгированный эффект в плане изучения их медико-биологических свойств как ранее зарегистрированные препараты [33–35].
Рецензенты:
Родионов И. В., д.т.н., профессор кафедры ТМС СГТУ им. Гагарина Ю. А., г.Саратов.
Соловьева Н. Д., д.т.н., профессор, зав. кафедрой ТЭП ЭТИ СГТУ, г.Саратов.
Библиографическая ссылка
Демидов А.А., Дмитриенко Т.Г. СЕНСИБИЛИЗАТОРЫ НА ОСНОВЕ НАНОСТРУКТУРИРОВАННЫХ СЕЛЕНСОДЕРЖАЩИХ ГЕТЕРОЦИКЛОВ // Современные проблемы науки и образования. 2013. № 5. ;URL: https://science-education.ru/ru/article/view?id=10232 (дата обращения: 16.05.2026).



