Введение
Область применения электроактивных органических материалов на основе гетероциклических соединений простирается за пределы простой замены металлов и включает в себя использование их в качестве проводников, сверхпроводников, полупроводников, аккумуляторов, транзисторов, сенсоров, светоизлучательных диодов и родственных электрохромных материалов, что имеет большое коммерческое значение [1, 11].
В последние годы в электрохимии и электрохимической технологии объектом пристального внимания стали ионные органические соли, в которых органические катионы тиоксантилия, тиохромилия или тиопирилия путем обычных обменных реакций соединяются с различными неорганическими анионами (Сl-, ClO4-, FeCl4-, BF4-, I-, H2PO4-, H2PO3-) [2, 13–18, 20, 22, 25, 27–29].
Многие из этих солей и их производные нашли применение как биологически-активные лекарственные препараты, ценные красители, индикаторы, сенсибилизаторы. Особенности сочетания распределения электронной плотности гетероатома и остальных атомов кольцевой системы, а также особенности кристаллического строения стимулируют в соединениях этого типа перемещение, как электронов, так и ионов. При этом активная роль принадлежит гетероатому в ароматическом кольце благодаря наличию у него неподеленных электронных пар [23, 28, 29].
Фундаментальные проблемы функционирования устройств при наличии твердофазных границ, образованных материалами с разными типами проводимости (электронной, ионной, смешанной), являются объектом исследований многих мировых научных центров. Одной из актуальных проблем является механизм спонтанного формирования ионпроводящих переходных слоев, возникающих как на границе твердого электролита с блокирующим электродом и обеспечивающих ее обратимость по ионам проводимости твердых электролитов, так и в системах непосредственного контакта анод | катод, исключающих эффект короткого замыкания. Впервые эффект образования пассивной пленки на аноде из щелочного металла наблюдали в системах с апротонными электролитами.
Органические полупроводники, относящиеся к комплексам с переносом заряда (КПЗ) и ион-радикальным солям (ИРС), с проводимостью 10-2–10-6 См/см, как правило, обладают электронной и ионной составляющими проводимости, высокой электрохимической активностью, что позволяет отнести их к перспективным катодным материалам для преобразователей энергии и информации. Следует отметить некоторые особенности суперионных проводников, отличающие их от жидких электролитов, а именно: перенос заряда может осуществляться только одним видом ионов, остальные ионы формируют жесткий каркас или матрицу, в виде кристаллической решетки, которая может обладать носителями заряда электронной составляющей проводимости: электронами и дырками. Поэтому явление переноса в объеме суперионного проводника и на гетеропереходах в контакте с электролитами зависит от строения электронных и ионных подсистем и их взаимного влияния. Органические полупроводники, в частности КПЗ, – это и есть структуры, в которых молекулы одного вещества играют роль доноров, а молекулы другого – акцепторов [23, 28, 29]. Использование КПЗ и ИРС в качестве катодных материалов, способных формировать ионпроводящий переходный слой на границе с твердым электролитом или со щелочным металлом, в электрохимической системе щелочной металл-органический полупроводник, где отсутствует какой-либо электролит, определило область их детального исследования и применения. Актуальность исследований свойств переходных слоев и условий их возникновения базируется на проблеме поиска эффективных электрохимических систем для автономных химических источников тока с высокими техническими и эксплуатационными характеристиками.
Поиск новых электрохимических систем для разработки высокоэффективных миниатюрных твердофазных химических источников тока является важной задачей. Перспективными являются электрохимические системы со щелочными металлами (литий, натрий) в качестве рабочего вещества анода, твердым электролитом на основе β-глинозема, проводящего по ионам щелочного металла и ионными органическими солями в качестве катода. Однако электрохимические свойства таких систем мало изучены.
Данные, полученные исследователями в работах [9, 21, 24], показали, что электрические характеристики катодов на основе ионных органических солей сильно зависят от природы и концентрации добавки в составе рабочего вещества катода, от скорости поляризации и длительности хранения в разомкнутой цепи. Причины этих эффектов не ясны. Отсутствие систематических исследований в этом направлении не позволяет перейти к решению технологических задач по разработке электродов на основе ионных органических солей для твердофазных химических источников тока. Поэтому результаты исследования электрохимических свойств солей тиопирилия на границе с твердым электролитом и установление зависимости между потенциалом, плотностью тока и составом вещества катода имеют научную ценность и практическое значение.
Ранее [3, 10, 19] электрохимические свойства некоторых гетероциклических соединений с гетероатомом серы были изучены в жидких фазах.
С целью получения предварительных результатов по оценке возможности использования указанных материалов в твердофазных химических источниках тока необходимо накопление систематических сведений об электрохимических свойствах этих соединений.
Объектами исследования служили электроды из ионной органической соли перхлората 4-метил-2-фенил-5,6-тетраметилентиопирилия (I) с добавками сажи и твердый электролит β-глинозем, проводящий по ионам натрия.
Перхлорат 4-метил-2-фенил-5,6-тетраметилентиопирилия синтезирован по методике [24] согласно уравнению:
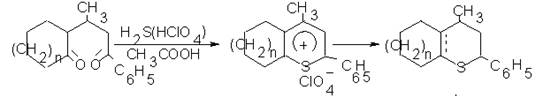
Первоначально методом циклической хроновольтамперометрии было исследовано электрохимическое поведение перхлората 4-метил-2-фенил-5,6 – тетраметилентиопирилия, на границе с натриевым β- глиноземом.
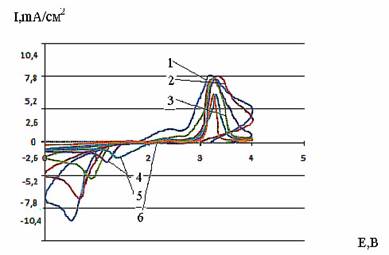
Рис. 1. ЦПДК электрохимического превращения cоли I при 20 °С и скоростях развертки потенциала (мВ/с): 1 - 80;2 - 40; 3 - 20; 4 - 8;5 - 4; 6 - 2; содержание сажи в катоде 30 масс. %, давление прессования 10 кгс/см2
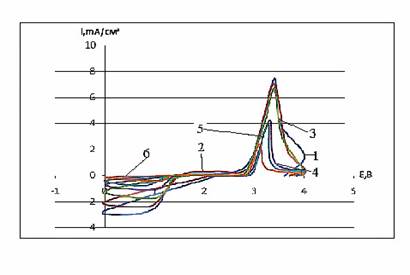
Рис. 2. ЦПДК электрода изперхлората 4-метил-2-фенил-5,6-тетра-метилентиопирилия на границе с натриевым β- глиноземом при 20 °С и скоростях развертки потенциала (мВ/с) : 1 - 30, 2 - 40, 3 - 20, 4 - 8, 5 - 4, 6 - 2; давление прессования 12,5 кгс/см2 ; содержание сажи в катоде 30 масс. %
На рис. 1 и рис. 2 приведены потенциодинамические кривые (хроновольтамперо-граммы) перхлората 4-метил-2-фенил-5,6-тетраметилентиопирилия при различных скоростях развертки потенциала на границе с натриевым β-глиноземом. Потенциодинамические кривые (рис. 2) были получены при одном выбранном постоянном давлении прессования.
Из хода кривых на рис. 1 и рис. 2 следует, что на катодном полуцикле электрохимическое восстановление соли тиопирилия характеризуется максимумом тока. После реверса тока в катодной области тока пик исчезает, однако на кривой обратного хода при потенциале пика имеется излом. В анодной области потенциалов на анодном полуцикле потенциодинамической кривой имеется второй максимум, которому на кривой обратного хода также отвечает излом. Таким образом, при катодной поляризации при потенциалах от 0 до 2,2 В (относительно натриевого электрода сравнения) протекает один катодный процесс. Спектры, полученные методом электронного парамагнитного резонанса (ЭПР), показали, что в этих условиях на катоде образуется органический катион-радикал. Таким катион-радикалом может быть катион-радикал 4-метил-2-фенил-5.6- тетраметилентиопирилия. При анодной поляризации протекает обратный процесс окисления продукта катодной реакции до исходного катиона. В анодной области идет процесс окисления сажи с образованием соединения внедрения с органическим катионом.
Образование такого соединения возможно уже в отсутствие тока при простом механическом перетирании. Соединение внедрения облегчает протекание процесса катодного восстановления органической соли и переводит этот процесс в диффузионный режим. Это подтверждается линейным характером зависимостей Емакс - ![]() на кривых рис. 3.
на кривых рис. 3.
Такое объяснение экспериментальных данных согласуется с установленной на последующем этапе исследования зависимостью хода циклических потенциодинамических кривых от количества сажи в составе электрода, приведенных на рис. 3.
С увеличением количества сажи от 10 до 50 масс. % плотность тока в максимумах потенциодинамических кривых на катодном и анодном полуциклах возрастает.
Снижение плотности тока на электроде при более высоком содержании сажи можно объяснить пересыщением структуры соли сажевыми частицами. Таким образом, сажа играет важную роль в твердофазных превращениях на электроде из ионной органической соли: она не только облегчает перенос электрического тока, но через образующиеся соединения внедрения оказывает каталитическое влияние на процесс восстановления ионной органической соли.
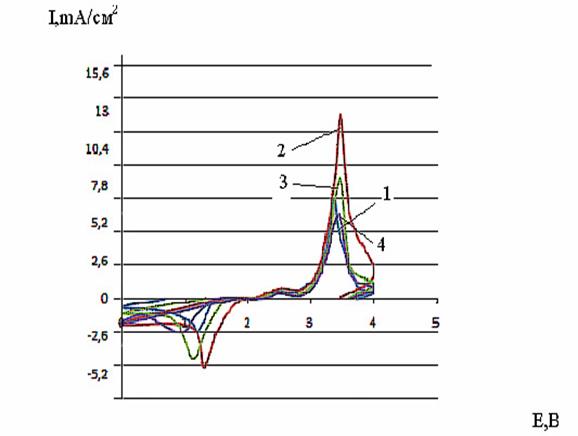
Рис. 3. ЦПДК электрода из перхлората 4-метил-2-фенил-5,6-тетраметилентиопирилия на границе с натриевым β-глинозёмом при 20 °С с различным содержанием сажи (мас. %) и скорости развертки потенциала 8 мВ/с: 1 - 30; 2 -50; 3 - 85; 4 - 90 мас.% соли тиопирилия; 70; 50; 15; 10 мас.% сажи
На возможность образования соединения внедрения уже при простом механическом перемешивании указывает анализ зависимости емкости и проводимости органической соли от времени при высоких частотах переменного тока (рис. 4, 5). Этот эффект может быть связан со сравнительно высокой подвижностью электронов в сопряженной цепи аромати-ческого кольца.
Свойства катиона тиопирилия обусловлены способностью неподеленной пары электронов гетероатома участвовать в сопряжении. При локализации электронного заряда на гетероатоме (O,S,Se) катион тиопирилия имеет структуру неустойчивого катиона пентадиенила.
Энергия делокализации электронного заряда для катиона тиопирилия составляет 192,46 кДж/моль и коррелирует по величине с эмпирически найденной энергией резонанса. Таким образом, можно говорить о большой степени делокализации плотности заряда неподеленной пары электронов в гетероцикле катиона тиопирилия.
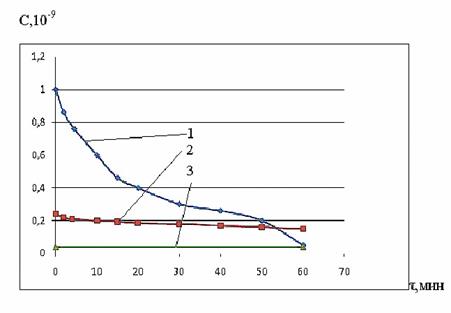
Рис. 4. Зависимость емкости ионной органической соли из перхлората 4-метил-2-фенил-5,6-тетраметилентиопирилия от времени при высоких частотах переменного тока; содержание сажи в механической смеси 30 мас.%;частоты; кГц :1 - 150; 2 - 120;
3 – 100
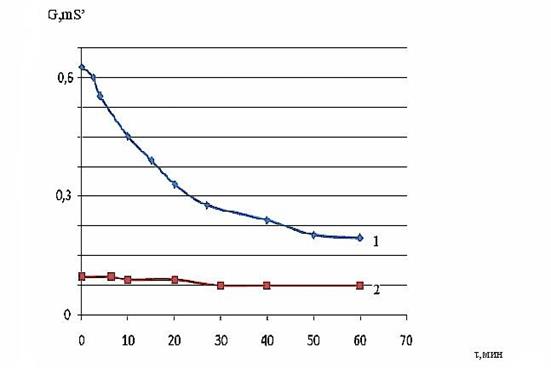
Рис. 5. Зависимость проводимости ионной органической соли из перхлората 4-метил-2-фенил-5,6-тетраметилентиопирилия от времени при высоких частотах переменного тока: 1 - 150; 2 - 120 кГц; содержание сажи в механической смеси 30 мас.%
Это подтверждается также величинами порядков связи. Катион тиопирилия можно представить как резонансный гибрид одной тиониевой (а) и трех карбониевых структур:
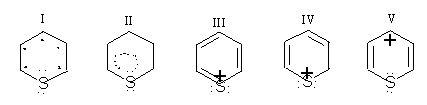
![]()
Тиониевая структура (а) в приведенном ряду отражает сопряжение ароматического типа и характеризует стабильность катиона тиопирилия, а структуры (б), (в) и (г) отражают его большую реакционную способность, в частности по отношению к нуклеофильным реакциям.
В таблице 1 показаны значения плотностей токов на максимумах потенциодинамических кривых. Из таблицы 1 следует, что по мере увеличения содержания сажи в электроде от 10 до 15 % максимальная плотность тока особенно существенно увеличивается.
Таблица 1
Значения плотности тока iмакс и потенциала Емакс в максимумах потенциодинамических кривых на катодном полуцикле для электрода из ИОСI при различном содержании сажи в зависимости от скорости развертки потенциала и температуре 20 0 С (потенциалы представлены относительно Na/Na+ электрода сравнения, также в табл. 2, 3).
|
Скорость развертки потенциала, Vр, мВ/с |
Содержание сажи в составе электрода, масс. % |
|||||||
|
30 |
50 |
80 |
90 |
|||||
|
iмакс, мА/см2 |
Емакс, В |
iмакс, мА/см2 |
Емакс, В |
iмакс, мА/см2 |
Емакс, В |
iмакс, мА/см2 |
Емакс, В |
|
|
2 |
0,91 |
1,08 |
5,2 |
1,3 |
0,39 |
|
1,30 |
1,12 |
|
4 |
2,34 |
0,95 |
1,89 |
1,41 |
1,89 |
1,14 |
||
|
8 |
2,60 |
0,80 |
2,65 |
1,22 |
2,60 |
0,75 |
||
|
20 |
5,20 |
0,61 |
4,68 |
0,95 |
4,94 |
0,50 |
||
|
40 |
7,70 |
0,46 |
7,54 |
0,74 |
7,49 |
0,35 |
||
|
80 |
12,5 |
0,48 |
10,40 |
0,52 |
9,75 |
0,40 |
||
C рассмотренных позиций возрастание плотности тока на электроде при многократном циклировании (более 10 циклов) можно объяснить накоплением соединения внедрения и увеличением скорости его образования, вследствие роста количества поверхностных дефектов, в результате такой катодно-анодной проработки электрода, что показано на циклических потенциодинамических кривых на рис. 6.
Результаты потенциодинамических исследований согласуются с гальваностатическими измерениями.
В таблице 2 прослеживается влияние добавки сажи в катодные материалы.
Таблица 2
Значения плотности тока iмакс и потенциала Eмакс в максимумах потенциодинамических кривых при реверсе тока в анодной области потенциалов (2,5–4В) для электрода из ионной органической солиI при 200 С и различном содержании сажи в зависимости от скорости развертки потенциала vр
|
vр, мВ/с |
Содержание сажи в составе электрода, масс. % |
|||||||
|
30 |
50 |
85 |
90 |
|||||
|
iмакс, мА/см2 |
Емакс, В |
iмакс, мА/см2 |
Емакс, В |
iмакс, мА/см2 |
Емакс, В |
iмакс, мА/см2 |
Емакс, В |
|
|
2 |
0,160 |
3,19 |
0, 018 |
3,18 |
0,021 |
3,19 |
0,014 |
3,20 |
|
4 |
0,122 |
3,35 |
0,024 |
3,32 |
0,027 |
3,35 |
0,018 |
3,32 |
|
8 |
0,028 |
3,50 |
0,032 |
3,50 |
0,038 |
3,48 |
0,020 |
3,50 |
|
20 |
0,030 |
3,68 |
0,040 |
3,70 |
0,047 |
3,69 |
0,023 |
3,70 |
|
40 |
0,032 |
3,80 |
0,045 |
3,79 |
0,053 |
3,80 |
0,025 |
3,78 |
|
80 |
0,034 |
4,07 |
0,048 |
4,06 |
0,060 |
3,99 |
0,026 |
4,06 |
Рассмотрим природу замедленной стадии процесса электрохимического восстановления 4-метил-2-фенил-5,6-тетраметилентиопирилия на границе с β- глиноземом.
На рис. 6 приведены гальваностатические кривые изменения потенциала электрода во времени. Из хода кривых видно, что в начальный момент времени имеет место резкий спад потенциала и образование небольшого пика. Спустя 20–30 сек. потенциал вновь растет и при более длительной поляризации сохраняется постоянным.
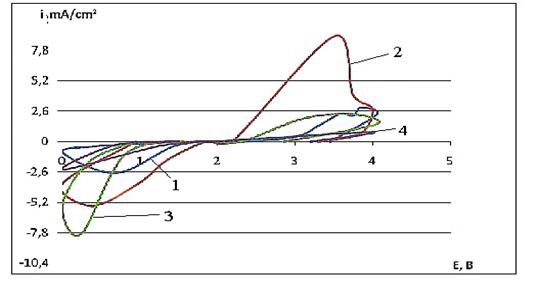
Рис. 6. Циклические потенциодинамические кривые электода изперхлората 4-метил-2-фенил-5,6-тетраметилентиопирилия с содержанием сажи 15 мас. % на границе с натриевым β- глиноземом при 20°С и скорости развертки потенциала 8 мВ/с при многократном циклировании (более 10 циклов)
Согласно литературным данным [5, 6], такая форма кривой потенциал – время может указывать на замедленность стадии кристаллизации, а именно – торможение скорости образования зародышей новой фазы. Значения разности потенциалов в пике и на площадке E, t – кривой для различных плотностей катодного тока приведены в таблице 3. Эта разность Екр известна в литературе как фазовое перенапряжение.
Значения разности потенциалов в пике и на площадке E, i – кривых.
Таблица 3
Значения разности потенциалов в пике и на площадке E, t – кривых при различных плотностях тока катодной поляризации ионной органической соли с добавкой 30 масс. % сажи при 200 С
|
ik, мА ∙см-2 |
Потенциал Е, В (отн. Na/Na+) |
||
|
Eпика |
Eплощадки |
ΔEкр |
|
|
0,015 |
1,75 |
1,725 |
0,02 |
|
0,025 |
1,60 |
1,57 |
0,03 |
|
0,045 |
1,52 |
1,47 |
0,05 |
|
0.065 |
1,35 |
1,28 |
0,07 |
|
0,075 |
1,27 |
1,19 |
0,08 |
|
0,085 |
1,18 |
1,08 |
0,10 |
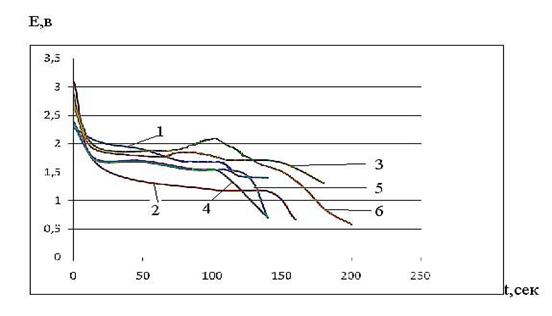
Рис. 7. Изменение потенциала Е (В) во времени t (c) для исследуемого электрода (соль I) при 200 при плотности тока 0,065 мА см-2 с различным содержанием соли в катоде ( масс.%): 1 - 30; 2 - 50; 3 - 70; 4 - 80; 5 - 85; 6 - 90
По зависимости lgi от 1/∆Eкр рис. 7 можно сделать заключение о механизме образования зародышей новой фазы и их росте. Для исследуемого нами процесса эта зависимость имеет вид прямой линии (рис. 8). Это является одним из доказательств протекания процесса по механизму образования двумерных зародышей и разрастания их по поверхности в сплошной слой. С закрытием поверхности сплошным слоем новой фазы катодный процесс начинает лимитироваться стадией диффузии.
Таким образом, скорость электрохимических процессов на границе ионной органической соли с твердым электролитом должна в значительной степени определяться состоянием этой границы.
Обнаруженные закономерности хорошо согласуются с результатами исследования межфазной границы органическая соль – твердый электролит в потенциостатическом режиме. Также нами изучена кинетика электрохимических превращений катиона 4-метил-2-фенил - 5,6 - тетраметилентиопирилия на границе с натриевым β- глиноземом.
С целью получения сведений о кинетике и механизме процессов образования новых фаз на границе катода с β-Al2O3 при потенциалах в области максимумов анодного и катодного пиков, на потенциодинамических кривых исследовали зависимость плотности тока на электроде от длительности поляризации в широком диапазоне температур от 70 до – 40 0С.
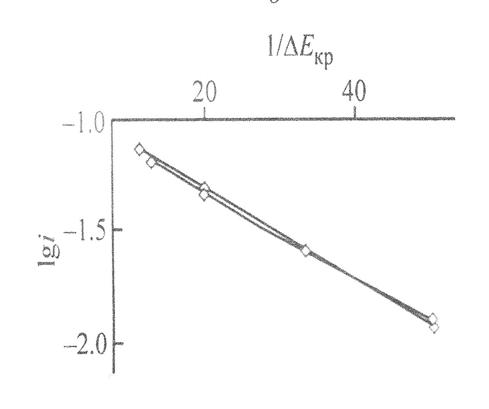
Рис. 8. Зависимость lgi (i, мА∙ см-2) – 1/ΔEкр (Eкр, В); содержание сажи в катоде 30 масс.%
Исследованный интервал потенциалов катодной поляризации: 1,4; 1,2; 1,0; 0,8; 0,6;0,4 В.
Интервал потенциалов анодной поляризации: 2,8; 3,0; 3,2; 3,4; 3,6 и 3,8 В. Область рабочих температур: 70, 60, 50,40, 30, 20, -10, -20, - 30, - 40 0C.
На рис. 9 приведены потенциостатические кривые, характеризующие электрохимическое поведение перхлората 4-метил-2-фенил- 5,6-тетраметилентиопирилия при различных потенциалах катодной и анодной поляризации и различных температурах.
Кривые i,t имеют характерный ход: быстрый рост плотности тока на начальном этапе поляризации, появление максимума или площадки и мало меняющихся значений плотности тока на следующем этапе, затем быстрый спад плотности тока и выход на площадку постоянных значений при более длительной поляризации.
Снижение температуры ячейки в область отрицательных значений (рис. 9) приводит к появлению на i,t – кривых двух максимумов на начальных этапах поляризации. Полученные данные хорошо согласуются с высказанными выше представлениями об образовании двух продуктов катодного восстановления перхлората 4-метил-2-фенил-5,6-тетраметилентиопирилия. При отрицательных температурах длительная поляризация приводит к смене лимитирующей стадии как катодного, так и анодного процессов – оба процесса переходят в режим диффузионного контроля.
В области максимумов тока на потенциодинамических кривых лимитирующей является химическая стадия, на что указывает линейный характер зависимости (i![]() - i), емкости от длительности поляризации и потенциостатических кривых.
- i), емкости от длительности поляризации и потенциостатических кривых.
На смену лимитирующей стадии на различных этапах процесса указывает и зависимость кажущейся энергии активации процесса от длительности поляризации.
Кажущаяся энергия активации рассчитывалась из величин угловых коэффициентов наклона прямых lgi– 1/T в соответствии с уравнением Аррениуса:
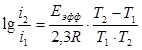 (1)
(1)
Зависимость lgi – 1/T анализировалась при условии E = const для различных температур. Значения эффективной энергии активации приведены в таблицах 4, 5.
Таблица 4
Значения кажущейся энергии активации Еэфф для процесса катодного восстановления перхлората 4-метил-2-фенил-5,6-тетраметилентиопирилия на границе с натриевым β- глиноземом в зависимости от величины ΔЕ и длительности катодной поляризации 8 с
|
Е, В |
Т1 = 313 К i1 (А/см2)·10-3 |
T2 = 343 K i2 (А/см2)·10-3 |
Eэфф, кДж/моль |
|
1,4 |
0,445 |
0,60 |
8,88 |
|
1,2 |
0,660 |
3,68 |
51,10 |
|
1,0 |
0,570 |
5,15 |
65,40 |
|
0,8 |
0,460 |
5,55 |
74,00 |
|
0,6 |
0,425 |
6,40 |
80,60 |
|
0,4 |
0,390 |
7,90 |
89,40 |
Таблица 5
Значение кажущейся энергии активации Еэфф в анодном процессе для перхлората 4-метил-2-фенил-5,6-тетраметилентиопирилия на границе с натриевым β- глиноземом в зависимости от величины ΔЕ и длительности катодной поляризации 8 с
|
EАП, В |
Т1 = 313 К i1 (А/см2)·10-3 |
T2 = 343 K i2 (А/см2)·10-3 |
Eэфф, кДж/моль |
|
2,8 |
0,35 |
1,07 |
48,40 |
|
3,0 |
0,26 |
1,84 |
84,70 |
|
3,2 |
2,02 |
2,00 |
0,43 |
|
3,4 |
0,63 |
1,70 |
42,90 |
|
3,6 |
0,11 |
1,55 |
114,50 |
|
3,8 |
0,07 |
1,12 |
120,00 |
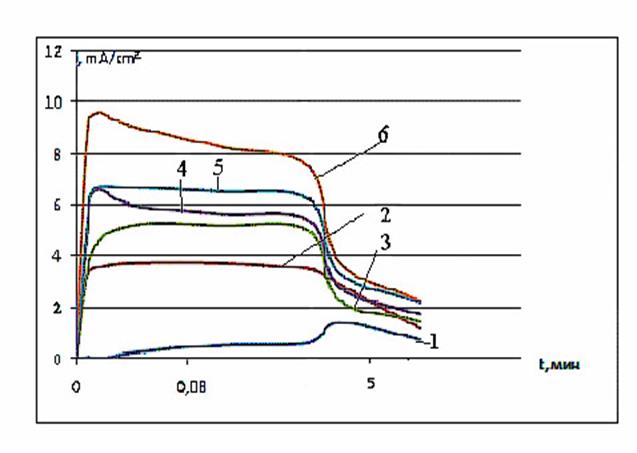
Рис. 9. Потенциостатические i,t-кривые катодного восстановления перхлората 4-метил-2-фенил-5,6-тетраметилентиопирилия на границе с натриевым β-глиноземом при 70 °С, давление прессования 10 кгс/см2 и различных потенциалах, В (относительно натриевого электрода сравнения): 1 - 1,4; 2 - 1,2; 3 - 1,0 ; 4 - 0,8; 5 - 0,6; 6 - 0,4; содержание сажи в катоде 30 масс. %
Анализ зависимости от температуры емкости, полученной QКП или отданной QАП электродом в процессе поляризации, показал, что при температурах 40…50 0C емкость мало меняется с температурой и составляет для катодного процесса (125…170)∙ 10-3 А ·с/см2, а для катодного (65…90) 10-3 А· с/см2.
В области более высоких температур емкость резко возрастает и меняется линейно с температурой. При этом температурный коэффициент для катодного процесса ![]() - 40· 10-3 А ·с/см2 град, а для анодного 12 ·10-3 А · с/см2 град. Анализ потенциодинамических кривых и все электрохимические расчеты проводились в соответствии с теоретическими основами электрохимической кинетики [301, 302].
- 40· 10-3 А ·с/см2 град, а для анодного 12 ·10-3 А · с/см2 град. Анализ потенциодинамических кривых и все электрохимические расчеты проводились в соответствии с теоретическими основами электрохимической кинетики [301, 302].
Рассмотрим роль сажи в электрохимических превращениях катиона 4-метил-2-фенил - 5,6 - тетраметилентиопирилия на границе с β- глиноземом.
С целью получения дополнительных сведений о роли сажи в электрохимических превращениях исследуемой органической соли на границе с β- глиноземом было изучено участие каждого из компонентов катодного материала в переносе заряда.
Был проведен рентгенофазовый анализ продуктов электрохимического превращения исследуемого соединения, который указал на тот факт, что в системе сажа – ионная органическая соль происходят химические взаимодействия уже в процессе приготовления катодного материала в результате механического перетирания и воздействия давления.
Микроструктурный анализ показал, что в результате электрохимической обработки происходит некоторое текстурирование органической соли в составе катодного материала. Влияние текстуры особенно сильно проявляется при содержании сажи 20 %. Такое явление возможно, если предположить, что в катодном материале происходит заполнение пустот углеродом – последний как бы создает подрешетку в структуре катода, вызывая как бы «разбухание» кристаллов ионной органической соли.
Полученные данные являются ценным справочным материалом, а установленные зависимости между потенциалом, плотностью тока и составом вещества катода являются новым вкладом в развитие электрохимии органических соединений. Результаты работы легли в основу разработок новых электродных материалов для химических источников тока с твердым электролитом и катодами на основе ионных органических солей.
Таким образом, 4- метил – 2- фенил – 5,6 – тетраметилентиопирилия перхлорат обладает низкой ионной проводимостью и может использоваться в качестве активного материала катода в химических источниках тока с твердым электролитом. Сажа снижает сопротивление границы Na / β- Al2O3, что согласуется с литературными данными об обратном внедрении натрия в углеродные материалы. Внедрение сажи в состав катодного материала облегчает внедрение ионов натрия в его структуру и способствует ускорению электрохимических превращений на границе β- Al2O3 | ИОС. Электрохимические превращения ионной органической соли на границе с β-глиноземом характеризуются высокой скоростью массопереноса ионов Na+ в структуре материала электрода. Скорость суммарного процесса на электроде с 4- метил – 2- фенил – 5,6 – тетраметилентиопирилия перхлоратом в качестве электрохимическиактивного материала определяется поведением катион-радикала и его димера.
В результате проведенного исследования нами проведено экспериментальное обоснование зависимости скорости электрохимических превращений на электроде из ионной органической соли ряда тиопирилия от величины и скорости изменения потенциала и от концентрации добавки сажи в составе электрода.
Установлено, что с наибольшей скоростью электрохимические превращения протекают на исследуемом электроде при содержании в его составе сажи в количестве 50 масс. %. Этот состав электрода можно рекомендовать для дальнейшей детальной технологической проработки с целью использования в твердофазных химических источниках тока.
Нами высказано предположение о возможном механизме электрохимического восстановления перхлората 4-метил-2-фенил-5,6-тетраметилентио-пирилия на границе с твердым электролитом, проводящим по ионам натрия. Показано, что процесс протекает по механизму образования двумерных зародышей. Если учесть, что стадия переноса заряда, благодаря высокой реакционной способности катиона тиопирилия, также должна протекать быстро и обратимо, тогда однозначно можно предположить, что скорость суммарного процесса на электроде с 4-метил-2-фенил-5,6-тетраметилентио-пирилия перхлоратом в качестве электрохимическиактивного материала должна определяться поведением катион-радикала и его димера.
Таким образом, экспериментально обоснована зависимость скорости электрохимических превращений на электроде из ионной органической соли ряда тиопирилия от величины и скорости изменения потенциала, концент-рации добавки сажи в составе электрода, температуры, давления прессования электродов. Рассчитаны кажущиеся энергии активации в зависимости от длительности поляризации. Установлено, что с наибольшей скоростью электрохимические превращения протекают на исследуемом электроде при содержании в его составе сажи в количестве 50 масс. % и такой состав электрода можно рекомендовать для дальнейшей технологической проработки с целью использования в твердофазных химических источниках тока. Показано, что процесс электрохимического восстановления перхлората 4-метил-2-фенил-5,6-тетраметилентиопирилия на границе с твердым электролитом, проводящим по ионам натрия, протекает по механизму образования двумерных зародышей.
Таким образом, высказано предположение о возможном механизме электрохимического восстановления перхлората 4-метил-2-фенил-5,6-тетраметилен-тиопирилия на границе с твердым электролитом, проводящим по ионам натрия. Образование новой фазы происходит по механизму двумерных зародышей. Хемосорбция атомов углерода на поверхности полупроводника происходит с частичным, либо полным переносом заряда электрона из полупроводника на атом сажевого углерода с образованием ад-атомов, способных в дальнейшем терять свои электроны и переходить в ад-ионы Указанные процессы облегчают протекание катодного восстановления органического катиона соли и способствуют переходу его в диффузионный режим. Такая интерпретация механизма процесса хорошо согласуется с результатами потенциостатических измерений и линейным характером зависимости потенциала и плотности тока в максимуме потенциодинамических кривых от скорости развертки потенциала.
Рецензенты:
Родионов И. В., д.т.н., профессор кафедры ТМС СГТУ им. Ю. А. Гагарина, г.Саратов.
Соловьева Н. Д., д.т.н., профессор, зав. кафедрой ТЭП ЭТИ СГТУ, г.Саратов.
Библиографическая ссылка
Дмитриенко Т.Г., Демидов А.А. ЭЛЕКТРОАКТИВНЫЕ ОРГАНИЧЕСКИЕ МАТЕРИАЛЫ НА ОСНОВЕ СОЛЕЙ ТИОПИРИЛИЯ И ИХ ЭЛЕКТРОХИМИЧЕСКОЕ ПОВЕДЕНИЕ В ТВЕРДОЙ ФАЗЕ // Современные проблемы науки и образования. 2013. № 5. ;URL: https://science-education.ru/ru/article/view?id=10160 (дата обращения: 17.05.2026).



