Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
REACTION USING THE NINGIDRIN FOR QUANTITATIVE DETERMINATION OF ALIPHATIC AMINES
Введение
В Пермской государственной фармацевтической академии синтезированы новые биологически активные соединения, превосходящие по антиамнестическому действию пирацетам: ВКВ-1 и ВКВ-2 из группы производных 5-арил-4-ацил-3-гидрокси-1-карбоксиалкил-3-пирролин-2-она и КОН-1 из группы производных 5-арил-4-ацил-3-гидрокси-1-гидроксиалкил-3-пирролин-2-она [1]. В связи с рекомендацией к проведению доклинических испытаний нами проводятся исследования по разработке методов контроля качества и стандартизации субстанций и лекарственных форм этих соединений [3–5].
Исходя из схемы получения соединений ВКВ-1, ВКВ-2, КОН-1, посторонней (специфической) примесью в их субстанциях может быть алифатический амин: соответственно аминокапроновая кислота (АКК), аминоуксусная кислота (АУК) или 3-аминопропанол (3-АПР). АУК (глицин) и АКК широко применяются в медицинской практике [6].
Целью настоящего исследования явилась разработка спектрофотометрической методики количественного определения алифатических аминов АКК, АУК и 3-АПР. Для получения окрашенных продуктов использована реакция с нингидрином.
Материалы и методы исследования
В исследованиях использовались спектрофотометр СФ-2000; колориметр фотометрический КФК-3.
Растворители и реагенты: спирт этиловый 95 %, вода очищенная, АКК, АУК, 3-АПР, нингидрин, аскорбиновая кислота, фосфатные буферные растворы (pH 6,0-7,4) [2].
Результаты исследований и их обсуждение
Предварительными исследованиями выбраны оптимальные условия проведения реакции алифатический амин – нингидрин: нагревание реакционной массы на кипящей водяной бане в течение 30 мин; среда – спирт этиловый (20–30 % в реакционной смеси); объём буферного раствора от 4 до 6 мл.
Сняты спектры поглощения продуктов реакции, полученных при различных значениях pH (фосфатный буферный раствор, pH от 6,0 до 7,2), в интервале длин волн от 350 до 700 нм на спектрофотометре СФ-2000 в кювете с толщиной слоя 1 см. В качестве раствора сравнения использовали воду очищенную. Концентрация исходных водных растворов аминов: АУК - 0,02 %; АКК- 0,05 %; 3-АПР – 0,03 %.
Спектры характеризуются двумя четко выраженными максимумами поглощения при длинах волн 400±2 нм и 568±2 нм и одним минимумом, лежащим в области 455–465 нм. Положение максимумов практически не зависит от pH буферного раствора. В качестве аналитической волны для алифатических аминов была выбрана 568 нм.
Реакция среды существенно влияет на интенсивность поглощения, максимальная оптическая плотность достигается при различных значениях рН: для АУК – 6,2; АКК – 6,8; 3-АПР – 6,8. Буферные растворы с этими значениями были использованы как оптимальные для соответствующих аминов.
Анализ литературных данных показал, что восстанавливающие вещества повышают чувствительность реакции. В качестве восстановителей чаще используют небольшие количества хлорида олова, хлорида титана, цианида калия, гидразина сульфата, аскорбиновой кислоты. Для исследования нами выбрана аскорбиновая кислота (нормальный окислительно-восстановительный потенциал +0,167 В), которая является наиболее доступным и нетоксичным реагентом [7].
Измеряли оптическую плотность продуктов реакции алифатический амин – нингидрин, полученных при оптимальных значениях рН, при длине волны 568 нм. Реакцию проводили в двух вариантах: без добавления и с добавлением аскорбиновой кислоты. Результаты опытов представлены в таблице 1. Введение аскорбиновой кислоты в реакционную массу не изменяет характера спектра поглощения продукта реакции амин – нингидрин, но значительно увеличивает интенсивность поглощения.
Таблица 1. Влияние аскорбиновой кислоты на интенсивность поглощения продуктов реакции алифатический амин – нингидрин
|
Алифатический амин |
Оптическая плотность продуктов реакции алифатический амин – нингидрин |
|
|
Без добавления аскорбиновой кислоты |
С добавлением аскорбиновой кислоты |
|
|
АУК |
0,328 |
0,505 (+ 54%) |
|
АКК |
0,324 |
0,473 (+ 46%) |
|
3-АПР |
0,101 |
0,485 (+ 380%) |
Для проверки соблюдения основного закона светопоглощения продуктов реакции алифатических аминов с нингидрином (определение линейности) построены графики зависимости оптической плотности (А) от концентрации амина в фотометрируемом растворе (С, мкг/мл) (рисунки 1–3; график № 1 – продукт получен без добавления аскорбиновой кислоты; график № 2 – с добавлением аскорбиновой кислоты).
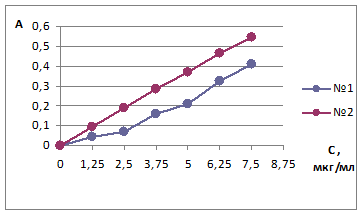
Рис. 1. Градуировочный график продукта реакции АКК – нингидрин
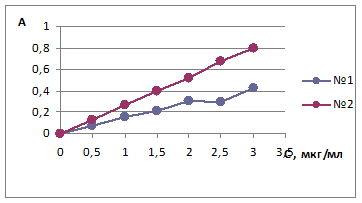
Рис. 2. Градуировочный график продукта реакции АУК – нингидрин
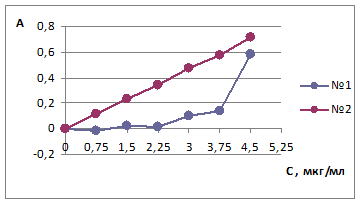
Рис. 3. Градуировочный график продукта реакции 3-АПР – нингидрин
Исследования показали, что введение аскорбиновой кислоты в реакционную массу значительно увеличивает интенсивность светопоглощения, придаёт зависимости оптической плотности от концентрации линейный характер (коэффициент корреляции линейной зависимости более 0,99). Поэтому в дальнейших опытах продукты реакций аминов с нингидрином получали в присутствии аскорбиновой кислоты.
Рассчитаны молярный и удельный показатели поглощения продуктов реакций и пределы обнаружения АКК, АУК и 3-АПР спектрофотометрическим методом (приняв Аmin 0,025) (таблица 2).
Таблица 2. Валидационные характеристики спектрофотометрической методики
|
Алифатический амин |
Область линейности графика, мкг/мл |
Показатели поглощения |
Предел обнаружения |
||
|
удельный |
молярный |
мкг/мл |
мкмоль/л |
||
|
АУК |
0,50–3,00 |
2500 |
18800 |
0,100 |
1,33 |
|
АКК |
1,25–7,50 |
757 |
9930 |
0,330 |
2,50 |
|
3-АПР |
0,75–4,50 |
1620 |
12200 |
0,155 |
2,05 |
Установлено, что исследуемые реакции достаточно чувствительны, поэтому могут быть использованы для анализа примесей алифатических аминов в субстанциях соединений ВКВ-1, ВКВ-2, КОН-1, а также количественного определения АУК (глицина) и АКК (субстанции, лекарственные препараты).
Методика определения АКК в растворах для инъекций.
В промышленности выпускают АКК в виде 5 % раствора для инфузий во флаконе
100 мл. В аптеке изготавливают 1 % и 5 % растворы АКК для инъекций [6]. Растворы содержат натрия хлорид (0,9 %).
Методика. 1 мл препарата помещают в мерную колбу вместимостью 50 мл (1 % раствор) или 250 мл (5 % раствор), доводят водой до метки, перемешивают (раствор А). В мерную колбу вместимостью 100 мл помещают 3 мл раствора А, добавляют 4 мл фосфатного буферного раствора с pH 6,8, 2 мл 1 % раствора нингидрина в спирте этиловом 95 %, 2 мл 0,05 % водного раствора аскорбиновой кислоты. Содержимое колбы нагревают на кипящей водяной бане в течение 30 мин, быстро охлаждают, доводят водой до метки и перемешивают.
У полученного раствора измеряют оптическую плотность при длине волны 568 нм в кювете толщиной 1 см.
В качестве раствора сравнения используют контрольный опыт: в мерную колбу вместимостью 100 мл помещают 2 мл воды, 4 мл фосфатного буферного раствора с pH 6,8, и далее поступают, как указано в основной методике.
Параллельно измеряют оптическую плотность раствора стандартного образца (СО).
Приготовление раствора СО. Около 0,0500 г (точная навеска) субстанции АКК помещают в мерную колбу вместимостью 250 мл, растворяют в воде, доводят объем колбы тем же растворителем до метки и перемешивают (раствор В). В мерную колбу вместимостью 100 мл помещают 3 мл раствора В и далее поступают, как указано в основной методике.
Содержание АКК (X) в 1 мл препарата вычисляют по формуле:
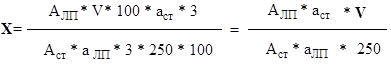
где АЛП – оптическая плотность исследуемого раствора;
Аст – оптическая плотность раствора СО;
аЛП – навеска лекарственного препарата, мл;
аст – навеска СО, г;
V – объём мерной колбы для приготовления разведения препарата.
Оценка правильности результатов осуществлялась путем статистической обработки выборок, полученных в ходе количественного анализа АКК в модельных пробах на трех уровнях концентрации в пределах рекомендуемой аналитической области методики (80,100,120 % от количества принятого за 100 % – 0,05 г). По полученным данным построен график зависимости оптической плотности от концентрации аминокапроновой кислоты. Линия тренда пересекает ось «Оптическая плотность» в точке 0, что свидетельствует о правильности разработанной методики.
Для определения повторяемости (сходимости) результатов методики готовили модельные смеси 1 % и 5 % растворов АКК и раствор СО. Проводили по семь параллельных определений. Результаты исследований приведены в таблицах 3 и 4.
Таблица 3. Повторяемость (сходимость) результатов определения 1 % раствора АКК
|
Xi |
f |
х (сред) |
S |
Sx |
|
0,0102; 0,0102; 0,0100; 0,0098; 0,0098; 0,0100; 0,0101 |
6 |
0,0100 |
0,000195 |
0,00008 |
|
t (P;f) |
Δ x |
Δ x (сред) |
ε, % |
ε (сред), % |
|
2,45 |
0,000478 |
0,000195 |
4,78 |
1,95 |
Таблица 4. Повторяемость (сходимость) результатов определения 5 % раствора АКК
|
Xi |
f |
х (сред) |
S |
Sx |
|
0,0502; 0,0503; 0,0501; 0,0502; 0,0503; 0,0502; 0,0502 |
6 |
0,0502 |
0,00094 |
0,00038 |
|
t (P;f) |
Δ x |
Δ x (сред) |
ε, % |
ε (сред), % |
|
2,45 |
0,0023 |
0,00094 |
4,58 |
1,88 |
Разработанная методика дает точные результаты, проста в исполнении, экономична, не требует использования токсичных реагентов.
Выводы
1. Выбраны оптимальные условия проведения реакции алифатический амин – нингидрин; аналитическая длина волны – 568 нм; максимальная оптическая плотность достигается при значениях рН: для АУК – 6,2; АКК – 6,8; 3-АПР – 6,8.
2. Введение аскорбиновой кислоты в реакционную массу не изменяет характера спектра поглощения продукта реакции амин – нингидрин, но значительно увеличивает интенсивность поглощения; придаёт зависимости оптической плотности от концентрации линейный характер (r более 0,99).
3. Исследуемые реакции достаточно чувствительны, поэтому могут быть использованы для анализа примесей алифатических аминов в субстанциях соединений ВКВ-1, ВКВ-2, КОН-1, а также количественного определения АУК (глицина) и АКК (субстанции, лекарственные препараты).
4. Разработана методика количественного определения АКК в 1 % и 5 % растворах для инъекций. Относительная ошибка среднего результата в модельных смесях не превышает ± 1,95 %.
Рецензенты:
Коркодинова Любовь Михайловна, доктор фармацевтических наук, профессор, заведующий кафедрой фармацевтической химии ФОО, ГБОУ ВПО ПГФА Минздрава России, г. Пермь.
Михайловский Александр Георгиевич, доктор фармацевтических наук, доцент, заведующий кафедрой неорганической химии ГБОУ ВПО ПГФА Минздрава России, г. Пермь.
Библиографическая ссылка
Кляшева О.Н., Ярыгина Т.И., Басс С.М., Ван К.В. ИСПОЛЬЗОВАНИЕ РЕАКЦИИ С НИНГИДРИНОМ В КОЛИЧЕСТВЕННОМ ОПРЕДЕЛЕНИИ АЛИФАТИЧЕСКИХ АМИНОВ // Современные проблемы науки и образования. 2013. № 3. ;URL: https://science-education.ru/en/article/view?id=9160 (дата обращения: 16.05.2026).



