Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
BILATERAL CORONARY CHRONIC TOTAL OCCLUSION RECANALIZATION. SARATOV SCIENTIFIC INSTITUTE OF CARDIOLOGY FIRST EXPERIENCE
Общеизвестно, что из всех морфологических форм атеросклеротического поражения коронарных артерий одной из наиболее технически сложных для реваскуляризации являются хронические окклюзии [7]. Хронические тотальные окклюзии коронарных артерий (ХОКА) выявляются при ангиографическом исследовании примерно у 20-30 % пациентов [1,13]. Наличие ХОКА является наиболее частым критерием в пользу выбора коронарного шунтирования [2,3], поскольку у пациентов с многососудистым поражением коронарного русла, ввиду невысокой частоты успешных реканализаций, процедура сводится к неполной анатомической реваскуляризации. Несмотря на значительный прогресс интервенционных технологий в последние годы, успешность чрескожных реканализаций ХОКА составляет от 47 до 80 % (в среднем 67 %) [11]. Наиболее частой причиной неудач при реканализации ХОКА является непроведение проводника интралюминально в дистальное русло. Дополнительную проблему создает неоптимальная антеградная визуализация дистального русла. Гистологические исследования выявили, что концентрация богатой коллагеном фиброзной ткани особенно высока в проксимальной части окклюзии и более низка в дистальной [6,9,10]. Кроме того, дистальная культя чаще, чем проксимальная, имеет сужающуюся (tapered) форму, более благоприятную для проводниковой пенетрации. С учетом вышеизложенного, с 2003-2004 годов усилиями главным образом японских операторов стали активно развиваться различные методики ретроградной (билатеральной) реканализации ХОКА [7]. Технология была усовершенствована, появились разнообразные стратегии на основе билатерального доступа, такие как: киссинг-проводник, проводник-ориентир, прямая и обратная CART методика, «ретроградное проведение в истинный просвет проксимальной культи» [8].
Целью настоящего исследования явился анализ ангиографических и клинических результатов реканализации ХОКА билатеральным способом.
Материалы и методы
В Саратовском НИИ кардиологии билатеральные вмешательства при ХОКА были выполнены 27 пациентам. Мужчин 21, женщин 6. Средний возраст 56±5 лет.
Показания к ретроградному вмешательству у всех больных определялись на основе ангиографических характеристик хронической окклюзии, неблагоприятных для проведения антеградной реканализации, таких как: протяженная окклюзия (более 20 мм) с плохой антеградной визуализацией дистального русла, наличие неоптимальных условий в области проксимальной части окклюзии (извитость сосуда, развитая боковая ветвь, отсутствие благоприятной культи окклюзированного сосуда, наличие мостовидных коллатералей), а также невозможность создания достаточного упора для пенетрации проксимально расположенной окклюзии. Обязательным условием являлось наличие хорошо развитой системы коллатералей из контра- ипсилатеральной артерии, одна или несколько из которых непрерывно прослеживались до дистального русла закрытой артерии и имели достаточный диаметр. Нескольким пациентам предварительно было выполнено стентирование стенозированной донорской артерии с целью минимизации вероятности ее тромбоза и ишемических осложнений. Баллонная дилатация коллатералей не применялась. При планировании вмешательства первичную попытку антеградной реканализации было решено провести у 18 пациентов. Из них 10 пациентам после неудачи антеградной попытки в дальнейшем единовременно проводилась попытка ретроградной реканализации (рисунок 1). У 8 пациентов вторичная попытка была отсрочена на 20-30 суток по причине высокого или предельного расхода контрастного вещества и/или высокой или предельной лучевой нагрузки. 12 пациентам были выставлены показания к первично ретроградному вмешательству.
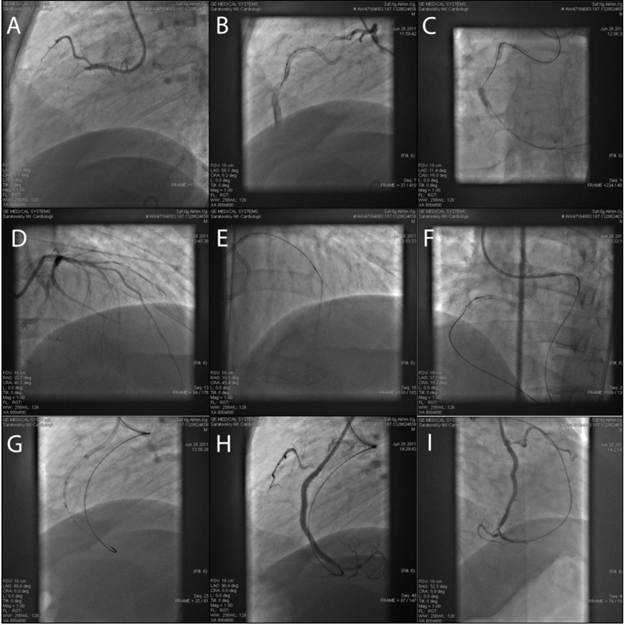
Рисунок 1. Пациент С., 47 лет. В 2010 году выполнена реканализация и стентирование хронической окклюзии проксимального сегмента правой коронарной артерии антеградным способом. В 2011 году на контрольной коронарограмме - реокклюзия стента (А). Выполнена попытка антеградной реканализации, осложнившаяся тубулярной диссекцией целевого коронарного сегмента без экстравазации (B). При ретроградном контрастировании отчетливо визуализируется дистальное русло правой коронарной артерии (С) и развитая сеть межкоронарных анастомозов (септальные коллатерали) из передней межжелудочковой артерии (D). Проводник и микрокатетер проведены из системы передней межжелудочковой артерии через септальную коллатераль (Е), в дистальное русло правой коронарной артерии. Окклюзированный сегмент успешно реканализован ретроградным проводником, сформирована коронарная петля с выведением проводника через антеградный проводниковый катетер (F). Далее по антеградному проводниковому катетеру проведен баллонный катетер, выполнено баллонирование (G) и стентирование целевого коронарного сегмента двумя стентами общей протяженностью 27 мм. Достигнут антеградный кровоток TIMI 3 с остаточным стенозом 0 % на всех стентах без признаков диссекции (H, I)
Все пациенты получали стандартную антикоагулянтную и дезагрегантную терапию.
Локализация хронической окклюзии: правая коронарная артерия (17 пациентов), передняя нисходящая артерия (9), огибающая артерия (1). Во всех случаях поражение располагалось в проксимальном и среднем сегментах, протяженность его составляла от 15 до 30 мм. Артерией-донором коллатералей являлась:
1. При локализации окклюзии в передней нисходящей артерии - правая коронарная артерия (8), огибающая артерия (1).
2. При локализации окклюзии в огибающей артерии - правая коронарная артерия (1).
3. При окклюзии правой коронарной артерии - во всех случаях использовалась передняя нисходящая артерия (табл. 1). У 5 пациентов при ангиографии был выявлен гемодинамически значимый стеноз артерии-донора коллатералей, который был устранен при помощи имплантации стента.
Таблица 1. Локализация ХОКА и пути коллатерализации
|
Артерия-донор коллатералей |
Локализация ХОКА |
||
|
Передняя межжелудочковая артерия N=9 |
Огибающая артерия N=1 |
Правая коронарная артерия N=17 |
|
|
Передняя межжелудочковая артерия |
|
|
17 |
|
Огибающая артерия |
1 |
|
|
|
Правая коронарная артерия |
8 |
1 |
|
Для ретроградного доступа наиболее часто использовались септальные коллатерали (24). Также использовались апикальные (2), задне-боковые эпикардиальные коллатерали (1) (табл. 2).
Таблица 2. Выбор коллатералей при выполнении реканализации ХОКА билатеральным способом
|
Выбранные коллатерали |
Количество процедур (N=27) |
|
Септальные |
24 |
|
Апикальные |
2 |
|
Заднее-боковые |
1 |
Оценивались ангиографические и непосредственные клинические результаты вмешательства. Под ангиографическим успехом понимали достижение финального антеградного кровотока TIMI 3 по дистальному руслу артерии с резидуальным стенозом менее 30 % от референтного диаметра артерии при отсутствии больших осложнений - смерть, ОИМ (в т.ч. ввиду острого тромбоза донорской артерии), ОНМК, тампонада, требующая перикардиоцентеза или хирургического вмешательства. Под непосредственным клиническим успехом понимали полное отсутствие симптомов стенокардии или снижение ее признаков на 2 и более функциональных класса (по данным клинического обследования, нагрузочных ЭКГ-проб).
Результаты
Провести ретроградный проводник в дистальное русло удалось в 19 наблюдениях. Далее применялись различные стратегии (табл. 3). Прямая и обратная CART-методика выполнялась наиболее часто (9). В 6 наблюдениях было возможно выполнить технику киссинг-проводников. У 4 больных при наличии развитой боковой ветви в проксимальной части бляшки, невозможности создания адекватного упора для проведения антеградного баллона, выполнено ретроградное проведение проводника в истинный просвет проксимальной культи. В дальнейшем для проведения антеградного баллона применялась техника анкерного баллона (3), у 2 пациентов при невозможности заведения антеградного проводника выполнен захват и выведение ретроградного проводника 300 см через антеградный проводниковый катетер.
Таблица 3. Выбор методики реканализации из билатерального доступа
|
Методика |
Количество процедур (N=19) |
|
Прямая и обратная CART-методика |
9 |
|
Kissing-wires |
6 |
|
Ретроградное проведение проводника в истинный просвет проксимальной культи |
4 |
Процедуру завершали баллонной ангиопластикой окклюзии и имплантацией стента с лекарственным покрытием. Ангиографический и клинический успех достигнут у всех 19 пациентов. При этом у 16 пациентов полностью отсутствовали клинические и объективные признаки стенокардии. У 3 больных отмечено снижение стенокардии на 2 функциональных класса, сохранялись объективные признаки ишемии миокарда.
У 8 пациентов проведение ретроградного проводника оказалось неуспешным (табл. 4). Всем им ранее выполнялись попытки антеградной реканализации. Процедура была прекращена у 4 больных по причине выраженного спазма коллатерального русла, сопровождавшегося ишемическими изменениями на ЭКГ, нарушениями ритма. Изменения были обратимы и после удаления проводника и микрокатетера купировались полностью. У 1 пациента произошла перфорация септальной артерии с формированием интрамуральной гематомы. У 3 пациентов процедура была прекращена за длительностью, с учетом количества израсходованного контрастного вещества, при явлениях спазма коллатералей, препятствующего проведению проводника, ригидного к селективному введению нитропрепаратов. Таким образом, сосудистый спазм стал причиной 7 неудач.
Таблица 4. Причины завершения вмешательства при неудачной попытке реканализации окклюзии билатеральным способом
|
Причина |
Количество (человек) |
|
Перфорация септальной коллатерали |
1 |
|
Спазм коллатералей |
4 |
|
Высокий или предельный расход контрастного вещества и/или высокая или предельная лучевая нагрузка |
3 |
Обсуждение
Остается открытым вопрос, следует ли проводить попытку эндоваскулярного лечения пациентам с хроническими окклюзиями, не поддающимися антеградной реканализации, или безопаснее рекомендовать операцию коронарного шунтирования. С одной стороны, эндоваскулярные технологии претерпели значительную эволюцию за последние годы, и их возможности вплотную приблизились к возможностям открытого хирургического лечения. В связи с этим в поле зрения эндоваскулярных хирургов попадают все более сложные в лечении коронарные окклюзии. Вместе с тем более агрессивные методики ассоциированы с более высоким риском фатальных осложнений. Ретроградные вмешательства при хронических коронарных окклюзиях потенциально опасны не только для целевой окклюзированной артерии с точки зрения перфорации, опасных диссекций, но и для артерии-донора коллатералей. Нарушение коллатерального кровотока может привести к ишемическим осложнениям [4]. Не стоит забывать о длительности процедуры, повышенном расходе контрастного вещества, лучевой нагрузке [5,8]. Поэтому авторы часто говорят о необходимости большого опыта эндоваскулярных вмешательств для выполнения таких процедур. Кроме того, для полноты оценки эффективности методики не хватает исследований на больших группах пациентов, существующие источники ограничены лишь ретроспективными обзорами на малых группах больных [8].
Вместе с тем существует и логичное обоснование для попытки ретроградной реканализации. Прежде всего, не всякая хроническая коронарная окклюзия при однососудистом поражении подлежит коронарному шунтированию (редко предлагается оперативное лечение при изолированной окклюзии правой коронарной артерии). Однако, по данным нерандомизированных исследований, реканализация любой хронической окклюзии, даже при наличии крупноочагового инфаркта, повышает качество жизни пациентов (снижение функционального класса стенокардии, повышение толерантности к физическим нагрузкам, повышение фракции выброса и улучшение локальной сократимости при эхокардиографии), а также улучшает показатели выживаемости в отдаленном периоде [5,12]. Кроме того, существует неподтвержденная гипотеза, согласно которой реканализованная коронарная артерия может в дальнейшем сама стать донором коллатералей при прогрессировании атеросклеротического процесса в бассейне другой артерии. Сопутствующая патология, препятствующая проведению коронарного шунтирования, возраст, отказ пациента от кардиохирургического лечения также позволяют сделать выбор в пользу малоинвазивного лечения.
Наш опыт проведения ретроградных вмешательств позволил выделить несколько методологических закономерностей. Антеградная попытка реканализации предпринималась при малейшей вероятности ее успеха. Ретроградный способ избирался при исчерпании всех других методик. Вместе с тем 12 пациентам была первично избрана методика ретроградной реканализации из-за сочетания ряда неблагоприятных ангиографических условий (проксимальная, неоптимальной формы культя или ее отсутствие, развитая боковая ветвь в месте проксимальной культи окклюзии), делающих невозможной антеградную попытку.
При проведении проводника в большинстве случаев использовались септальные коллатерали, что было связано с меньшим риском кровотечения в полость перикарда и развития тампонады сердца в случае перфорации коллатерали. При повреждении септальной коллатерали у одного пациента образовался небольших размеров экстравазат (интрамуральная гематома), не повлекший никаких ишемических последствий. Кроме того, эпикардиальные коллатерали часто были недостаточно развиты, что делало их непригодными для проведения инструментов. В сравнении с апикальными коллатералями, септальный доступ был связан с лучшей визуализацией и управляемостью инструментария. При планировании вмешательства предпочтение отдавалось лишь крупным, визуализируемым коллатералям СС2, что было обусловлено меньшей вероятностью спазма, ведущего к невозможности проведения проводника по коллатерали.
Выбор методики ретроградной реканализации зависел в основном от ангиографической характеристики окклюзии. Предпочтение отдавалось методике ретроградного проведения проводника в истинный просвет проксимального сосудистого русла с дальнейшим проведением в антеградный проводниковый катетер и созданием петли, как наиболее безопасной. При невозможности проведения проводника в истинное русло применяли прямую и обратную CART-методику. Также в таких случаях, особенно при выраженной извитости сосуда, применяли технику киссинг-проводников.
Что касается осложнений, то наиболее частым препятствием для проведения процедуры был спазм коллатералей, ригидный к селективному введению нитропрепаратов.
Выводы
1. Билатеральный способ реканализации ХОКА позволяет добиться более высокой ангиографической и клинической эффективности эндоваскулярных вмешательств за счет расширения показаний к последним.
2. Реканализации хронических коронарных окклюзий билатеральным способом являются технически сложными вмешательствами, сопряженными с повышенным риском осложнений. Однако применение данной методики вполне оправдано при невозможности антеградного доступа, высоком анестезиологическом риске коронарного шунтирования, а также при категорическом отказе пациента от кардиохирургического лечения.
3. Для минимизации количества и тяжести осложнений необходим тщательный отбор пациентов, правильный выбор стратегии и достаточный хирургический опыт.
4. Для развития метода необходимо дальнейшее пополнение методологической базы, проведение рандомизированных исследований по оценке эффективности ретроградных вмешательств на коронарных артериях.
Рецензенты:
Агапов Валерий Владимирович, доктор медицинских наук, главный врач ГУЗ «Областной кардиохирургический центр» Министерства здравоохранения Саратовской области, г. Саратов.
Прелатов Вадим Алексеевич, доктор медицинских наук, профессор, профессор кафедры хирургии ФПК и ППС ГБОУ ВПО «Саратовский государственный медицинский университет им. В. И. Разумовского» Министерства здравоохранения России, г. Саратов.
Библиографическая ссылка
Рузанов И.С., Глухов Е.А., Титков И.В., Глухов Е.А., Шитиков И.В., Олейник А.О., Баратова К.Ю. РЕКАНАЛИЗАЦИЯ ХРОНИЧЕСКИХ ОККЛЮЗИЙ КОРОНАРНЫХ АРТЕРИЙ БИЛАТЕРАЛЬНЫМ СПОСОБОМ. ОПЫТ САРАТОВСКОГО НИИ КАРДИОЛОГИИ. // Современные проблемы науки и образования. 2012. № 6. ;URL: https://science-education.ru/en/article/view?id=8055 (дата обращения: 16.05.2026).



