Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
SYNTHESIS AND PSYCHO-PHARMACOLOGICAL ANALYSIS OF NEW DERIVATIVES OF 5-(N-PYRROLIDINO)- AND 5-(N-PIPERAZINO)-URACIL
В настоящее время установлено, что соединения, содержащие в своей структуре фрагмент пиперазина, связанный с другой гетероциклической системой, часто обладают выраженными психотропными свойствами с высоким аффинитетом к серотониновым рецепторам [1, 2, 3, 8]. Некоторые психоактивные соединения, имеющие в своем составе прообраз пирролидинового цикла, демонстрируют сходный фармакологический эффект с этими производными пиперазина [4]. С другой стороны, результаты исследований фармакологических свойств производных пиримидина позволяют рассматривать эти вещества в качестве лигандов к интрацентральным рецепторам психотропных агентов [7]. В связи с этим целенаправленный синтез и исследование психофармакологических свойств новых производных пиримидинового ряда, дополнительно содержащих пирролидиновые и пиперазиновые фрагменты в качестве заместителей, представляет значительный теоретический и практический интерес.
С целью поиска новых и селективных анксиолитиков и антидепрессантов нами был синтезирован ряд производных 5-аминоурацила, аминогруппа которых в положении С-5 пиримидинового ядра входит в состав пирролидинового или пиперазинового цикла.
В качестве исходных соединений для синтеза целевых веществ были использованы урацил и 6-метилурацил, последний получали конденсацией ацетоуксусного эфира с мочевиной [5]. Урацилы бромировались в среде водной уксусной кислоты и в дальнейшем подвергались N-алкилированию a-хлорэфирами или реакционноспособными бромидами. a-Хлорэфиры синтезировали из соответствующих спиртов и формальдегида по реакции Анри [9]. Алкилирование осуществляли по методу Гилберта-Джонсона, для чего 5-бромурацил и 5-бром-6-метилурацил превращали в соответствующие триметилсилильные производные путем кипячения в среде гексаметилдисилазана. Алкилирование a-хлорэфирами, фенацилхлоридом или п-феноксибензилбромидом проводили в среде безводного 1,2-дихлорэтана по способу, описанному нами ранее [6]. Заключительное аминирование протекало при кипячении в среде избытка пирролидина, пиперазина, метилпиперазина или фенилпиперазина с использованием безводного 2-бутанола или этоксиэтанола в качестве растворителя по схеме:
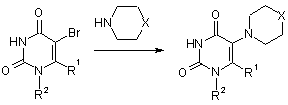
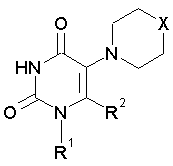
Таблица 1. Физико-химические свойства производных 5-аминоурацила
|
Соеди-нение |
R1 |
R2 |
X |
Т.пл., оС |
Брутто-формула |
Выход,% |
Rf (система) |
|
•1 |
H |
H |
Связь |
211-213 |
C8H11N3O2 |
54 |
0,43 (A) |
|
•2 |
H |
CH3 |
Связь |
242-244 |
C9H13N3O2 |
49 |
0,38 (A) |
|
•3 |
H |
H |
NH |
257-259 |
C8H12N4O2 |
51 |
0,21 (А) |
|
•4 |
H |
H |
N(CH3) |
291-293 |
C9H14N4O2 |
55 |
0,35 (А) |
|
•5 |
H |
H |
N(C6H5) |
275-277 |
C14H16N4O2 |
78 |
0,74 (A) |
|
•6 |
CH2C6H5 |
H |
Связь |
226-228 |
C15H17N3O2 |
82 |
0,71 (A) |
|
•7 |
CH2C6H5 |
H |
N(CH3) |
145-147 |
C16H20N4O2 |
67 |
0,16 (А) |
|
•8 |
CH2C6H5 |
H |
N(C6H5) |
167-169 |
C21H22N4O2 |
53 |
0,86 (А) |
|
•9 |
CH2OCH3 |
H |
Связь |
211-213 |
C9H13N3O3 |
54 |
0,75 (A) |
|
•10 |
CH2OCH3 |
CH3 |
Связь |
242-244 |
C10H15N3O3 |
43 |
0,71 (A) |
|
•11 |
CH2OC2H5 |
H |
Связь |
154-156 |
C11H17N3O3 |
56 |
0,77 (A) |
|
•12 |
CH2OC2H5 |
CH3 |
Связь |
158-159 |
C12H19N3O3 |
64 |
0,75 (A) |
|
•13 |
CH2OC2H5 |
CH3 |
N(CH3) |
243-245 |
C13H22N4O3 |
52 |
0,55 (B) |
|
•14 |
CH2OCH(CH3)2 |
H |
Связь |
187-189 |
C12H19N3O3 |
59 |
0,64 (C) |
Таблица 1. Продолжение
|
•15 |
CH2OCH(CH3)2 |
CH3 |
Связь |
153-154 |
C12H19N3O3 |
83 |
0,41 (A) |
|
•16 |
CH2OC2H4Cl |
H |
Связь |
201-203 |
C11H17ClN3O3 |
61 |
0,59 (A) |
|
•17 |
CH2OC2H4Cl |
CH3 |
Связь |
286-288 |
C12H18ClN3O3 |
62 |
0,74 (A) |
|
•18 |
CH2C(O)C6H5 |
H |
Связь |
229-230 |
C16H17N3O3 |
61 |
0,31 (D) |
|
•19 |
CH2OCH2C6H5 |
H |
NH |
157-158 |
C16H20N4O3 |
68 |
0,20 (B) |
|
•20 |
CH2OCH2C6H5 |
H |
Связь |
155-157 |
C16H19N3O3 |
55 |
0,65 (D) |
|
•21 |
CH2OCH2C6H5 |
H |
N(CH3) |
184-186 |
C17H22N4O3 |
55 |
0,37 (А) |
|
•22 |
CH2OCH2C6H5 |
H |
N(C6H5) |
163-165 |
C22H24N4O3 |
55 |
0,83 (А) |
|
•23 |
CH2OCH2C6H5 |
CH3 |
Связь |
202-203 |
C17H21N3O3 |
58 |
0,78 (A) |
|
•24 |
CH2OCH2C6H5 |
CH3 |
N(CH3) |
197-199 |
C18H24N4O3 |
61 |
0,47 (A) |
|
•25 |
CH2OCH2C6H5 |
CH3 |
N(C6H5) |
173-175 |
C23H26N4O3 |
54 |
0,81 (А) |
|
•26 |
CH2O(п-C6H4Cl) |
H |
Связь |
211-213 |
C15H16ClN3O3 |
54 |
0,68 (D) |
|
•27 |
CH2(п-C6H4OC6H5) |
H |
Связь |
192-194 |
C21H21N3O3 |
55 |
0,56 (D) |
|
•28 |
CH2O(CH2)2OC2H5 |
CH3 |
Связь |
174-175 |
C14H23N3O4 |
58 |
0,72 (A) |
|
•29 |
CH2C6H4O(CH2)2OC6H5 |
H |
Связь |
146-148 |
C23H25N3O4 |
63 |
0,74 (A) |
где X = ординарная связь, NH, NCH3, NC6H5; R1 = H, CH3; R2 = CH2OCH3, CH2OC2H5, CH2OCH(CH3)2, CH2OC2H4Cl, CH2OCH2C6H5, CH2O(п-C6H4Cl), CH2OCH2CH2OC2H5, CH2C(O)C6H5.
Выход и физико-химические характеристики полученных веществ представлены в таблице.
Исследование психотропных свойств синтезированных соединений осуществлялось с использованием традиционных моделей фармакологического скрининга in vivo - теста «открытое поле», приподнятого «плюс»-лабиринта, теста форсированного плавания, выработки условной реакции пассивного избегания и определения порога болевой чувствительности при электрораздражении переменным током. Опыты были выполнены на белых беспородных крысах обоего пола массой 180 - 250 г. Исследуемые вещества в физиологическом растворе (опытным группам) или физиологический раствор (контрольным группам) вводили внутрибрюшинно за 1 ч до начала тестирования в дозах 10 и 50 мг/кг.
На основании данных фармакологического скрининга новых производных 5-аминоурацила наиболее сбалансированный спектр психотропной активности был выявлен у соединения 18. Это соединение в обеих исследованных дозах проявило антидепрессивную активность, которая не сопровождалась влиянием на поведение животных в тесте «открытого поля», что свидетельствует о наличии у него специфической антидепрессивной, а не общей психостимулирующей активности. Кроме того, указанное вещество не оказывало анксиогенного действия и не понижало порог болевой чувствительности животных. Соединения 11, 20 и 24 также проявили антидепрессивную активность в дозах 50 мг/кг, однако в этой же дозе у них был выявлен и психоседативный эффект, а соединение 20 снижало порог болевой чувствительности. На основании этого можно сделать вывод о том, что соединение 18 - 1-бензоилметил-5-(N-пирролидино)урацил обладает отчетливыми антидепрессантными свойствами и может служить основой для дальнейшей направленной модификации с целью усиления выявленных психофармакологических эффектов.
СПИСОК ЛИТЕРАТУРЫ:
- 1. Boer D., Bosman I.J., Hidvegi E. // Forensic Sci. Int. - 2001. - Vol. 121. - No. 1-2. - P. 47-56.
- 2. Eguchi J., Inomata Y., Yuasa T. // Arzneimittelforschung. - 1997. - Bd. 47. - No. 12. - S. 1337-1347.
- 3. Prakash C., Cui D., Baxter J.G. // Drug Metab. Dispos. - 1998. - Vol. 26. - No. 5. - P. 448-456.
- 4. Комиссаров И.В., Харин Н.А., Вошула В.Н. // Xим.-фаpм. жуpн. - 1991. - Т. 25. - Вып. 3. - С. 40-42.
- 5. Wiley J. // Organic Syntheses. - 1937. - Vol. 17. - P. 63.
- 6. Брель А.К., Новиков М.С., Озеров А.А. // В сб.: Химия и технология элементоорганических мономеров и полимерных материалов. - Волгоград, 2001. - С. 70-74.
- 7. Каркищенко Н.Н. Психоунитропизм лекарственных средств. - М.: Медицина, 1993. - 256 с.
- 8. Островская Р.У. Антидепрессанты и ноотропы. - М.: Медицина, 1982. - С. 101-113.
- 9. Поконова Ю.В. Химия и технология галогенэфиров. - Ленинград: Изд. ЛенГУ, 1982. - 272 с.
Библиографическая ссылка
Кубеков К.В., Ковалев Д.Г., Озеров А.А. СИНТЕЗ И ПСИХОФАРМАКОЛОГИЧЕСКИЙ АНАЛИЗ НОВЫХ ПРОИЗВОДНЫХ // Современные проблемы науки и образования. 2007. № 6-1. ;URL: https://science-education.ru/en/article/view?id=755 (дата обращения: 27.05.2026).



