Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
HAEMOSTATIC DISORDERS CORRECTION IN A PRYZM OF ENERGY DEFICIENCY CONCEPT
Введение
У многих пациентов, поступающих в отделения реанимации и интенсивной терапии (ОРИТ), имеются те или иные нарушения системы гемостаза. Они могут варьировать от умеренных изменений, выявляемых только с помощью лабораторных тестов, до комплексных нарушений с развернутой клинической картиной, таких как синдром диссеминированного внутрисосудистого свертывания. По данным литературы, клинические признаки коагулопатии (кровотечения) наблюдаются у 16 % пациентов, находящихся на лечении в ОРИТ, а лабораторные признаки коагулопатии – у 66 % пациентов [9]. Нарушения системы гемостаза у реанимационных больных значительно ухудшают прогноз их заболевания [13].
В настоящее время основным способом коррекции нарушений гемостаза, а именно коагулопатий, является заместительная терапия препаратами донорской крови. Концентрат протромбинового комплекса (КПК) и рекомбинантный VIIa фактор наиболее эффективны и показаны при низкой толерантности пациента к волемической нагрузке; при изолированном дефиците отдельных факторов свертывания показано применение концентратов соответствующих факторов. Рекомбинантный VIIa фактор может с успехом применяться даже при наличии ингибиторов к VIII, IX фактору и фактору Виллебранда. Однако по-прежнему наиболее востребованным препаратом, применяемым для устранения дефицита факторов свертывания, особенно множественного, связанного с патологией печени, диссеминированным внутрисосудистым свертыванием (ДВС) или действием варфарина, остается свежезамороженная плазма (СЗП) [10].
Известно, что трансфузия аллогенной крови связана с определенными рисками и неблагоприятными последствиями, наиболее значимыми из которых являются: инфекционные осложнения, аллергические реакции, иммуносупрессия и ошибочное переливание препаратов несовместимой (иногруппной) крови. Риск передачи вирусных инфекций с препаратами донорской крови за последние годы значительно снизился, и в настоящее время на первом месте среди осложнений трансфузии аллогенной крови находится острое повреждение легких (TRALI – transfusion-related acute lung injury), затем следуют гемолитические трансфузионные реакции (ГТР) и трансфузионный сепсис (ТС). TRALI – потенциально фатальное осложнение, представляющее собой иммуно-опосредованный некардиогенный отек легких, развивающийся в течение первых 6 часов после трансфузии плазмосодержащих препаратов аллогенной крови, – регистрируется примерно в одном случае на каждые 5000 трансфузий [11]. Несмотря на совершенствование методов забора, консервации и хранения остается также довольно высокой частота бактериального загрязнения препаратов донорской крови: так, частота инфицирования тромбоконцентрата – наиболее подверженного контаминации препарата крови, достигает 1,2 % [14]. Использование препаратов крови вообще отрицательным образом сказывается на летальности, заболеваемости и длительности пребывания пациентов в ОРИТ и стационаре. Имеется множество данных о повышении риска развития синдрома полиорганной недостаточности (СПОН) и острого респираторного дистресс-синдрома (ОРДС), связанного с переливанием СЗП [15]. Показано существование дозозависимой корреляции между трансфузией препаратов крови, и в первую очередь СЗП, и неблагоприятными исходами (в виде повышения смертности и частоты развития инфекции) у пациентов с кровопотерей: риск смерти повышается на 3,5 % на каждую перелитую дозу СЗП [8]. Наконец, всегда существует вероятность ошибки и переливания реципиенту иногруппной несовместимой крови; частота подобных ошибок достигает 1/33000 [12].
В тех клинических ситуациях, которые требуют скорейшей коррекции нарушений системы гемостаза (травма, геморрагический шок, продолжающееся кровотечение), применение аллогенных препаратов крови, несомненно, оправдано; однако, при отсутствии угрожающего жизни кровотечения следует более тщательно подходить к оценке возможных рисков и ожидаемой выгоды от их использования, ведь наиболее эффективным способом профилактики всех трансфузионных осложнений является исключение ненужных (не необходимых) трансфузий. В таких случаях необходимо искать иные пути коррекции нарушений гемостаза.
Ключевым патогенетическим звеном любого критического состояния в настоящее время считается дизрегуляция аэробного энергетического обмена, сопровождающаяся качественно однотипными метаболическими и структурными изменениям во всех органах, следствием которых является развитие системного энергодефицита. Понятие энергодефицита (энергетической недостаточности) включает несоответствие между потребностью организма (органа, ткани, клетки) в энергии и тем ограниченным количеством макроэргов (аденозинтрифосфата – АТФ), которое может в данный момент использоваться для поддержания его структурной целостности и функциональной активности. Известно, что способность любой клетки выполнять специфические для нее энергозависимые функции зависит от содержания в ней АТФ: уменьшение его концентрации всего на 15–20 % приводит к снижении интенсивности всех энергозависимых процессов в клетке на 75–80 %. На организменном уровне это приводит к нарушениям деятельности ЦНС, работы сердца, синтетических процессов в печени, почках и т.д. Энергодефицит может возникать вследствие отставания скорости ресинтеза АТФ от возрастания интенсивности общего метаболизма (гиперметаболический энергодефицит), несоответствия доставки кислорода его потреблению (гипоксический энергодефицит), ингибировании клеточных ферментов (ферментативный энергодефицит), недостаточного количества субстратов окисления в клетке (субстратный энергодефицит) [3]. Системный энергодефицит – исход практически любого патологического процесса, дошедшего до критического уровня, когда возникает полиорганная недостаточность, обусловленная истощением энергетических ресурсов клеток и предельной формой тканевой гипоксии.
Система гемостаза, отображающая тонко сбалансированный механизм регуляции функционального состояния организма в целом, неизбежно вовлекается в ответ на патологическое состояние, инициирующее развитие органной или, тем более, полиорганной недостаточности [1], именно поэтому практически у всех пациентов, находящихся в отделениях реанимации и интенсивной терапии, имеются в разной степени выраженные нарушения гемостаза. Эффективность функционирования системы гемостаза по предотвращению кровопотери, нарушений кровотока и восстановлению поврежденных сосудов и тканей определяется состоянием энергетического обмена организма: скорость образования и потребления различных компонентов системы гемостаза зависит от уровня метаболизма тканей [2]. Объемы гемостаз-корригирующей и заместительной терапии, необходимой пациентам со сходными по этиологии и степени выраженности гемостазиологическими нарушениями, варьируют в широких пределах. Определение взаимосвязи между энергетическим статусом организма и функциональным состоянием системы гемостаза представляет возможности для повышения эффективности коррекции нарушений системы гемостаза, уменьшения количества осложнений и стоимости лечения.
Цель исследования:
провести сравнение стандартного подхода к коррекции нарушений системы гемостаза с широким использованием препаратов донорской крови и патогенетически обоснованного воздействия на систему гемостаза с позиций энергодефицитных состояний у пациентов с различными типами энергодефицита.
Материал и методы
Исследование включало 156 пациентов отделения реанимации и интенсивной терапии как хирургического, так и терапевтического профиля, у которых при поступлении в ОРИТ
диагностировался один из типов энергодефицита. Критериями исключения из исследования были наличие у пациентов смешанной формы энергодефицита или его отсутствие. Дифференциальная диагностика энергодефицита проводилась на основании анализа биохимических показателей кислородного и кислотно-основного гомеостаза: доставки (Do2), потребления (Vo2) и коэффициента утилизации кислорода (КУо2), сатурации кислорода смешанной венозной крови (SpVo2), концентрации лактата и глюкозы сыворотки и данных нутриционного статуса: фактического расхода энергии (ФРЭ) и количества доставленных калорий (ДК) (рис. 1) [4]. Параметры доставки, потребления и утилизации кислорода рассчитывались по следующим формулам:
(1) Dо2 = СИ ´ Сaо2 = СИ ´ (1,3 ´ Hb ´ Saо2);
(2) Vo2 = СИ ´ (Сaо2 - Cvо2) = СИ ´ (1,3 ´ Нb) ´ (Saо2 - Svо2);
(3) КУо2 = Vo2/Dо2;
где СИ – сердечный индекс, л/(мин´м2); Hb – уровень гемоглобина, г/л; Saо2 – сатурация кислорода артериальной крови; Svо2 – сатурация кислорода смешанной венозной крови. Параметры гемодинамики рассчитывались с использованием модифицированной формулы Старра [5].
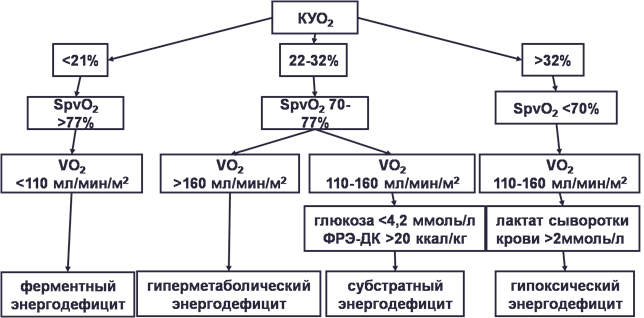
Рисунок 1. Алгоритм диагностики энергодефицита [4]
Примечания: КУО2 – коэффициент утилизации кислорода, VO2 – потребление кислорода, SрvO2 – сатурация крови смешанной венозной крови, ФРЭ – фактические расходы энергии, ДК – доставленные калории.
В зависимости от типа энергодефицита все пациенты были разделены на 4 группы, в каждой из которых было выделено 2 подгруппы: контрольная ретроспективная и проспективная группа сравнения – группа оптимизированной интенсивной терапии. Пациенты в составе каждой из групп статистически значимо не различались по возрасту и по тяжести состояния на момент госпитализации в ОРИТ; исходные баллы по шкале APACHE III были несколько выше в группе ферментного энергодефицита, как наиболее тяжелого (таблица 1).
Таблица 1
Общая характеристика пациентов в исследуемых группах (Ме (25-75 персентили))
|
|
1 группа |
2 группа |
3 группа |
4 группа |
||||
|
1р |
1с |
2р |
2с |
3р |
3с |
4р |
4с |
|
|
Тип энергодефицита |
||||||||
|
Гипер-метаболический |
Гипоксический |
Ферментный |
Субстратный |
|||||
|
n |
20 |
22 |
23 |
23 |
18 |
17 |
17 |
16 |
|
APACHE III, баллы |
45,4 (25,3-82,4) |
48,5 (25,5-88,2) |
48,3 (41,7-78,4) |
52,5 (42,3-73,5) |
56,4 (22,6-85) |
58,2 (25,2-82,4) |
45,1 (21,5-59,5) |
44,2 (23-56,7) |
|
Возраст, лет |
56 (30-82) |
52 (32-84) |
54 (35-72) |
52 (34-70) |
59 (32-72) |
60 (35-74) |
55 (44-72) |
54 (40-71) |
Стандартный комплекс интенсивной терапии при данной патологии, который получали пациенты ретроспективных подгрупп, включал:
1) инфузионно-трансфузионную терапию, которая подбиралась индивидуально исходя из состояния больного с широким применением препаратов аллогенной крови;
2) антибактериальную терапию (вначале эмпирически, затем – по данным бактериальных посевов сред организма);
3) антитромботическую терапию – по показаниям;
4) антисекреторную терапию на фоне установленного назогастрального зонда и дренирования желудочного содержимого;
5) аналгезию – с помощью продленной эпидуральной анальгезии и/или анальгетиками опиоидного ряда;
6) энергетическую поддержку согласно стандартным рекомендациям по энтеральному и парентеральному питанию и приказу МЗ РФ№330 без учета метаболического статуса.
Алгоритм оптимизированной интенсивной терапии, которую получали пациенты проспективных подгрупп, представлен в таблице 2.
Таблица 2
Алгоритм оптимизации интенсивной терапии в зависимости от типа энергодефицита
|
Гипер-метаболический энергодефицит |
Гипоксический энергодефицит |
Ферментный энергодефицит |
Субстратный энергодефицит |
|
Гипералиментация (30-40 ккал/кг/мин)
|
Стандартная ИТ и НП для данной патологии (25 ккал/кг/сут)
|
Гипоалиментация (15-20 ккал/кг/сут)
|
Стандартная ИТ и НП для данной патологии (25 ккал/кг/сут) |
|
+ |
+ |
+ |
+ |
|
Препараты, ↓ интенсивность ОО · поликомпонент-ная н/в блокада · мульти-модальная аналгезия |
Оптимизация DO2 · Hb ≥ 100 г/л · коррекция гипоксе-мии/нарушений внешнего дыхания · коррекция гемодинамики |
Препараты, ↑ интенсивность ОО · препараты янтарной кислоты, · витамины в х2 суточной дозе, · актовегин до 4 г/сут |
· Поливитамины · витамин К в/м 60 мг/сут
|
Коррекция гиперметаболического энергодефицита включала оптимизированную нутритивную поддержку в режиме гипералиментации из расчета 30–40 ккал/кг/сут и препараты, снижающие интенсивность основного обмена: адекватное мультимодальное обезболивание, поликомпонентная нейровегетативная блокада.
Пациентам обеих подгрупп (ретроспективной и группы сравнения) с гипоксическим энергодефицитом проводилась стандартная противошоковая инфузионно-трансфузионная терапия, однако, применение препаратов донорской крови в проспективной группе – группе сравнения – было ограничено геморрагическими эпизодами. Нутритивная поддержка проводилась согласно стандартным рекомендациям по энтеральному и парентеральному питанию для пациентов с дефицитом питания (приказ МЗ РФ № 330).
Оптимизированная метаболическая коррекция ферментативного энергодефицита включала нутритивную поддержку в режиме гипоалиментации из расчета 15–20 ккал/кг/сут и препараты, повышающие интенсивность основного обмена: поливитамины в двойной суточной дозе (церневит), препараты янтарной кислоты (реамберин), актовегин до 4 г/сут; заместительной терапии препаратами аллогенной крови не проводилось.
Пациентам обеих подгрупп 4 группы (с субстратным энергодефицитом) проводилась интенсивная терапия, включавшая нутритивную поддержку на основе стандартных расчетов и рекомендаций для основной патологии; пациентам проспективной группы дополнительно назначались поливитаминные препараты и витамин К в дозе 60 мг/сут; заместительной терапии препаратами аллогенной крови не проводилось.
Ежедневно осуществлялся подсчет ФРЭ (по способу Харриса – Бенедикта) и азотистого баланса (АБ), определялся уровень общего белка, альбумина плазмы и абсолютного числа лимфоцитов (АЧЛ) и на основании полученных результатов в проспективной группе проводилась коррекция нутритивной поддержки. Диагностика энергодефицитных состояний осуществлялась на основании предложенного алгоритма (рис. 1).
Забор образцов крови для мониторинга показателей системы гемостаза осуществлялся из центральной вены. Среди гемостазиологических параметров регистрировались активированное частичное тромбопластиновое время (АЧТВ), протромбиновое время (ПТВ), уровень растворимых фибрин-мономерных комплексов (РФМК), количество тромбоцитов и степень их агрегации (на основании данных агрегатометрии). В качестве интегрального способа оценки функционального состояния системы гемостаза использовалась электрокоагулография. Для интерпретации полученных данных проводился расчет интегральных параметров: коагуляционной активности (КА) (норма – 12,0-16,2 у.е.) и фибринолитического потенциала (ФП) (норма – 0,7-1,1 у.е.) [6, 7]. На основании анализа направленности и выраженности изменений системы гемостаза делался вывод о степени компенсации системы гемостаза [6, 7]. Так, различные количественные нарушения одного или нескольких компонентов системы гемостаза, не отражающиеся на качествах формирующегося кровяного сгустка, характеризовались как компенсированная дисфункция гемостаза. Для субкомпенсированной дисфункции гемостаза были характерны различные структурные изменения образующегося сгустка, которые вели к формированию как протромботического, так и геморрагического статуса (соответственно, тромботический и геморрагический вариант субкомпенсации гемостаза). При декомпенсированной дисфункции гемостаза хронометрические и структурные нарушения формирующегося кровяного сгустка были достаточно выражены и сопровождались развитием соответствующих клинических проявлений (тромбозов/ кровотечений) [6, 7].
При статистическом анализе оценка межгрупповых отличий проводилась непараметрическим критерием Крускала – Уолиса и критерием Данна.
Результаты исследования и их обсуждение
Для больных 1 группы – группы гиперметаболического энергодефицита – на момент включения в исследование была характерна тенденция к гипергликемии – следствие активации процессов глюконеогнеза и статистически значимое повышение потребления кислорода по сравнению с пациентами других групп (р <0.05 по критерию Крускала –Уолиса), что отражает резко возросшие потребности клетки в энергии. При этом отмечалось адекватное повышение доставки кислорода за счет выраженной гипердинамии кровообращения (статистически значимое отличие СИ от других групп по критерию Крускала – Уолиса (р <0.05), в связи с чем коэффициент утилизации кислорода оставался в пределах нормальных значений (таблица 3). Со стороны показателей системы гемостаза наблюдалась высокая коагуляционнная активность, повышение уровня РФМК, тенденция к тромбоцитопении и угнетению фибринолиза. Следствием отмеченных закономерностей было формирование плотного сгустка по данным ЭлКоГ. Данное состояние системы гемостаза характеризуется как тромботический вариант субкомпенсации [6]. Нутриционный статус пациентов с гиперметаболическим энергодефицитом на момент включения в исследование характеризовался как белково-энергетическая недостаточность: низкие значения абсолютного числа лимфоцитов, уровня альбумина и общего белка плазмы, высокие потери азота и отрицательный азотный баланс.
Таблица 3
Значения параметров гемостаза, кислородного гомеостаза и нутриционного статуса у пациентов 1 группы (с гиперметаболическим энергодефицитом) при поступлении (1 сутки), на 3 и 5 сутки лечения в ОРИТ (Ме (25-75 персентили))
|
Параметр (N-нормальные значения) |
Контрольная группа, n=20 |
Группа сравнения, n=22 |
||||
|
1 сутки |
3 сутки |
5 сутки |
1 сутки |
3 сутки |
5 сутки |
|
|
УИ, мл/м2 (N=40-60) |
40 (35,6-44,3) |
51,6 (47,1-53,7) |
40,9 (38,2-43,8) |
38,5 (34,1-41,5) |
53,1 (47,8-55,2) |
42,8 (38,7-44,4) |
|
СИ, л/(мин´м2) (N=2,6-4,2) |
5,6 (5-6,2) |
5,7 (5,2-5,9) |
4,5 (4,2-4,8) |
5,4 (4,8-5,8) |
5,2 (4,8-5,5) |
3,8* (3,5-4) |
|
ОПСС, дин´с´см-5 (N=800-1600) |
908 (805-1026) |
1462 (1185-1637) |
1402 (1180-1626) |
882 (801-978) |
945* (796-1112) |
1026* (842-1205) |
|
DO2, мл/мин´м2 (N=520-720) |
841 (789-896) |
858 (794-892) |
680 (625-732) |
828 (762-873) |
796 (760-838) |
571* (529-612) |
|
VO2, мл/мин´м2 (N=110-160) |
242 (195-288) |
260 (246-279) |
189 (168-223) |
228 (183-265) |
224 (180-268) |
142* (115-163) |
|
КУО2, % (N=22-32) |
29 (26-32) |
30 (26-32) |
28 (25-33) |
28 (25-32) |
28 (23-32) |
25 (22-28) |
|
SрvO2, % |
72,1 (69-74,3) |
72,8 (71,8-74,3) |
72,6 (70,0-77,5) |
74 (71,1-77,3) |
74,4 (72,2-76,9) |
71,2 (70,2-73,4) |
|
Лактат, ммоль/л (N=0-2) |
1,8 (1,6-2,0) |
1,6 (1,3-1,9) |
1,7 (1,5-2,0) |
1,7 (1,5-2,0) |
1,4 (1,2-1,7) |
1,5 (1,2-1,8) |
|
ФРЭ-ДК, ккал/кг´сут (N=0 – 10 ) |
7,2 (6,0-8,4) |
8,2 (7,3-9) |
3,5 (2,8-4,2) |
-7,6* (-712-17) |
-2,8* (0-6) |
-1* (-2 – 0,2) |
|
АЧТВ, с (N=21-31) |
32,5 (30,2-35,1) |
31,6 (28,4-34,8) |
28,4 (25,7-32,1) |
33,2 (29,8-36,2) |
29,4 (26,2-34,7) |
25,8 (23,4-28,6) |
|
ПТВ, с (N=9-13) |
10,2 (8,8-13,9) |
11,4 (9,2-14,1) |
14,0 (11,8-17,6) |
9,7 (8,5-13,1) |
8,9 (8-11,2) |
11,3 (10,2-14,8) |
|
РФМК, мг% (N=0-4) |
11,6 (9,6-13,7) |
12 (9,2-14,6) |
8,5 (6,4-10,2) |
11,9 (9,5-14,5) |
11,4 (8,6-13,2) |
7 (4,5-9,8) |
|
Тр-ты, тыс./мкл (N=150-400) |
169 (140-220) |
165 (144-202) |
176 (151-227) |
176 (138-232) |
187 (156-235) |
192 (164-266) |
|
АДФ-индуцир. агрег. тр-тов, % (N=20-40) |
65 (44-89) |
67 (46-88) |
60 (41-78) |
67 (45-89) |
56 (38-75) |
48 (34-60) |
|
КА, у.е. (N=12-16,2) |
20,2 (17,4-22,5) |
21,7 (18,5-23,5) |
18,1 (16,4-20,6) |
19,8 (16,9-21,6) |
16,6 (14,9-19) |
15,2* (14,0-16,1) |
|
ФП, у.е. (N=0,7-1,1) |
0,8 (0,2-1,2) |
0,6 (0,3-1) |
0,6 (0,4-1) |
0,7 (0,2-1,1) |
0,9 (0,4-1,3) |
0,9* (0,6-1,2) |
|
Ао, у.е. (N=0,2-0,4) |
0,1 (0-0,2) |
0,2 (0,1-0,3) |
0,3 (0,1-0,4) |
0,1 (0-0,3) |
0,3 (0,2-0,4) |
0,3 (0,2-0,4) |
|
Общий белок, г/л (N=64-83 ) |
52,5 (50,2-56,2) |
54,6 (52,4-56,2) |
56,0 (53,5-57,8) |
51,8 (50,0-54,8) |
56,2 (54,8-58,6) |
59,2 (56,9-61,4) |
|
Альбумин, г/л (N=34-48 ) |
22,3 (20,0-23,6) |
23,0 (21,4-25,1) |
24,2 (23,1-25,4) |
22,6 (21,2-23,8) |
24,1 (23,6-26,4) |
27,2* (26,1-28,5) |
|
АЧЛ, 106/л (N>1,8 X 106/л) |
1,3 (1,24-1,34) |
1,36 (1,3-1,4) |
1,4 (1,38-1,43) |
1,3 (1,23-1,34) |
1,45 (1,3-1,54) |
1,61* (1,5-1,75) |
|
Потери азота, г/кг/сут (N=0,01-0,12 ) |
0,23 (0,22-0,25) |
0,21 (0,19-0,24) |
0,2 (0,17-0,22) |
0,24 (0,22-0,25) |
0,2 (0,19-0,22) |
0,17 (0,15-0,18) |
|
АБ, г/сут (N= - 3 - 0 ) |
-7 (-6,5- (-7,4)) |
-5,6 (-5,0- (-6,2)) |
-5,5 (-4,9- (-5,8)) |
-7,3 (-6,9- (-7,6)) |
-2,7 (-1,8- (-3,0)) |
-2,6* (-1,9- (-2,9)) |
|
Глюкоза, ммоль/л (N=4,2-6,2) |
9,0 (8,1-9,3) |
8,2 (7,2-9,6) |
7,6 (7,3-8,5) |
10,0 (9,1-10,4) |
8,5 (7,8-9,2) |
6,4* (6,0-7,2) |
* p<0,05 по критерию Данна между соответствующими показателями двух подгрупп
К 5-ым суткам лечения у пациентов подгруппы сравнения на фоне оптимизированной интенсивной терапии показатели гемодинамики и кислородного гомеостаза вернулись к нормальным значениям (статистически значимая разница по СИ и ОПСС, Do2, Vo2: p<0,05 по критерию Данна), зарегистрирована положительная динамика показателей нутриционного статуса. Одновременно с нормализацией кислородного гомеостаза к 5-ым суткам лечения в подгруппе сравнения отмечена положительная динамика показателей системы гемостаза: АЧТВ, ПТВ, уровня тромбоцитов и РФМК, КА, ФП, А0. В контрольной группе также отмечена менее выраженная положительная динамика регистрируемых параметров (таблица 3).
У больных с гипоксическим энергодефицитом (группа 2) отмечались низкая венозная сатурация, высокий коэффициент утилизации кислорода, что являлось следствием нарушения поступления кислорода в ткани и несоответствия доставки потреблению кислорода. Параметр СИ у пациентов с гипоксическим энергодефицитом статистически значимо не отличался от соответствующего показателей других групп, однако, варьировал в более широких пределах, что, вероятно, отражает гетерогенность патогенеза гипоксического энергодефицита (артериально-гипоксемическая, гемическая, гемодинамическая гипоксия и гипоксия периферического шунтирования). Наличие подобного энергодефицитного состояния было ассоциировано с тенденцией к гипокоагуляции вследствие дефицита факторов свертывания (потребление), повышением уровня РФМК, активацией фибринолиза и тромбоцитопенией. Все отмеченное привело к формированию рыхлого сгустка по данным ЭлКоГ, что характерно для геморрагического варианта субкомпенсации системы гемостаза [6].
К 5-ым суткам лечения у пациентов обеих подгрупп на фоне коррекции и нормализации показателей доставки/потребления кислорода отмечено улучшение показателей нутриционного статуса и системы гемостаза. В контрольной группе на фоне более широкого применения СЗП динамика изменений показателей системы гемостаза была более выраженной (таблица 4).
Таблица 4
Значения параметров гемостаза, кислородного гомеостаза и нутриционного статуса у пациентов 2 группы (с гипоксическим энергодефицитом) при поступлении (1 сутки), на 3 и 5 сутки лечения в ОРИТ (Ме (25–75 персентили))
|
Параметр (N-нормальные значения) |
Контрольная группа, n=23 |
Группа сравнения, n=23 |
||||
|
1 сутки |
3 сутки |
5 сутки |
1 сутки |
3 сутки |
5 сутки |
|
|
УИ, мл/м2 (N=40-60) |
34,2 (31,9-36,7) |
44 (41,2-47,4) |
38,9 (36,5-43) |
34,5 (32,1-37) |
43,2 (40-46,3) |
44,1 (42-46,3) |
|
СИ, л/(мин´м2) (N=2,6-4,2) |
3,3 (1,6-5,0) |
4,2 (3,2-5,3) |
3,6 (2,7-4,5) |
3,4 (1,7-5,1) |
4,1 (3-5,2) |
4 (2,9-5,2) |
|
ОПСС, дин´с´см-5 (N=800-1600) |
1531 (1390-1695) |
1300 (992-1558) |
1213 (901-1482) |
1662 (1496-1814) |
1403 (1109-1689) |
1242 (893-1560) |
|
DO2, мл/мин´м2 (N=520-720) |
395 (290-493) |
572 (464-689) |
486 (362-670) |
392 (308-470) |
562 (436-752) |
576 (454-705) |
|
VO2, мл/мин´м2 (N=110-160) |
141 (115-162) |
150 (134-168) |
142 (119-178) |
139 (119-156) |
152 (138-176) |
145 (123-170) |
|
КУО2, % (N=22-32) |
36 (33,1-40) |
26,5 (24-28,7) |
29,2 (26,5-32,8) |
35,1 (32,9-38,6) |
27,2 (23,2-32) |
28 (24,8-31,1) |
|
SрvO2, % |
60,5 (52-70,3) |
70 (65,4-74,8) |
74 (70-77,6) |
62,5 (54-71,1) |
69,5 (66-74,5) |
72,2 (68,9-76,4) |
|
Лактат, ммоль/л (N=0-2) |
2,1 (2-2,5) |
1,8 (1,3-2,1) |
1 (0,5-1,8) |
2,3 (1,9-2,6) |
1,6 (1,1-2,2) |
0,8 (0,6-2,0) |
|
ФРЭ-ДК, ккал/кг´сут (N=0 – 10 ) |
2,8 (1,2-4,3) |
4,1 (1,8-6,7) |
2,1 (-1 – 3,4) |
3,2 (1-5,4) |
3,6 (1,2 – 6) |
1,8 (-1 – 4,5) |
|
АЧТВ, с (N=21-31) |
42,1 (36,3-48,7) |
32,5 (29,6-36,8) |
32 (28,9-35,4) |
40,5 (34,8-46,2) |
36,7 (34,2-39) |
33,4 (28-37,9) |
|
ПТВ, с (N=9-13) |
19,4 (17,1-24) |
15,2 (11-17,8) |
12,7 (9-15,4) |
20,1 (16,7-25,2) |
18,5 (16,3-21) |
15 (12,2-17,9) |
|
РФМК, мг% (N=0-4) |
16,7 (12,4-22) |
10 (6-15,6) |
10 (5,2-15,4) |
15,3 (11,9-19,9) |
14 (9-18,5) |
9,6 (5-16,1) |
|
Тр-ты, тыс./мкл (N=150-400) |
137 (108-166) |
158 (122-186) |
166 (124-205) |
125 (98-155) |
152 (112-201) |
178 (140-214) |
|
АДФ-индуцир. агрег. тр-тов, % (N=20-40) |
16 (13-19) |
21 (18-23) |
25 (20-29) |
14 (12-17) |
22 (19-25) |
24 (20-28) |
|
КА, у.е. (N=12-16,2) |
11 (7,9-15,6) |
14,4 (12,3-16,5) |
15,6 (14-17,2) |
10,5 (7-13,8) |
11,2 (9,5-13,6) |
14,7 (12-16,9) |
|
ФП, у.е. (N=0,7-1,1) |
1,5 (0,9-2,2) |
1,1 (0,7-1,7) |
0,8 (0,5-1,4) |
1,6 (1-2,3) |
1,5 (1,1-1,9) |
0,9 (0,7-1,2) |
|
Ао, у.е. (N=0,2-0,4) |
0,7 (0,4-1) |
0,4 (0,2-0,7) |
0,3 (0,2-0,5) |
0,8 (0,4-1,2) |
0,6 (0,2-1) |
0,5 (0,2-0,8) |
|
Общий белок, г/л (N=64-83 ) |
52 (51-54) |
54 (51-57) |
58 (53-62) |
52 (50-55) |
53 (52-55) |
55 (53-58) |
|
Альбумин, г/л (N=34-48 ) |
22,4 (21-23,7) |
27,7 (25,2-30,5) |
28,3 (26,1-31,5) |
22 (21-24,6) |
23,6 (22-26,1) |
23,9 (22,5-26,5) |
|
АЧЛ, 106/л (N>1,8 X 106/л) |
1,4 (1,32-1,44) |
1,5 (1,42-1,62) |
1,58 (1,52-1,63) |
1,42 (1,31-1,44) |
1,52 (1,46-1,6) |
1,7 (1,62-1,76) |
|
Потери азота, г/кг/сут (N=0,01-0,12 ) |
0,22 (0,17-0,25) |
0,19 (0,16-0,21) |
0,16 (0,14-0,17) |
0,23 (0,21-0,24) |
0,18 (0,14-0,2) |
0,15 (0,13-0),17 |
|
АБ, г/сут (N= - 3 - 0 ) |
-6,4 (-5,6- (-7,5)) |
-5,2 (-4,8- (-5,7)) |
-3,7 (-3- (-4,5)) |
-6,2 (-4,9- (-7,6)) |
-5,5 (-4,3- (-6,2)) |
-4,1 (-3,2- (-4,9)) |
|
Глюкоза, ммоль/л (N=4,2-6,2) |
6,3 (5,8-7) |
7,2 (6,5-8) |
6,9 (6,5-7,4) |
6,9 (6,2-7,6) |
8 (6,4-9,3) |
7,2 (6-8,1) |
* p<0,05 по критерию Данна между соответствующими показателями двух подгрупп.
Для больных с ферментативным энергодефицитом (группа 3) были характерны: низкие значения потребления кислорода, высокая венозная сатурация кислорода (снижение артерио-венозной разницы содержания кислорода), тенденция к гиподинамии кровообращения (показатель СИ был наиболее низким среди всех групп, по сравнению с группами гиперметаболического и гипоксического энергодефицита отличие было статистически значимым (р <0.05 по критерию Крускала – Уолиса)). Данное состояние вызвано снижением активности ферментных систем (в том числе ферментов дыхательной цепи митохондрий) клетки, участвующих в процессах окисления и фосфорилирования, что ведет к угнетению метаболизма и развитию ферментативного энергодефицита. Изменения параметров гемостаза носили ярко выраженный характер: выраженная гипокоагуляция и тромбоцитопения со снижением агрегационной активности тромбоцитов, активацией системы гемостаза (самое значительное среди групп статистически значимое повышение уровня РФМК (р <0.05 по критерию Крускала – Уолиса)) и угнетением фибринолиза. Вследствие этого по данным ЭлКоГ формировался гемостатически неполноценный рыхлый сгусток, что соответствует декомпенсированному состояния системы гемостаза [6].
К 5-ым суткам у пациентов подгруппы сравнения на фоне оптимизированной интенсивной терапии показатели кислородного гомеостаза вернулись к нормальным значениям, следовательно, ферментный энергодефицит был купирован; в контрольной группе существенной динамики показателей кислородного гомеостаза не наблюдалось. Одновременно с нормализацией кислородного гомеостаза к 5-ым суткам лечения в группе сравнения отмечена положительная динамика показателей системы гемостаза: АЧТВ, ПТВ, уровня тромбоцитов и РФМК. В контрольной подгруппе на фоне применения СЗП положительная динамика изменения показателей системы гемостаза имела более быстрый, однако, преходящий характер и не сопровождалась улучшением состояния показателей энергетического обмена (таблица 5).
Таблица 5
Значения параметров гемостаза, кислородного гомеостаза и нутриционного статуса у пациентов 3 группы (с ферментативным энергодефицитом) при поступлении (1 сутки), на 3 и 5 сутки лечения в ОРИТ (Ме (25–75 персентили))
|
Параметр (N-нормальные значения) |
Контрольная группа, n=18 |
Группа сравнения, n=17 |
||||
|
1 сутки |
3 сутки |
5 сутки |
1 сутки |
3 сутки |
5 сутки |
|
|
УИ, мл/м2 (N=40-60) |
38,7 (35,6-41) |
37,6 (35,2-38,9) |
37,7 (34,6-40,9) |
37,8 (34,6-40) |
37,2 (34,5-40,4) |
41,4 (39,2-43,7) |
|
СИ, л/(мин´м2) (N=2,6-4,2) |
2,4 (2-2,7) |
2,7 (2,2-3,3) |
2,5 (2,2-3,1) |
2,3 (2-2,5) |
2,9 (2,5-3,4) |
3,7* (3,2-4,2) |
|
ОПСС, дин´с´см-5 (N=800-1600) |
1132 (988-1312) |
1116 (960-1270) |
1099 (942-1264) |
1132 (988-1312) |
1150 (962-1320) |
1073 (980-1168) |
|
DO2, мл/мин´м2 (N=520-720) |
527 (498-548) |
525 (489-559) |
528 (493-526) |
514 (479-553) |
524 (501-547) |
574* (560-599) |
|
VO2, мл/мин´м2 (N=110-160) |
99 (91-106) |
95 (86-107) |
92 (84-115) |
95 (86-104) |
111 (102-122) |
128* (117-149) |
|
КУО2, % (N=22-32) |
18 (16-20) |
19 (17-23) |
17 (16-20) |
19 (17-21) |
22 (19-24) |
24* (22-26) |
|
SрvO2, % |
86,5 (80,4-92,2) |
84,2 (81,9-88,1) |
82,6 (78,5-87,8) |
85,3 (79,5-95,1) |
79,4 (76,9-84,2) |
75,2* (73,2-78,1) |
|
Лактат, ммоль/л (N=0-2) |
1,2 (0,8-1,5) |
1,4 (0,9-2) |
1,3 (0,9-1,8) |
1,4 (0,8-1,9) |
1,2 (0,7-1,6) |
1,1 (0,7-1,6) |
|
ФРЭ-ДК, ккал/кг´сут (N=0 – 10 ) |
2,9 (1,4-4,6) |
4 (1,5-6,6) |
2,5 (1,1-3,8) |
14,6* (17,1-12,2) |
12,5* (8-14,9) |
5,4 (2-8,7) |
|
АЧТВ, с (N=21-31) |
38,1 (36,9-42,6) |
33,2 (29,4-35,2) |
34,8 (31,5-37,1) |
40,0 (36,9-42,5) |
32,6 (30,1-36,4) |
24,1* (20,9-27,8) |
|
ПТВ, с (N=9-13) |
25,2 (16,3-29,0) |
18,4 (15,2-25,9) |
21,7 (16,8-27,6) |
27,2 (15,5-31,2) |
22,4 (14,2-26,9) |
13,7* (11,4-16,1) |
|
РФМК, мг% (N=0-4) |
22 (12-28) |
18 (12-24) |
22 (12-28) |
24 (14-28) |
15 (10-20) |
8* (4-12) |
|
Тр-ты, тыс./мкл (N=150-400) |
98 (84-120) |
112 (109-152) |
129 (101-177) |
108 (91-142) |
135 (116-187) |
162 (114-210) |
|
АДФ-индуцир. агрег. тр-тов, % (N=20-40) |
13 (7-18) |
16 (12-20) |
18 (14-21) |
15 (9-20) |
21 (16-25) |
28* (23-35) |
|
КА, у.е. (N=12-16,2) |
9,2 (6,1-12,2) |
14,1 (12-16,1) |
12,3 (11,6-13,1) |
9,5 (6,8-12,9) |
11,1 (9,2-13,1) |
12,9 (11-14,7) |
|
ФП, у.е. (N=0,7-1,1) |
0,4 (0-0,8) |
0,6 (0,2-0,9) |
0,6 (0,3-0,8) |
0,4 (0-0,8) |
0,6 (0,3-0,9) |
0,9 (0,6-1,1) |
|
Ао, у.е. (N=0,2-0,4) |
0,5 (0,3-0,9) |
0,3 (0,1-0,5) |
0,3 (0,1-0,5) |
0,7 (0,4-1,1) |
0,5 (0,3-0,7) |
0,3 (0,2-0,5) |
|
Общий белок, г/л (N=64-83 ) |
45,2 (40,0-51,3) |
45,6 (42,5-49,1) |
44,2 (42,3-48,6) |
44,4 (41,8-49,6) |
47,2 (43,6-52,1) |
46,5 (43,2-52,6) |
|
Альбумин, г/л (N=34-48 ) |
20,0 (16,3-25,5) |
29,0 (26,5-31,3) |
28,6 (26,2-30,4) |
21,2 (17,0-25,2) |
24,5 (22,1-27,6) |
27,5 (25,2-30,4) |
|
АЧЛ, 106/л (N>1,8 X 106/л) |
1,2 (1,0-1,5) |
1,2 (1,0-1,5) |
1,2 (1,0-1,4) |
1,3 (1,1-1,4) |
1,5 (1,3-1,8) |
1,6* (1,5-2,0) |
|
Потери азота, г/кг/сут (N=0,01-0,12 ) |
13 (11-15) |
11 (7-16) |
12 (10-15) |
12 (10-15) |
10 (7-12) |
10 (8-11) |
|
АБ, г/сут (N= - 3 - 0 ) |
-6 (-6,2-(-5,4)) |
-5,5 (-6-(-4,9)) |
-4,8 (-5-(-4,2)) |
-6,2 (-6,6-(-5,6)) |
-4,1 (-4,8-(-3,6)) |
-2,9* (-3,2-(-2,4)) |
|
Глюкоза, ммоль/л (N=4,2-6,2) |
8,2 (6,9-9,8) |
10,1 (8,7-11,6) |
11 (8,9-13) |
7,8 (6,2-9,5) |
7* (5,5-8,6) |
6,4* (5,6-7,8) |
* p<0,05 по критерию Данна между соответствующими показателями двух подгрупп.
У больных с субстратным энергодефицитом (4 группа) была выявлена гипогликемия (р <0.05 по критерию Крускала – Уолиса) на фоне сниженного количества доставленных калорий, которые существенно не соответствовали расчетной энергопотребности (р <0.05 по критерию Крускала – Уолиса). Все пациенты находились на энтеральном питании, а инфузии растворов, содержащих инсулин, не проводилось. Изменения параметров гемодинамики и показателей кислородного гомеостаза по своей направленности не отличались от таковых в группе ферментативного энергодефицита (тенденция к гиподинамии кровообращения, умеренное снижение потребления и коэффициента утилизации кислорода), но были менее выражены (однако разница с группой ферментативного энергодефицита не была статистически значимой). Для больных этой группы было характерно развитие гипокоагуляции с преимущественным поражением внешнего пути свертывания (регистрировалось значительное удлинение протромбинового времени на фоне нормальных или умеренно повышенных значений АЧТВ), что, вероятно, в немалой мере отражает дефицит витамина К. Следствием этих закономерностей явилось формирование рыхлого сгустка на фоне тенденции к гипокоагуляции и угнетению фибринолиза по данным электрокоагулографии.
Уже к 3-им суткам лечения в обеих подгруппах на фоне адекватной нутритивной поддержки отмечалась нормализация показателей углеводного обмена, в результате чего пациенты перестали удовлетворять биохимическим диагностическим критериям субстратного энергодефицита; на 5-ые сутки нормализовались показатели нутриционного статуса: концентрация альбумина и общего белка, АЧЛ, на фоне терапии основного заболевания снизились потери азота. К 5 суткам лечения в обеих подгруппах нормализовались показатели АЧТВ и ПТВ (таблица 6). Эффективность терапии, направленной на повышение интенсивности метаболизма у пациентов группы сравнения, может свидетельствовать о наличии у пациентов с субстратным энергодефицитом латентного ферментативного гипоэргоза.
Таблица 6
Значения параметров гемостаза, кислородного гомеостаза и нутриционного статуса у пациентов 4 группы (с субстратным энергодефицитом) при поступлении (1 сутки), на 3 и 5 сутки лечения в ОРИТ (Ме (25–75 персентили))
|
Параметр (N-нормальные значения) |
Контрольная группа, n=17 |
Группа сравнения, n=16 |
||||
|
1 сутки |
3 сутки |
5 сутки |
1 сутки |
3 сутки |
5 сутки |
|
|
УИ, мл/м2 (N=40-60) |
38 (35,9-41,2) |
38,5 (37,2-39,9) |
40,4 (38,8-42,7) |
40 (37,5-42,2) |
39,6 (38,6-41,7) |
42,5 (40-44,9) |
|
СИ, л/(мин´м2) (N=2,6-4,2) |
2,5 (2,1-2,8) |
2,8 (2,5-3,2) |
3 (2,5-3,6) |
2,3 (2-2,6) |
2,9 (2,6-3,3) |
3,2 (2,7-3,6) |
|
ОПСС, дин´с´см-5 (N=800-1600) |
1200 (925-1481) |
1126 (1005-1242) |
1339 (1194-1504) |
1184 (915-1448) |
1381 (1260-1498) |
1263 (1065-1474) |
|
DO2, мл/мин´м2 (N=520-720) |
500 (472-532) |
532 (505-563) |
525 (485-562) |
518 (485-548) |
572 (547-602) |
570 (556-587) |
|
VO2, мл/мин´м2 (N=110-160) |
128 (119-134) |
132 (115-152) |
152 (134-169) |
131 (122-140) |
146 (128-167) |
160 (138-182) |
|
КУО2, % (N=22-32) |
26 (24-28) |
25 (22-28) |
29 (27-32) |
25 (23-27) |
25 (23-29) |
28 (26-31) |
|
SрvO2, % |
73,8 (71,7-76,0) |
72,8 (69,6-74,9) |
71,8 (70,2-74,3) |
74,6 (72-77,2) |
71 (68,1-74) |
70,5 (68,9-72,2) |
|
Лактат, оль/л (N=0-2) |
0,8 (0,4-1,3) |
1,6 (1,1-2,1) |
1,5 (0,9-2) |
0,6 (0,3-0,9) |
1,8 (0,5-2,2) |
1,2 (0,7-1,8) |
|
ФРЭ-ДК, ккал/кг´сут (N=0 – 10 ) |
22 (15-23) |
4 (0-10) |
4 (-2-10) |
23 (18-24) |
5 (1-9) |
4 (-1-9) |
|
АЧТВ, с (N=21-31) |
31 (27,5-37,6) |
27,4 (24,3-30,1) |
24,2* (22,3-28,0) |
32 (26,5-35,4) |
24,6 (22,1-32,3) |
22,0* (19,8-25,6) |
|
ПТВ, с (N=9-13) |
26,5 (19,4-29,8) |
19,4 (15,8-24,6) |
13,0* (10,4-16,2) |
22,8 (17,1-25,3) |
14,9 (10,7-18,2) |
12,2* (11,4-14,6) |
|
РФМК, мг% (N=0-4) |
10 (5-12) |
9 (4-15) |
5 (4-10) |
9 (4-13) |
5 (2-8) |
8 (4-11) |
|
Тр-ты, тыс./мкл (N=150-400) |
152 (112-205) |
148 (119-212) |
153 (124-167) |
144 (118-205) |
159 (126-187) |
175 (114-250) |
|
АДФ-индуцир. агрег. тр-тов, % (N=20-40) |
20 (18-24) |
22 (18-26) |
24 (20-29) |
21 (17-25) |
22 (16-28) |
23 (20-25) |
|
КА, у.е. (N=12-16,2) |
10,4 (8,1-12,5) |
14,1 (12,2-16) |
13,2 (11,9-14,5) |
11,2 (8,7-13,5) |
12,3 (11,2-13,5) |
12,9 (12-13,7) |
|
ФП, у.е. (N=0,7-1,1) |
0,6 (0,5-0,7) |
1 (0,9-1,1) |
0,9 (0,7-1,1) |
0,5 (0,3-0,8) |
0,6 (0,3-0,9) |
1 (0,8-1,1) |
|
Ао, у.е. (N=0,2-0,4) |
0,6 (0,4-0,9) |
0,2 (0,1-0,4) |
0,3 (0,2-0,5) |
0,6 (0,4-1) |
0,5 (0,3-0,7) |
0,3 (0,1-0,6) |
|
Общий белок, г/л (N=64-83 ) |
55,1 (46,0-58,2) |
62,6 (60,4-65,1) |
64,2 (59,8-66,7) |
53,0 (45,8-60,1) |
56,2 (46,7-61,8) |
59,2 (48,0-61,4) |
|
Альбумин, г/л (N=34-48 ) |
24,0 (22,3-28,6) |
32,2 (30,5-37,4) |
36,7 (33,1-39,2) |
22,1 (20,5-24,1) |
25,5 (23,1-27,4) |
29,8 (26,2-33,4) |
|
АЧЛ, 106/л (N>1,8 X 106/л) |
1,3 (1,2-1,5) |
1,6 (1,3-2,1) |
2,1 (1,8-3,0) |
1,2 (1,1-1,5) |
1,4 (1,2-1,8) |
2,4 (2,0-3,0) |
|
Потери азота, г/кг/сут (N=0,01-0,12 ) |
0,16 (0,13-0,2) |
0,11 (0,08-0,13) |
0,1 (0,08-0,13) |
0,15 (0,13-0,23) |
0,09 (0,06-0,13) |
0,11 (0,09-0,13) |
|
АБ, г/сут (N= - 3 – 0 ) |
-6,4 (-7-(-5,1)) |
-2,3* (-3,1-(-1,6)) |
-1,4* (-2,5-(0,2)) |
-6,9 (-7,6-(-6,1)) |
-2,1* (-2,9-(-1,5)) |
-1,2* (-2,2-0) |
|
Глюкоза, оль/л (N=4,2-6,2) |
3,6 (3,2-4,2) |
5,0 (4,2-6,2) |
6,6 (5,2-7,8) |
3,2 (2,8-4,0) |
5,5 (4,8-6,4) |
7,0 (5,8-8,8) |
* p<0,05 по критерию Данна по сравнению с 1 сутками лечения в каждой из подгрупп.
В таблице 7 представлены обобщенные данные по расходу СЗП в подгруппах за первые 5 суток лечения и по длительности пребывания в ОРИТ.
Таблица 7
Расход СЗП за первые 5 суток и сроки госпитализации в ОРИТ (Ме (25–75 персентили))
|
Тип ЭД |
Гипермета-болический |
Гипоксический |
Ферментный |
Субстратный |
||||
|
|
к |
с |
к |
с |
к |
с |
к |
с |
|
СЗП, мл/кг |
0 |
0 |
21 (15-29) |
4*1 |
39 (30-48) |
13* (9-16) |
43 (35-65) |
0* |
|
Сутки в ОРИТ |
13 (9-16) |
9* (6-15) |
10 (6-14) |
11 (7-16) |
19 (14-23) |
14 (12-17) |
7 (5-10) |
8 (6-10) |
* p<0,05 по критерию Крускала – Уолиса между подгруппами.
Выводы
Стандартная нутриционная поддержка, рассчитанная по 330 приказу МЗ РФ, оказалась эффективной при субстратном энергодефиците: уже к 5-ым суткам лечения основные показатели нутриционного статуса вернулись к нормальным значениям; нормализовались также и показатели АЧТВ и ПТВ, в том числе и в подгруппе сравнения, пациенты которой не получали СЗП; результаты лечения на 5-ые сутки в обеих подгруппах 2 группы достоверно не различались, однако, стоимость лечения во второй подгруппе была очевидно ниже. При гипоксическом энергодефиците стандартная нутриционная поддержка эффективна при условии своевременной коррекции гипоксии, применение СЗП для коррекции ассоциированных нарушений гемостаза следует ограничить случаями активного кровотечения. При ферментном и гиперметаболическом энергодефиците стандартная нутриционная и интенсивная терапия оказалась не адекватной, при этом коррекция нарушений системы гемостаза при ферментом энергодефиците надежна лишь на фоне коррекции энергетического статуса организма. Индивидуализация интенсивной терапии у пациентов с гиперметаболическим энергодефицитом позволяет снизить степень нутриционной недостаточности и нарушений системы гемостаза к 5 суткам лечения.
Таким образом, оптимизация нутриционной поддержки с учетом состояния аэробного метаболизма организма позволяет в более сжатые сроки достигать положительных результатов. Нормализация параметров гемостаза на фоне коррекции энергодефицита в группах сравнения косвенно свидетельствует о наличии взаимосвязи между уровнем энергообеспечения организма и функциональным состоянием системы гемостаза. Применение СЗП для коррекции ассоциированных нарушений гемостаза не является необходимым, за исключением случаев активного кровотечения.
Полученные данные свидетельствуют о целесообразности более аргументированного применения СЗП при коррекции нарушений гемостаза, ассоциируемых с различными вариантами гипоэргоза, и позволяют рекомендовать патогенетически обоснованную терапию энергетического статуса организма в качестве эффективного и экономически выгодного способа коррекции нарушений системы гемостаза у пациентов с энергодефицитом.
Рецензенты:Заболотских Игорь Борисович, доктор медицинских наук, профессор, заведующий кафедрой анестезиологии, реаниматологии и трансфузиологии ФПК и ППС ГБОУ ВПО КубГМУ Минздравсоцразвития России, г. Краснодар.
Голубцов Владислав Викторович, доктор медицинских наук, профессор кафедры анестезиологии, реаниматологии и трансфузиологии ФПК и ППС ГБОУ ВПО КубГМУ Минздравсоцразвития России, руководитель центра трансфузиологии МБУЗ ГБ №2 «КМЛДО», г. Краснодар.
Библиографическая ссылка
Величко Д. С., Шапошников С. А., Синьков С. В. КОРРЕКЦИЯ НАРУШЕНИЙ СИСТЕМЫ ГЕМОСТАЗА С ПОЗИЦИИ ЭНЕРГОДЕФИЦИТНЫХ СОСТОЯНИЙ // Современные проблемы науки и образования. 2012. № 6. ;URL: https://science-education.ru/en/article/view?id=7384 (дата обращения: 27.05.2026).



