Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
RADIOFREQUENCY ABLATION IN THE TREATMENT OF TRIGEMINAL NEURALGIA
Введение
Известно, что невралгия тройничного нерва (НТН) является одной из наиболее распространенных видов краниофациальной боли [1]. Как правило, у большинства пациентов заболевание протекает циклично с периодами ремиссий (частичной или полной) и рецидивами, а спонтанное выздоровление встречается редко [2]. По данным мировой статистики ежегодная частота заболеваемости НТН колеблется от 4 до 13–27 чел. на 100000 [3, 4], а общая распространенность среди популяции составляет от 0,03 до 0,3% [5]. Чаще заболевание встречается у женщин старше 50 лет [6]. Данное состояние не только значительно снижает качество жизни пациентов, но и приводит к выраженным социальным и психологическим последствиям [7].
В 2018г. классификация тригеминальной боли была пересмотрена, и последний вариант CHD-3 (International Classification of Headache Disorders, 3-rd edition) выделяет классическую, обусловленную нейроваскулярным конфликтом, идиопатическую, когда компримирующего сосуда нет, и вторичную невралгию, вызванную новообразованиями тройничного нерва и мостомозжечкового угла, артериовенозными мальформациями или рассеянным склерозом [8].
Многочисленные работы подтвердили предположение P.Jannetta о том, что причиной классической невралгии тройничного нерва является сосудистый конфликт с пятой парой черепно-мозговых нервов [9]. Классическая невралгия тройничного нерва является наиболее распространенным вариантом невралгии и встречается в 75% всех случаев невралгии тройничного нерва [3]. Диагноз обычно не вызывает трудностей, поскольку для данной патологии характерен ряд уникальных клинических особенностей: приступообразная острая боль, наличие триггерных зон, провоцирующих приступ поверхностным механическим раздражением, наличие рефрактерного периода после приступа. Поскольку специфических для НТН диагностических тестов не существует, диагноз выставляется исключительно на основе клинических симптомов, имеющих решающее значение [3, 6].
МРТ на сегодняшний день обладает высокой диагностической точностью в верификации нейроваскулярного конфликта, позволяет идентифицировать или опровергнуть его наличие, а также определить его тип и, таким образом, верифицировать клинические варианты нейропатии.
Стандартом первой линии терапии НТН остается медикаментозное лечение, преимущественно антиконвульсантами (карбамазепин, окскарбазепин, габапентин и др.). Однако, по различным данным, до 30–40% пациентов оказываются резистентными к фармакологической терапии или не переносят ее из-за выраженных побочных эффектов [10]. В таких случаях на первый план выходят хирургические методы лечения. Микроваскулярная декомпрессия является операцией выбора у пациентов с классической невралгией тройничного нерва [11, 12].
Наряду с этим, среди хирургических подходов значительное внимание уделяется малоинвазивным методам, таким как перкутанная радиочастотная абляции (РЧА) Гассерова узла – одна из самых распространенных манипуляций, применяемых для хирургического лечения хронических болевых синдромов. Данный метод зарекомендовал себя как относительно безопасный и эффективный способ купирования болевого синдрома при НТН, обеспечивая быстрый регресс симптомов и возможность проведения вмешательства особенно у пациентов старших возрастных групп с сопутствующей соматической патологией [13, 14].
Несмотря на накопленный клинический опыт, остаются дискуссионными вопросы, касающиеся долгосрочной эффективности радиочастотной абляции, риска рецидивов, а также возможных осложнений, связанных с повреждением чувствительных волокон тройничного нерва [15]. В связи с этим актуальным представляется проведение дальнейших исследований, направленных на оценку клинических исходов и безопасности данного метода лечения у различных категорий пациентов с данной патологией.
Цель исследования – оценить клинические исходы перкутанной радиочастотной абляции Гассерова узла у пациентов с идиопатической невралгией тройничного нерва.
Материал и методы исследования
Выполнено открытое наблюдательное неконтролируемое нерандомизированное одноцентровое ретроспективное исследование. В данное исследование включены 26 пациентов с диагнозом невралгия тройничного нерва, которым в период с января 2024 г. по сентябрь 2025 г. в многопрофильной клинике Compas Hospital г. Ферганы выполнена перкутанная радиочастотная абляция Гассерова узла. Возраст обследованных пациентов варьировал от 26 до 78 лет, медиана возраста составила 48 лет. Среди исследуемых 12 мужчин (46,1%) и 14 женщин (53,9%). Длительность заболевания до вмешательства колебалась от 1 до 20 лет, медианное значение равнялось 7 лет.
Наиболее часто пораженной являлась первая ветвь тройничного нерва, вовлечение которой выявлено у 11 пациентов (42,3%). Поражение второй ветви регистрировалось у 6 больных (23,1%), третьей – у 2 (7,7%), а сочетанное поражение нескольких ветвей отмечено у 7 чел. (26,9%).
Все включенные в исследование больные для купирования боли ранее получали медикаментозную терапию (карбамазепин, габапентин и др.), однако, несмотря на многолетнее длительное применение препаратов, у 85% развилась медикаментозная резистентность, а у 15% непереносимость препаратов, что и явилось основанием для проведения хирургического вмешательства.
Критерии включения: наличие идиопатической НТН, соответствующей диагностическим критериям классификации ICHD-3, отсутствие при МРТ-исследовании нейроваскулярного конфликта, отсутствие стеноза овального отверстия, неэффективность или непереносимость консервативной терапии, а также письменное информированное согласие пациента на проведение вмешательства.
Критерии исключения: Нейроваскулярный конфликт тройничного нерва, выраженный стеноз овального отверстия, симптоматическая НТН, ассоциированная с опухолевыми и демиелинизирующими заболеваниями (рассеянным склерозом), а также тяжелые соматические состояния, препятствующие хирургическому лечению.
С целью диагностики причины болевого синдрома и подтверждения или исключения нейроваскулярного конфликта всем больным проводилась МРТ с мощностью магнитного поля 1,5 Тесла по программе «нейроваскулярный конфликт».
Для определения размера овального отверстия в основании черепа использовалась КТ. Она позволяла установить размеры отверстия и исключить его выраженный стеноз, чтобы при проведении прохождения иглы в полость черепа и манипуляции не повредить корешки тройничного нерва.
Операция выполнялась под местной анестезией по стандартной методике Хартеля под контролем рентгеноскопии с использованием медицинского аппарата Cosman G4 (рис.1). Метки Хартеля наносились на лицо маркировочным карандашом, и точка вхождения иглы обычно находилась на расстоянии 3 см от угла рта.Двумя другими точками были медиальный край зрачка и точка на скуловой дуге на 2,5 см кпереди от козелка, которые служили ориентирами для направления иглы к овальному отверстию. Радиочастотная абляция проводится изолированными иглами длиной 100 мм с рабочим оголенным концом на срезе 5 мм. Под контролем визуализации кончик иглы помещался в овальное отверстие к Гассерову узлу.
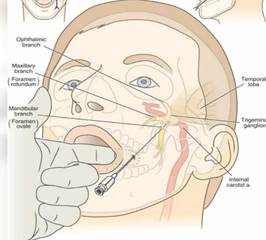
Рис.1. Доступ по стандартной методике Хартеля.
Примечание: рисунок взят из Lord SM, Bogduk N. Radiofrequency procedures in chronic pain. Best Pract Res Clin Anaesthesiol. 2002 Dec. Vol. 16 (4). P. 597–617.
DOI: 10.1053/bean.2002.0250. PMID: 12516894
После установки иглы проводится стимуляция малым током частотой 100 Гц для чувствительных волокон и 2 Гц для двигательных, при этом ощущение покалывания при менее 0,5 В указывает на оптимальное приближение иглы к пораженному нерву. Проводится стимуляция нерва током и поиск нужной ветви тройничного нерва. Затем стилет извлекали из канюли и проводили аспирацию, чтобы убедиться, что в канюле нет спинномозговой жидкости (ликвора) или крови. Введение 2% лидокаина (0,2 мл) в тройничный ганглий помогало уменьшить боль при термокоагуляции.После определения ветви проводилась процедура абляции – кончик иглы нагревался до 70 °С в течение 25–30 с, что соответствует общепринятым протоколам малоинвазивного хирургического лечения НТН. Для эффективного обезболивания кончик канюли обычно перемещали и проводили дополнительную термокоагуляцию. После этого канюлю извлекали, пациентов переводили в палату и выписывали через 48 ч.
Оценка эффективности вмешательства проводилась с использованием визуально-аналоговой шкалы (VAS, 0–10 баллов), шкалы интенсивности боли Барроу (BNI Pain Intensity Scale). Неврологический статус оценивался до и после оперативного вмешательства. При проведении операции особое внимание уделялось оценке чувствительности на лице в зоне иннервации скомпроментированных корешков тройничного нерва. В дальнейшем оперированные обследованы через 1, 3, 6 и 12 месяцев после операции.
Все данные анализировались с использованием статистического пакета SPSS 26.0 (IBM, США). Для сравнения групп применялись t-тест Стьюдента и χ²-тест. Статистически значимыми считались различия при p<0,05.
Результаты исследования и их обсуждение
До оперативного вмешательства у всех пациентов регистрировался выраженный болевой синдром. Средний показатель боли по VAS составил 8,4±0,9 баллов, а по шкале BNI большинство больных соответствовали III–IV категориям (рис.2, 3). Уже в первые сутки после процедуры полное исчезновение боли (BNI I–II) отмечалось у 20 из 26 оперированных больных (76,9%), а значительное уменьшение болевого синдрома было достигнуто у 4 чел. (15,4%). Через месяц средний уровень боли по VAS снизился до 1,3±0,7 баллов.
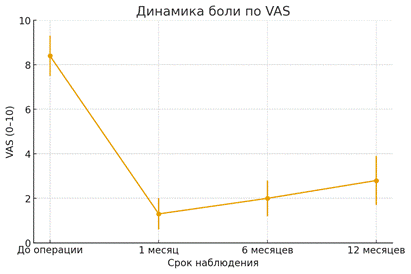
Рис.2. Динамика боли по шкале VAS.
Примечание: составлен авторами по результатам данного исследования
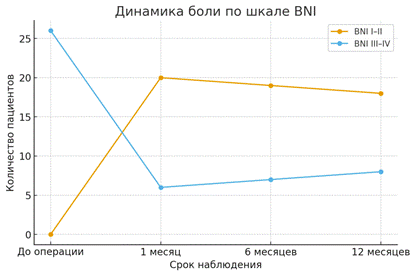
Рис.3. Динамика боли у оперированных по категориям BNI.
Примечание: составлен авторами по результатам данного исследования
При последующем наблюдении установлено, что через 6 месяцев стойкий обезболивающий эффект сохранялся у 22 чел. (84,6%), а через 12 месяцев – у 18 (69,2%). У 8 больных (30,8%) спустя 5–12 месяцев зафиксирован рецидив болевого синдрома, причем в трех случаях потребовалось повторное проведение радиочастотной абляции.
Наиболее частым осложнением проведения абляции являлась транзиторная гипестезия лица, которая наблюдалась у 10 пациентов (38,5%), которая в большинстве случаев регрессировала в течение 1–3 месяцев. У трех больных (11,5%) стойкая умеренная гипестезия на лице сохранялась в течение года после проведения операции.
Тяжелые осложнения, такие как анестезия долороза, офтальмологические нарушения или инфекционные осложнения, в ходе исследования зарегистрированы не были.
В настоящем исследовании перкутанной радиочастотной абляции Гассерова узла у 26 пациентов продемонстрирован высокий ранний клинический эффект: значительное облегчение боли в первые сутки достигнуто у 15,4% (n=4) пациентов, а полное исчезновение болевого синдрома (BNI I–II) –у 76,9% (n=20). Эти данные соответствуют опубликованным сериям и обзорам, в которых сообщается о высоком начальном уровне эффективности РЧА (часто >80–90% пациентов с выраженным облегчением в раннем послеоперационном периоде). Аналогичные крупные очаговые серии и ретроспективные исследования подтверждают высокие показатели раннего pain-free (безболевого) – статуса после радиочастотной абляции [16–18]. Полученные авторами клинические результаты абляции сопоставлены с имеющимися литературными данными, отраженными в таблице.
Долгосрочная эффективность в серии также сопоставима с опубликованными результатами литературы (таблица). Стойкий обезболивающий эффект сохранялся у 84,6% пациентов через 6 месяцев и у 69,2% через 12 месяцев с момента операции, при общей частоте рецидивов 30,8% и необходимости повторного вмешательства у 3 (11,5%) человек. Результаты работ по изучению результатов РЧА в позднем периоде с большими сериями оперированных показывают схожую тенденцию: высокая начальная эффективность с постепенным снижением доли полностью безболевых пациентов по мере увеличения времени наблюдения (например, в крупных сериях показатели безболевого статуса: ≈90% через 1 год, ≈75% через 5 лет). Эти результаты согласуются с данными ретроспективных когорт, где медиана pain-free survival (выживаемость без боли) измеряется в десятках месяцев и наблюдается постепенный рост числа рецидивов в долгосрочной перспективе [19].
Профиль осложнений у оперированных отражает типичную картину для РЧА: наиболее частым побочным эффектом была транзиторная гипестезия лица (38,5%), которая в большинстве случаев регрессировала в течение 1–3 месяцев; стойкая умеренная гипестезия сохранялась у 11,5% пациентов.
В литературе сенсорные нарушения описываются как наиболее распространенный побочный эффект РЧА: преходящие сенсорные расстройства встречаются часто, стойкие осложнения – реже, и их частота зависит от методики, целевых температур и объема термических поражений. Соотношение транзиторных и стойких сенсорных эффектов в проведенном исследовании укладывается в диапазон, описанный в обзорах и оригинальных сериях [18].
В ряде исследований анализировались факторы, ассоциированные с риском рецидива и осложнений. Вовлечение первой ветви тройничного нерва традиционно связывают с более высоким риском офтальмологических осложнений при агрессивном термовоздействии, а также с необходимостью аккуратного подбора режима электростимуляции и температуры. Параметры термокоагуляции – температура и длительность – варьируют в разных медицинских центрах. Стандартные протоколы (например, 65–75°C в течение 20–30с) дают компромисс между эффективностью и частотой сенсорных побочных эффектов, но оптимальные параметры требуют индивидуализации. Используемый в центре протокол (70°C, 25с) соответствует широко используемым клиническим практикам и сопоставим с протоколами, описанными в крупных сериях [17].
Ограничения исследования включают небольшой объем выборки, одноцентровый характер и относительную краткосрочность наблюдения (максимум 12 месяцев).
Отсутствие набора данных по качеству жизни в данной серии (SF-36) у всех пациентов ограничивает возможность всесторонней оценки функционального эффекта вмешательства. Для более надежной оценки устойчивости результата и факторов риска необходимы проспективные мультицентровые исследования в Республике Узбекистан с длительным наблюдением, стандартизованной оценкой исходов и более детализированной стратификацией по вовлеченным ветвям тройничного нерва и параметрам РЧА [20].
Сравнение ключевых показателей исследуемой серии и данных литературы
|
Показатель |
Наша серия (n=26) |
Kanpolat et al., 2001 (n≈1600) |
Zhao et al., 2022 (n=1070) |
Систематический обзор / метаанализ |
|
Ранняя pain-free (первые сутки/1 мес.) |
76,9% (BNI I–II); 92,3% облегчение в сутки |
Очень высокий начальный успех (>85–90%). PubMed |
~89,9% pain-free at 1 year; высокий ранний эффект. PubMed |
Общая оценка успеха RFT ≈85–90% (начальный период). PMC+1 |
|
Pain-free через 6 мес. / 12 мес. |
84,6% / 69,2% |
Показатели снижаются с годами; в долгосрочных сериях значимая доля остается pain-free на годы. PubMed |
1 год ~90%; 5 лет ~75%. PubMed |
Средние long-term pain-free rates варьируют: 5-летние ≈70–80% (в разных сериях). journals.lww.com+1 |
|
Рецидив / необходимость повторной РЧА |
30,8% / 3 повторных вмешательства |
Рецидивы описаны, необходимость повторных процедур – частая практика в ретроспективных сериях. PubMed |
Повторные процедуры и рецидивы описаны; медиана pain-free survival – десятки месяцев. PubMed |
Рецидивы отмечаются в значительной доле пациентов при длительном наблюдении. PMC |
|
Транзиторная гипестезия |
38,5% |
Частые сенсорные нарушения, большинство – временные. Wiley Online Library |
Сенсорные эффекты отмечены; частота зависит от техники и параметров. PubMed |
|
|
Постоянная гипестезия |
11,5% |
В разных сериях частота постоянных дефектов варьирует (прибл. 5–15%). PubMed+1 |
Сообщается в отдельных сериях; вариабельность в зависимости от методики. PubMed |
|
Примечание: составлена авторами на основе полученных данных в ходе исследования и на основе литературных источников
Заключение
Радиочастотная абляция Гассерова узла является эффективным и относительно безопасным методом лечения резистентной идиопатической невралгии тройничного нерва, обеспечивающим быстрое купирование боли и стойкий обезболивающий эффект у большинства пациентов в течение года. При этом у трети больных возможны рецидивы болевого синдрома.
Наиболее частым осложнением является транзиторная гипестезия лица, редко приводящая к стойким нарушениям чувствительности.
Полученные результаты подтверждают целесообразность применения данной методики как предпочтительного хирургического подхода у пациентов с идиопатической невралгией тройничного нерва при неэффективности медикаментозной терапии.
Conflict of interest
Financing
Библиографическая ссылка
Ступак В.В., Абдурохмонов А.А., Кузиев О.И., Жалолов Ж.И. ПРИМЕНЕНИЕ РАДИОЧАСТОТНОЙ АБЛЯЦИИ ПРИ ЛЕЧЕНИИ НЕВРАЛГИИ ТРОЙНИЧНОГО НЕРВА // Современные проблемы науки и образования. 2026. № 4. ;URL: https://science-education.ru/en/article/view?id=34579 (дата обращения: 13.05.2026).
DOI: https://doi.org/10.17513/spno.34579



