Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
THE EFFECT OF THERAPEUTIC PLASMAPHERESIS ON THE COURSE OF ENDOGENOUS INTOXICATION IN THE PERIOPERATIVE PERIOD OF PATIENTS WITH NON-SMALL CELL LUNG CANCER COMPLICATED BY A SECONDARY INFLAMMATORY PROCESS
Введение
В настоящее время рак лёгкого (РЛ) представляет собой доминирующую форму злокачественных новообразований, что делает его одной из наиболее значимых медико-социальных и экономических проблем как в Российской Федерации, так и на мировом уровне [1]. Современная тактика лечения немелкоклеточного рака лёгкого (НМРЛ) основывается на комплексном подходе, который включает радикальное оперативное вмешательство, лучевую и химиотерапию. Данная стратегия направлена на оптимизацию выживаемости пациентов на всех этапах течения онкологического заболевания, обеспечивая индивидуализированный и патогенетически обоснованный подход к лечению [2]. Общеизвестно, что прогностические параметры течения НМРЛ определяются совокупностью факторов, влияющих на риск опухолевой прогрессии. К числу ключевых детерминант относятся: стадия заболевания, морфологическая структура опухоли, степень её дифференцировки, а также наличие регионарного и/или отдаленного метастазирования. Эти параметры играют важную роль в формировании прогноза заболевания и планировании лечебных мероприятий [3]. К неблагоприятным прогностическим факторам следует отнести наличие у больных РЛ коморбидной патологии с потенциальным риском возникновения острой кардиальной и критической дыхательной недостаточности, а также развитие воспалительных послеоперационных осложнений [4]. На вероятность возникновения локальных и системных воспалительных осложнений существенно влияет степень распространения опухолевого процесса в лёгком [5]. Известно, что у 70% пациентов НМРЛ выявляется на поздних стадиях заболевания с местным распространением процесса или метастазированием. Примерно в половине случаев опухолевый процесс сопровождается инфильтрацией лёгочной ткани воспалительного генеза, что, как правило, обусловлено распадом опухоли [4]. Радикальные и агрессивные методы хирургического лечения РЛ, несомненно, увеличивают риск развития послеоперационных осложнений. Стандартный объем операции включает анатомическую резекцию лёгкого или пневмонэктомию с медиастинальной лимфодиссекцией [3]. Проблема пульмогенных воспалительных осложнений возникает на ранних сроках послеоперационного лечения и связана не только с уменьшением объема легочной ткани, но и с механическим исключением лёгкого из процесса дыхания в ходе операции. Хирургическая мобилизация, сопровождаемая кратковременным прекращением газообмена в лёгком, приводит к активации воспалительных реакций и интенсивной секреции медиаторов воспаления и может инициировать развитие острого повреждения лёгких, что подтверждается клиническими исследованиями в области респираторной физиологии и патологии [5]. Кроме того, дисфункция лёгочного кровотока и нарушение газообмена приводят к снижению парциального давления кислорода в крови, что вызывает неадекватный сердечный выброс и ухудшение перфузионно-вентиляционного соотношения. В коллабированном лёгком нарушается равновесие пре- и посткапиллярного сопротивления с изменением капиллярно-гидростатического давления, что, в свою очередь, сопровождается формированием тканевой гипоксемии и гиперкапнии, нарушением характера течения окислительных реакций и энергетического баланса [6]. Этот процесс приводит к развитию неконтролируемого каскада иммуноопосредованных гипервоспалительных реакций, вызываемых молекулярными паттернами, ассоциированными с патогенами и клеточными повреждениями [4].
Очевидно, что успех лечения таких пациентов зависит не только от стадии опухолевого процесса, но и от возможности организма к компенсации стресс-индуцированных реакций на проведение расширенных онкохирургических операций при РЛ. В данном контексте существует необходимость тщательного контроля и адаптации терапевтических подходов, а также модернизации традиционной предоперационной подготовки больных НМРЛ с возможностью коррекции эндотоксикоза путём интеграции методов экстракорпоральной детоксикации, в частности терапевтического плазмообмена. Это позволит снизить предельно высокие концентрации токсических субстанций, воспалительных и антифибринолитических медиаторов, обеспечивая восполнение антикоагулянтных белков и ADAMTS13 путем плазмопоэза, повышение реактивности организма посредством оптимизации метаболических процессов и активации гемопоэза, способствуя снижению риска развития в послеоперационном периоде воспалительных пульмогенных осложнений [7-9].
Цель исследования: оценить результативность детоксикационного воздействия предоперационного терапевтического плазмообмена при НМРЛ с воспалительным компонентом в качестве упреждающего фактора развития воспалительных пульмогенных осложнений после радикального хирургического лечения.
Материал и методы исследования
В данном исследовании основную группу составили 30 пациентов (27 мужчин и 3 женщины), госпитализированных в ФГБУ «Национальный медицинский исследовательский центр онкологии» Минздрава РФ (НМИЦ онкологии) в период с 2021 по 2023 год для хирургического лечения первично выявленного НМРЛ, осложненного воспалительным процессом. Исследование получило одобрение Этического комитета «НМИЦ онкологии» и зафиксировано в протоколе № 19 от 22.11.2021 года. Критерии включения в исследование: возраст старше 18 лет, проведение радикального хирургического вмешательства по поводу НМРЛ с воспалительным компонентом, согласие на проведение ТПО и использование полученных клинических данных для научных целей. Критерии невключения: возрастное ограничение до 18 лет, наличие психиатрической коморбидной патологии, выполнение нерадикального хирургического лечения, отказ от проведения ТПО и участия в научном исследовании.
На основании данных обследования консилиумом врачей с участием хирурга-онколога, радио- и химиотерапевтов определяли объем противоопухолевого лечения. Диагностические и лечебные мероприятия проводили по рекомендациям Российского общества клинической онкологии RUSSCO (2025). Все пациенты, вошедшие в исследование, перед хирургическим лечением получали стандартную подготовку, направленную на профилактику воспалительных и кардиореспираторных осложнений [3]. В основной группе в рамках предоперационной подготовки был проведен ТПО. Возрастная медиана в основной группе составила 66 лет (47–75). Группа сравнения была представлена 28 пациентами (ретроспективное исследование), сопоставимыми с основной группой, у которых в послеоперационном периоде диагностировали развитие пульмогенных воспалительных осложнений. Возрастные критерии соответствовали основной группе: средний возраст составил 64+1,6 года. Классификация НМРЛ (по системе TNM, 9-е издание, 2025 г.) и другие параметры исследуемых групп представлены в таблице 1.
Таблица 1
Распределение больных в группах исследования по стадиям онкологического заболевания, классификации в системе TNM, клинико-анатомической форме, локализации, видам операции, гистологическому типу опухоли
|
Параметры |
Группы исследования |
||||
|
|
Основная (n=30) |
Сравнения (n=28) |
Основная (n=30) |
Сравнения (n=28) |
|
|
Стадии, TNM |
St IB |
4(13,3%) |
T2aN0M0 |
3 (10,0 %) |
2 (7,1 %) |
|
St IIA |
3 (10,0%) |
T2bN0M0 |
4 (13,3 %) |
3 (10,7 %) |
|
|
St IIB |
7 (23,3%) |
T3N0M0 |
7 (23,4 %) |
5 (17,9 %) |
|
|
St IIIA |
8 (26,7%) |
T3N1M0 |
5 (16,7 %) |
5 (17,9 %) |
|
|
|
|
T0M0 |
2 (6,7 %) |
3 (10,7 %) |
|
|
|
|
T4N1M0 |
1 (3,3 %) |
4 (14,3 %) |
|
|
St IIIB |
8 (26,7%) |
T3N2M0 |
7 (23,3 %) |
6 (21,4 %) |
|
|
|
|
T4N2M0 |
1 (3,3 %) |
0,0 |
|
|
Клинико-анатомическая форма |
Центральный НМРЛ |
15 (50 %) |
14 (50,0 %) |
||
|
Периферический НМРЛ |
11 (36,7 %) |
11 (39,3 %) |
|||
|
Периферический рак с централизацией |
4 (13,3 %) |
3 (10,7 %) |
|||
|
Виды операции |
Лоб-, билобэктомия |
6 (20,0%) |
6 (21,4%) |
||
|
Пневмонэктомия |
16 (53,3%) |
14 (50,0%) |
|||
|
Плевропневмонэктомия |
2 (6,7%) |
3 (10,7%) |
|||
|
Комбинированные пневмонэктомии |
6 (20,0%) |
5 (17,9%) |
|||
|
Гистотип |
Аденокарцинома |
8 (26,7%) |
8 (28.6%) |
||
|
Плоскоклеточный рак |
19 (63,3%) |
17 (60,7%) |
|||
|
Крупноклеточный рак |
1 (3,3%) |
2 (7,1%) |
|||
|
Железисто-плоскоклеточный рак |
2 (6,7%) |
1 (3,6%) |
|||
Примечание: распределение больных в таблице рассчитано автором.
Характер пульмогенных воспалительных осложнений в основной группе и группе сравнения статистически значимых различий не имел: пульмонит 14 (46,7%) и 13 (46,4%) случаев, пневмония 4 (13,3%) и 9 (32,1%), распад опухоли, параканкрозная пневмония 8 (26,7%) и 5 (17,9%), эмпиема плевры 3 (10,0%) и 1 (3,3%) случай соответственно, абсцесс наблюдали у 1 (3,3%) пациента основной группы.
Средняя продолжительность хирургических вмешательств в основной группе составила 120±11 мин., в группе сравнения 115±10 мин. У всех пациентов применяли комбинированную эндотрахеальную анестезию с раздельной интубацией бронхов на основе ингаляционного анестетика Севофлюран в сочетании с мультимодальным обезболиванием. Эпидуральную анальгезию использовали у всех пациентов обеих групп интраоперационно и в первые 48 часов послеоперационного периода. Интраоперационный мониторинг включал: измерение артериального давления неинвазивным методом, электрокардиографию, капнографию, пульсоксиметрию и термометрию. Эффективность анестезии и анальгезии контролировали с помощью данных биспектрального индекса и показателей нейромышечного блока.
Методика терапевтического плазмообмена
Терапевтический плазмообмен проводили в интервале от 24 до 48 часов до хирургического вмешательства аппаратом Plazauto Sigma (Япония) с использованием плазмофильтра Plazmaflo ОР-02W/L на основе технологии полых волокон из полиэтилена с диаметром пор 0,3 мкм (Asahi Kasei Medical, Япония). ТПО осуществляли в соответствии с протоколом терапевтического плазмообмена. Сосудистый доступ - v. jugularis или v. subclavia со стороны опухолевого поражения с установкой двухходового перфузионного катетера 14 F. Объем плазмофильтрата составлял не менее 70% объема циркулирующей плазмы со 100% плазмозамещением: сбалансированными кристаллоидными (Стерофундин, Фриостерин), коллоидными растворами – 4% раствор Гелафузина, препаратами 20% Альбумина и одногруппной, однорезусной свежезамороженной плазмой в соотношении 1:1:2. Антикоагуляцию проводили нефракционированным гепарином в дозе, соответствующей показателям активированного частичного тромбопластинового времени.
В целях определения степени тяжести течения эндогенной интоксикации (ЭИ) на основании данных гемостазиограмм (анализатор Advia 60 (Bayer, Германия)) изучали показатели гематологических индексов интоксикации: лейкоцитарного индекса интоксикации, индекса резистентности организма, индекса реактивного ответа нейтрофилов и нейтрофильно-лимфоцитарного соотношения [10; 11]. Для объективной оценки уровня воспалительных маркеров в организме в сыворотке крови проводили количественное определение прокальцитонина и интерлейкина-6 (Bi-Plex Pro Human Cytokine Assays, USA). Для проведения анализа биоматериала осуществляли забор венозной крови из локтевой вены в утренние часы. Клинико-лабораторные исследования выполняли при поступлении пациента в стационар, а также на первые и 3-5-е сутки после операции. В основной группе дополнительно исследовали данные показатели через 24 часа после ТПО. В качестве контроля использовали данные лабораторного обследования 24 здоровых мужчин и женщин без онкологических заболеваний, сопоставимых по возрасту и полу с группами исследования.
Статистическую проверку на соответствие нормальному распределению проводили по W-критерию Шапиро - Уилка и Колмогорова - Смирнова, результаты представлены в виде М±m (М - выборочное среднее, m – ошибка среднего, медиана (Me), которая во всех группах практически не отличалась от M); интерквартильный разброс в виде подсчета нижнего и верхнего квартилей (Q25 и Q75).
Результаты исследования и их обсуждение
Эндогенная интоксикация представляет собой патологическое состояние, характеризующееся нарушением гомеостаза и накоплением в биологических жидкостях и тканях значительного количества токсичных метаболитов эндогенного происхождения [10]. Показатели гематологических индексов эндогенной интоксикации (лейкоцитарный индекс интоксикации (ЛИИ)), индекс резистентности организма (ИРО), индекс реактивного ответа нейтрофилов (РОН), нейтрофильно-лимфоцитарное соотношение (НЛС) и маркеров системного воспаления прокальцитонина (ПКТ) и интерлейкина-6 (ИЛ-6) в исследуемых группах пациентов до начала лечения были статистически однородными и не имели значимых различий. Данные представлены в таблице 2.
Таблица 2
Показатели гематологических индексов эндогенной интоксикации и маркеров системного воспаления у больных НМРЛ, осложненным воспалительным процессом (исходные данные), Me [L25Q;U75]
|
Показатель |
Группы исследования |
||
|
Здоровые люди (n=24) |
Основная группа (n=30) |
Группа сравнения (n=28) |
|
|
ЛИИ, у. е. |
1,1 [1,04; 1,2] |
3,98 [3,8; 4,15] p1=0,0001* p2=0,84 |
3,56 [2,96; 5,1] p1=0,001* |
|
ИРО, у. е. |
61,0 [59,0; 73,0] |
30,32 [24,7; 30,32] p1=0,0001* p2=0,43 |
32,87 [26,4; 41,9] p1=0,0001* |
|
РОН, у. е. |
10,6 [9,2; 12,2] |
27,31 [23,9; 33,87] p1=0,0001* p2=0,154 |
27,68 [22,2; 33,11] p1=0,0001* |
|
НЛС, у. е. |
2,22 [2,10; 2,28] |
7,08 [7,81; 10,70] p1=0,001* p2=0,161 |
9,99 [8,60; 12,11] p1=0,0001* |
|
Маркеры воспалительного ответа |
|||
|
ПКТ, нг/мл |
0,11 [0,097;0,121]
|
0,775 [0,68; 0,82] p1=0,001* p2=0,06 |
0,670 [0,49; 0,82] p1=0,0001* |
|
ИЛ-6, пг/мл |
4,68 [4,48;4,89]
|
92,60 [86,2; 100,4] p1=0,001* p2=0,06 |
116,59 [108,4; 124,5] p1=0,001* |
Примечание: ЛИИ – лейкоцитарный индекс интоксикации, ИРО – индекс резистентности организма, РОН – индекс реактивного ответа нейтрофилов, НЛС –нейтрофильно-лимфоцитарное соотношение, ПКТ – прокальцитонин, ИЛ-6 –интерлейкин -6; p1 – значимость различий в группе относительно здоровых людей; р2 – значимость. Различия относительно показателей в группе сравнения; * - р<0,05. В таблице указаны данные собственного исследования авторов.
Как следует из данных исследования, у всех пациентов на фоне вторичного воспаления, которое сопровождало течение опухолевого процесса, было выявлено наличие ЭИ с явной дезадаптацией иммунного ответа на дооперационном этапе. Исходное состояние пациентов характеризовалось увеличением ЛИИ и РОН более чем в 2 и 3 раза соответственно, при этом ИРО был почти вдвое ниже по сравнению с показателями здоровых людей. При этом индекс НЛС у всех больных превышал в 3,9 раза значение в группе «здоровые». Это состояние сопровождалось увеличением концентрации сывороточных маркеров системного воспаления. Показатели ПКТ в 6,4 раза и ИЛ-6 в 22,4 раза превышали соответствующие данные в контрольной группе здоровых людей (табл. 2) (p<0,05).
Проведение ТПО в рамках предоперационной подготовки пациентов с НМРЛ, осложненным воспалением, несколько улучшил компенсаторные реакции организма на фоне ЭИ. Так, через 24 часа после ТПО в основной группе наблюдали увеличение изначально низкого показателя ИРО в 1,3 раза. Одновременно регистрировали уменьшение индексов РОН и НЛС в 2 и 1,8 раза соответственно (p<0,05) (рис.).
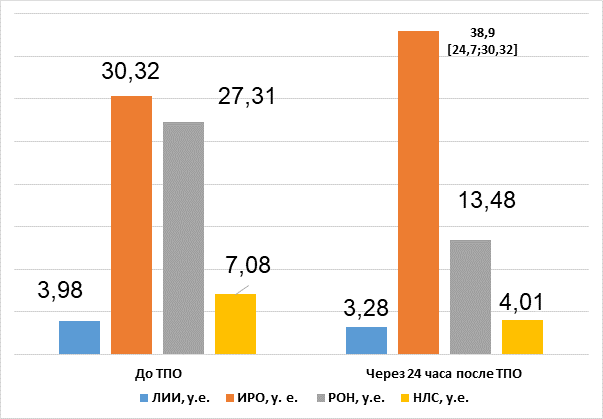
Динамика показателей гематологических индексов эндогенной интоксикации (ЛИИ, РОН, ИРО, НЛС) в основной группе больных до и через 24 часа после проведения ТПО, Me [LQ;UQ]. Примечание: * – значимость различий по сравнению с предыдущим этапом исследования (p<0,05). В рисунке использованы данные собственного исследования авторов
Исследование динамики гематологических показателей эндогенной интоксикации и маркеров системного воспаления в периоперационном периоде с использованием ТПО и без него показало значительные различия в исследуемых группах (табл. 3).
Таблица 3
Динамика показателей гематологических индексов эндогенной интоксикации и маркеров системного воспаления у больных НМРЛ, осложненным воспалительным процессом, в основной группе больных (1) и группе сравнения (2) на этапах исследования Ме [L25;U75]
|
Показатель |
Значение показателей на этапах исследования |
|||||
|
До операции |
1-е сутки п/о периода |
3-5 сутки п/о периода |
||||
|
1 |
2 |
1 |
2 |
1 |
2 |
|
|
ЛИИ, у. е. |
3,98 [3,80; 4,15]
|
3,56 [2,96; 5,1]
|
6,20 [5,8; 6,71] p1=0,001* p2=0,001* |
9,65 [5,8; 6,71] p1=0,000* |
2,9 [2,76; 3,18] p1=0,05* p2=0,0003* |
6,38 [5,67; 8,10] p1=0,01* |
|
ИРО у. е. |
30,32 [24,7; 30,32]
|
32,87 [26,4; 41,9]
|
27,0 [25,6; 28,7] p1=0,14 p2=0,001* |
22,6 [21,4; 26,2] p1=0,23 |
26,06 [25,4; 33,1] p1=0,32 p2=0,001* |
20,9 [16,1; 22,2] p1=0,002* |
|
РОН, у. е. |
27,31 [23,9; 33,87] |
27,68 [22,2; 33,11] |
30,2 [26,5; 29,1] p1=0,05* p2=0,001*
|
127,2 [82,0; 140,0] p1=0,000*
|
21,05 [19,6; 23,2] p1=0,05* p2=0,000* |
150,2 [80,4;163,3] p1=0,000* p2=0,001* |
|
НЛС, у. е. |
7,08 [7,81; 10,70]
|
9,99 [8,60; 12,11] |
10,21 [6,67; 12,4] р1=0,0001* p2=0,061 |
13,36 [11,33;15,1] р1=0,0001* |
8,98±1,6 [4,63; 8,9] р1=0,098 p2=0,000* |
15,21 [12,31;15,82] р1=0,000* |
|
Маркеры воспалительного ответа |
||||||
|
ПКТ, нг/мл |
0,775 [0,68; 0,82]
|
0,670 [0,49; 0,82]
|
0,890 [0,55; 1,02] p1=0,5 p2=0,08 |
1,590 [5,77; 7,16] p1=0,5 |
0,550 [0,42; 0,65] p1=0,001* p2=0,000 * |
10,930 [10,58; 11,93] p1=0,000* |
|
ИЛ-6, пг/мл |
92,60 [86,2; 100,4]
|
116,59 [108,4;124,5] |
129,70 [121,9; 135,2] p1=0,001* p2= 0,05*
|
166,05 [148,15;188,15] p1=0,001* |
63,24 [59,1; 67,2] p1=0,001* p2=0,000 |
400,05 [305,8; 462,55] p1=0,000* |
Примечание: ЛИИ – лейкоцитарный индекс интоксикации, ИРО – индекс резистентности организма, РОН – индекс реактивного ответа нейтрофилов, НЛС –нейтрофильно-лимфоцитарное соотношение, ПКТ – прокальцитонин, ИЛ-6 –интерлейкин -6; p1 – значимость различий относительно исходных значений; р2 – значимость межгрупповых различий на этапе исследования; * - р<0,05. Данные таблицы рассчитаны коллективом авторов на основании проведенного исследования.
Согласно полученным данным, у всех пациентов обеих групп в 1-е сутки после операции уровень ЛИИ увеличился по сравнению с предоперационными показателями в 1,5 раза в основной группе и в 2,4 раза в группе сравнения (p<0,05). Однако у пациентов основной группы с применением в предоперационном периоде ТПО уровень ЛИИ был в 1,2 раза ниже по сравнению с группой сравнения (p<0,05). К 3-5-м суткам послеоперационного периода показатель ЛИИ в основной группе возвращался к исходным значениям, а в группе сравнения сохранял те же высокие значения, превышающие исходные в 1,7 раза (p<0,05) (табл. 3).
У пациентов группы сравнения с изначально низкими показателями ИРО эти значения продолжали статистически значимо снижаться в течение 3-5 дней после операции. В основной группе гематологический индекс реактивности организма оставался практически неизменным на протяжении всего исследования (табл. 3). В процессе динамического мониторинга уровня РОН у пациентов основной группы, которым в рамках предоперационной подготовки применяли ТПО, наблюдали сохранение стабильных значений данного показателя. В отличие от этого, в группе сравнения наблюдали значительный рост уровня РОН в 1-е и 3-5-е сутки исследования, что было в 4,6 и 5,4 раза выше исходных значений соответственно (p<0,05) (табл. 3).
В контексте анализа динамики индекса НЛС в периоперационном периоде у пациентов основной группы отмечали статистически значимое повышение данного показателя в 1,3 раза на 1-е сутки после проведения хирургического вмешательства с постепенным снижением индекса к 3-5-м суткам послеоперационного периода. Следует подчеркнуть, что значения НЛС к 3-5-м суткам демонстрировали статистически значимое снижение по сравнению с предоперационным уровнем, что свидетельствовало о нормализации и адекватном ответе на воспалительную реакцию.
Параллельно с этим наблюдали идентичную динамику показателей сывороточных маркеров системного воспалительного ответа, что свидетельствовало о синхронном характере изменений в течении воспалительного процесса. Концентрации ПКТ и ИЛ-6 в сыворотке крови имели значимое повышение в 1-е сутки после хирургического вмешательства. Уровень ПКТ в основной группе увеличился в 1,2 раза, а ИЛ-6 - в 1,4 раза по сравнению с исходными значениями (p<0,05). Впоследствии отмечали тенденцию к снижению этих показателей, достигая статистически значимых значений ниже исходных уровней к 3-5-м суткам послеоперационного периода. В группе сравнения регистрировали кардинально отличные изменения исследуемых параметров. Индекс НЛС демонстрировал статистически значимое увеличение в 1-е сутки послеоперационного периода, с увеличением в 1,3 раза по сравнению с исходными значениями. Дальнейшая динамика характеризовалась прогрессирующим ростом к 3-5-м суткам, что приводило к его дополнительному увеличению в 1,5 раза относительно начального уровня (p<0,05). Одновременно наблюдали рост показателей ПКТ и ИЛ-6 к первым суткам в 2,4 и 1,4 раза, а к 3-5-м суткам - в 16,3 и 3,4 раза соответственно в сравнении с исходом (p<0,05) (табл. 3). Отрицательная динамика показателей в группе сравнения демонстрирует реакцию организма больного на хирургическую травму без компенсаторного звена адаптации с предпосылками развития более глубоких изменений воспалительного характера системного действия с компонентом острого повреждения лёгких, полиорганной недостаточности и неблагоприятного исхода.
Обсуждение
Сочетание опухолевого и воспалительного процессов у пациентов НМРЛ выступает в качестве триггерного механизма, инициирующего развитие послеоперационных пульмоногенных воспалительных осложнений. Эти осложнения характеризуются стремительным и непредсказуемым течением, что может привести к серьезным полиорганным дисфункциям, включая потенциально фатальные последствия для пациента [12]. Несомненно, прогрессирование онкологического процесса в условиях исходного воспалительного компонента сопровождается значительным риском развития патологических изменений при проведении агрессивной противоопухолевой терапии. Ранее авторами было проведено ретроспективное исследование больных НМРЛ на этапе радикального хирургического лечения, в котором отмечено, что развитие послеоперационных пульмоногенных воспалительных осложнений у исследуемой когорты пациентов коррелирует с уровнем исходной эндогенной интоксикации, которая, в свою очередь, характеризуется дезадаптацией иммунного ответа и последующей активацией системной воспалительной реакции [7].
Весьма очевидно, что в условиях современных терапевтических стратегий закономерно использовать детоксикационный эффект, достигаемый посредством ТПО у клинически сложной группы пациентов НМРЛ с воспалительным компонентом. Как известно, ТПО представляет собой высокоэффективный метод экстракорпорального удаления токсических лигандов, который способствует значительному повышению адаптационного потенциала организма, оптимизирует метаболические и пластические процессы, стимулирует активацию симпатоадреналовой системы и гемопоэза [13]. В данном контексте настоящее исследование было направлено на проведение сравнительного анализа динамики гематологических индексов эндогенной интоксикации (ЛИИ, ИРО, РОН, НЛС) и сывороточных маркеров системного воспаления (ПКТ, ИЛ-6) в периоперационном периоде у больных НМРЛ с воспалительным компонентом при использовании ТПО в комплексной предоперационной подготовке и в условиях стандартной терапии.
Известно, что гематологические индексы являются интегральными показателями, позволяющими оценить степень исходной реактивности пациента, а также выявить дезадаптивность иммунного ответа с риском развития септических осложнений и изолированными органными нарушениями [11]. ЛИИ служит важным индикатором степени тканевой деструкции и различных уровней ЭИ. Формула индекса представляет собой соотношение числа нейтрофильных лейкоцитов к моноцитам, лимфоцитам и эозинофилам. Повышение ЛИИ более 9 усл. ед. свидетельствует о наличии острого воспалительного ответа на действие бактериальных токсинов. Индекс резистентности организма напрямую связан с показателями ЛИИ и возрастом пациента. Это отношение абсолютного количества лейкоцитов к произведению коэффициента ЛИИ с количеством лет пациента (ИРО = Л (тыс./л) / ЛИИ × возраст пациента). Низкие показатели индекса ИРО (менее 50 усл. ед.) указывают на наличие острого септического процесса. Показатели РОН определяют уровень компенсаторных возможностей пациента. Параметры индекса более 40 усл. ед. характерны для декомпенсации воспалительного процесса [12]. Использование НЛС и анализ динамики сывороточной концентрации маркеров воспалительной реакции также может служить не только предиктором, но и маркером характера развития и исходов послеоперационных воспалительных осложнений. Суждение авторов согласуется с данными исследований, определяющих роль НЛС в качестве динамического индикатора воспаления, а также одного из инструментов для прогнозирования клинического течения и исхода пульмоногенных воспалительных осложнений [11]. Уровень ПКТ выступает в качестве специфического биологического маркера бактериальной инфекции, доподлинно отражающего динамику развития воспалительного процесса. ПКТ является одним из основных предикторов и потенциальным индикатором в ранней диагностике бактериальной инфекции у пациентов в критическом состоянии, в том числе при тяжелой пневмонии, осложненной сепсисом [14]. ИЛ-6 (он же IFNB2, интерферон-бета-2, фактор дифференцировки В-клеток, HSF или фактор стимуляции гепатоцитов) – один из наиболее изученных провоспалительных цитокинов. Участвует в ряде биологических процессов, необходимых для нормального функционирования организма. ИЛ-6 обладает широким спектром свойств: дифференцировка В-лимфоцитов, регуляция противоопухолевой защиты, участие в развитии пирогенной реакции, стимуляция синтеза белков острой фазы воспаления, таких как С-реактивный белок, фибриноген, сывороточный амилоид A и гепсидин, повышает экспрессию фибриногена, фактора III, VIII и фактора Виллебранда, является мощным индуктором активности ангиотензина II и т. д. [15]. Бесспорно, показатели динамики ПКТ и ИЛ-6 демонстрируют прогностическую значимость иммунных реакций в структуре воспалительного ответа. Их увеличение указывает на стремительное ухудшение состояния пациента с развитием неблагоприятного течения заболевания [16].
Таким образом, проведенный в исследовании анализ позволяет с высокой степенью уверенности сделать вывод об эффективности применения ТПО в качестве профилактической меры для поддержания гомеостаза у пациентов с НМРЛ в периоперационном периоде. Данный вывод основывается на комплексном рассмотрении клинико-лабораторных показателей гематологических индексов эндогенной интоксикации и маркеров системного воспаления. Увеличение показателей ЛИИ, РОН, НЛС, ПКТ и ИЛ-6 обусловлено активацией неспецифического иммунного ответа. Снижение индексов и маркеров воспаления ПКТ и ИЛ-6 к 3-5-м суткам в основной группе может свидетельствовать о нормализации системного иммунного ответа с восстановлением баланса клеточного состава крови.
Заключение
Безусловно, результаты исследования весьма очевидно демонстрируют эффективную роль комплексной предоперационной подготовки с использованием терапевтического плазмообмена у пациентов с НМРЛ и сопутствующим воспалительным компонентом. Нивелирование явных предикторов эндогенной интоксикации способствует формированию адаптивного воспалительного ответа на хирургическое вмешательство с признаками функциональной стабильности. Вместе с тем отмечено, что в ходе стандартной подготовки у данной категории пациентов в раннем послеоперационном периоде наблюдается усугубление изначальной дезадаптации воспалительного ответа с характерным превалированием провоспалительных медиаторов, что, несомненно, может стать причиной неконтролируемых изменений, ведущих к развитию генерализованного воспаления, органным и системным повреждениям.
Conflict of interest
Financing
Библиографическая ссылка
Тихонова С.Н., Ушакова Н.Д., Розенко Д.А., Харагезов Д.А., Попова Н.Н., Демьяненко А.В., Фоменко Ю.А., Петров Д.С. ВЛИЯНИЕ ТЕРАПЕВТИЧЕСКОГО ПЛАЗМООБМЕНА НА ХАРАКТЕР ТЕЧЕНИЯ ЭНДОГЕННОЙ ИНТОКСИКАЦИИ В ПЕРИОПЕРАЦИОННОМ ПЕРИОДЕ БОЛЬНЫХ НЕМЕЛКОКЛЕТОЧНЫМ РАКОМ ЛЕГКОГО, ОСЛОЖНЕННЫМ ВТОРИЧНЫМ ВОСПАЛИТЕЛЬНЫМ ПРОЦЕССОМ // Современные проблемы науки и образования. 2026. № 4. ;URL: https://science-education.ru/en/article/view?id=34578 (дата обращения: 13.05.2026).
DOI: https://doi.org/10.17513/spno.34578



