Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
EFFECT OF BERBERINE ON THE FUNCTIONAL ACTIVITY OF PERIPHERAL BLOOD MONONUCLEAR CELLS IN PATIENTS WITH DIFFUSE LARGE B-CELL LYMPHOMA WITH DIFFERENT RESPONSES TO THERAPY
Введение
Современная онкогематология продолжает сталкиваться с проблемой рефрактерности к стандартной терапии при диффузной В-клеточной крупноклеточной лимфоме (ДВКЛ). Несмотря на применение современных протоколов лечения, включающих иммунохимиотерапию, у 30–40% пациентов развивается рецидив или резистентность к терапии [1]. Формирование неблагоприятного исхода связано не только с молекулярными особенностями опухолевых клеток, но и с состоянием иммунного микроокружения. Показано, что состав и функциональная активность иммунных клеток, включая Т-лимфоциты и NK-клетки, ассоциированы с прогнозом при ДВКЛ [2]. Нарушение противоопухолевого иммунного надзора способствует прогрессированию заболевания и снижению чувствительности к терапии.
Терапевтическое воздействие может быть направлено как на опухолевые клетки, так и на модуляцию иммунного ответа, способного привести к улучшению прогноза и повышению эффективности терапии [3]. В связи с этим одним из перспективных направлений является поиск подходов к целенаправленной регуляции функциональной активности иммунокомпетентных клеток. В настоящее время активно изучаются различные иммуномодулирующие агенты, среди которых особый интерес представляет берберин – природный алкалоид, демонстрирующий противоопухолевую активность в доклинических исследованиях [4, 5]. Известно, что берберин способен индуцировать апоптоз опухолевых клеток и подавлять их пролиферацию [6, 7]. В экспериментальных моделях ДВКЛ показано, что берберин способен усиливать противоопухолевый иммунный ответ [8]. Кроме того, описано его влияние на функциональную активность B- и T-лимфоцитов [9].
В то же время влияние берберина на функциональные характеристики иммунокомпетентных клеток у пациентов с ДВКЛ изучено недостаточно.Исследование его воздействия на мононуклеарные клетки периферической кровиможет способствовать выявлению новых предикторов ответа на терапию, разработке персонализированных подходов к лечению, а следовательно, улучшению клинических исходов у пациентов с ДВКЛ.
Цель исследования – провести сравнительную оценку исходного иммунного статуса и функциональной активности мононуклеарных клеток периферической крови (МНПК) при воздействии берберина in vitro у пациентов с ДВКЛ с противоположным клиническим ответом на терапию.
Материал и методы исследования
В основу исследования положен анализ двух клинических случаев впервые диагностированной ДВКЛ с идентичной стадией заболевания по классификации Ann Arbor и сопоставимыми значениями международного прогностического индекса (IPI), но принципиально различными клиническими исходами терапии первой линии: достижение полного метаболического ответа и раннее прогрессирование заболевания с летальным исходом.
Все пациенты прошли комплексное клинико-лабораторное и инструментальное обследование в соответствии с действующими стандартами диагностики агрессивных В-клеточных лимфом. Терапия первой линии проводилась по схеме R-CHOP (ритуксимаб 375 мг/м², циклофосфамид 750 мг/м², доксорубицин 50 мг/м², винкристин 1,4 мг/м², преднизолон 100 мг).
Был осуществлен забор периферической крови до начала химиотерапии с последующим проведением общего анализа крови на автоматическом гематологическом анализаторе Mindray BC-30s (Mindray, Китай), оценкой иммунного статуса методом проточной цитометрии, а также выделением мононуклеарных клеток из периферической крови и исследованием влияния берберина на их функциональные характеристики в опытахin vitro. Иммунофенотипированиелейкоцитов периферической крови проводили методом проточнойцитометриинацитофлуориметреBDFACSCanto(BectonDickinson,USA) с использованиемпанелеймоноклональных антител(табл.1) в соответствии с инструкцией фирм-производителей по стандартному протоколу для данного типа исследований.
Таблица1
Панели моноклональных антител
|
Панель |
Набор моноклональных антител |
Производитель моноклональных антител |
|
1 |
CD3 FITC / CD16+CD56 PE / CD45 PcP-Cy5.5 / CD4 PE-Cy7 / CD19 APC / CD8 APC-Cy7 |
BioLegend, USA
|
|
2 |
CD8 BV510 /GranzimB FITC / CD16 PE / HLA-DR PcP-Cy5.5 / CD 56 PE-Cy7 /PerforinAPC / CD45 APC-Cy7 |
BD Biosciences, USA |
|
3 |
CD3 BV421 / CD45 BV605 / CD279 FITC / CD127 PE / CD4 PE-Cy7 / CD25 APC-Cy7 |
BioLegend, USA |
Примечание: составлена авторами на основе использованных материалов в ходе исследования
Вторым этапом работы в ходе экспериментальной части in vitro оценивалось влияние берберина на выделенные мононуклеарные клетки периферической крови. Кровь, собранную в пробирки с ЭДТА (Минимед, Россия), разводили неполной средой RPMI 1640 (Биолот, Россия) в соотношении 1:1 и наносили на фиколл 1,077 г/см3 (Биолот, Россия), после чего центрифугировали 30 мин при 1275 g. Далее собирали кольцо мононуклеаров в приготовленные пробирки с буфером Дальбекко (Биолот, Россия) без ионов кальция и магния, содержащим 2% фетальной коровьей сыворотки (Биолот, Россия), после чего центрифугировали 15 мин при 125 g. В полученной клеточной суспензии проводили подсчет количества живых клеток в камере Горяева с трипановым синим 0,4% (Биолот, Россия). Пролиферативный ответ исследовали с помощью анализа колониеобразования. Известно, что под действием митогенного стимула Т-клетки образуют колонии, являющиеся потомками одной клетки [10].
Оценка количества и размера колоний является классическим подходом при анализе пролиферативной активности Т-клеток под действием различных факторов [11]. В данной работе примененамодифицированнаяверсияклассического протокола, который предполагал использование агара. Мононуклеарные клетки высаживали по 10 тыс. клеток на лунку 96-луночного планшета в полной питательной среде (ППС) RPMI1640 (Биолот, Россия) с добавлением 10% фетальной коровьей сыворотки (Gibco, США).
Предварительно был проведен подбор подходящих концентраций берберина (в данной работе результаты не представлены). В результате тестовых экспериментов было установлено, что при инкубации в течение 72 ч концентрации берберина выше 4мкМ оказывают выраженное цитотоксическое действие на МНПК, в то время как диапазон 1–4мкМ позволяет оценивать функциональные эффекты без значимого снижения жизнеспособности клеток. На основании полученных данных для дальнейших функциональных исследований МНПКin vitroбыли выбраны концентрации берберина 1, 2 и 4мкМ как не оказывающие выраженного цитотоксического действия и позволяющие оценить его иммуномодулирующее влияние.
Для индукции пролиферативного ответа использовали фитогемагглютинин (ФГА) в концентрации 4мкг/мл. Экспериментальные условия включали пробы без митогенной стимуляции (интактный контроль и МНПК с берберином в концентрациях 1, 2 и 4мкМ) и пробы с митогенной стимуляцией (позитивный контроль – МНПК + ФГА, а также МНПК + ФГА в сочетании с берберином в концентрациях 1, 2 и 4мкМ). Каждый вариант опыта выполняли в четырех технических повторах.
Культивирование проводили в течение 72 ч в условиях 5% CO₂ при 37°C. По окончании инкубации в лунки добавляли ядерный краситель Hoechst233342 (Sigma Aldrich, США) (1 мг/мл) с последующей документацией и количественным анализом колоний на автоматическом клеточном анализаторе Lionheart FX (BioTek, США). В исследовании определяли количество колоний (объект с диаметром, превышающим средний диаметр ядра одиночной клетки на изображении) на лунку и среднюю площадь колоний.
Для описания данных использовали среднее значение и стандартное отклонение. Ввиду ограниченного размера выборки (n=2) статистическая обработка данных не проводилась. Интерпретация данных носит описательный и сравнительный характеры. Работа носит пилотный характер и направлена на выявление тенденций и формирование гипотез для последующих исследований на расширенной выборке.
Исследование выполнено с использованием оборудования ЦКП «НМИЦ онкологии» МЗ РФ (рег. № 3554742, https://ckp-rf.ru/catalog/ckp/3554742/).
Результаты исследования и их обсуждение
Клинические характеристики обследованных
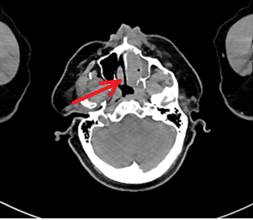
Пациент 1. Мужчина, 69 лет. По данным обследования установлен диагноз ДВКЛ стадии IIАE: выявлено поражение левой верхнечелюстной пазухи, ячеек решетчатой кости слева и левой орбиты (рис.1, А). ИГХ-исследование биоптата мягких тканях левой верхнечелюстной пазухи показало: CD20+, Bcl-2+, MUM1+/-, Bcl-6-/+, CD10-, CD23-, Cyclin D1-, индекс пролиферативной активности Ki-67 – 80%. На основании профиля экспрессии (CD10-, Bcl-6-/+, MUM1+/-) опухоль отнесена к non-GCB подтипу. Сопутствующая патология: ишемическая болезнь сердца, гипертоническая болезнь III стадии, хроническая болезнь почек (ХБП) 3А стадии (расчетная скорость клубочковой фильтрации, рСКФ, по формуле CKD-EPI – 48 мл/мин/1,73 м²), ожирение III степени. Перед началом терапии уровень лактатдегидрогеназы (ЛДГ) был в пределах нормы (167 Е/л). После проведения шести курсов терапии по схеме R-CHOP (ритуксимаб, циклофосфамид, доксорубицин, винкристин, преднизолон), по данным ПЭТ/КТ зарегистрирован полный метаболический ответ.
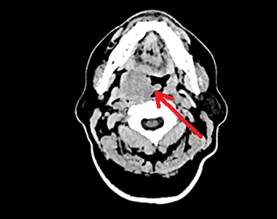
Пациент 2. Мужчина, 63 лет. По результатам обследования установлен диагноз ДВКЛ IIА стадии: выявлено поражение правой небной миндалины и лимфоузлов шеи (рис.1, Б). ИГХ-исследование биоптата лимфоузла шеи справа показало: CD20+, Bcl-2+, Bcl-6+/-, MuM1+, CD10-, c-MYC+/-, индекс пролиферации Ki-67 – ~95%. Морфологическая и иммунофенотипическая характеристика соответствовала ДВКЛ высокой степени злокачественности (High-grade). Сопутствующая патология: ишемическая болезнь сердца, хроническая сердечная недостаточность I стадии (ФК 2), сахарный диабет 2 типа, ХБП смешанного генеза 4 стадии (СКФ по CKD-EPI-27,1 мл/мин/1,73 м²). Перед началом терапии уровень ЛДГ был в пределах нормы (200 Е/л). Пациенту была назначена терапия первой линии по схеме R-CHOP. После проведения первого курса химиотерапии было отмечено раннее прогрессирование заболевания. В связи с резистентностью опухоли и развитием полиорганной недостаточности пациент скончался.
|
А |
Б |
Рис.1. Аксиальный срез компьютерной томографии. Красной стрелкой отмечена область патологического очага. А – пациент 1; Б – пациент 2.
Примечание: составлен авторами по результатам данного исследования
Сводные данные по пациентам представлены в табл. 2.
Таблица2
Сравнительная характеристика пациентов с ДВКЛ
|
Характеристики |
Пациент 1 |
Пациент 2 |
|
Возраст |
69 |
63 |
|
Пол |
мужской |
мужской |
|
Стадия |
2ЕА |
2А |
|
IPI |
1 |
1 |
|
Подтип по данным ИГХ |
non-GCB |
High-grade |
|
Ответ на терапию |
Полный ответ |
Прогрессирование |
Примечание: составлена авторами на основе полученных данных в ходе исследования
Анализ показателей периферической крови, проведенный до начала химиотерапии, позволил выявить различия между пациентами. У пациента с благоприятным клиническим исходом отмечались более высокие исходные значения общего числа лейкоцитов, а также абсолютного содержания нейтрофилов, лимфоцитов и моноцитов. В то же время уровень нейтрофил-лимфоцитарного индекса был ниже по сравнению с пациентом с летальным исходом заболевания (табл.3). Выявленные различия могут свидетельствовать о наличии количественных нарушений иммунной системы у пациента с прогрессирующим течением заболевания.
Таблица3
Лабораторные данные пациентов до начала лечения
|
|
RBC (10*12/л) |
HGB (г/л) |
WBC (10*9/л) |
NEUT (10*9/л) |
LYMPH (10*9/л) |
MONO (10*9/л) |
EO (10*9/л) |
BASO (10*9/л) |
NLR
|
|
Пациент 1 |
4,22 |
130 |
8,2 |
4,52 |
2,52 |
0,88 |
0,18 |
0,07 |
1,8 |
|
Пациент 2 |
5,29 |
140 |
6,08 |
4,1 |
1,43 |
0,4 |
0,08 |
0,03 |
2,9 |
Примечание: RBC – эритроциты, HGB – гемоглобин, WBC – лейкоциты, NEUT – нейтрофилы, LYMPH – лимфоциты, MONO – моноциты, EO – эозинофилы, BASO – базофилы, NLR – нейтрофил-лимфоцитарный индекс.
Составлена авторами на основе полученных данных в ходе исследования
Сравнительный анализ исходного иммунного статуса пациентов продемонстрировал выраженные различия в субпопуляционном составе лейкоцитов периферической крови (рис.2). У пациента с благоприятным клиническим исходом отмечалось повышение абсолютного и относительного содержания лимфоцитов, CD4⁺-клеток, NK- и NKT-клеток, а также T-регуляторных клеток и моноцитов. В то же время у пациента с неблагоприятным исходом преобладали гранулоциты и цитотоксические CD8⁺-клетки.
Выявленные различия могут отражать особенности формирования противоопухолевого иммунного ответа у пациентов с различным клиническим исходом заболевания. Преобладание гранулоцитов и функционально истощенных CD8⁺-клеток у пациента с неблагоприятным исходом может указывать на дисбаланс иммунной регуляции. Накопление гранулоцитарного звена и истощенных CD8⁺-клеток ассоциировано с формированием иммуносупрессивного опухолевого микроокружения, снижением эффективности противоопухолевого иммунного контроля и прогрессированием заболевания, что продемонстрировано, в частности, для ДВКЛ [12]. Аналогично CD8⁺-лимфоцитам, NK-клетки в опухолевом микроокружении могут приобретать истощенный фенотип, что сопровождается снижением их цитотоксической активности и способствует иммунному уклонению опухоли [13]. Напротив, повышенное содержание CD4⁺-клеток, а также сохранность функциональной активности NK- и NKT-клеток, вероятно, отражают более сбалансированное взаимодействие врожденного и адаптивного звеньев иммунной системы и ассоциированы с более эффективным противоопухолевым иммунным надзором [14].
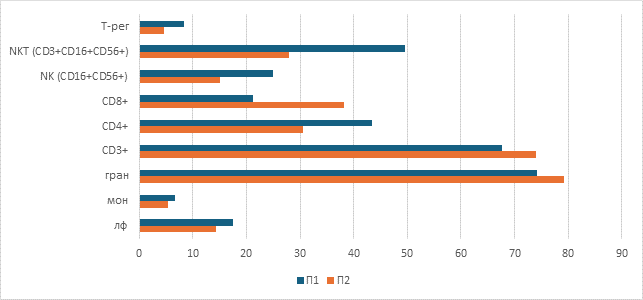
Рис.2. Инициальный иммунофенотип клеток периферической крови пациентов с ДВКЛ. Лф – лимфоциты, мон – моноциты, гран – гранулоциты, Т-реr – Т-регуляторные клетки.
Примечание: составлен авторами по результатам данного исследования
При исследовании чувствительности мононуклеарных клеток периферической крови к берберинуin vitroбыло выявлено стимулирующее влияние берберина на их пролиферативную способность, проявлявшееся увеличением количества и площади формируемых колоний. При этом благоприятный клинический исход ассоциировался не с более высокой базальной колониеобразующей активностью, а с формированием более крупных колоний, что может отражать наличие лимфоцитарных клонов с более высоким пролиферативным и метаболическим потенциалом. Это позволяет предположить, что прогностическое значение может иметь не общее число клеток, а качественные характеристики клонального пролиферативного ответа (рис.3, 4).

Рис.3. Микрофотографии образовавшихся колоний мононуклеарных клеток периферической крови пациента с благоприятным исходом: а – контрольная проба, б – контрольная проба с добавлением ФГА, в – проба с добавлением 1мкмоль/л берберина, г – проба с добавлением 1мкмоль/л берберина и ФГА, д – проба с добавлением 2мкмоль/л берберина, е – проба с добавлением 2мкмоль/л берберина и ФГА, ж – проба с добавлением 4мкмоль/л берберина, з – проба с добавлением 4мкмоль/л берберина и ФГА.
Примечание: составлен авторами по результатам данного исследования

Рис.4. Микрофотографии образовавшихся колоний мононуклеарных клеток периферической крови пациента с неблагоприятным исходом: а – контрольная проба, б – контрольная проба с добавлением ФГА, в – проба с добавлением 1мкмоль/л берберина, г – проба с добавлением 1мкмоль/л берберина и ФГА, д – проба с добавлением 2мкмоль/л берберина, е – проба с добавлением 2мкмоль/л берберина и ФГА, ж – проба с добавлением 4мкмоль/л берберина, з – проба с добавлением 4мкмоль/л берберина и ФГА.
Примечание: составлен авторами по результатам данного исследования
У пациента с благоприятным клиническим ответом изначально отмечалась более низкая базальная колониеобразующая активность МНПК: количество колоний было на 56% меньше по сравнению с пациентом с рефрактерным течением заболевания, однако их средняя площадь превышала данный показатель на 22%. Воздействие берберина в исследованных концентрациях вызывало дозозависимое усиление колониеобразующей способности МНПК у обоих пациентов, при этом наибольшая стимуляция наблюдалась при сочетанном применении берберина и фитогемагглютинина, что свидетельствует о синергическом эффекте изучаемого соединения с митогенной стимуляцией (рис.5, 6). Использование ФГА позволило оценить влияние берберина в условиях активированной иммунной реакции, что приближаетмодель in vitro к условиям реализации противоопухолевого иммунного ответаin vivo.
Кроме того, были выявлены индивидуальные различия в чувствительности МНПК к берберину: у пациента с полным ответом на терапию наибольшее увеличение количества колоний наблюдалось при концентрации 1мкмоль/л, тогда как у пациента с неблагоприятным исходом пик пролиферативного ответа смещался на 2мкмоль/л (рис.5). Полученные различия могут объясняться особенностями метаболической и пролиферативной активности отдельных лимфоцитарных клонов. Более крупные колонии у пациента с благоприятным исходом могут отражать наличие клонов с высоким метаболическим потенциалом и способностью к интенсивному клеточному делению, тогда как большее число, но мелких колоний у пациента с неблагоприятным исходом может соответствовать функционально менее активным клональным линиям.
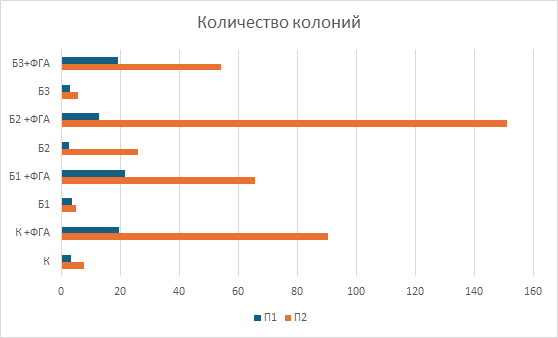
Рис.5. Количество образовавшихся колоний мононуклеарных клеток периферической крови при добавлении различных концентраций берберина. К – контроль, К + ФГА – контроль + ФГА, Б1 – берберин 1мкмоль, Б1 + ФГА – берберин 1мкмоль + ФГА, Б2 – берберин 2мкмоль, Б2 + ФГА – берберин 2мкмоль + ФГА, Б3 – берберин 4мкмоль, Б3 + ФГА – берберин 4мкмоль + ФГА.
Примечание: составлен авторами по результатам данного исследования
Анализ средней площади колоний позволил оценить качественные характеристики пролиферативного ответа МНПК при воздействии берберина и его комбинаций с ФГА (рис.6). У пациента с благоприятным клиническим исходом колонии отличались более крупными размерами, что указывает на наличие лимфоцитарных клонов с высоким пролиферативным и метаболическим потенциалом. Эти наблюдения подчеркивают, что размер колонии, а не только общее количество пролиферирующих клеток может быть важным показателем функциональной активности клеточных клонов и их потенциальной способности к эффективному противоопухолевому иммунному надзору.
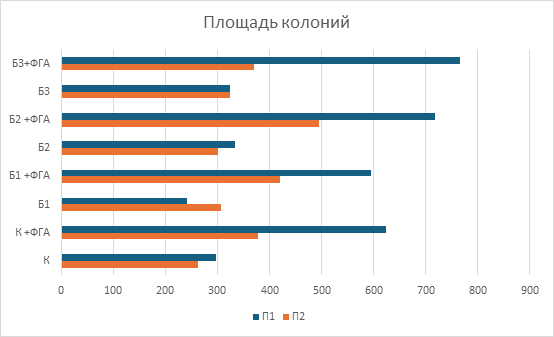
Рис.6. Средняя площадь образовавшихся колоний мононуклеарных клеток периферической крови при добавлении различных концентраций берберина.
К – контроль, К + ФГА – контроль + ФГА, Б1 – берберин 1мкмоль, Б1 + ФГА – берберин 1мкмоль + ФГА, Б2 – берберин 2мкмоль, Б2 + ФГА – берберин 2мкмоль + ФГА, Б3 – берберин 4мкмоль, Б3 + ФГА – берберин 4мкмоль + ФГА.
Примечание: составлен авторами по результатам данного исследования
Представленное описание двух случаев выявило различия в исходном иммунном статусе, функциональной активности мононуклеарных клеток периферической крови и их чувствительности к берберину in vitro у пациентов с противоположным клиническим ответом на терапию ДВКЛ. Следует отметить, что наблюдаемые различия могут быть связаны не только с воздействием берберина, но и с исходными биологическими различиями опухолевых клеток, в частности с различными молекулярными подтипами [15]. Полученные данные соответствуют результатам других исследований, демонстрирующих важную роль иммунного микроокружения в патогенезе ДВКЛ и ответа на терапию [2, 16].
Выявленные иммунофенотипические различия, в частности более высокое содержание NK-клеток и соотношение CD4+/CD8+-лимфоцитов у пациента с благоприятным прогнозом, согласуются с литературными данными о важности клеточного иммунитета в контроле над опухолевым ростом при лимфопролиферативных заболеваниях [17, 18].
Заключение
В работе на примере двух клинических случаев ДВКЛ показано, что функциональное состояние мононуклеарных клеток периферической крови и их реакция на иммуномодулирующее воздействие берберинаin vitroмогут различаться в зависимости от клинического исхода. Наблюдения указывают на потенциальную значимость качественных характеристик пролиферирующих клеток, таких как размер колоний и метаболический потенциал, а также исходного иммунного статуса для формирования эффективного противоопухолевого ответа. Полученные данные обосновывают необходимость дальнейших исследований на более широких выборках для подтверждения выявленных тенденций.
Conflict of interest
Financing
Библиографическая ссылка
Казанчян М.С., Сагакянц А.Б., Лысенко И.Б., Филиппова С.Ю., Бондаренко Е.С., Межевова И.В., Златник Е.Ю., Гайсултанова Я.С. ВЛИЯНИЕ БЕРБЕРИНА НА ФУНКЦИОНАЛЬНЫЕ СВОЙСТВА МОНОНУКЛЕАРНЫХ КЛЕТОК ПЕРИФЕРИЧЕСКОЙ КРОВИ У ПАЦИЕНТОВ С ДИФФУЗНОЙ В-КЛЕТОЧНОЙ КРУПНОКЛЕТОЧНОЙ ЛИМФОМОЙ С РАЗЛИЧНЫМ ОТВЕТОМ НА ТЕРАПИЮ // Современные проблемы науки и образования. 2026. № 5. ;URL: https://science-education.ru/en/article/view?id=34575 (дата обращения: 29.04.2026).
DOI: https://doi.org/10.17513/spno.34575