Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
PERSONALIZED EYE MODELS FOR DETERMINING OPTIMIZED INTRAOCULAR LENSES POWER
Введение
Современные тенденции развития офтальмологии устанавливают новые критерии и требования к результатам хирургического лечения катаракты, включающие получение высокого функционального результата на разных дистанциях и повышение расчетной точности существующих формул. Выполнение первого условия напрямую обусловлено потребностями пациента и зависит от нескольких факторов: условий работы, образа жизни и наличия увлечений. При этом, согласно принятым стандартам попадания в рефракцию цели, значения должны находиться в пределах ±0,50 дптр более чем в 70% случаев и ±1,00 дптр более чем в 90% глаз [1].
Особую сложность представляют пациенты, имеющие кераторефракционные операции в анамнезе, такие как радиальная кератотомия (РКТ) и рефракционно-лазерные вмешательства. Хирургические вмешательства, выполненные с рефракционной целью, вызывают изменения передней и задней поверхностей роговицы. Деформация роговицы в большинстве случаев приводит к неравномерному и неправильному распределению ее преломляющей силы вдоль основных меридианов, что особенно характерно для пациентов после РКТ. Следствием наличия такой иррегулярности может стать невозможность точного определения преломляющей силы роговицы в центральной зоне и использование усредненных значений последней, что ведет к неправильному прогнозированию эффективной позиции интраокулярной линзы (ИОЛ), получению заниженных значений оптической силы ИОЛ и значительных отклонений в расчетах, сопровождающихся непредсказуемым функциональным результатом [2].
В настоящее время установлено 6 основных топографических типов деформаций роговицы после РКТ в зависимости от вида ее элевационного профиля [3]. Процесс изменений роговицы после РКТ многофакторен и зависит от методики выполнения роговичных разрезов, морфологических изменений самой роговицы, влияющих на ее биомеханические свойства, внутриглазного давления, типа рубцевания и др. Все эти факторы оказывают непосредственное влияние на прогнозирование послеоперационного рефракционного результата. По данным литературы, существующие методы расчета на посткератотомических глазах позволяют достигать рефракции цели в пределах ±0,5 дптр в 29-48% случаев, в пределах ±1,00 дптр – в 65% [4].
В настоящее время существуют различные подходы, направленные на повышение достижения запланированного рефракционного результата у пациентов после РКТ [5-7]. Использование расчетов, основанных на предоперационных значениях кривизны роговицы, не всегда возможно ввиду их ограниченности. Разработанные формулы, включающие поправки в зависимости от толщины роговицы, чаще основаны на эмпирическом подходе и характеризуются сложностью применения [8-10]. Вместе с тем для расчета оптической силы ИОЛ в данной группе пациентов необходим учет не только преломляющей силы в центральной зоне, но и анализ всей поверхности роговицы ввиду ее выраженной нерегулярности. В связи с этим требуется разработка нового, более совершенного способа расчёта оптической силы ИОЛ, позволяющего достоверно прогнозировать итоговый рефракционный результат операции.
Одним из способов, направленным на повышение точности расчетов, является метод трассировки лучей. Данный метод позволяет моделировать процесс прохождения световых лучей через преломляющие элементы глаза в каждом конкретном случае посредством построения персонализированной модели глазного яблока. К преимуществам метода относятся независимость результата от использования кератометрического индекса и отсутствие необходимости учитывать эффективную позицию ИОЛ. Точность полученных расчетов не зависит от биометрических параметров и особенностей преломляющих поверхностей, что особенно актуально для пациентов после кераторефракционных вмешательств в анамнезе. В настоящее время метод трассировки лучей используется некоторыми фирмами-производителями в онлайн-калькуляторах. Примером применения способа трассировки лучей в расчете силы ИОЛ без использования элементов искусственного интеллекта (ИИ) является формула Olsen Phaco Optics (IOL InnovationsApS, Орхус, Дания) и программное обеспечение Okulix IOL (Okulix, Дортмунд, Германия), доступные в коммерческих топографах. Калькулятором, совмещающим подход ИИ с трассировкой лучей, является калькулятор Zeiss AI IOL [11], который имеет ограничения для пациентов после кераторефракционных операций. Одним из путей решения может быть разработка алгоритма, основанного на последовательном построении индивидуальной модели глаза с помощью специального программного обеспечения, предназначенного для проектирования и моделирования оптических систем, включая создание 3D-модели роговицы.
Программное обеспечение Ansys Zemax OpticStudio (Ansys, Inc., США) позволяет выполнить моделирование передней и задней поверхностей роговицы с учетом присущих посткератотомическим глазам нерегулярных деформаций и реализовать возможность геометрического построения хода световых лучей с расчетом их отклонений при прохождении через последовательно расположенные оптические среды. Использование режима non-sequential делает возможным анализ рассеяния, отражения и взаимодействия лучей света, а использование в качестве предикторов качества зрения передаточной функции модуляции (MTF) и функции рассеяния точки (PSF) позволяет оптимизировать выбор оптической силы ИОЛ.
Целью исследования стала разработка и тестирование метода расчета оптической силы ИОЛ на основе построения персонализированной модели глаза у пациентов с иррегулярной роговицей.
Материал и методы исследования
С целью разработки модели глаза было использовано программное обеспечение Ansys Zemax OpticStudio 2023 R1 (Ansys, Inc., США). Моделирование прохождения света через основные преломляющие поверхности в артифакичном глазу проводилось в режиме non-sequential. Режим non-sequential позволяет проводить расчет хода луча в сложных трехмерных оптических системах, которые не описываются простой моделью последовательных поверхностей, в том числе через тела и объекты, построенные в системе автоматизированного проектирования (САПР).
Модель глаза строилась на основании следующих базовых параметров: данных о поверхности роговицы (облако точек, описывающие отдельно переднюю и заднюю поверхность), радиусы кривизны передней и задней поверхностей ИОЛ, толщина ИОЛ, положение поверхности сетчатки. Для каждой оптической структуры были заданы соответствующие показатели преломления: роговица –1,376, ИОЛ – 1,492, стекловидное тело – 1,336.
ИОЛ описывалась как оптическая линза с заданными значениями толщины, радиуса кривизны передней и задней поверхностей. Определение толщины ИОЛ проводилось в программе «Компас-3D LTV 12» («Аскон», Россия) по известным значениям передней и задней кривизны, а также диаметру линзы. Зрачок был задан как диафрагма диаметром 4,0 мм с центром на оптической оси глаза. Диаметр смоделированной поверхности роговицы составил 8,0 мм. Данные о параметрах роговицы были получены путем экспорта измерений оптического когерентного томографа переднего отрезка (ОКТ) Casia 2 (Tomey, Япония). Биометрические параметры глазного яблока были получены с помощью оптического биометра АО-2000 (Tomey, Япония).
В исследование вошли 19 пациентов с фемтолазер-ассистированной факоэмульсификацией катаракты и РКТ в анамнезе. Из них 10 женщин, 9 мужчин. Средний возраст составил 65±7,23 года. Фемтосопровождение осуществлялось на приборе Catalys (Johnson & Johnson, США). Средние предоперационные значения передне-задней длины глаза составили 25,51±1,11 мм, глубины передней камеры - 3,32±0,27 мм, толщины хрусталика - 4,46±0,38 мм. Центральная толщина роговицы была равна 0,530±0,03 мм, средние значения кератометрии сильного и слабого меридианов по данным кератотопографа составили 37,82±2,74 и 36,18±2,73 дптр соответственно.
Во всех случаях была имплантирована ИОЛ – РПР-2 («Репер НН», Н. Новгород), расчетные значения которой определялись на основании анализа существующих формул с применением индивидуальных поправок хирурга. Сравнительный анализ эффективности разработанного метода проводился ретроспективно с расчетными значениями, выполненными по формуле Hoffer QST (https://hofferqst.com/) и калькулятора ASCRS (www.ascrs.org) путем вычисления средней абсолютной ошибки (MedAE) с оптической силой фактически имплантированной ИОЛ [12; 13]. Во всех случаях целевая рефракция была максимально приближена к эмметропии.
Для выполнения поставленной цели была определена последовательность этапов построения модели глаза:
1) получение информации о геометрии поверхностей роговицы по данным ОКТ в виде облака точек с последующим 3D-моделированием роговицы в САПР;
2) импорт 3D-модели роговицы в модель глаза, построенную в программе Ansys Zemax OpticStudio;
3) расчёт имитационной модели методом трассировки лучей и определение оптимальной оптической силы ИОЛ;
4) оценка качества изображения посредством определения конфигурации оптической системы с наибольшими значениями MTF и определения PSF (рис. 1). MTF оценивалась с использованием двух компонентов, описывающих ориентацию линий: Sagittal - радиальное расположение линий и Tangential - меридиональное расположение линий.
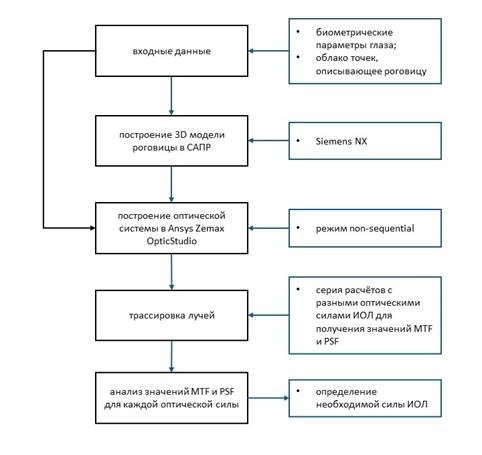
Рис. 1. Блок-схема разработанного алгоритма.
Примечание: составлено авторами на основе полученных данных в ходе исследования
Создание 3D-модели роговицы – многоэтапный процесс. У роговицы две поверхности: передняя и задняя, поэтому по данным ОКТ в САПР импортировалось два облака точек, каждое из которых описывало отдельную поверхность. При этом данные высот позволяли дать полное пространственное описание поверхности роговицы, создавая ее реальную трехмерную геометрию. Результат моделирования роговицы представляет собой объект, состоящий из множества треугольников, вершинами которых являются точки, получаемые при сканировании (стереолитография).
Построение поверхности по точкам производилось с некоторым приближением: точки аппроксимировались полиномом некоторой степени. Для исключения влияния степени аппроксимации на результаты трассировки определялась степень полинома, выше которой изменение описываемой поверхности не влияло на результат трассировки и, следовательно, на выбор необходимой оптической силы ИОЛ.
На этапе создания имитационной модели глазного яблока положение ИОЛ в оптической системе определялось на основании расчета прогнозируемой глубины передней камеры по формуле (1):
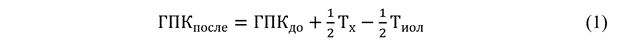
 где ГПКпосле – глубина передней камеры после операции, мм; ГПКдо – глубина передней камеры до операции, мм; Тх – толщина хрусталика, мм, Тиол – толщина ИОЛ, мм.
где ГПКпосле – глубина передней камеры после операции, мм; ГПКдо – глубина передней камеры до операции, мм; Тх – толщина хрусталика, мм, Тиол – толщина ИОЛ, мм.
Параметры ИОЛ, подлежащие анализу, импортировались в персонализированную модель глаза для расчета. Выбор ИОЛ проводился на основании нахождения такой конфигурации оптической системы, при которой MTF имела наиболее высокие значения согласно разработанному патенту (Патент 2814629 РФ от29.06.2023. Способ расчета оптической силы интраокулярной линзы на основе персонализированного моделирования глаза / Тимофеева Н. С., Поздеева Н. А., Абраменко Д. Б., Тимофеев Н. С.) [14]. Анализ PSF позволял определить оптимальную преломляющую силу ИОЛ на основании значений среднего радиуса пятна RMS Spot Radius. Данный параметр описывал эффект фокусировки лучей, прошедших через оптическую систему смоделированного глаза, на плоскости сетчатки – чем меньше было его значение, тем выше была четкость изображения.
Эффективность применяемых методов расчета оценивалась по данным сферического компонента рефракции и сфероэквивалента (СЭ) через 3 месяца после операции. Статистический анализ выполнялся с использованием программного обеспечения Statistica 10. Нормальность распределения данных оценивалась с помощью теста Шапиро - Уилка. Различия между данными оценивались с использованием U-критерия Манна - Уитни и Краскела - Уоллиса. Для всех исследований значение р<0,05 считалось статистически значимым.
Результаты исследования и их обсуждение
Во всех случаях было получено улучшение показателей некорригированной (НКОЗ) и корригированной остроты зрения (КОЗ). НКОЗ после операции повысилась с 0,13±0,07 до 0,6±0,18, КОЗ – с 0,49±0,25 до 0,85±0,13. Средние послеоперационные значения сферического компонента рефракции составили 0,65±0,41 дптр и определялись в пределах от -0,75 до 1,25 дптр, СЭ был равен 0,91±0,86 дптр с разбросом от -2,13 до 0,5 дптр.
Полученные значения MedAE показали статистически значимую разницу между результатами персонализированного моделирования и средними значениями, полученными по ASCRS (р=0,000) и формуле Hoffer QST (р=0,003) с наименьшими значениями в группе персонализированного моделирования (табл. 1).
Таблица 1
Сравнительный анализ значений средней абсолютной ошибки (MedAE)
|
Методы расчета оптической силы ИОЛ |
Значения средней абсолютной ошибки Ме (Min-Mаx) |
р |
|
1Персонализированное моделирование |
0,25 (0,00-1,25) |
р=0,000 р1-2=0,000 р1-3=0,003 р2-3=0,059 |
|
2ASCRS |
1,77 (0,58-2,90) |
|
|
3Hoffer QST |
0,75 (0,00-3,15) |
Примечание: составлено авторами на основе полученных данных в ходе исследования.
Для каждого из анализируемых случаев был оценен средний радиус пятна RMS Spot Radius. На рисунке 2 приведена точечная диаграмма сравнительного анализа значений RMS Spot Radius, полученных по формулам ASCRS, Hoffer QST, фактически установленным ИОЛ и значениям, полученным в результате персонализированного моделирования. Пятно рассеяния (PSF), полученное методом персонализированного моделирования, обеспечивало наименьшие значения RMS Spot Radius.
Сферический компонент рефракции находился в пределах ±0,5 дптр в группе персонализированного моделирования в 94,74% анализируемых случаев, в группе ASCRS - в 15,78%, в группе Hoffer QST - в 31,5%. Рефракционный результат в пределах ±1,0 дптр в группе персонализированного моделирования был достигнут в 100% случаев, в группе ASCRS - в 42,1%, Hoffer QST - в 63,2%. СЭ в пределах ±0,5 дптр в группе персонализированного моделирования составил 47,4%, ASCRS - 15,8%, Hoffer QST - 26,3%. СЭ в пределах ±1,0 дптр в группе персонализированного моделирования был зафиксирован в 79% случаев, ASCRS - в 57,8%, Hoffer QST – в 63,1% (рис. 3 и 4).
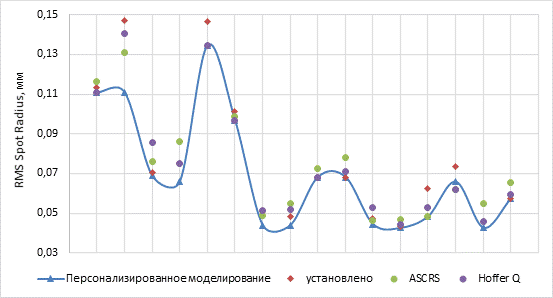
Рис. 2. Значения RMS Spot Radius в зависимости от методов расчета оптической силы ИОЛ. Примечание: составлено авторами по результатам данного исследования
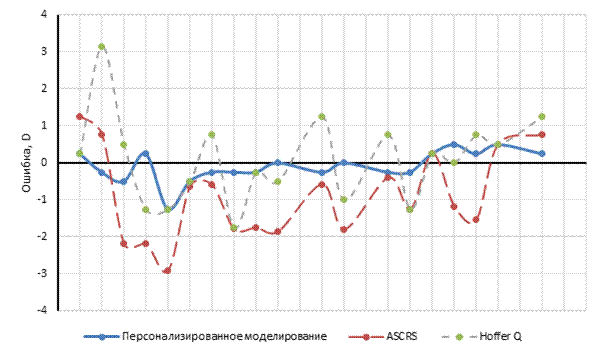
Рис. 3. Отклонения по сферическому компоненту рефракции предсказанной оптической силы ИОЛ. Примечание: составлено авторами по результатам данного исследования
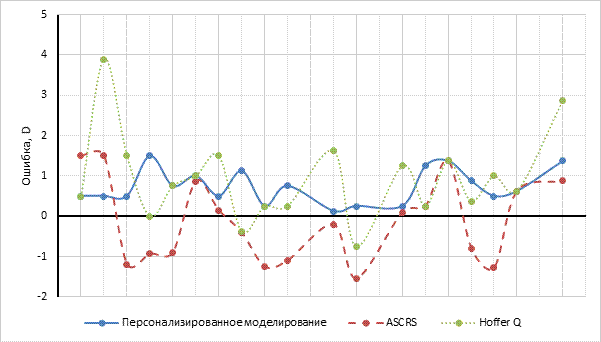
Рис. 4. Отклонения по СЭ предсказанной оптической силы ИОЛ.
Примечание: составлено авторами по результатам данного исследования
В качестве примера расчета оптической силы ИОЛ приведен клинический случай пациента с РКТ в анамнезе. На рисунке 5 представлены графики MTF, вычисленные методом трассировки лучей с использованием оптической силы линз 22,0-25,0 дптр. Также в качестве анализируемого параметра рассматривался средний размер RMS Spot Radius (табл. 2, 3; рис. 6). В результате была выбрана линза с оптической силой 24,0 дптр, обеспечившая попадание в рефракцию цели по сферическому компоненту рефракции, СЭ и обеспечившая наилучшие показатели RMS Spot Radius.
Таблица 2
Расчет предсказанной рефракции оптической силы ИОЛ
|
Метод расчета |
Результат расчёта, дптр |
Отклонение от рефракции цели, дптр |
|
Персонализированное моделирование |
24,0 |
0,25 |
|
ASCRS |
23,0 |
0,75 |
|
Hoffer QST |
25,5 |
1,25 |
Примечание: составлено авторами на основе полученных данных в ходе исследования.
Таблица 3
Оптическая сила ИОЛ, рассчитанная методом персонализированного моделирования по данным MTF и RMS Spot Radius
|
Параметры расчета |
22,0 дптр |
23,0 дптр |
24,0 дптр |
25,0 дптр |
|
|
Geometric MTF |
Tangential |
73,58754 |
75,1872 |
63,60325 |
45,398 |
|
Sagittal |
38,34732 |
45,04224 |
55,42378 |
70,2751 |
|
|
RMS Spot Radius |
0,065776 |
0,058407 |
0,055881 |
0,059394 |
|
Примечание: составлено авторами на основе полученных данных в ходе исследования.
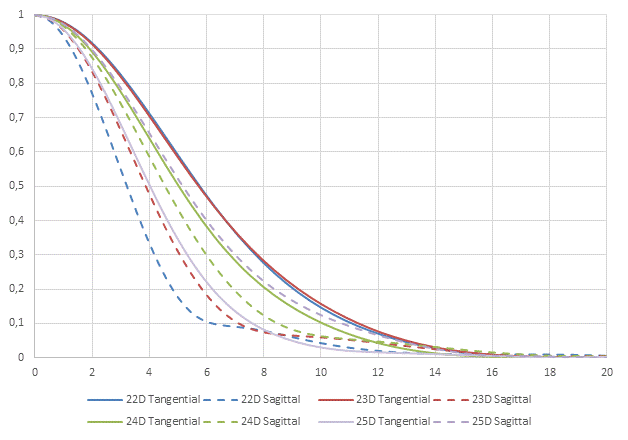
Рис. 5. Графики MTF для ИОЛ 22,0-25,0 дптр. Примечание: составлено авторами по результатам данного исследования
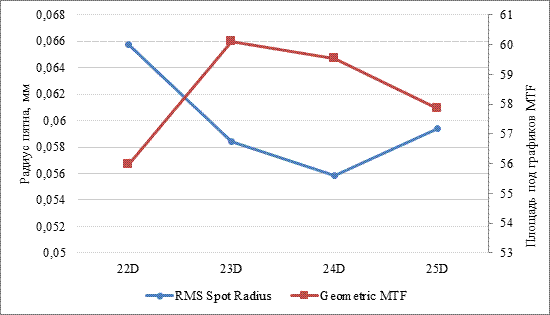
Рис. 6. График площади MTF и величины радиуса пятна для ИОЛ 22,0-25,0 дптр. Примечание: составлено авторами по результатам данного исследования
На рисунке 7 приведены пятна рассеяния, получаемые в результате трассировки с применением линз с оптической силой 23,0, 24,0 и 25,0 дптр, на которых видно, что максимальные значения отдельных компонентов MTF приводят к получению вытянутых пятен. При этом линза 24,0 дптр, несмотря на то что она не обеспечивает получение предельных значений компонента MTF, демонстрирует равномерное (близкое к круглому) пятно рассеивания.
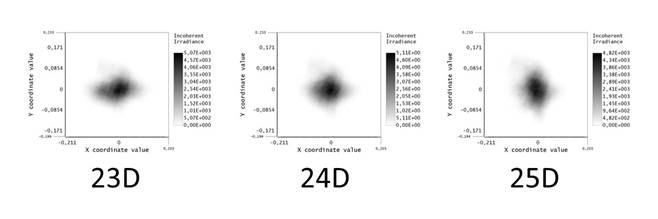
Рис. 7. Пятна рассеяния, полученные в результате использования ИОЛ 23,0-25,0 дптр. Примечание: составлено авторами по результатам данного исследования
Применение теоретических формул, базирующихся на принципах Гауссовской оптики, демонстрирует высокую эффективность в подборе силы оптической коррекции у пациентов со среднестатистическими биометрическими параметрами и интактной роговицей. Но могут вызывать значительные погрешности в определении эффективной позиции ИОЛ у пациентов с хирургически измененной формой роговицы [15]. Сложность расчета обусловлена сильным уплощением роговицы и невозможностью точного определения ее преломляющей силы. Использование данных только центральной зоны роговицы может привести к ошибочным представлениям о радиусах кривизны всей корнеальной поверхности. При этом изменения основных параметров роговицы на глазах с РКТ, как правило, имеют выраженную полиморфность со значительным вкладом задней поверхности роговицы, что требует использования приборов, способных анализировать обе поверхности роговицы [16].
Моделирование роговицы является основной и самой трудоемкой задачей при работе с измененными и нерегулярными поверхностями. Учитывая наличие различных деформаций роговицы у пациентов после РКТ, необходимо, помимо стандартных значений крутого и плоского меридианов, использовать показатели офтальмологических приборов, измеряющих переднюю и заднюю поверхности роговицы в различных точках трехмерной системы координат.
В настоящее время для создания имитационной модели оптической системы глаза можно использовать ОКТ и кератотопографы на основе Шеймплюг-сканирования. Данные приборы имеют отличия в технологии проведения сканирования и используемой длины волны [17]. Особенно перспективным в настоящее время является применение прибора Sirius (CSO, Scandicci, Италия), который, благодаря сочетанию Шеймпфлюг-камеры и колец Пласидо, создает трёхмерное изображение переднего сегмента глазного яблока. Помимо точного измерения высоты, кривизны, преломляющей силы и толщины роговицы, программное обеспечение формирует координаты точек, лежащих на поверхности роговицы, что позволяет выполнять процесс математической интерполяции и точного воспроизведения геометрии передней и задней поверхностей для последующего воссоздания оптических изменений [18].
Функциональность оптического когерентного томографа Casia 2 основана на методе преобразования сигнала Фурье между измерительным, направленным на исследуемые ткани, и эталонным лучами (принцип оптической рефлектометрии). Полученная разница во времени фиксации прохождения лучей позволяет с помощью детектора и компьютерного анализа напрямую формировать трехмерное изображение исследуемых поверхностей с данными о высотах роговицы в цилиндрических координатах, обеспечивая высокую точность и воспроизводимость измерений поверхностей и толщины роговицы [16; 19]. Данный подход очень важен в сложных клинических ситуациях, сопровождающихся выраженной нерегулярностью. Он не учитывает физические процессы, оказывающие влияние на сферическую форму роговицы (внутриглазное давление, отек роговицы и др.), а использует фактическую (реальную) модель роговицы.
Оптическая модель глаза представляет собой пять последовательно расположенных структур (роговица, зрачок, хрусталик/ИОЛ, стекловидное тело, сетчатка). По данным литературы, ошибки в прогнозировании глубины передней камеры являются наиболее частой причиной непопадания в рефракцию цели и могут составлять до 42% [20]. Доказанным считается наличие корреляции между длиной глаза и глубиной передней камеры, что служит важным ориентиром при проведении расчета по различным формулам для тонких линз. Эффективная позиция линзы (ELP) часто коррелирует с другими клиническими переменными, такими как осевая длина, кривизна роговицы, глубина передней камеры до операции, формируя множественную зависимость. При этом ELP при построении индивидуальной имитационной модели заменяется на прогноз фактического положения ИОЛ.
Полученные в ходе персонализированного моделирования результаты продемонстрировали высокий процент попадания послеоперационных значений рефракции в пределы ±0,5 дптр (94,74%) и ±1,0 дптр (100%), что значительно превышает эффективность расчета с помощью трассировки лучей, представленную Thomas О. в 2012 г. (± 0,50 дптр в 79,6%) [20].
При расчете оптической силы линзы также важно учитывать дизайн ее оптической части. В настоящем исследовании использовался каталог сферических ИОЛ, оптическая часть которых представляет собой полусферу с постоянным радиусом кривизны, имеющим одинаковую преломляющую силу от центра к периферии. Это позволило нам проводить расчет глубины передней камеры, основываясь на использовании биометрических значений, измеренных до операции, включая определение толщины хрусталика в центре, и 1/2 толщины оптической части ИОЛ в центре. Одновременно в процессе подбора подходящей оптической силы ИОЛ в модели изменялась только толщина расчетной линзы. За счёт того, что расположение поверхностей задаётся в абсолютных координатах изменение формы и размеров линзы не оказывает влияние на корректировку положения сетчатки. Это отличает предложенный алгоритм от используемых в формулах третьего поколения, в которых положение ИОЛ рассчитывается согласно эмпирическим формулам, или четвертого поколения, использующих для этого оптимизируемые константы и ИИ [21]. При этом точность расчета оптической силы линзы ограничивается прогнозируемой послеоперационной остаточной рефракцией, выраженной в диоптриях, в то время как трассировка лучей потенциально может учитывать объективные показатели качества зрения, коррелирующие с рефракцией [22].
В данном исследовании определение оптимальной силы ИОЛ выполнялось согласно предикторам качественных характеристик зрения: передаточной функции модуляции (MTF) и функции рассеяния точки (PSF). В ходе проведенного анализа были выявлены случаи, когда максимизация одного из компонентов MTF не приводила к получению пятна с наименьшими диаметром. Для получения наиболее симметричного пятна MTF Sagittal и MTF Tangential должны иметь приблизительно одинаковые значения. Приведенный клинический пример позволил продемонстрировать, как изменения кривизны поверхностей роговицы в противоположных меридианах могут сказываться на качестве получаемого изображения и выборе оптической силы ИОЛ.
В литературе имеется ряд исследований, выполненных с помощью математического численного моделирования, целью которых было получение количественной информации об изменениях преломляющей силы и описание напряженного состояния роговицы, в том числе для предсказания рефракционного эффекта после РКТ и кераторефракционных операций [23; 24]. Исследования возможности применения метода моделирования для расчета оптической силы ИОЛ, в том числе у пациентов после операции «Лазик», были описаны в работе F. J. Ribeiro [25]. Применение моделирования оптической системы также позволяет решать сложные вопросы, связанные с прогнозированием влияния оптических конструкций на величину и компенсацию различных видов аберраций, позволяя совершенствовать существующие подходы к интраокулярной коррекции с целью достижения максимально возможных визуальных показателей [26]. В данном аспекте использование персонализированного моделирования открывает широкие возможности перед практикующими хирургами, основанные на теоретическом предоперационным анализе качества послеоперационного зрения.
Таким образом, данные проведенного исследования продемонстрировали, что разработанный метод персонализированного моделирования имеет перспективы у наиболее сложных групп пациентов, имеющих отличные от стандартных кератометрические и биометрические параметры и трудно поддающиеся систематизации деформации роговицы, к которым можно отнести пациентов после РКТ. Проведенный сравнительный анализ установил меньшее значение остаточной аметропии при расчете оптической силы ИОЛ методом персонализированного моделирования на основе трассировки лучей по сравнению с использованием онлайн-калькулятора ASCRS или формулы Hoffer QST. Клинический пример продемонстрировал эффективность использования моделирования геометрических поверхностей у пациентов с измененной роговицей после перенесенной ранее РКТ.
Заключение
Предложенный метод персонализированного моделирования глаза, основанный на трассировке лучей, позволяет с высокой точностью создавать трехмерную поверхность роговицы, точно прогнозировать положение оптической части ИОЛ после операции по замене хрусталика и анализировать возможность получения оптимальных рефракционных и качественных характеристик остроты зрения в послеоперационном периоде.
Conflict of interest
Financing
Библиографическая ссылка
Тимофеева Н.С., Тимофеев Н.С. ПЕРСОНАЛИЗИРОВАННОЕ МОДЕЛИРОВАНИЕ ДЛЯ РАСЧЕТА ОПТИЧЕСКОЙ СИЛЫ ИНТРАОКУЛЯРНЫХ ЛИНЗ // Современные проблемы науки и образования. 2026. № 4. ;URL: https://science-education.ru/en/article/view?id=34570 (дата обращения: 13.05.2026).
DOI: https://doi.org/10.17513/spno.34570



