Введение
Химиоэмболизация – один из современных высокоэффективных рентгенэндоваскулярных методов лечения новообразований различных локализаций, суть которого заключается в локальной химиотерапии злокачественных новообразований путем эмболизации питающей опухоль артерии эмболизирующим материалом, содержащим противоопухолевый препарат [1–3]. Данное вмешательство, благодаря эффективности и меньшей травматичности, применяется как альтернатива хирургическому удалению объемных образований [4–6].
Несмотря на высокую эффективность, данный метод, как и любое другое инвазивное вмешательство, сопровождается рядом осложнений, одним из которых является постэмболизационный синдром, который представляет собой неспецифическую воспалительную реакцию в ответ на ишемию и некроз тканей, которые ранее кровоснабжались от эмболизированной артерии. Частота встречаемости данного осложнения значительно варьирует, что обусловлено сложностью диагностики и отсутствием четких клинических критериев [7–9].
Основными клинико-лабораторными проявлениями постэмболизационного синдрома являются боль, гипертермия, диспепсия, лейкоцитоз, нарушения коагуляции [10–12].
Согласно современным представлениям о патогенезе постэмболизационного синдрома, вследствие контролируемой ишемии и некроза опухолевой паренхимы происходит локальная активация медиаторов воспаления (гистамин, серотонин, простагландины, лейкотриены, кинины), накопление продуктов некроза тканей, отек опухолевого узла со сдавлением окружающих тканей, раздражение ноцицепторов. В то же время формирование коллатерального кровообращения способствует распространению указанных биологически активных веществ в системном кровотоке, что обусловливает системные проявления данного осложнения [13–15].
В связи с этим важнейшим компонентом анестезиологического пособия у пациентов с высоким риском развития постэмболизационного синдрома является эффективная коррекция болевого синдрома и воспалительной реакции в течение всего периоперационного периода.
Цель исследования – сравнительная оценка эффективности различных способов коррекции боли как одного из проявлений постэмболизационного синдрома у пациентов, подвергшихся химиоэмболизации новообразований печени.
Материал и методы исследования
В проведенном проспективном одноцентровом рандомизированном контролируемом исследовании за период с марта по декабрь 2025 г. приняли участие 40 пациентов, сопоставимых по возрасту, полу, нозологии, объему вмешательства и длительности процедуры. Главными критериями включения пациентов в исследование было наличие новообразований печени (гепатоцеллюлярный рак или метастазы при колоректальном раке), а также наличие показаний, клинической целесообразности и технической возможности выполнения процедуры химиоэмболизации. По физикальному статусу и выраженности системных нарушений, связанных или не связанных с основной хирургической патологией, все участники исследования были отнесены к II классу по шкале ASA. Учитывая объем, характер и специфику хирургического вмешательства, оптимальным методом проведения анестезиологического пособия были выбраны местная анестезия и анестезиологическое сопровождение. Все пациенты, включенные в исследование, были разделены на четыре группы.
У пациентов группы 1 (n=10) коррекция болевого синдрома осуществлялась по мере его возникновения интраоперационно или в раннем послеоперационном периоде с использованием комбинации парентеральных форм парацетамола, нестероидных противовоспалительных препаратов (декскетопрофен) с добавлением опиоидных анальгетиков (тримеперидин) в случае недостаточной эффективности указанной комбинации.
Коррекция болевого синдрома у пациентов группы 2 (n=10) осуществлялась по мере его возникновения интраоперационно или в раннем послеоперационном периоде с использованием комбинации парентеральных форм парацетамола, нестероидных противовоспалительных препаратов (декскетопрофен) и препарата нефопам внутримышечно в случае недостаточной эффективности указанной комбинации.
Пациентам группы 3 (n=10) комбинация парентеральных форм парацетамола, нестероидных противовоспалительных препаратов (декскетопрофен) назначалась в премедикацию за 40 мин до начала оперативного вмешательства.
Пациентам группы 4 (n=10) комбинация парентеральных форм парацетамола, нестероидных противовоспалительных препаратов (декскетопрофен) назначалась в премедикацию за 40 мин до начала оперативного вмешательства, с началом введения препарата нефопам в виде продленной инфузии интраоперационно, сразу после начала вмешательства.
Для объективной оценки интенсивности болевого синдрома (интраоперационно, через 2 и 6 ч после оперативного вмешательства) использовались вербально-рейтинговая (ВРШ) и цифровая рейтинговая (ЦРШ) шкалы оценки боли. Выбор дозировок и способов введения препаратов был строго регламентирован официальными инструкциями к препаратам, а также действующими клиническими рекомендациями.
Для проведения исследования использовались препараты, зарегистрированные в Российской Федерации: парацетамол (раствор во флаконах для инфузий 10 мг/мл – 100 мл); декскетопрофен (раствор в ампулах для внутривенного и внутримышечного введения 25 мг/мл – 2 мл); тримеперидин (раствор для инъекций 20 мг/мл – 1 мл); нефопам (раствор в ампулах для инфузий и внутримышечного введения 10 мг/мл – 2 мл).
Исследование проведено с соблюдением правил международного стандарта этических норм и качества научных исследований GCP (Good Clinical Practice, Надлежащая клиническая практика) согласно принципам, заложенным Хельсинкской декларацией Всемирной медицинской ассоциации, одобрено локальным этическим комитетом (протокол №1 от 3.02.2025). От всех пациентов, принявших участие в исследовании, получено информированное добровольное согласие. Статистическая обработка данных проводилась с использованием программы SPSS Statistics 26. Для сравнения интенсивности болевого синдрома у пациентов четырех групп в качестве статистического метода применяли критерий Краскела – Уоллиса, с последующими попарными сравнениями с помощью критерия Манна – Уитни. Результаты представляли в виде Me [МКИ] (где Ме – медиана, МКИ – межквартильный интервал). Коррекция множественных сравнений проводилась методом Бонферрони. Для объективной оценки удовлетворенности пациентов течением послеоперационного периода использовался критерий χ² Пирсона с поправками. Различия считали статистически значимыми при р<0,05 (после пересчета на число сравнений).
Проведенное исследование не лишено ограничений, к которым можно отнести малый объем выборок, субъективность шкал оценки интенсивности болевого синдрома, отсутствие ослепления.
Результаты исследования и их обсуждение
Проведенное исследование показало различную эффективность указанных схем применения препаратов для коррекции болевого синдрома у пациентов, которым проводилась химиоэмболизация новообразований печени.
Установлено, что в группе 1 пациентов, которым осуществлялась коррекция болевого синдрома по показаниям, то есть после его манифестации, с использованием комбинации парацетамола, декскетопрофена и, в большинстве случаев, с необходимостью применения промедола, интенсивность боли в интра- и послеоперационном периоде характеризовалась ими по ВРШ от средней интенсивности до сильной в соотношении с показателями по ЦРШ Me [МКИ] = 6 [4] баллов.
Аналогичные результаты были получены и в группе 2, в ней осуществлялось купирование болевого синдрома непосредственно после его возникновения с использованием комбинации парацетамола, декскетопрофена и, в большинстве случаев, необходимостью введения нефопама. Пациенты этой группы также характеризовали интенсивность боли среднюю и сильную по СРШ и Me [МКИ] = 6 [4] баллов по ЦРШ соответственно.
У пациентов группы 3, которым комбинация парацетамола и декскетопрофена применялась перед оперативным вмешательством, отмечалась менее выраженная тенденция к нарастанию интенсивности боли в интра- и послеоперационном периоде. Участники этой группы в основном характеризовали боль как среднеинтенсивную по СРШ и Me [МКИ] = 4 [2] балла по ЦРШ.
Наименьшая интенсивность боли отмечалась у пациентов группы 4, у которых применялась комбинация парацетамола и декскетопрофена перед оперативным вмешательством и началом введения нефопама сразу после начала оперативного вмешательства в виде продленной инфузии и характеризовалась ими как слабая по СРШ и Me [МКИ] = 2 [1] балла по ЦРШ.
Стоит отметить, что во временном аспекте интенсивность болевого синдрома внутри групп не отличалась интраоперационно, через 2 и 6 ч после операции (таблица).
Интенсивность болевого синдрома у пациентов, подвергшихся химиоэмболизации новообразований печени, в зависимости от способа медикаментозной коррекции
|
Способ медикаментозной коррекции |
Парацетамол + Декскетопрофен + Промедол по показаниям (n=10) |
Парацетамол + Декскетопрофен + Нефопам по показаниям (n=10) |
Парацетамол + Декскетопрофен в премедикацию (n=10) |
Парацетамол + Декскетопрофен в премедикацию + Нефопам интраоперационно (n=10) |
|
Интенсивность болевого синдрома интраоперационно, по ВРШ, ЦРШ (баллы, Me [МКИ]) |
Средней интенсивности / Сильная 6 [4] |
Средней интенсивности / Сильная 6 [4] |
Средней интенсивности 4 [2] |
Слабая 2 [1] |
|
Интенсивность болевого синдрома через 2 ч после операции, по ВРШ, ЦРШ (баллы, Me [МКИ]) |
Средней интенсивности / Сильная 6 [4] |
Средней интенсивности / Сильная 6 [4] |
Средней интенсивности 4 [2] |
Слабая 2 [1] |
|
Интенсивность болевого синдрома через 6 ч после операции, по ВРШ, ЦРШ (баллы, Me [МКИ]) |
Средней интенсивности/ Сильная 6 [4] |
Средней интенсивности/ Сильная 6 [4] |
Средней интенсивности 4 [2] |
Слабая 2 [1] |
Примечание: n – количество наблюдений, статистическая значимость для всех показателей р<0,05. Составлено авторами.
Таким образом, из выбранных способов коррекции болевого синдрома наибольшую эффективность показала комбинация парацетамола и декскетопрофена перед оперативным вмешательством с началом введения нефопама сразу после начала оперативного вмешательства в виде продленной инфузии.
Результаты проведенного исследования продемонстрировали высокую эффективность и целесообразность превентивного комбинированного применения парацетамола и декскетопрофена в предоперационном периоде в сочетании с продленной инфузией нефопама в начале оперативного вмешательства с целью минимизации интенсивности боли у пациентов, подвергшихся химиоэмболизации новообразований печени (рис.1).
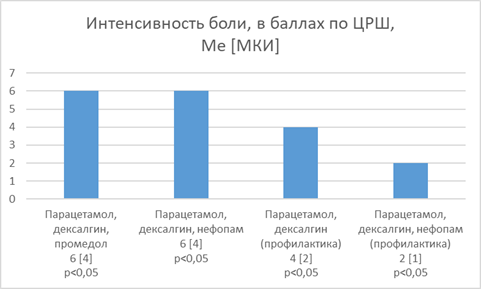
Рис.1. Интенсивность болевого синдрома в зависимости от схемы применения препаратов для коррекции болевого синдрома у пациентов, которым проводилась химиоэмболизация новообразований печени (р<0,05).
Составлено авторами
Стоит указать, что, помимо различия интенсивности болевого синдрома у пациентов исследованных групп интраоперационно, через 2 и 6 ч после операции, пациенты различных групп имели различную потребность в опиоидных анальгетиках (промедол). Так, суммарная суточная доза промедола для послеоперационного обезболивания у пациентов групп 1 и 2 составила 30 мг, группы 3 – 10 мг, а пациентам группы 4 не требовалось введение опиоидных анальгетиков в послеоперационном периоде.
Следует отметить, что на сегодняшний день, наряду с отсутствием единых подходов к профилактике и лечению постэмболизационного синдрома, в арсенале клиницистов существует большое количество препаратов различных фармакологических групп, применение которых допустимо с целью профилактики и лечения постэмболизационного синдрома.
Выбор препаратов для профилактики и коррекции болевого синдрома у пациентов, подвергшихся химиоэмболизации новообразований печени, в рамках проведенного исследования был продиктован их распространенностью и доступностью, а также низкой вероятностью развития нежелательных побочных эффектов.
Парацетамол, являясь анальгетиком-антипиретиком, обладает жаропонижающим и анальгезирующим эффектом, селективно блокирует циклооксигеназу-3 (ЦОГ 3), специфичную для центральной нервной системы, воздействуя на центры боли и терморегуляции.
Декскетопрофен относится к нестероидным противовоспалительным препаратам и обладает обезболивающим, противовоспалительным и жаропонижающим действием. Механизм действия декскетопрофена связан с уменьшением синтеза простагландинов за счет подавления активности циклооксигеназ 1 и 2. Препарат ингибирует превращение арахидоновой кислоты в циклические эндопероксиды PGG2 и PGH2, которые продуцируют простагландины PGE1, PGE2, PGF2α и PGD2, а также простациклин PGI2 и тромбоксаны TxA2 и TxB2. Кроме того, ингибирование синтеза простагландинов может влиять на другие медиаторы воспаления, такие как кинины, обеспечивая не только прямое, но и опосредованное действие.
Нефопам, являясь ненаркотическим анальгезирующим средством центрального действия, ингибирует обратный захват дофамина, норадреналина и серотонина проявляет антиноцицептивную активность путем возможного снижения освобождения глутамата на пресинаптическом уровне и активации рецепторов N-метил-D-аспартата на постсинаптическом уровне. При этом нефопам не оказывает противовоспалительного или жаропонижающего действия, не угнетает дыхание и не влияет на перистальтику кишечника, а также обладает незначительным м-холиноблокирующим эффектом.
Результаты опроса пациентов, проводимого по истечении первых суток послеоперационного периода и касающегося субъективной удовлетворенности респондентов качеством анестезиологического пособия и течением послеоперационного периода, отличались внутри различных групп (рис.2).
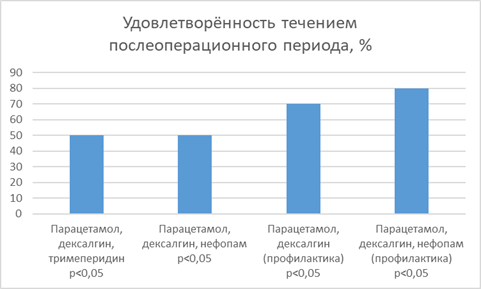
Рис.2. Уровень субъективной удовлетворенности респондентов качеством анестезиологического пособия и течением послеоперационного периода в зависимости от схемы применения препаратов для коррекции болевого синдрома у пациентов, которым проводилась химиоэмболизация новообразований печени (р<0,05). Составлено авторами
Так, в группах 1 и 2 субъективную удовлетворенность течением послеоперационного периода выразили 50% пациентов, в третьей – 70%, а в четвертой группе – 80%.
Данные, полученные в ходе проведения данного исследования, свидетельствуют о целесообразности превентивного пред- и интраоперационного применения комбинации парацетамола, декскетопрофена и нефопама для минимизации интенсивности боли при постэмболизационном синдроме, демонстрируя большую эффективность данной схемы периоперационного обезболивания в сравнении с остальными, представленными в данном исследовании, что, однако, требует подтверждения в рандомизированном исследовании с расчетом мощности.
Заключение
Постэмболизационный синдром является часто встречающимся осложнением послеоперационного периода у пациентов, подвергшихся химиоэмболизации новообразований печени, одним из ведущих клинических проявлений которого является интенсивная боль. Рациональная коррекция и профилактика развития болевого синдрома представляется чрезвычайно важным аспектом повышения качества оказания медицинской помощи онкологического профиля. В рамках проведенного исследования получены данные, свидетельствующие о вероятной целесообразности и эффективности комбинированной фармакологической коррекции болевого синдрома превентивным предоперационным введением парацетамола и декскетопрофена и интраоперационным введением нефопама. Показано, что применение данной комбинации способствует существенному снижению интенсивности болевого синдрома, а также снижению потребности в неопиоидных и опиоидных анальгетиках в послеоперационном периоде что, однако, требует подтверждения в рандомизированном исследовании с расчетом мощности. Кроме того, полученные результаты показывают тенденцию к эффективности и целесообразности реализации стратегии превентивной, или упреждающей, анальгезии – фармакологической стратегии, направленной на предотвращение или уменьшение интенсивности послеоперационной боли путем блокирования ноцицептивных механизмов до возникновения болевой импульсации с соблюдением принципов мультимодальности и своевременности.
Библиографическая ссылка
Федосов М.И., Абкеримов А.Р. СРАВНИТЕЛЬНАЯ ОЦЕНКА ЭФФЕКТИВНОСТИ МЕТОДОВ КОРРЕКЦИИ БОЛЕВОГО СИНДРОМА У ПАЦИЕНТОВ ПРИ ХИМИОЭМБОЛИЗАЦИИ НОВООБРАЗОВАНИЙ ПЕЧЕНИ // Современные проблемы науки и образования. 2026. № 4. ;URL: https://science-education.ru/en/article/view?id=34540 (дата обращения: 21.04.2026).
DOI: https://doi.org/10.17513/spno.34540



