Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
CLINICAL AND PATHOGENETIC EVALUATION OF MEDICAL REHABILITATION OF BREAST CANCER PATIENTS
Введение
На основании данных Международного агентства по изучению рака (МАИР) Всемирной организации здравоохранения, рак молочной железы (РМЖ) занимает второе место в мире по распространенности среди всех злокачественных новообразований (с зарегистрированными 2,3 млн случаев) и является четвертой ведущей причиной смертности от онкологических заболеваний у женщин (666103 случая) [1; 2]. Согласно прогнозам МАИР, к 2050 г. ожидается рост заболеваемости РМЖ на 77% относительно текущих показателей. Указанный прогноз обусловлен, прежде всего, демографическими тенденциями, включая увеличение численности и постарение населения, а также потенциальным возрастанием влияния факторов риска [1; 2]. Несмотря на значительный прогресс в области диагностики и терапии, который привел к увеличению 10-летней выживаемости пациентов с РМЖ с 40 до 78% за последние два десятилетия [3], сохраняются серьезные проблемы, связанные с отдаленными последствиями лечения.
В частности, даже на фоне успехов специализированной противоопухолевой помощи качество жизни и уровень трудоспособности пациенток, перенесших хирургическое лечение по поводу РМЖ, остаются существенно сниженными. Данное обстоятельство нивелирует эффективность оказываемой высокотехнологичной медицинской помощи и актуализирует задачу разработки и внедрения комплексных программ медицинской реабилитации (МР) [3–5]. Увеличение продолжительности жизни в результате комплексного лечения часто сопровождается стойким снижением показателей качества жизни, в то время как активное функционирование признается одной из ключевых детерминант здоровья [6; 7]. Основной целью современных реабилитационных технологий является восстановление функциональной активности пациентов до преморбидного уровня и минимизация негативных последствий проведенного противоопухолевого лечения [3; 8; 9]. Разработка персонализированных реабилитационных программ, учитывающих клинические особенности заболевания, патогенетические механизмы развившихся функциональных нарушений и индивидуальные характеристики пациенток, представляет собой стратегическое направление для нивелирования последствий болезни, обеспечения высокого качества жизни и снижения инвалидизации [10].
Цель исследования – повышение эффективности восстановительного лечения пациентов с раком молочной железы на основе разработки клинико-патогенетически обоснованных моделей реабилитации.
Материал и методы исследования
Исследование реализовано в соответствии с протоколом сравнительного проспективно-ретроспективного исследования и выполнено в три последовательных этапа.
Первый этап предполагал проспективный набор пациентов в основную (наблюдаемую) группу на предоперационном этапе в соответствии с установленными критериями включения. Всем пациентам данной группы на дооперационном этапе проводилась комплексная клинико-инструментальная диагностика с целью выявления существующих нарушений функций. На основании структуры и объема выявленных нарушений для каждого пациента осуществлялся подбор методов реабилитации, которые применялись в предоперационном периоде. В раннем послеоперационном периоде проводилась повторная оценка функционального статуса пациентов, и на основе вновь выявленных нарушений формировалась персонализированная программа медицинской реабилитации. Далее следовала реализация данной индивидуальной программы в послеоперационном периоде с последующей оценкой клинических показателей ее эффективности.
На втором этапе был проведен ретроспективный попарный подбор пациентов в группу сравнения. Критерием подбора служила сопоставимость с пациентами основной группы по ключевым клиническим параметрам: возрасту, стадии заболевания и объему полученного противоопухолевого лечения.
Третий этап был посвящен клинико-патогенетической оценке отдаленных результатов. Эффективность комплексного противоопухолевого лечения и восстановительных мероприятий у пациентов основной группы анализировалась через год после завершения реализации персонализированных реабилитационных программ.
Характеристика выборки. В исследование были включены данные 150 пациенток с раком молочной железы в возрасте от 18 до 44 лет (медиана возраста – 31 год). У всех пациенток был верифицирован диагноз неметастатического РМЖ (включая как истинный ранний, так и местно-распространенный рак), и все они получили комплексное противоопухолевое лечение. Детальная клиническая характеристика когорты представлена в табл.1.
Статистический анализ. Для оценки значимости различий между сравниваемыми подгруппами использовался параметрический двухвыборочный t-критерий Стьюдента. Анализ годичной бессобытийной выживаемости проводился с применением метода Каплана – Майера. Для исследования взаимосвязи между клиническими показателями эффективности реабилитационных мероприятий и общим качеством жизни был применен факторный анализ методом главных компонент.
Таблица1
Клиническая характеристика пациенток, включенных в исследование
|
Критерии |
Общее число пациентов (n=150) |
||||
|
исследуемая группа (n=75) |
контрольная группа (n=75) |
||||
|
n |
% |
n |
% |
||
|
Стадия |
1а |
9 |
12 |
11 |
14,7 |
|
2а |
22 |
29,3 |
23 |
30,7 |
|
|
2b |
24 |
32 |
24 |
32 |
|
|
3a |
18 |
26,7 |
17 |
22,6 |
|
|
Биологический подтип опухоли |
люминальный А |
21 |
28 |
23 |
30,7 |
|
люминальный В |
20 |
27 |
19 |
25,3 |
|
|
трижды негативный |
14 |
18,7 |
15 |
20 |
|
|
HER2+ |
20 |
26,6 |
18 |
24 |
|
|
Неоадьювантная полихимиотерапия (НАПХТ)
|
проводилась |
48 |
64 |
45 |
60 |
|
не проводилась |
27 |
36 |
30 |
40 |
|
|
Реконструктивно-пластическая операция
|
выполнялась |
51 |
68 |
49 |
65,3 |
|
не выполнялась |
24 |
32 |
26 |
34,7 |
|
Примечание: составлена авторами на основе источников [2; 4; 5]
В ходе проведенного исследования сравнительный анализ базовых клинико-морфологических характеристик пациенток в исследуемой и контрольной группах продемонстрировал их статистически однородный характер, что является принципиально важным условием для последующего корректного сравнения результатов лечения. Распределение больных по стадиям заболевания было сопоставимым в обеих когортах. Во всех группах преобладали пациентки со II стадией рака молочной железы (РМЖ): в исследуемой группе их было 46 (61,3%), в том числе с подстадией IIa – 22 (29,3%), с IIb – 24 (32%); в контрольной группе – 47 пациенток (62,7%), из которых с подстадией IIa – 23 (30,7%), с IIb – 24 (32%). Пациенток с I стадией (Ia) было включено 9 (12%) и 11 (14,7%) соответственно, а с III стадией (IIIa) – 18 (26,7%) и 17 (22,6%) в исследуемой и контрольной группах.
Аналогичная картина наблюдалась и при анализе биологических подтипов опухоли. В обеих группах доминировали люминальные подтипы РМЖ, что соответствует общей эпидемиологической картине заболевания: в исследуемой группе этот подтип был выявлен у 41 пациентки (54,7%), в контрольной – у 42 (56%).
Важно отметить, что стратегия лечения также была унифицирована. Неоадъювантная лекарственная терапия в рамках комплексного противоопухолевого лечения была проведена 48 пациенткам (64%) в основной группе и 45 (60%) в группе сравнения. Все пациентки получали стандартные режимы химиотерапии (на основе антрациклинов и таксанов), гормонотерапию (тамоксифен, ингибиторы ароматазы) и таргетную терапию (трастузумаб) в зависимости от биологического подтипа опухоли.
Критерий проведения адъювантной лучевой терапии (ЛТ) не включался в анализ, так как проведенное исследование было сфокусировано на раннем послеоперационном периоде до момента принятия решения о проведении ЛТ либо старта ее проведения
Реконструктивно-пластический компонент хирургического вмешательства выполнен 51 пациентке (68%) в исследуемой группе и 49 пациенткам (65,3%) в контрольной, что подчеркивает сопоставимость объемов и агрессивности проведенного хирургического лечения.
Таким образом, установленная однородность групп по ключевым прогностическим параметрам – стадийности, молекулярно-биологическому профилю опухоли и примененным видам лечения позволяла считать группы репрезентативными и обеспечивала валидность дальнейшего сравнительного анализа отдаленных онкологических и эстетических результатов.
Результаты исследования и их обсуждение
В последние годы наблюдается устойчивый рост научного интереса к разработке и внедрению технологий физической и реабилитационной медицины (ФРМ) в комплексную терапию онкологических заболеваний. Данная тенденция в равной степени характерна как для международного, так и для отечественного здравоохранения, при этом особое внимание уделяется реабилитации пациентов с раком молочной железы (РМЖ). Реабилитационные вмешательства рассматриваются в неразрывной связи с лечебным процессом, что обусловлено необходимостью обеспечения преемственности и непрерывности помощи на всех этапах противоопухолевого лечения.
Для анализа сложившегося исследовательского ландшафта был проведен количественный, качественный и структурный анализ публикационной активности. Поиск осуществлялся в международных (PubMed, PEDro) и российских (eLibrary) библиографических базах данных по состоянию на 1 января 2024 г. Всего было отобрано 852 источника, включая оригинальные клинические исследования, систематические обзоры и метаанализы, которые были классифицированы по восьми основным тематическим модулям.
Результаты анализа демонстрируют, что доля исследований, посвященных технологиям ФРМ при РМЖ, в общем массиве работ по данному заболеванию остается относительно невысокой. В зарубежных базах данный показатель составляет 1,6%, в то время как в российских – 4,2%. Значимым является хронологическое распределение публикаций: 56,3% работ в международных и 73,3% в отечественных базах данных опубликованы за последнее десятилетие. Этот выраженный всплеск научной продуктивности, по-видимому, коррелирует с прогрессом в методах противоопухолевой терапии РМЖ, который, увеличивая выживаемость пациентов, смещает фокус медицинского сообщества на вопросы качества жизни, функционального восстановления и долгосрочной адаптации. Таким образом, наблюдаемый рост публикационной активности отражает формирование новой парадигмы в онкологии, где реабилитация перестает быть факультативным дополнением и становится интегральным, научно обоснованным компонентом персонализированной помощи онкологическому пациенту. Детальная оценка публикационной активности по базам данных представлена в табл.2.
Таблица2
Оценка публикационной активности по базам данных (p<0,05)
|
База данных исследований |
Всего статей по РМЖ |
Из них по применению технологий ФРМ у больных РМЖ по всем модулям |
Из них на русском языке |
||
|
Всего |
За 10 лет |
Всего |
За 10 лет |
||
|
Pubmed |
485533 |
7697 (1,6%) |
4475 (0,9%) |
113 (0,002%) |
29 (0,0006%) |
|
E-library |
10442 |
435 (4,2%) |
401 (3,8%) |
435 (4,2%) |
401 (3,8%) |
|
PEDro |
852 |
852 (100%) |
622 (73%) |
9 (1,1%) |
5 (0,6%) |
Примечание: составлена авторами на основе источников [2; 4]
На основании проведенного наукометрического анализа массива публикаций отечественных и зарубежных авторов были систематизированы и выделены ключевые компоненты программ медицинской реабилитации для пациентов с раком молочной железы (РМЖ). Данные компоненты были структурированы в виде отдельных тематических модулей, что позволило перейти от теоретического обобщения к практическому построению комплексных вмешательств. В результате комплексного анализа сформирован рекомендуемый доказательный профиль технологий физической и реабилитационной медицины, распределенный по всем выделенным модулям для данной категории больных.
Методологической основой формирования программ в настоящем исследовании стал модульный принцип, обеспечивающий персонализацию и гибкость реабилитационного процесса. Его основу составляют следующие взаимодополняющие блоки: применение физических факторов, лечебная физкультура (ЛФК), психологическая коррекция, эрготерапия, образовательные программы для пациентов и их родственников, фармакологическая поддержка в реабилитационном периоде, использование ортезов, протезов и технических средств реабилитации, нутритивная поддержка, коррекция образа жизни и факторов риска рецидива или прогрессирования заболевания, а также вспомогательные и специальные технологии, включая телемедицинские (рис.1). Таким образом, предложенная модульная архитектура программ реабилитации представляет собой интегративную модель, синтезирующую доказательные практики в единую, адаптируемую к индивидуальным клиническим задачам систему. Это позволяет не только стандартизировать подход, но и научно обосновать выбор конкретных вмешательств, направленных на кумулятивное улучшение функциональных исходов и качества жизни пациентов.
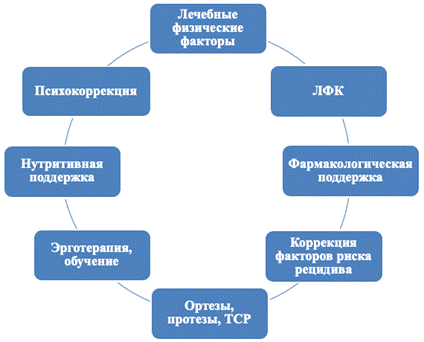
Рис.1. Модульная структура программ медицинской реабилитации больных РМЖ. Примечание: составлен авторами на основе источников [2; 4; 5]
Динамическое наблюдение за пациентами осуществлялось в четырех ключевых временных точках: до начала специализированного противоопухолевого лечения, непосредственно после его завершения, по окончании курса медицинской реабилитации, а также в отдаленном периоде – спустя год. Такой поэтапный план обследования позволяет объективно отслеживать как непосредственные результаты терапии, так и долгосрочные эффекты реабилитационных мероприятий.
Комплексное обследование включало оценку широкого спектра параметров, интегрированных в единую аналитическую модель. Методология основывалась на всестороннем анализе 21 объективного клинико-функционального показателя, данных инструментальных методов диагностики, а также субъективных критериев. Особое внимание уделялось психофизиологическому статусу пациентов и оценке качества жизни. Для количественного и качественного анализа ограничений жизнедеятельности был применен структурированный биопсихосоциальный подход, что нашло отражение в использовании соответствующих валидированных опросников и шкал [4; 8].
Важнейшим научно-методологическим компонентом исследования стала стандартизированная оценка ограничений в рамках категорий Международной классификации функционирования, ограничений жизнедеятельности и здоровья (МКФ). Использование универсального языка и концептуальной основы МКФ (табл.3) позволило не только детализировать характер и степень нарушений на уровнях функций организма, активности и участия, но и учесть влияние контекстуальных факторов (средовых и личностных). Тем самым была обеспечена комплексная, холистическая оценка состояния пациента, выходящая за рамки традиционной нозоцентрической парадигмы и ориентированная на интегральные показатели здоровья и социальной адаптации.
Таблица3
Применяемые шкалы и оценочные методики
|
Уровень функционирования |
Клинико-функциональные методы оценки |
Ограничения жизнедеятельности (категория МКФ) |
|
Биологический
|
ОАК, антропометрия, физикальный осмотр, ЭКГ, ЭХО-КГ (ФВЛЖ), индекс массы тела (ИМТ), калиперометрия, импедансометрия Визуально-аналоговая шкала боли (ВАШ) Диагностический опросник нейропатической боли DN4 Опросник исходов и неспособности руки и кисти (QUICK DASH) Тест с 6-минутной ходьбой Электронейромиография (ЭНМГ) Оценка болевой и вибрационной чувствительности Ультразвуковая оценка постмастэктомической зоны |
b280 Ощущение боли b4552 Утомляемость b530 Функции сохранения массы тела b7100 Подвижность одного сустава b455 Функции толерантности к физической нагрузки b134 Функции сна b640 Сексуальные функции b440 Функции дыхания b4450 Функции грудных дыхательных мышц S720 Структура области плеча S6302 Структура молочной железы S420 (0) Структура иммунной системы (лимфатические сосуды) d445 Использование кисти и руки |
|
Психологический
|
Госпитальная шкала тревоги и депрессии (HADS) Индекс женской сексуальной функции (FSFI) Шкала оценки образа тела (BISS) Шкала оценки отношений (RAS) Монреальская шкала оценки когнитивных функций (MoCA-тест) Опросник качества жизни (EORTC-QLQ-C30) |
d240 Преодоление стресса и других психологических нагрузок d760 Семейные отношения d770 Интимные отношения b640 Сексуальные функции b117 Интеллектуальные функции b122 Глобальныепсихо-социальныефункции b130 Волевые и побудительные функции b134 Функции сна b140 Функции внимания b144 Функции памяти b152 Функции эмоций b160 Функции мышления |
|
Социальный
|
Шкала функциональной независимости (FIM) Канадская шкала выполнения деятельности (СОРМ) |
d540 Одевание d640 Выполнение работы по дому
|
Примечание: составлена авторами на основе источников [2; 4; 5; 7]
При формировании набора информативных признаков рассматривалась задача проанализировать влияние применяемых технологий медицинской реабилитации и их сочетаний на функциональную активность пациентов с РМЖ, качество их жизни и негативные симптомы осложнений, возникающих в ходе комплексного лечения РМЖ.
В ходе исследования анализировалось 28 клинических и инструментальных показателей (признаков):
1) ОАК (тромбоциты, лейкоциты, уровень гемоглобина);
2) лимфатический отек ипсилатеральной верхней конечности;
3) объем движений верхней конечности (гониометрия);
4) оценка болевого синдрома (ВАШ, DN–4);
5) биоимпедансометрия (общий вес, активная клеточная масса, безжировая масса тела, жировая масса);
6) калиперометрия (толщина кожной складки в см);
7) фракция выброса левого желудочка (ФВЛЖ);
8) электронейромиография (ЭНМГ – скорость, порог, амплитуда);
9) электрокардиография (ЭКГ– ЧСС, интервалы PQ, QRS, QT, QT);
10) тест с 6-минутной ходьбой;
11) оценка повседневной деятельности (COPM);
12) оценка тревоги/депрессии (шкала HADS);
13) оценка отношений с партнером (шкала RAS);
14) оценка сексуального дистресса (шкала FSFI);
15) оценка когнитивных функций (шкала MoCA);
16) оценка образа тела (шкала BISS).
В рамках проведенного исследования для решения задачи снижения размерности исходного информационного массива данных был применен метод факторного анализа [11, с. 256–310]. Данный метод является одним из ключевых инструментов многомерного статистического анализа и позволяет редуцировать множество наблюдаемых взаимосвязанных признаков к ограниченному набору скрытых (латентных) переменных, называемых факторами. Факторы формируются таким образом, что каждый из них объединяет признаки с высокой взаимной корреляцией, одновременно демонстрируя низкую корреляцию с признаками, входящими в иные факторные группы. Это обеспечивает содержательную интерпретируемость выделенных латентных конструктов.
Процедура выделения значимых факторов была реализована на основе метода главных компонент (МГК) [12, с. 88–96]. Принципиальным методологическим преимуществом МГК является то, что линейное преобразование исходных переменных в главные компоненты сохраняет полную дисперсию исходного набора данных. Это позволяет последовательно извлекать компоненты, максимизирующие объясненную дисперсию. В результате исследователь получает возможность ограничиться анализом первых нескольких наиболее информативных главных компонент, совокупная дисперсия которых составляет значительную долю общей дисперсии. Последующие компоненты, вносящие незначительный вклад, могут быть исключены из рассмотрения без существенной потери информации. Таким образом, применение связки методов – факторного анализа на базе МГК – решает двуединую задачу: во-первых, осуществляет эффективное сжатие данных, а во-вторых, обеспечивает содержательную реинтерпретацию многообразия исходных признаков через систему латентных факторов, что значительно упрощает дальнейшую содержательную интерпретацию результатов и построение теоретических моделей.
Методом факторного анализа (с использованием метода главных компонент) в группе наблюдения была выявлена многомерная структура взаимосвязей исследуемых параметров. Анализ позволил экстрагировать 8 значимых компонент, совокупно объясняющих 68,2% общей дисперсии данных, что свидетельствует о репрезентативности полученной факторной модели.
Первая компонента, объясняющая 12,9% дисперсии, продемонстрировала высокие факторные нагрузки по показателям уровня тромбоцитов и лейкоцитов в периферической крови. Сила выявленных корреляционных связей позволяет интерпретировать данную латентную переменную как биологический фактор «Гематологический профиль», отражающий базовое состояние системы крови.
Вторая компонента (11,9% объясненной дисперсии) объединила показатели концентрации гемоглобина и шкалы функциональной независимости. Положительный характер связей указывает на то, что данный латентный фактор, условно обозначенный как «Двигательное функционирование и кислородтранспортная функция», интегрирует аспекты физической автономии и обеспеченности организма кислородом.
Третья компонента, на которую приходится 8,9% дисперсии, включила параметры, характеризующие лимфатический отек и ограничение подвижности верхней конечности на стороне оперативного вмешательства. Эта совокупность была интерпретирована как фактор «Локомоторная функция оперированной конечности», отражающий специфические послеоперационные осложнения, напрямую влияющие на качество жизни.
Четвертая компонента (8,2% дисперсии) выявила сильную ковариацию между показателями выполнения повседневной деятельности и интенсивности болевого синдрома. Данная интеграция позволяет определить ее как фактор «Повседневное (бытовое) функционирование», центральным элементом которого является способность к самообслуживанию, модулируемая уровнем боли.
Пятая компонента объяснила 7,3% вариативности и объединила антропометрические (безжировая масса тела, процент подкожного жира) и кардиологический (функция выброса левого желудочка) параметры. Эта констелляция показателей была определена как фактор «Соматический ресурс и физическая выносливость», выступающий маркером общего физиологического потенциала организма.
Шестая компонента (6,8% дисперсии) показала умеренные связи между скоростью моторного ответа мышц конечностей на стимулы и нейропатическим компонентом боли. Предлагается трактовать эту латентную переменную как фактор «Нейромышечная проводимость и сенсорное восприятие», затрагивающий целостность периферических нервных путей.
Седьмая компонента, объясняющая 5,5% дисперсии, интегрировала показатели психоэмоционального (депрессия, тревога) и когнитивного статуса. Выявленные синергические связи обосновывают выделение комплексного «Когнитивно-аффективного фактора», подчеркивая неразрывную взаимосвязь психических и познавательных функций в клинической картине.
Восьмая компонента (5,5% дисперсии) сгруппировала переменные, относящиеся к сексуальному дистрессу, восприятию образа тела и качеству партнерских отношений. Данный кластер интерпретирован как «Интимно-личностный и психосоциальный фактор», отражающий глубокое влияние заболевания и лечения на приватную сферу и межличностные отношения.
Полученная 8-факторная модель демонстрирует, что состояние пациентов носит мультисистемный, гетерогенный характер и не может быть сведено к единому показателю. Выделенные латентные конструкты охватывают биологический, функциональный, неврологический и психосоциальный уровни функционирования. Это подчеркивает необходимость комплексного, междисциплинарного подхода к реабилитации, направленного не только на коррекцию ведущих симптомов, но и на синергичное воздействие на все выявленные независимые измерения здоровья. Наличие четко структурированных компонент подтверждает гипотезу о существовании внутренней логики в формировании клинического статуса, где нарушения в одной сфере закономерно сопряжены с изменениями в других, что открывает перспективы для разработки таргетированных реабилитационных программ.
Факторный анализ в группе сравнения позволил также выделить 8 компонент, объясняющих 67,6% суммарной совокупной дисперсии.
Результаты факторного анализа, проведенного для выявления структуры взаимосвязей ключевых показателей у пациентов после хирургического лечения, позволили выделить 8 значимых компонент, совокупно объясняющих большую часть наблюдаемой дисперсии. Первая компонента, объясняющая 14,7% общей дисперсии, объединила показатели, характеризующие клинически выраженные депрессивные симптомы, интенсивность болевого синдрома и ограничение подвижности верхней конечности на стороне оперативного вмешательства. Наличие сильной прямой корреляции депрессивной симптоматики и умеренных прямых связей боли и функциональных ограничений с данной компонентой позволило интерпретировать ее как фактор «функционирование кисти/руки».
Вторая компонента, описывающая 9,6% дисперсии, продемонстрировала сильную положительную корреляцию с уровнем тромбоцитов, лейкоцитов и показателем безжировой массы тела. Эта совокупность параметров была концептуализирована как фактор «сохранение нутритивного и гематологического статуса», отражающий важность метаболических и иммунных резервов организма.
Третья компонента (8,7% дисперсии) показала тесную связь с параметрами сексуального дистресса, негативного образа тела и качества отношений с партнером, что определило ее как «интимно-личностный» фактор, играющий существенную роль в психосоциальной адаптации.
Четвертая компонента (8,0% дисперсии) сгруппировала показатели выполнения повседневной деятельности и уровня функциональной независимости, что обосновало ее определение в качестве фактора «повседневное функционирование».
Пятая компонента, объясняющая 7,5% дисперсии, обнаружила сильные связи с показателями нарушения фракции выброса левого желудочка и уровнем гемоглобина. Данная комбинация была интерпретирована как фактор «физическая выносливость и кардиореспираторный резерв».
Шестая компонента (6,9% дисперсии) включила показатели скорости моторного ответа мышц конечностей на стимулы и нейропатический компонент боли, что позволило обозначить ее как фактор «нейромышечное функционирование».
Седьмая компонента (6,6% дисперсии) объединила параметры когнитивного функционирования и выраженности симптомов тревоги, формируя «когнитивно-психологический» фактор.
Восьмая компонента (5,4% дисперсии) коррелировала с наличием лимфатического отека и увеличением толщины жировой складки, что определило ее как фактор «двигательное функционирование и локальные трофические изменения».
Проведенный анализ выявил многомерную структуру детерминант качества жизни в постоперационном периоде. Высокое качество жизни в группе наблюдения через год после лечения, сопровождавшегося индивидуализированной реабилитацией, было ассоциировано с благоприятными значениями по всем восьми выделенным факторам: стабильным гематологическим и нутритивным статусом, сохраненным двигательным и нейромышечным функционированием, адекватным повседневным и физическим функционированием, а также благополучным психологическим, когнитивным и интимно-личностным статусом.
В противоположность этому, снижение общего качества жизни в группе сравнения может быть научно объяснено дефицитарностью по указанным факторам. Нарушения в сфере функционирования кисти, нутритивного статуса, интимно-личностных отношений, повседневной и физической активности, а также нейромышечного, когнитивно-психологического и двигательного функционирования формируют комплексный негативный синдром, приводящий к ухудшению интегрального показателя качества жизни. Таким образом, эффективность долгосрочной реабилитации должна быть направлена на комплексную коррекцию именно этих ключевых биопсихосоциальных факторов.
Оценка бессобытийной выживаемости
В рамках настоящего исследования одной из ключевых задач являлась оценка бессобытийной выживаемости (event-free survival, EFS) пациентов на протяжении установленного периода наблюдения. Под бессобытийной выживаемостью понимается временной интервал от момента начала терапии до наступления первого регистрируемого неблагоприятного исхода (события) [13]. При анализе каждое наблюдение кодируется парой переменных: индикатором наступления события (да/нет) и временем до события либо до окончания периода наблюдения за пациентом (цензурирование данных) [13]. Для статистического анализа EFS был применен непараметрический метод Каплана – Мейера, позволяющий оценить функцию выживаемости как кумулятивное произведение вероятностей «переживания» последовательных временных интервалов, в которых происходили события [14, с. 17–24]. Графическим отображением данной оценки является ступенчатая кривая выживаемости, демонстрирующая долю пациентов, остающихся свободными от изучаемого события к каждому моменту времени [15].
Наблюдение за пациентами обеих групп осуществлялось в течение 12 месяцев после проведения реабилитационных мероприятий. Критерием прекращения наблюдения для конкретного пациента являлось возникновение осложнений, классифицированных по следующим группам: сердечно-сосудистые, гематологические, неврологические, желудочно-кишечные, психические расстройства, рецидив первичного онкологического заболевания или развитие новой злокачественной опухоли.
Проведенный анализ выявил существенные различия в структуре и частоте осложнений между группами. В группе наблюдения было зарегистрировано 23 события, из которых 74,4% составили гематологические осложнения, а 25,6% – неврологические. В группе сравнения отмечена тенденция к хронизации нарушений к 5-му месяцу после лечения, а общее число осложнений к концу года наблюдения достигло 59. Их структура распределилась следующим образом: 41,3% – сердечно-сосудистые, 23,7% – гематологические, 19,1% – неврологические и 15,9% – желудочно-кишечные осложнения (табл.4).
Полученные данные подчеркивают не только количественное, но и качественное различие в профилях безопасности между сравниваемыми группами. Доминирование гематологических осложнений в группе наблюдения, в отличие от полиморфного спектра с преобладанием сердечно-сосудистой патологии в группе сравнения, может указывать на различные патофизиологические механизмы отсроченных последствий терапии. Это свидетельствует о необходимости разработки дифференцированных программ мониторинга и вторичной профилактики, ориентированных на конкретные профили риска, а не только на общий показатель выживаемости.
Таблица4
Количество завершенных событий, наступивших в группах (p<0,05)
|
Группы пациентов |
Завершенные события |
% |
Незавершенные события |
% |
|
Группа наблюдения (n=75) |
23 |
0,7 |
52 |
9,3 |
|
Группа контроля (n=75) |
59 |
8,7 |
16 |
1,3 |
|
Всего (n=150) |
82 |
4,7 |
68 |
5,3 |
Примечание: составлена авторами на основе источников [4; 5; 7]
Проведенный анализ показателей бессобытийной выживаемости выявил статистически значимые различия между группами наблюдения и сравнения. В группе наблюдения среднее время бессобытийной выживаемости составило 10,935 месяца. Квартильный анализ демонстрирует, что у 25% пациентов в этой группе событие наступило по истечении 11 месяцев, что указывает на более благоприятный профиль отдаленных результатов.
В группе сравнения зафиксировано существенно меньшее значение годовой бессобытийной выживаемости – 7,455 месяца. Медиана времени до наступления события в данной когорте составила 7 месяцев, что означает, что у половины пациентов осложнение или рецидив заболевания развились ранее этого срока. Более того, у 75% пациентов группы сравнения события регистрировались в срок до 5 месяцев после завершения лечения, что свидетельствует о высоком кумулятивном риске ранней хронизации патологического процесса или развития осложнений в этой популяции.
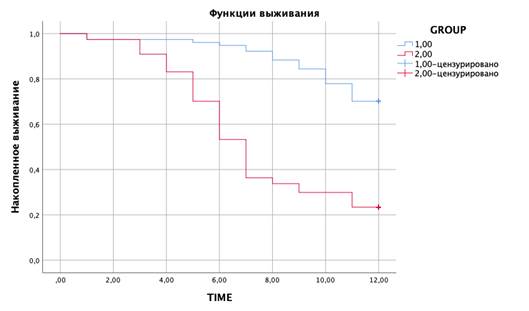
Выявленные различия носят статистически значимый характер. Рассчитанные медианы и средние значения бессобытийной выживаемости достоверно различаются между группами (p<0,001). Это подтверждается результатом непараметрического теста Log-Rank (Mantel – Cox): χ² = 44,873; p = 0,000, использованного для сравнения распределений времени до наступления события в двух или более независимых группах. Критерий применен нами для сравнения кривых Каплана – Майера (рис.2) и исключения случайных различия между группами.
Полученные данные позволяют сделать вывод о существенно более высокой эффективности применяемых в группе наблюдения реабилитационных или лечебных мероприятий, направленных на увеличение периода ремиссии и отсрочку наступления неблагоприятных исходов. Таким образом, дифференциация в подходах к ведению пациентов имеет принципиальное значение для улучшения долгосрочных прогнозов. Графическое отображение однолетней бессобытийной выживаемости в группах наблюдения и контроля представлено на рис.2.
|
|
Рис.2. Однолетняя бессобытийная выживаемость в группах наблюдения (А) и контроля (В).
Примечание: составлен авторами на основе источников [2; 4; 5; 7]
Заключение
Проведенное исследование было направлено на оценку клинико-функциональных исходов при внедрении персонализированных модульных программ реабилитации (ПМПР) у пациенток, завершивших первичное противоопухолевое лечение по поводу рака молочной железы (РМЖ). Полученные данные свидетельствуют о статистически значимом превосходстве данного подхода по сравнению со стандартной схемой восстановления. Ключевым научным положением, легшим в основу работы, является концепция прецизионной реабилитологии, которая предполагает адаптацию восстановительных вмешательств не только к нозологической форме (РМЖ), но и к индивидуальному клинико-функциональному профилю пациента, включая соматический статус, психоэмоциональное состояние и социальные детерминанты.
Реализованные ПМПР привели к статистически значимому улучшению интегрального показателя – качества жизни, что оценивалось по валидированным опросникам EORTC QLQ-C30 и BR23. Более того, в основной группе зафиксировано увеличение показателя бессобытийной выживаемости (Event-Free Survival, EFS), что указывает на потенциальное долгосрочное позитивное влияние комплексной реабилитации на прогноз заболевания. Факторный анализ с применением метода главных компонент выявил детерминанты, вносящие наибольший вклад в успешность реабилитационного процесса. К ним отнесены: стабильность гематологических и биохимических показателей, уровень двигательного функционирования (по шкале FIM), параметры психологического благополучия (уровень тревоги и депрессии по HADS) и толерантность к физической нагрузке (по результатам теста с 6-минутной ходьбой). Важным результатом явилось значимое снижение в основной группе частоты посттерапевтических осложнений (таких как лимфедема, контрактура плечевого сустава, стойкий астенический синдром) и процессов хронизации сопутствующей патологии. Данные показатели в группе сравнения, получавшей общие рекомендации, оставались существенно выше.
Таким образом, исследование эмпирически подтверждает, что внедрение клинико-патогенетически обоснованных, индивидуализированных моделей реабилитации в рутинную клиническую практику является необходимым условием для достижения оптимальных отдаленных результатов лечения. Это обеспечивает не только улучшение функционального состояния и качества жизни пациентов, перенесших РМЖ, но и может влиять на прогностические показатели, формируя новую парадигму онкологической помощи, ориентированной на пациента.
Conflict of interest
Financing
Библиографическая ссылка
Ковлен Д.В., Каспаров Б.С., Семиглазова Т.Ю., Фролов О.Н., Кондратьева К.О., Заозерский О.В., Салпагарова А.В. КЛИНИКО-ПАТОГЕНЕТИЧЕСКАЯ ОЦЕНКА ЭФФЕКТИВНОСТИ МЕДИЦИНСКОЙ РЕАБИЛИТАЦИИ БОЛЬНЫХ РАКОМ МОЛОЧНОЙ ЖЕЛЕЗЫ // Современные проблемы науки и образования. 2026. № 3. ;URL: https://science-education.ru/en/article/view?id=34538 (дата обращения: 10.06.2026).
DOI: https://doi.org/10.17513/spno.34538



