Введение
На сегодняшний день аппаратная косметология представляет собой одно из наиболее востребованных и динамично развивающихся направлений эстетической медицины. Современный рынок косметологических услуг располагает широким спектром аппаратных методик эстетической коррекции, направленных на активизацию регенеративных процессов, нормализацию трофических процессов в тканях, регуляцию синтеза структурных белков (коллагена и эластина) и активацию клеточного метаболизма. Перечень показаний к применению аппаратных методик достаточно велик и включает множество различных эстетических несовершенств: возрастные изменения кожи, нарушения пигментации, сосудистые патологии, акне и постакне, рубцовые дефекты, локальные жировые отложения и т.д.[1].
Среди всего разнообразия методов аппаратного воздействия, применяемых в эстетической медицине, лидирующие позиции занимают процедуры, включающие проведение лазерной и радиочастотной терапии[2], которые позволяют не только устранять эстетические дефекты, но и влиять на первопричины их появления, предупреждая рецидивы.
Современные лазерные технологии дают возможность генерирования излучения с различной длиной волны, плотностью энергии и длительностью импульса. Данные характеристики определяют глубину поглощения энергии биологическими тканями и интенсивность терапевтического воздействия на окружающие структуры. Принцип действия фракционного углекислотного (СО2) лазера, объединяющего высокую эффективность абляционных лазеров и благоприятный профиль безопасности неабляционных систем, основан на технологии дермального оптического термолиза (dermal optical thermolysis, DOT), предусматривающей целенаправленное воздействие на определенные структуры кожи при минимальном повреждении окружающих тканей. Технология реализуется за счет избирательного поглощения световой энергии определенными хромофорами-мишенями. Основным хромофором СО2-лазера, излучающего на длине волны 10600нм, является вода, эффективно адсорбирующая инфракрасное излучение[3]. В результате поглощения интенсивного излучения вода нагревается до испарения, а световая энергия трансформируется в тепловую, вызывая контролируемое повреждение в микрозонах абляции, деструкцию целевых структур кожи и стимуляцию регенеративных процессов[4]. Расположение микрозон абляции на некотором расстоянии друг от друга обеспечивает лишь частичное повреждение кожных структур, оставляя интактными окружающие участки, за счет которых происходит регенерация, сопровождающаяся выраженным ремоделированием коллагена в дерме[5].
Радиочастотная (radiofrequency, RF) терапия с микроиглами (RF-микроиглы) сочетает в себе преимущества RF-методики и механической чрескожной индукции коллагена с помощью микроигл. Принцип действия метода состоит в контролируемом механическом повреждении кожи микроиглами, через которые проходит импульс радиочастотного электрического тока, вызывая выработку тепловой энергии и обеспечивая избирательное нагревание кожи на определенной глубине. В результате происходит запуск каскада воспалительных реакций, сопровождающихся процессами неоангиогенеза, неоколлагеногенеза и ремоделирования дермы[6]. Степень деструкции кожных структур и клинический эффект, достигаемый при проведении RF-терапии с микроиглами, зависит от ряда параметров, в число которых входят глубина проникновения микроигл, наличие их изоляции, мощность и частота излучения, а также длительность воздействия[7; 8]. Было установлено, что распределение радиочастотной энергии и, как следствие, объем и глубина зон термокоагуляции напрямую зависит от электрического сопротивления того или иного слоя кожи и определяет сроки постпроцедурного восстановления и достигнутый клинический результат[9], а глубина воздействия положительно коррелирует с высотой зоны термокоагуляции[10]. Гистологические исследования позволили подтвердить активацию процессов ранозаживления и усиление ремоделирования дермы с образованием нового коллагена[7; 11].
Несмотря на ряд преимуществ аппаратных методик- минимальную инвазивность, широкий спектр показаний к применению, получение долгосрочных результатов, короткий период реабилитации, более глубокое воздействие на кожу по сравнению с фармакологическими методами- остается множество вопросов, касающихся научного подтверждения их эффективности. Отсутствие достаточной доказательной базы в определенной степени ограничивает возможности разработки стандартизированных протоколов лечения.
В связи с этим целью настоящего исследования стало экспериментальное изучение и сравнение результатов воздействия косметологических аппаратов для лазерной и радиочастотной терапии с микроиглами на клеточные структуры и внеклеточный матрикс.
Материалы и методы исследования
Настоящее пилотное исследование проводили на базе ГБУЗ МО «МОНИКИ им. М.Ф.Владимирского» с соблюдением принципов этического и гуманного отношения к лабораторным животным. Протокол исследования был одобрен Независимым комитетом по этике. Содержание животных и проведение эксперимента осуществлялись в соответствии с требованиями ГОСТ33216-2014 «Руководство по содержанию и уходу за лабораторными животными. Правила содержания и ухода за лабораторными грызунами и кроликами» [12].
При проведении исследования было использовано 9здоровых крыс линии Wistar с массой тела на момент начала эксперимента 250–350г. После получения из сертифицированного питомника животные содержались в отдельном помещении c контролем температуры (20–24°С) и относительной влажности воздуха (45–65%). Все животные находились на кормлении сухим полнорационным гранулированным комбикормом со свободным доступом к чистой питьевой воде.
Для изучения влияния CO2-лазера и RF-микроигл на состояние кожного покрова животные были разделены на 3группы. Группу1 составляли 3особи, которым выполняли процедуру термолиза CO2-лазером на участках спины размером 1,5х1,5см, расположенных слева и справа от позвоночника. В группе2 аналогичные участки спины животных подвергали воздействию RF-микроигл. Особи группы3 (контрольной группы) воздействию не подвергались.
При проведении исследования энергетическое воздействие в экспериментальных группах осуществляли с помощью следующего оборудования:
1) группа1 - лазерный аппарат SmartXide DOT (длина волны 10600нм; мощность лазера 9Вт; длительность импульса 400мкс; расстояние между микротермальными зонами 1000мкм);
2) группа2 - аппаратная платформа EndyMed PRO с применением технологии 3DEEP®, обеспечивающей контролируемую подачу энергии в дерму, и манипулы с 25позолоченными микроиглами (длительность импульса до 200 имп/мс; общая выделяемая энергия до 62мДж/микроигла; глубина погружения 0,1–5,0мм).
Перед началом процедуры экспериментальным животным (группы1 и 2) под общим неингаляционным наркозом на участках воздействия выбривали шерстный покров, после чего проводили обработку антисептическим раствором. После окончания процедуры животных помещали в индивидуальные клетки. Наблюдение в условиях вивария продолжали в течение 47дней. Ежедневно на протяжении всего периода наблюдения регистрировали показатели массы тела, общее состояние животных и состояние кожных покровов, а при наличии изменений выполняли фотофиксацию участков воздействия.
В ходе эксперимента с целью выявления гистологических и патоморфологических изменений в структуре кожных слоев по сравнению с интактной кожей после энергетического воздействия проводили забор биологического материала путем взятия фрагмента кожи спины слева и справа от позвоночника с последующим ушиванием раны простым узловатым швом. Все оперативные вмешательства на животных выполняли с применением двухкомпонентного инъекционного наркоза (золетил/ксилазин). График проведения экспериментальной части исследования с указанием сроков получения образцов представлен в таблице.
График проведения экспериментальной части исследования Schedule of experimental procedures
|
День эксперимента Experimental day |
Процедура исследования Study procedure |
|
День –2 Day –2 |
Отбор контрольных животных (группа3) Selection of control animals (Group 3) |
|
День –1 Day –1 |
Отбор экспериментальных животных (группы 1 и 2) Selection of experimental animals (Groups 1 and 2) Забор биологического материала у контрольных животных (группа3) Biological sample collection from control animals (Group 3) |
|
День 0 Day 0 |
Проведение процедуры воздействия на кожу животных с помощью CO2-лазера (SmartXide DOT; группа1) и RF-микроигл (группа2) Treatment with CO2 laser (SmartXide DOT; Group 1) or RF microneedles (Group 2) |
|
День 14 Day 14 |
Забор биологического материала (фрагмент кожи спины слева от позвоночника) у экспериментальных животных (группы1 и 2) Biological sample collection (a portion of dorsal skin to the left of the spinal column) from experimental animals (Groups 1 and 2) |
|
День 47 Day 47 |
Окончание наблюдения End of the observation period Эвтаназия экспериментальных и контрольных животных (группы 1, 2 и 3) Euthanasia of experimental and control animals (Groups 1, 2 and 3) Забор биологического материала у контрольных животных (группа3) Biological sample collection from control animals (Group 3) Забор биологического материала (фрагмент кожи спины справа от позвоночника) у экспериментальных животных Biological sample collection (a portion of dorsal skin to the right of the spinal column) from experimental animals (Groups 1 and 2) |
Примечание: таблица составлена авторами при подготовке к данному исследованию.
Серийные парафиновые срезы толщиной 3мкм готовили по стандартной методике и окрашивали гематоксилином и эозином. Для выявления в тканях коллагеновых волокон использовали гистохимический метод трихромного окрашивания по Массону. В ходе микроскопического исследования определяли толщину и сохранность эпидермиса, структуру дермы, наличие сально-волосяных комплексов и воспалительного инфильтрата для дальнейшего проведения патоморфологического исследования.
Результаты исследования и их обсуждение
Общее состояние. На протяжении всего периода наблюдения каких-либо отклонений в состоянии их здоровья выявлено не было. Во всех группах была отмечена стабильная динамика набора массы тела. Поведение животных в период наблюдения характеризовалось высокой активностью, естественностью и сопровождалось стабильным эмоциональным состоянием и отсутствием нарушения аппетита. Кроме того, обследование систем и органов животных показало отсутствие патологических изменений.
Состояние кожных покровов. Признаков тусклости, взъерошенности или облысения шерстного покрова не наблюдалось. В первые сутки после проведения процедуры у животных группы1 (CO2-лазер) были выявлены покраснения в местах облучения (рис.1).
Рис. 1. Покраснение кожи у особи из группы1 после процедуры воздействия CO2-лазером. Примечание: рисунок составлен авторами по результатам данного исследования
У двух особей внешние признаки изменений разрешились в течение 2суток и отсутствовали до окончания наблюдения. Процесс регенерации послеоперационной раны (с 14-го дня) протекал удовлетворительно при отсутствии инфекционно-воспалительных осложнений. У особей группы2 (RF-микроиглы) в первые дни после процедуры наблюдалась более выраженная и длительная реакция, проявлявшаяся в виде зуда, покраснения и отека кожи. У одной из особей (№1) реакция была наиболее длительной и выраженной, с сохранением отека и покраснения в течение 5 и 7дней соответственно (рис.2).

Рис. 2. Покраснение кожи и расчесы у особи из группы2 после процедуры воздействия RF-микроиглами. Примечание: рисунок составлен авторами по результатам данного исследования
Морфологическое исследование образцов. Результаты микроскопического исследования биоматериала, полученного у экспериментальных животных на 14-й день, свидетельствовали о наличии более выраженных морфологических изменений в группе1. Помимо истончения эпидермиса у одной особи (№3), лазерное воздействие способствовало изменениям стратификации сетчатого слоя дермы (особь №2; рис.3) и коллагеновых волокон (особь №3). При этом изменения в дерме у животных из группы2 были выражены в меньшей степени, за исключением ангиоматоза у крысы №3, который сопровождался воспалительной реакцией в поверхностном слое дермы (рис. 4).
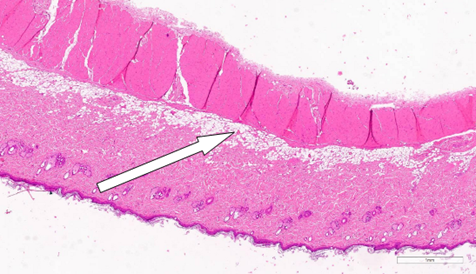
Рис. 3. Очаговое нарушение стратификации сетчатого слоя дермы на 14-й деньпосле процедуры воздействия CO2-лазером. Окрашивание гематоксилином и эозином (х200). Примечание: рисунок составлен авторами по результатам данного исследования
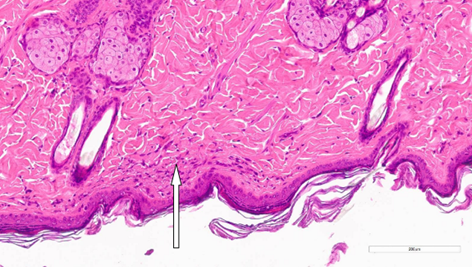
Рис. 4. Скудная воспалительная инфильтрация в поверхностном слое дермы на 14-й день после процедуры воздействия RF-микроиглами. Окрашивание гематоксилином и эозином (х400). Примечание: рисунок составлен авторами по результатам данного исследования
Гистологическая картина, полученная по результатам микроскопического исследования образцов на 47-й день, отражала более показательные изменения, свидетельствующие о пролонгированном действии аппаратов. Так, у всех экспериментальных животных во второй контрольной точке наблюдалось истончение эпидермиса, сопровождавшееся развитием выраженного фиброза дермы у 2особей из каждой группы. Микроскопическое исследование образцов особей из группы1 при малом увеличении (х5) демонстрирует выраженное уменьшение количества сально-волосяных комплексов вплоть до полного их исчезновения при отсутствии атрофии. При большем увеличении (х400) гистологическая картина характеризуется уплотнением сетчатого слоя дермы при наличии фиброза. После окрашивания по Массону просматривается сосочковый слой дермы, представленный плотно упакованными коллагеновыми волокнами (рис.5–7).
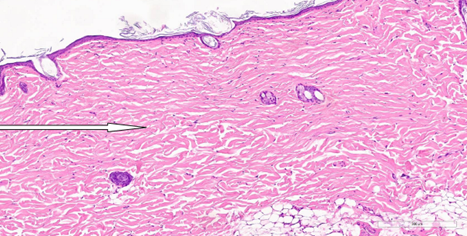
Рис. 5. Уплотнение сетчатого слоя дермы с фиброзом на 47-й день после процедуры воздействия CO2-лазером. Окрашивание гематоксилином и эозином (х400).
Примечание: рисунок составлен авторами по результатам данного исследования
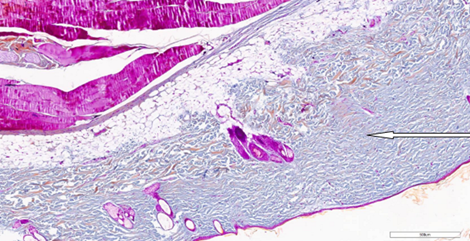
Рис. 6. Плотно упакованные коллагеновые волокна в сосочковом слое дермы на 47-й день после процедуры воздействия CO2-лазером. Окрашивание по Массону (х200).
Примечание: рисунок составлен авторами по результатам данного исследования
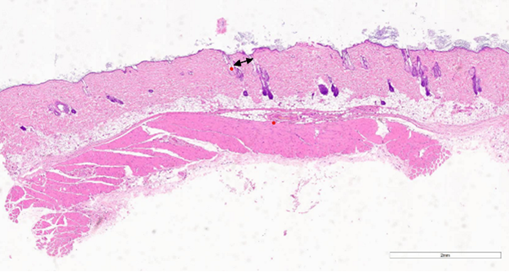
Рис. 7. Уменьшение количества сально-волосяных комплексов на 47-й день после процедуры воздействия CO2-лазером. Окрашивание гематоксилином и эозином (х5). Примечание: рисунок составлен авторами по результатам данного исследования
При проведении гистологического исследования образцов, полученных у особей из группы 2, можно проследить наличие очагового истончения эпидермиса и фиброза (рис.8) при выраженном уменьшении количества сально-волосяных комплексов (рис.9). Вместе с тем у одной из особей группы2 можно наблюдать отсутствие морфологических изменений в дерме, которые могли бы указывать на эффект энергетического воздействия (рис.10).
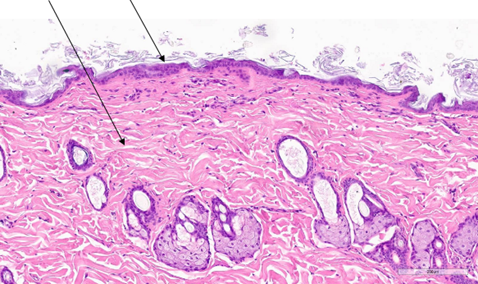
Рис. 8. Очаговое истончение эпидермиса и очаговый фиброз поверхностного слоя дермы на 47-й день после процедуры воздействия RF-микроиглами.
Окрашивание гематоксилином и эозином (х400).
Примечание: рисунок составлен авторами по результатам данного исследования
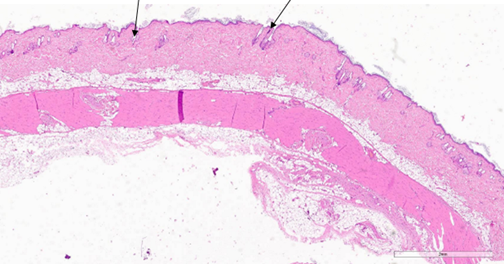
Рис. 9. Уменьшение количества сально-волосяных комплексов на 47-й день после процедуры воздействия RF-микроиглами. Окрашивание гематоксилином и эозином (х5).
Примечание: рисунок составлен авторами по результатам данного исследования
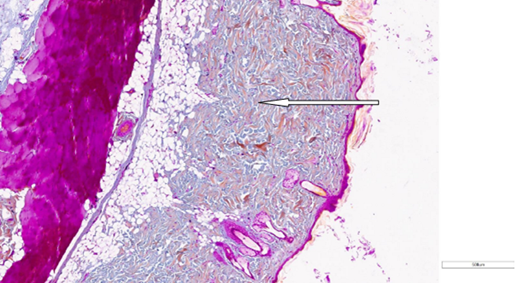
Рис. 10. Сохранение стратификация сетчатого слоя дермы на 47-й день после процедуры воздействия RF-микроиглами. Окрашивание по Массону (х200).
Примечание: рисунок составлен авторами по результатам данного исследования
Во всех образцах, полученных у животных контрольной группы в обеих контрольных точках, отмечены отсутствие изменений со стороны эпидермиса и дермы, равномерное расположение сально-волосяных комплексов по всему периметру кожи при отсутствии признаков воспалительной инфильтрации. Сетчатый слой дермы был представлен волокнистой соединительной тканью (рис.11).
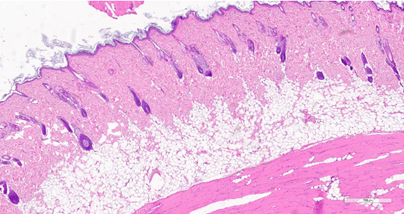
Рис. 11. Образец кожи особи из контрольной группы.
Окрашивание гематоксилином и эозином (х5).
Примечание: рисунок составлен авторами по результатам данного исследования
Обсуждение
Как показывают результаты проведенного исследования, косметологические аппараты на основе CO2-лазера и RF-микроигл оказали в целом схожее влияние на клеточные структуры кожи лабораторных животных. Особого внимания заслуживает тот факт, что наиболее выраженные изменения были зафиксированы во второй контрольной точке (47-й день), что свидетельствует о наличии отсроченного терапевтического действия аппаратов. Принцип действия методов энергетического воздействия основан на создании контролируемых микроповреждений кожного покрова, в результате чего происходит запуск естественных репаративных процессов в тканях, которые сопровождаются обновлением клеточного состава кожи и стимуляцией выработки коллагена и эластина.
Проведенный J.Feng и соавт. транскриптомный анализ показал, что после энергетического воздействия максимальная экспрессия генов, отвечающих за регенерацию коллагена, была зарегистрирована спустя 1месяц после проведенной процедуры с постепенным снижением в течение полугода[13]. J.S.Orringer и соавт.[14] в своем исследовании отмечают, что непосредственно после применения аппаратных методов воздействия, в частности после абляционной лазерной терапии, закономерно наблюдается повышение уровней провоспалительных цитокинов интерлейкина1 (IL-1) и фактора некроза опухоли-альфа (TNF-α) с достижением максимальной концентрации на 6-й день. Поскольку данные цитокины являются индукторами матриксных металлопротеиназ (MMP), в течение первых трех суток после процедуры можно наблюдать значительное повышение уровней MMP-1, MMP-3, MMP-9, MMP-13, сохраняющееся в течение 14–28дней. При этом внеклеточная MMP-1, катализирующая деградацию поврежденного коллагена, возрастает почти в 40000 раз по сравнению с исходным уровнем. Процесс образования нового коллагена запускается на фоне снижения концентрации MMP и выработки профиброгенного трансформирующего фактора роста β1 (TGF-β1). Данные наблюдения были позднее подтверждены в работе B.M.Hantash и соавт. применительно к процедурам радиочастотной терапии[15].
В настоящем исследовании процесс активации TGF-β1 отражен фиброзной трансформацией дермы в раннем постпроцедурном периоде, результатом чего является увеличение интенсивности образования новых коллагеновых волокон в исследуемых образцах. Аналогичные наблюдения, свидетельствующие об увеличении фиброзной ткани в сосочковом слое дермы через 8недель после воздействия CO2-лазером, были отмечены в исследовании A.L.Berlin и соавт.[16]. Возникновение фиброза после абляционной лазерной терапии, по мнению B.S.Wind[17] и соавт., может являться признаком ремоделирования дермального матрикса, обеспечивающего эффект повышения плотности и эластичности кожи.
При этом на запуск процесса неоколлагеногенеза также указывало отсутствие параллельной ориентации коллагеновых волокон, представляющее собой естественный этап первичной репарации и ремоделирования дермы после контролируемого энергетического воздействия. Подобная гистологическая картина, отражающая процесс коагуляции коллагена в результате воздействия CO2-лазером с последующим образованием нового коллагена, описана в исследовании S.M.A.Baleg и соавт.[4].
Одним из значимых терапевтических эффектов проведенных процедур является ремоделирование эпидермального слоя, проявляющееся в виде его истончения. В группе1 (CO2-лазер) подобное изменение можно было наблюдать уже через 2недели после воздействия, тогда как в группе2 (RF-микроиглы) процесс возник значительно позже. Данный результат имеет существенное клиническое значение, поскольку гипертрофированный роговой слой является одним из факторов, обусловливающих формирование неровного микрорельефа кожи. При этом радиочастотные устройства предназначены для контролируемого воздействия на структуры дермы при минимизации повреждения эпидермиса. RF-терапия характеризуется способностью стимулировать пролиферацию эпидермальных клеток за счет активации выработки различных факторов роста. Так, S.B.Cho и соавт. в раннем постпроцедурном периоде (3, 7 и 14-й дни после биполярной РЧ-терапии) обнаружили увеличение толщины эпидермиса и дермы у мышей[18]. В другом исследовании реэпителизация эпидермиса после RF-процедуры с неизолированными микроиглами у свиней полностью завершилась через 2недели после процедуры[19]. Вместе с тем, как указывают I.Snast и соавт., воздействие CO2-лазером может сопровождаться даже более короткими сроками реэпителизации (7–14дней)[20].
В то же время контролируемое истончение поверхностного слоя кожи в результате воздействия комплекса биостимулирующих эффектов обеспечивает индукцию процессов регенерации за счет активации фибробластов, оптимизацию клеточной архитектоники, восстановление межклеточных связей и, как следствие, нормализацию обновления кожи на клеточном уровне. В одном из исследований по изучению гистологических эффектов воздействия CO2-лазером у крыс наблюдалось статистически значимое уменьшение толщины эпидермиса после процедуры (р=0,009)[4].
изменение морфологии сально-волосяных комплексов и уменьшение их количества после CO2-лазера и воздействия RF-микроиглами можно рассматривать как благоприятный эффект, опосредующий снижение секреторной активности сальных желез и объема продуцируемого кожного сала. Данные факторы способствуют уменьшению риска формирования акне и других воспалительных элементов.
Полученные клинико-экспериментальные данные свидетельствуют о том, что методика с применением RF-микроигл, объединяющая энергетическую и механическую составляющие, характеризуется более выраженной агрессивностью воздействия. Мониторинг состояния кожных покровов в первые дни после проведения процедуры выявил более интенсивную и продолжительную воспалительную реакцию в группе2, проявлявшуюся в виде зуда, стойкой гиперемии и локального отека тканей, что согласуется с результатами других экспериментальных исследований[18; 19]. Выраженная клиническая симптоматика в постпроцедурном периоде, наряду с замедленной динамикой регрессии побочных эффектов при проведении воздействия RF-микроиглами, свидетельствует о более глубоком и интенсивном повреждении тканей по сравнению с CO2-лазером.
Заключение
Спектр показаний к применению РЧ-терапии и CO₂-лазеров постоянно расширяется благодаря совершенствованию технологий и накоплению клинического опыта. Вместе с тем для достоверной оценки клинических результатов необходимо располагать объективными гистологическими данными, отражающими структурные преобразования на клеточном уровне в динамике. Несмотря на наличие существенных различий в принципах действия, механизмах и динамике процессов ремоделирования, косметологические аппараты на основе CO2-лазера и RF-микроигл позволяют получить схожие клинические результаты. Течение постпроцедурного периода после проведения процедур с применением каждой из методик сопровождалось развитием ожидаемых клинических и гистологических эффектов. Более интенсивный характер гистологических изменений, в том числе отсроченных, наблюдавшихся после воздействия CO₂-лазером, свидетельствует о возможности получения более значимого клинического улучшения. Вместе с тем, учитывая выраженность побочных эффектов, отмеченных после терапии РЧ-микроиглами, следует помнить о необходимости тщательного подбора параметров воздействия для минимизации рисков и достижения оптимальных результатов.



