Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
ASPECTS OF COMORBIDITY AND DIFFERENTIAL DIAGNOSTICS OF DISFAGIA, OWN CLINICAL OBSERVATION
Введение
Дисфагия может быть симптомом широкого спектра заболеваний как хирургического, так и терапевтического профиля [1], может иметь смешанную этиологию [2]. В ряде случаев можно рассматривать дисфагию как гериатрический синдром: так, по данным различных источников, от 10 до 33% пожилых людей, перенесших инсульт или страдающих нейродегенеративными заболеваниями, такими как болезнь Альцгеймера или болезнь Паркинсона, имеют жалобы на нарушение глотания. Пациенты с диагнозом дисфагии могут страдать от недоедания, пневмонии и обезвоживания, что, безусловно, приводит к необходимости длительного пребывания в лечебном учреждении, снижает качество жизни пациента и может быть причиной летального исхода [3].
Симптом дисфагии – это прежде всего жалоба пациента на ощущение дискомфорта при проглатывании пищи или жидкости от полости рта до желудка, которое не сопровождается болью. Дисфагия ухудшает физическое состояние пациента [4].
Дисфагия по происхождению может быть ротоглоточной или пищеводной. Установлено, что встречаемость дисфагии зависит от возраста пациентов и нозологии, при которых развивается данный симптом [5]. Дисфагия диагностируется чаще при травмах головы, шеи, при онкологических заболеваниях полости рта и горла у молодых пациентов, при поражении ЦНС у людей старшего возраста [1] (рис.1).
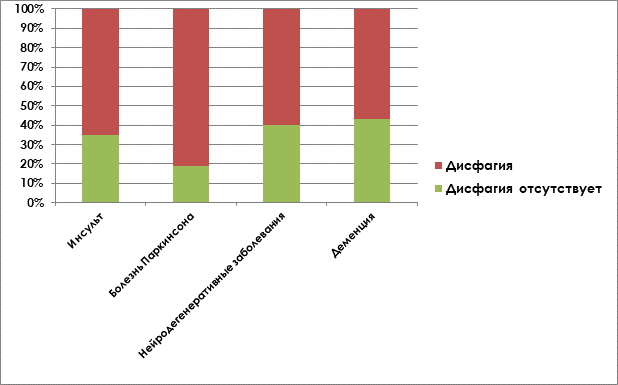
Рис.1. Распространенность дисфагии при различных неврологических заболеваниях.
Примечание: составлен авторами по результатам источников [1–5]
В то же время дисфагия может быть симптомом и достаточно редких заболеваний. Она наблюдается, например, при поражении пищевода красным плоским лишаем [6; 7].
Глотание – сложный физиологический акт, в реализации которого участвуют мышцы языка, челюстно-лицевого аппарата, мягкого неба, глотки и пищевода. Согласованная деятельность этих структур обеспечивает продвижение пищевого комка из полости рта в пищевод и желудок. В реализации этого физиологического процесса задействованы 26 мышц, он иннервируется шестью парами черепных нервов, тремя парами верхних шейных нервов. Координирует работу челюстно-лицевого, глоточного и языкового аппарата центр глотания, расположенный в продолговатом мозге. Со стороны ЦНС происходит эфферентная иннервация из прецентральной извилины через волокна кортико-нуклеарного тракта [8]. Патологические процессы на любом из перечисленных выше уровней (кора головного мозга, эфферентные пути или ядра черепных нервов (IX, X, XII), расположенные в стволе) могут привести к развитию дисфагии.
Можно выделить следующие виды дисфагии по этиологическому принципу: нейрогенная дисфагия, органическая дисфагия, ятрогенная дисфагия, психогенная дисфагия.
Определить уровень и механизм дисфагии достаточно трудно без знания анатомо-физиологических особенностей акта глотания, в котором выделяют четыре фазы [1] (рис.2).
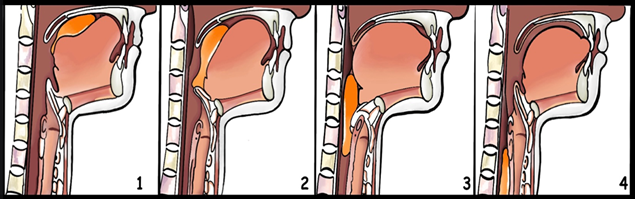
Рис.2. Механизм физиологического акта глотания (фазы: 1 – ротовая фаза; 2 – ротоглоточная фаза; 3 – глоточная фаза; 4 – пищеводная фаза).
Примечание: составлен авторами по источнику [1]
Цель исследования – провести дифференциальную диагностику дисфагии и представить клинический случай, в котором отражается сложность диагностики коморбидного пациента с нарушением глотания.
Материал и методы исследования
Материалом исследования послужил клинический случай пациента П., 75 лет, поступившего в Госпиталь для ветеранов войн Санкт-Петербурга для диагностики и лечения нарушения глотания. Использовались как клинические, так и лабораторно-инструментальные методы, такие как оценка неврологического статуса пациента, осмотр логопеда, клинический и биохимический анализы крови, серологический анализ крови, клинический и биохимический анализ ликвора, спектральная компьютерная томография, гибридная технология визуализации, которая сочетает позитронно-эмиссионную томографию и магнитно-резонансную томографию (ПЭТ-МРТ) пищевода.
Результаты исследования и их обсуждение
Жалобы при поступлении: затруднение глотания жидкой и твердой пищи, отрыжка, слюнотечение, общая слабость, головокружение, похудение на 36 кг за 2 года.
Anamnesis morbi. Пациента П. в последние 1,5 года беспокоит затруднение проглатывания пищи, ощущение «застревания» пищи за грудиной, ротовые срыгивания, пациент похудел на 36 кг за 2 года. Обращался в поликлинику по месту жительства, была попытка выполнения фиброгастродуоденоскопии, однако полноценно выполнить исследование не удалось, результаты были малоинформативны. Других исследований не выполнялось.
Anamnesis vitae. Пациент П., родился в 1950 г. в Ленинграде. Образование – специальное среднее. Пенсионер, живет с взрослым сыном. Бытовые условия удовлетворительные. Вредные привычки: курение (1 пачка / 30 лет). Употребление алкоголя умеренное. Эпидемиологический анамнез не отягощен. Выезд за пределы Ленинградской области отрицает. Контакт с инфекционными больными отрицает. Переливание крови и ее компонентов отрицает. Аллергологический анамнез спокойный. Наследственность не отягощена.
Данные физикального осмотра. Состояние пациента средней степени тяжести. Пациент астеничен, фон настроения снижен. При осмотре положение в постели активное. Телосложение астеническое: рост – 175 см, масса тела – 58 кг. Осанка прямая, походка атаксическая. Температура тела: 36,7 ºС. Выражение лица: спокойное. Кожные покровы обычного цвета, высыпаний нет, подкожно-жировая клетчатка слабо выражена, периферических отеков нет. Лимфатические узлы пальпаторно не увеличены. Язык обложен белым налетом. Костно-суставная система без патологии, объем активных и пассивных движений в суставах полный. Грудная клетка правильной формы, дыхание везикулярное, хрипов нет, SpO2 – 98%, ЧДД – 16 в минуту. Тоны сердца приглушены, ритмичные, АД – 125/85ммрт.ст., Ps – 75 ударов в минуту. Печень по правому краю реберной дуги, селезенка не пальпируется, стул, со слов больного, обычного цвета и консистенции, со склонностью к запорам. При осмотре per rectum: на перчатке следы кала коричневого цвета Живот при пальпации мягкий, безболезненный. Мочеиспускание, со слов больного, самостоятельное, безболезненное.
Неврологический статус. Сознание ясное. Общемозговых симптомов не наблюдается. Черепные нервы: обоняние сохранено. Снижения остроты зрения не отмечает, поля зрения ориентировочным методом не нарушены. Движения глазных яблок в полном объеме. Зрачки правильной формы, среднего диаметра, D=S. Реакция зрачков на свет живая, симметричная (прямая и содружественная). Чувствительность лица: гипостезия слева, пальпация точек выхода веточек тройничного нерва безболезненна. Жевательная мускулатура сохранна. Лицо асимметрично, надбровные и роговичные рефлексы снижены слева. Слух снижен по возрасту на оба уха. Глотание и фонация умеренно нарушены, глоточный рефлекс снижен. Язык без патологических изменений, по средней линии, фасцикуляции не наблюдаются. Рефлексы орального автоматизма отсутствуют. Двигательная активность в плечевом поясе и мышцах шеи сохранена. Двигательная система: мышцы гипотрофичны, мышечный тонус в руках и ногах физиологический. Сила в мышцах рук и ног сохранена. Рефлексы с рук: карпорадиальные, бицепс- и трицепс-рефлексы средней живости D=S; с ног – коленные, ахилловы снижены D=S. Патологических рефлексов с рук и ног не выявлено. Чувствительность сохранена. Координаторные пробы: пальценосовую пробу выполняет с интенцией с двух сторон, пяточно-коленную пробу – удовлетворительно с двух сторон. В позе Ромберга простой и усложненной неустойчив без выраженной латерализации. Менингеальные знаки не выявлены. Пальпация паравертебральных точек безболезненная.
Таким образом, клиническая картина представлена поражением черепных нервов (V, VII, IX) по периферическому типу, вестибуломозжечковым синдромом и кахексией, так как потеря массы тела составляла на момент осмотра 38% от исходного. Нарушения глотания у данного пациента имели смешанный характер: затруднения при глотания жидкой пищи в сочетании с результатами неврологического осмотра (поражением черепных нервов (V, VII, IX) по периферическому типу) указывало на наличие бульбарного синдрома, а затруднение глотания твердой пищи с ротовыми срыгивания – на проблемы в пищеводе или органах средостения. Таким образом, пациент требовал комплексного обследования не только со стороны нервной системы, но и желудочно-кишечного тракта и органов средостения, в том числе щитовидной железы.
Дифференциальная диагностика в данном клиническом случае проводилась между вирусным поражением черепных нервов, сосудистым поражением головного мозга с преобладанием в вертебрально-базилярном бассейне и неопластическим процессом пищевода.
Лабораторные результаты. По данным биохимического анализа крови выявлен повышенный уровень креатинфосфокиназы до 859 ед/л. (норма – 30–200), общий анализ мочи – в пределах нормы. Выявлены серологические признаки обострения хронической латентной вирусной инфекции Эпштейна – Барр и рецидива инфекции ВПГ-1,2.
В ликворе был выявлен сначала лимфоцитарный (99%), а затем нейтрофильный (11%) плеоцитоз, гиперпротеинархия (3,3 г/л) в обеих пробах, гипогликархия (1,81 ммоль/л) во второй пробе, имело место нарастание степени помутнения в реакции Панди.
Компьютерная томография головы без введения контрастного вещества. В аксиальной плоскости с последующим построением многоплоскостных реконструкций, определяется: «свежие» участки патологической плотности вещества головного мозга не определяются. Ликворные кисты в базально-ядерной области с двух сторон до 5 мм.
Пара- и перивентрикулярно боковым желудочкам отмечаются поля лейкоареоза.
Дифференцировка белого и серого вещества в остальных отделах сохранена.
Срединные структуры головного мозга не смещены. Миндалины мозжечка на уровне БЗО.
Боковые желудочки не расширены, асимметричны. III и IV желудочки не расширены. Охватывающая цистерна не расширена, не деформирована. Субарахноидальное пространство головного мозга выражено неравномерно, расширено. Отмечается физиологическое обызвествление шишковидной железы и сосудистых сплетений задних рогов боковых желудочков.
В сифонах внутренних сонных артерий, обеих позвоночных артериях кальцинированные атеросклеротические бляшки.
Отмечаются расширенные периваскулярные пространства.
Утолщение слизистой оболочки единичных клеток решетчатого лабиринта. Подушкообразное утолщение слизистой оболочки в левой верхнечелюстной пазухе. Пневматизация остальных околоносовых пазух в зоне сканирования сохранена. Воздушность ячеек сосцевидных отростков, барабанных полостей не изменена.
Костных травматических и деструктивных изменений костей мозгового черепа не выявлено.
Заключение
Свежих ишемических изменений на момент исследования, участков кровоизлияний и образований в веществе головного мозга не выявлено. Ликворные кисты в базально-ядерной области с двух сторон. Расширение наружных ликворных пространств, вероятно, заместительного характера. Атеросклероз церебральных артерий. КТ-признаки ангиоэнцефалопатии. Утолщение слизистой оболочки единичных клеток решетчатого лабиринта. Подушкообразное утолщение слизистой оболочки в левой верхнечелюстной пазухе.
Спектральная компьютерная томография пищевода. Выявлена усиленная и дискоординированная перистальтика в средней и нижней трети пищевода, отмечено диффузное утолщение стенки средней трети до 7 мм на протяжении 6 см (рис.3).
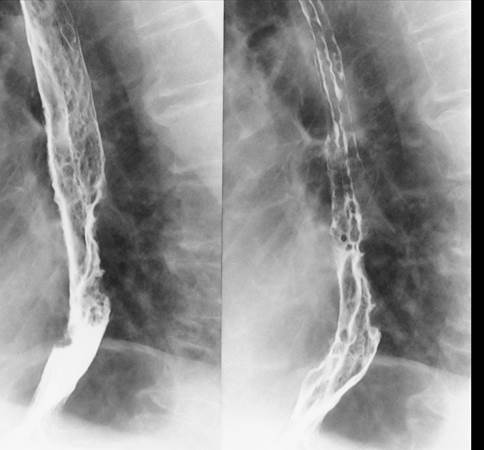
Рис.3. Гастроптоз со спадением, деформацией и циркулярным сужением нижней трети пищевода при выявленной онкологии (КТ-гастро-томографии пациента с контрастным усилением висмутом бария).
Примечание: из личного архива авторов
Учитывая полученные данные неврологического статуса, лабораторных и инструментальных исследований, был поставлен вопрос о происхождении дисфагии у пациента П. С одной стороны, развитие дисфагии могло быть связано с невропатией черепных нервов вирусного генеза (с учетом лабораторных данных), но, принимая во внимание, что пациент болеет на протяжении двух лет и основной его жалобой было постепенное снижение массы тела и нарушение глотания жидкой и твердой пищи, было принято решение, что дисфагия может иметь смешанный генез, в том числе и пищеводный, и возникла вследствие сужения нижней трети пищевода, что приводило к нарушению прохождения пищи в желудок. Было проведено ПЭТ-МРТ пищевода и желудочно-кишечного тракта, которое выявило очаг новообразования пищевода, иммуногистохимическое исследование биопсийного материала верифицировало его как лейомиосаркому пищевода (T1N0M0).
Пациенту П. был поставлен диагноз: лейкосаркома пищевода (Т1N0M0), пищеводная органическая дисфагия; сопутствующий диагноз цереброваскулярная болезнь 2 ст., энцефалопатия смешанного генеза (сосудистая, постинфекционная) преимущественно в вертебрально-базилярном бассейне с поражением ядер черепных нервов V, VII, IX, X пар черепных нервов в виде бульбарного синдрома. Пациент был прооперирован. В послеоперационном периоде проводилось лечение, направленное на улучшение функции черепных нервов. На момент выписки глотание было полностью восстановлено, отмечено увеличение массы тела пациента на 4,5 кг.
Определение вида дисфагии имеет принципиальное значение для дальнейшей тактики лечения пациента. Рассмотрим особенности фаз глотания и клинические проявления у пациентов. Ротовая фаза осуществляется иннервацией из коры головного мозга предцентральной извилины при участии V, VII, XII пар черепных нервов. Клинические проявления нарушения на уровне этой фазы представлены следующими симптомами: дисфагия на уровне поражения ротовой полости и глотки, сложность начала глотания, удушье или кашель при глотании, слюнотечение, носовые срыгивания. Сопутствующие симптомы: «носовая речь» (назолалия), ослабленный кашлевой рефлекс, дизартрия или диплопия при взгляде. Ротоглоточная и глоточная фазы – это непроизвольный двигательный акт представлен врожденным (безусловным) рефлексом, который реализуется на уровне ствола головного мозга при участии V, IX, X, XI пар черепных нервов. Пищевой комок проходит через глотку за 0,3–0,5с, что является быстрой непроизвольной фазой. Клинические проявления этих фаз аналогичны ротовой. Пищеводная фаза – медленная непроизвольная фаза, непроизвольный двигательный акт. Осуществляется при участии Х пары черепных нервов, трех пар верхних шейных нервов. По пищеводу жидкость продвигается за 2–3с, пищевой комок – за 7–8с. При поражении на уровне пищевода дисфагия сопровождается ощущением «застревания» пищи за грудиной, ротовыми или носовыми срыгиваниями, необходимостью пациента запивать пищу.
Для диагностики нарушений глотания используются рентгенологические методы – исследование акта глотания с барием и эндоскопия [10, с. 35]. Эндоскопия пищеварительного тракта играет важную роль как в диагностике, так и в лечении многих заболеваний пищевода. Например, пероральная эндоскопическая миотомия – относительно новая методика, которая позволила добиться прогресса в малоинвазивном лечении ахалазии. Манометрия высокого разрешения является специфическим методом диагностики эзофагеальной дисплазии [11]. Фибробронхоскопия и pH-метрия пищевода проводятся пациентам по показаниям [12; 13].
Нарушение глотания может быть симптомом широкого спектра заболеваний. Это может быть связано с поражением IX и X пар черепных нервов сосудистого, постинфекционного, интоксикационного, неопластического и аутоиммунного генеза в виде периферического поражения с клинической картиной невропатии или при поражении ядер данных нервов в виде бульбарного или волокон кортико-нуклеарного пути в виде псевдобульбарного паралича. Помогают в диагностике современные методы лучевой диагностики: мультиспиральная компьютерная томография, сверхвысокопольная МРТ. В настоящее время используются гибридные методы: ПЭТ-КТ и ПЭТ-МРТ, которые дают возможность оценить как морфологические, так и метаболические изменения при патологических состояниях пищевода [14; 15].
Заключение
В представленном клиническом случае рассмотрено коморбидное состояние пациента, обусловленное поражением нервной системы (сосудистым и постинфекционным) и онкологическим заболеванием пищевода. Данные патологические состояния привели к развитию дисфагии, которая была обусловлена как поражением двигательных ядер черепно-мозговых нервов, так и поражением мышечного слоя нижней трети пищевода. Следует отметить, что грамотно собранный анамнез, внимательно проведенный неврологический осмотр с детализацией оценки функции глотания с привлечением логопеда, а также широта клинического мышления, позволившая врачу-неврологу рассмотреть иные механизмы нарушения глотания, в том числе связанные с заболеваниями пищевода, позволили правильно выстроить план диагностических мероприятий и поставить верный клинический диагноз. Все вышеизложенное привело к своевременной адекватной терапии онкологического заболевания и привело к улучшению общего состояния пациента и регрессу дисфагии. Использование современного метода лучевой диагностики (ПЭТ-МРТ) обеспечило выявление опухоли пищевода и проведение оперативного лечения, которое способствовало своевременному удалению выявленного первичного очага новообразования пищевода. Необходимо отметить, что обследование пациентов с дисфагией требует мультидисциплинарного подхода, должно быть максимально ориентированным на пациента и комплексным так как причиной нарушения глотания могут быть и соматические заболевания.
Conflict of interest
Financing
Библиографическая ссылка
Соколова М.Г., Привалова М.А., Поляков Ю.И., Шавуров В.А., Осипова М.В., Сотников Н.С. АСПЕКТЫ КОМОРБИДНОСТИ И ДИФФЕРЕНЦИАЛЬНАЯ ДИАГНОСТИКА ДИСФАГИИ, СОБСТВЕННОЕ КЛИНИЧЕСКОЕ НАБЛЮДЕНИЕ // Современные проблемы науки и образования. 2026. № 3. ;URL: https://science-education.ru/en/article/view?id=34519 (дата обращения: 10.06.2026).
DOI: https://doi.org/10.17513/spno.34519



