Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
THE ROLE OF FLUORESCENCE ANGIOGRAPHY, BIOMICROSCOPY, SEVEN-FIELD COLOR FUNDUS PHOTOGRAPHY IN ASSESSING THE ACTIVITY OF NEOVASCULARIZATION AFTER PANRETINAL LASER COAGULATION IN THE TREATMENT OF PROLIFERATIVE DIABETIC RETINOPATHY
Введение
Сахарный диабет (СД) во всем мире признан одной из основных причин инвалидности и смертности. Количество больных постоянно увеличивается в связи с ростом численности и возраста населения, увеличения распространенности обменных нарушений и гиподинамии. На сегодняшний день число больных СД в мире достигает более 589 миллионов, а к 2050 году увеличится до 853 миллионов [1-3]. В Российской Федерации диабетическая ретинопатия (ДР) занимает 5 место в структуре глазных болезней после нарушений рефракции, катаракты, конъюнктивита и глаукомы [4]. Среди пациентов с СД I и II типа ДР диагностируется в 7-8% случаев [5].
Впервые метод фотокоагуляции при лечении пролиферативной ретинопатии (ПДР) был применен в 1959 году Meyer-SchwickerathG. R. c использованием излучения ксеноновой лампы [6], и до сих пор, уже более 65 лет, панретинальная лазерная коагуляция (ПРК) является стандартом лечения и методом профилактики слепоты при ПДР.
Первым методом оценки ДР стала прямая и непрямая офтальмоскопия, которая при наличии опыта, расширенном зрачке и достаточно высокой прозрачности оптических сред глаза пациента позволяет достаточно точно поставить диагноз диабетической ретинопатии и определить ее стадию. Полученные данные при данном варианте исследования можно описать словами или зарисовать, рискуя упустить ряд важных деталей для последующего динамического наблюдения, контроля эффективности лечения или получения второго мнения.
Стандартное фотографирование глазного дна [7], которое захватывает лишь 30 градусов глазного дна, позволило документировать состояние сетчатки пациента, а при использовании цифровых технологий увеличивать изображение для поиска мелких деталей, характеризующих патологический процесс. Съемка нескольких полей глазного дна, объединенных в композиционное изображение с углом обзора 75°, значительно увеличивает возможности (рис. 1). Семипольное фотографирование глазного дна со съёмкой стереопар изображений использовалось в самом известном исследовании ETDRS [8; 9]. Данная технология позволила зафиксировать зоны интраретинальной микрососудистой аномалии (ИРМА) и эпиретинальной неоваскуляризации на значительном удалении от заднего полюса и тем самым повысить диагностическую ценность исследования.
Не так давно была разработана широкоугольная фундус-камера, которая позволяет получать изображения периферической части сетчатки. Новые фундус-камеры могут снимать с углом обзора до 200°, даже если зрачок не расширен, что позволяет просматривать более 80% общей площади сетчатки [10]. С одной стороны, это дает большие преимущества для выявления периферических изменений сетчатки быстро и максимально неинвазивно. С другой стороны, возможно искажение периферических изображений, обусловленных сферический формой глазного яблока. Данная фундус-камера является весьма дорогостоящей, и ее регистрация не проведена в Российской Федерации, что делает ее использование в России невозможным. Как у нас в стране, так и за рубежом семипольное 30-градусное фотографирование остается «золотым стандартом» до сих пор.
Американская диабетическая ассоциация (ADA) утверждает, что фундус-фотография может использоваться в качестве инструмента скрининга для выявления ретинопатии у пациентов с диабетом, но не заменяет офтальмологическое обследование. Ассоциация по-прежнему рекомендовала всем пациентам с диабетом проходить обследование у офтальмолога, включающее осмотр глаз с широким зрачком [11].
В 1961 году была описана и в 1967 году внедрена в клиническую офтальмологию Гассом флюоресцентная ангиография (ФАГ), которая стала «золотым стандартом» оценки сосудистой сети сетчатки, в том числе и при сахарном диабете [12-14]. Данная технология позволила визуализировать зоны с отсутствующим кровообращением в капиллярах сетчатки, получившие название зон ишемии, а также аномальные кровеносные сосуды, расположенные внутри сетчатки – ИРМА, эпиретинальную и папилловитреальную неоваскуляризации, вызывающие просачивание красителя, по которому можно определить даже незначительную по площади неоваскуляризацию.
С появлением широкопольных фундус-камер стала возможной и широкопольная ФАГ, которая позволила оценивать кровообращение в периферических отделах сетчатки и прежде всего выявлять области с отсутствием капиллярной перфузии, которые трудно, а порой и невозможно визуализировать с помощью стандартной ФАГ [15; 16]. Данная технология представляется весьма полезной для пациентов с ДР для выявления риск-факторов развития неоваскулярной глаукомы и оценки эффективности прецизионной лазеркоагуляции, направленной только на зоны ишемии.
ФАГ позволяет визуализировать только поверхностные сосуды сетчатки и не дает информации о сосудах глубокого сплетения и хориоидеи, что не ограничивает ее использования при мониторинге пациентов с ДР. Важно отметить, что данная процедура является инвазивной и может вызвать ряд побочных эффектов от тошноты (у 2,9%) и рвоты (1,2%) до разной степени выраженности аллергических реакций вплоть до анафилактического шока и летального исхода, которые встречаются крайне редко [17-19].
Оптическая когерентная томография в ангиорежиме (ОКТ-А) – это неинвазивный метод исследования, который позволяет получить детальное непрямое изображение физиологических и патологических сосудов в сетчатке и сосудистой оболочке глаза [20].ОКТ-А является относительно новым методом исследования, клиническое применение которого стало возможным благодаря десятилетию исследований, направленных на увеличение скорости сканирования, устранения фоновых шумов и других. В 2012 году была продемонстрирована оптическая когерентная топографическая ангиография микроциркуляторного русла сетчатки человеческого глаза с использованием методов, основанных на амплитуде или интенсивности [21].
Данная технология имеет ряд преимуществ перед ФАГ, являясь неинвазивной, быстровыполнимой, позволяющей выявить новообразованные сосуды, расположенные над внутренней пограничной мембраной и диском зрительного нерва [22]. Однако она не позволяет оценить «активность» неоваскуляризации, так как ее наличие не всегда говорит о том, что сосудистая стенка новообразованных сосудов проницаема.
Целью исследования стало сравнение информативности биомикроскопии глазного дна с широким зрачком, семипольного цветного фотографирования, с семипольной ФАГ, проводимыми для оценки эффективности ПРК, выполненной по поводу ПДР.
Материалы и методы исследования
Материалом для данного исследования послужили наблюдения за 14 пациентами (28 глаз) с ПДР до и после проведения им ПРК, выполняемой с использованием лазерного излучения с длиной волны 532 нм.
Все пациенты до и после лечения подвергались офтальмологическому обследованию, в которое входили стандартные методы обследования, а также биомикроскопия стекловидного тела и сетчатки (БМ), цветное фотографирование, ФАГ.
Биомикроскопия стекловидного тела и сетчатки проводилась в условиях медикаментозного мидриаза с использованием бесконтактной линзы + 60D (Ocular instruments inc., США) и трехзеркальной линзы Гольдмана OG3MA (Ocular instruments inc., США) на щелевой лампе.
Цветное фотографирование и ФАГ выполнялись в 7 зонах (полях) сетчатки по Airlie House с помощью фундус-камеры TRC-NW7FF фирмы Topcon (Япония) с использованием цифровой системы IMAGEnet в условиях медикаментозного мидриаза до проведения ПРК (рис. 1) и через 3, 6, 12 месяцев после лазерного вмешательства. ФАГ проводилась в условиях медикаментозного мидриаза, достигаемого путем инстилляции 1% раствора мидриацила. Оценка флюоресцентных ангиограмм проводилась путем их визуальной расшифровки.
Активность неоваскуляризации оценивали по изменению ее размеров с помощью биомикроскопии сетчатки и цветным фотографиям, а также по результатам ФАГ, позволяющей определить размеры неоваскуляризации на ранних этапах исследования и масштабы просачивания красителя на поздних её фазах.
Статистический анализ проводился отдельно для каждого срока наблюдения - через 3, 6 и 12 месяцев. Исходные данные представляли собой категориальные переменные с тремя градациями: «уменьшение», «стабилизация» и «увеличение» активности неоваскуляризации. Сравнение частот выявления каждой категории между методами осуществлялось попарно: между ФАГ и БМ, а также между ФАГ и цветным фотографированием. Учитывая ограниченный объём выборки (n = 28), для оценки статистической значимости различий использовался точный критерий Фишера (двусторонний тест). Обработка данных выполнена с помощью программного пакета Statistica 12.0 (StatSoft, США). Различия принимались статистически значимыми при p<0,05.
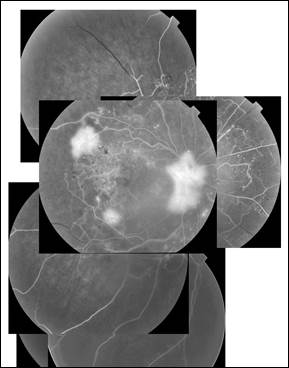
Рис. 1. Композиционный снимок данных флуоресцентной ангиографии левого глаза пациентки О. с тяжелой ПДР до проведения лазерного лечения.
Составлено авторами по результатам данного исследования
Результаты проведенного исследования и их обсуждение
Во все периоды наблюдения (3, 6 и 12 месяцев) статистический анализ с использованием точного критерия Фишера показал (табл.), что БМ и фото достоверно реже выявляют уменьшение активности неоваскуляризации по сравнению с ФАГ через 6 и 12 месяцев наблюдения. Статистически достоверная разница в стабилизации неоваскулярного процесса видна на протяжении всего периода наблюдения. В то время как увеличение активности достоверно через 3 месяца при сравнении БМ и ФАГ, на протяжении дальнейшего периода наблюдения эти различия полностью нивелировались. Нулевая гипотеза о равенстве частот выявления этих категорий между ФАГ и другими методами была отвергнута (p < 0.05, Фишера), что свидетельствует о более высокой чувствительности ФАГ к данным проявлениям динамики патологического процесса.
Динамика неоваскуляризации в различные сроки после ПРК, оцененной с помощью различных методов исследования
|
Срок наблюдения |
3 месяца |
6 месяцев |
12 месяцев |
||||||
|
Динамика активности неоваскуляризации (количество случаев, методы исследования) |
БМ |
Фото |
ФАГ |
БМ |
Фото |
ФАГ |
БМ |
Фото |
ФАГ |
|
Уменьшение |
4 |
2 |
8 |
2 |
6 |
14 |
9 |
10 |
20 |
|
Сравнение с ФАГ (p, Фишера) |
0.3290 |
0.0776 |
- |
0.0008 |
0.0496 |
- |
0.0069 |
0.0151 |
- |
|
Стабилизация |
18 |
15 |
4 |
22 |
16 |
6 |
17 |
14 |
4 |
|
Сравнение с ФАГ (p, Фишера) |
0.0003 |
0.0041 |
- |
0.0000 |
0.0129 |
- |
0.0007 |
0.0090 |
- |
|
Увеличение |
6 |
11 |
16 |
4 |
6 |
8 |
2 |
4 |
4 |
|
Сравнение с ФАГ (p, Фишера) |
0.0129 |
0.2847 |
- |
0.3290 |
0.7585 |
- |
0.6695 |
1.0000 |
- |
Примечание: составлено авторами на основе полученных данных в ходе исследования.
Объяснить полученные данные можно тем, что на фоне хориоретинальных очагов, вызванных ПРК, выявить неоваскуляризацию небольшого размера и оценить степень ее активности очень сложно из-за затруднения визуализации и начавшихся признаков рубцевания фиброваскулярной ткани, которая может еще содержать сосуды с неполноценной сосудистой стенкой, представляющих риск гемофтальма.
ФАГ позволяет более четко визуализировать границы неоваскуляризации, определить ее размер и выраженность транссудации, отражающей активность процесса. Как и предполагалось, наиболее информативным методом оказалась ФАГ.
В качестве примера приводятся цветные фотографии глазного дна и ангиограммы обоих глаз пациента П. (рис. 2). На левом глазу неоваскуляризация видна как на фотографии, так и на ангиограммах. На правом глазу мелкая неоваскуляризация не видна на фотографии и выявляется только на ФАГ.
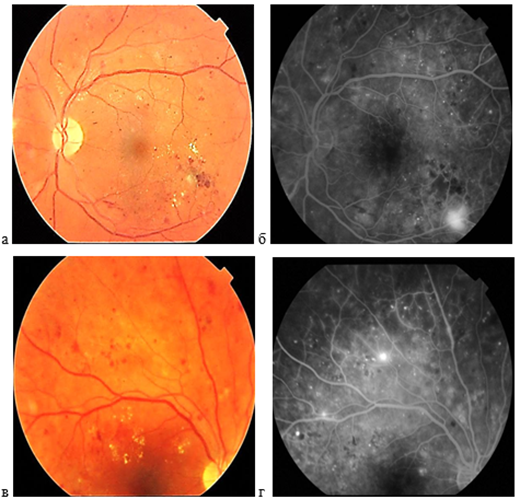
Рис. 2. Цветная фотография глазного дна левого (а) и правого глаза (в) и артериовенозная фаза ФАГ левого глаза (б) и правого глаза (г) больного П.
Составлено авторами по результатам данного исследования
В качестве примера постепенного уменьшения размеров и активности неоваскуляризации через 3 месяца после ПРК и ее постепенного регресса к 12 месяцам наблюдения приводятся ангиографические данные пациентки М. (рис. 3). Такие маленькие по размерам неоваскуляризации на фото и биомикроскопически, как правило, не видны.
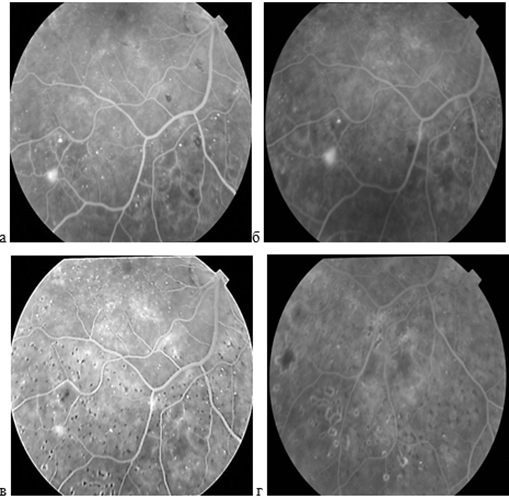
Рис. 3. Данные ФАГ правого глаза пациента М.: а - до ПРК – отчетливо видна зона накопления красителя и просачивания из эпиретинальной неоваскуляризации; б - через 3 месяца эпиретинальная неоваскуляризация немного увеличилась в размере и появилась новая правее и немного выше; в - через 6 месяцев отмечается уменьшение активности неоваскуляризации; г - через 12 месяцев – отсутствие просачивания красителя, полный регресс неоваскуляризации.
Составлено авторами по результатам данного исследования
Только при усилении активности неоваскуляризации все три метода исследования оказались сопоставимы по частоте выявления данного признака. В качестве примера усиления активности неоваскуляризации, ее активного роста, несмотря на проведенную ПРК, приводится динамика данных ангиографической картины пациента В. (рис. 4).
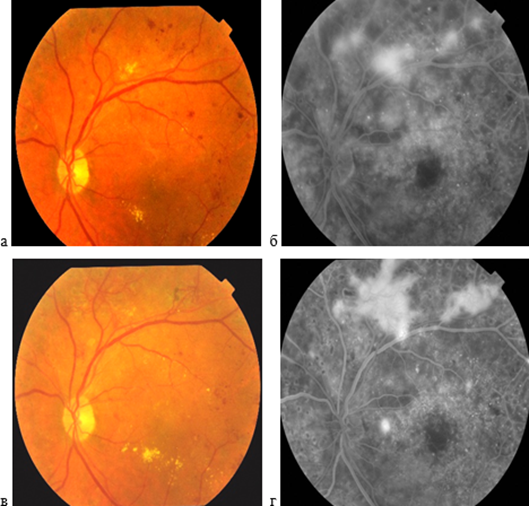
Рис. 4. Цветные фото и ФА левого глаза пациента В. с ПДР 1 стадии: а, б - через 6 месяцев после проведения панретинальной коагуляции; в, г - через 12 месяцев наблюдения.
Составлено авторами по результатам данного исследования
Данный феномен можно объяснить тем, что рост неоваскуляризации, являющийся признаком ее активности, легко заметить даже на фоне выполненной коагуляции сетчатки, так как активно растущие сосуды имеют яркую окраску, мелкую «кружевную» сосудистую сеть, в отличие от рубцующейся фиброваскулярной ткани.
Заключение
Во все периоды наблюдения (3, 6 и 12 месяцев) статистический анализ с использованием точного критерия Фишера показал, что БМ и цветное фотографирование достоверно реже выявляют уменьшение и стабилизацию активности неоваскуляризации по сравнению с ФАГ. В то же время при оценке увеличения активности неоваскуляризации различия между методами через 6 и 12 месяцев наблюдения не достигали уровня статистической значимости (p>0.05, Фишера), что говорит о сопоставимой способности выявления прогрессирования неоваскулярного процесса всех трёх методов исследования.
Полученные результаты исследования свидетельствуют о том, что при проведении научных исследований, связанных с оценкой динамики неоваскулярного процесса, а также в клинической практике недостаточно руководствоваться данными, полученными только с помощью биомикроскопии и цветного фотографирования. Роль ФАГ остается наиболее информативной технологией исследования.
Conflict of interest
Financing
Библиографическая ссылка
Гацу М.В., Борзилова Ю.А. РОЛЬ ФЛЮОРЕСЦЕНТНОЙ АНГИОГРАФИИ, БИОМИКРОСКОПИИ, СЕМИПОЛЬНОГО ЦВЕТНОГО ФОТОГРАФИРОВАНИЯ ГЛАЗНОГО ДНА В ОЦЕНКЕ АКТИВНОСТИ НЕОВАСКУЛЯРИЗАЦИИ ПОСЛЕ ПРОВЕДЕНИЯ ПАНРЕТИНАЛЬНОЙ ЛАЗЕРОКОАГУЛЯЦИИ ПРИ ЛЕЧЕНИИ ПРОЛИФЕРАТИВНОЙ ДИАБЕТИЧЕСКОЙ РЕТИНОПАТИИ // Современные проблемы науки и образования. 2026. № 3. ;URL: https://science-education.ru/en/article/view?id=34515 (дата обращения: 10.06.2026).
DOI: https://doi.org/10.17513/spno.34515



