Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
THE ROLE OF THE MICROENVIRONMENT IN NEOADJUVANT THERAPY FOR TRIPLE-NEGATIVE BREAST CANCER
Введение
Рак молочной железы – наиболее распространенное злокачественное новообразование женщин в мире [1]. В зависимости от наличия или отсутствия экспрессии на опухолевых клетках рецепторов стероидных гормонов (эстрогеновых рецепторов, ER, и прогестероновых рецепторов, PR) и рецептора эпидермального фактора роста человека 2 типа (Her2/neu), а также уровня пролиферативной активности Ki-67, выделяют несколько суррогатных молекулярно-биологических подтипов рака молочной железы: люминальный А (ER+/PR+≥20%, Her2/neu-негативный, Ki-67<20%), люминальный В Her2/neu-негативный (ER+/PR-любой, Her2/neu-негативный, Ki-67≥20%), люминальный В Her2/neu-позитивный (ER+/PR-любой, Her2/neu-позитивный, Ki-67-любой), классический Her2/neu-позитивный (ER-/PR-, Her2/neu-позитивный, Ki-67-любой) и тройной негативный (ER-/PR-, Her2/neu-негативный, Ki-67-любой) [1, 2]. Тройной негативный подтип рака молочной железы – агрессивная опухоль, характеризующаяся отсутствием ER, PR и Her2/neu, в связи с чем возможности терапевтического воздействия при этом заболевании ограничены и химиотерапия является стандартным методом лечения данной группы пациентов, в том числе и в неоадъювантном режиме [3, 4]. При этом тройной негативный подтип рака молочной железы является гетерогенным заболеванием, в котором можно выделить подгруппы, отличающиеся по степени выраженности ответа на неоадъювантную химиотерапию (НАХТ) и прогнозом общей и безрецидивной выживаемости [1]. Около половины пациентов после проведения НАХТ имеют полный патоморфологический регресс опухоли (Pathologic Complete Response, pCR), однако для части пациентов стандартная химиотерапия малоэффективна [1].
В связи с ограниченностью возможности таргетного воздействия на опухолевые клетки при тройном негативном подтипе рака ведутся активные исследования в области изучения микроокружения таких опухолей, как в плане поиска предикторных биомаркеров прогноза и ответа на НАХТ, так и выявления новых терапевтических мишеней [5–7].
Тройной негативный подтип рака молочной железы является наиболее иммуногенным по сравнению с Her2/neu-позитивным и особенно люминальными подтипами, часто характеризуется высоким уровнем опухоль-инфильтрирующих лимфоцитов (tumor-infiltrating lymphocytes, TILs), количественный и качественный состав которых стали активно изучать в эру развития иммунотерапии злокачественных опухолей [6, 8, 9]. В ряде работ было показано, что высокий уровень TILs является предикторным фактором для полного морфологического регресса опухоли (pathologic complete response, pCR) в ответ на НАХТ при раке молочной железы [4, 10, 11]. При этом не определена группа лимфоцитов, имеющая решающее значение в регрессе опухоли. Общепринятым является выделение двух групп клеток опухолевого микроокружения: обладающих противоопухолевым воздействием и проопухолевым, способствующим прогрессированию заболевания. Известно, что CD4-позитивные Т-хелперы 1 типа, CD8-позитивные цитотоксические Т-лимфоциты, NK-клетки, TNK-клетки 1 типа, дендритные клетки и макрофаги 1 типа обладают противоопухолевым воздействием, в то время как CD4-позитивные Т-хелперы 2 типа, TNK-клетки 2 типа, CD4-позитивных Т-регуляторные клетки, макрофаги 2 типа и супрессорные клетки миелоидного происхождения играют туморогенную роль [5]. В ряде исследований показано, что высокие уровни CD8-позитивных цитотоксических Т-лимфоцитов имеют решающее значение в противоопухолевом иммунитете и являются благоприятным прогностическим фактором ответа на НАХТ, в то время как субпопуляция CD4-позитивных Т-регуляторных клеток имеет проопухолевое воздействие [4, 8, 12].
Клинический интерес представляет возможность воздействовать на TILs с целью модулирования так называемых контрольных точек – системы трансмембранных белков на поверхности иммунных клеток, которые регулируют иммунный ответ. Наиболее изученными с этой точки зрения являются лиганд запрограммированной клеточной смерти 1 (programmed cell death ligand 1, PD-L1) и цитотоксический Т-лимфоцит-ассоциированный антиген 4 (cytotoxic T-lymphocyte-associated antigen 4, CTLA-4), имеющие клиническое применение в качестве терапевтических мишеней при иммунотерапии рака молочной железы [10].
С другой стороны, важную роль в прогрессировании рака играют особенности самих опухолевых клеток, в частности уровень пролиферативной активности, экспрессия при тройном негативном раке молочной железы рецепторов андрогена, трансмембранных белков (EGFR, FGFR4, E-cadherin и др.), молекул клеточной адгезии CD54 (ICAM-1) и CD15 [13, 14]. Так, частота pCR при тройном негативном раке молочной железы положительно коррелирует с отсутствием рецепторов андрогена и высоким уровнем пролиферативной активности Ki-67 [4].
В ряде исследований сделаны выводы о том, что сверхэкспрессия ICAM-1 характерна для тройного негативного рака молочной железы [13], а дефицит экспрессии ICAM-1 на опухолевых клетках ассоциирован с высокой частотой метастазирования в легкие [14]. Экспрессия CD15 на поверхности опухолевых клеток может также служить прогностическим маркером и потенциальной биомишенью для таргетных препаратов при раке молочной железы; в частности, экспрессия CD15 важна при метастазировании опухолевых клеток в связи с высокой адгезией к эндотелию [14].
НАХТ является методом лечения пациентов с местно распространенным тройным негативным раком молочной железы [4]. Ее эффективность, а также прогноз заболевания не могут быть достоверно оценены только с применением лабораторно-инструментальных методов. Точно оценить регресс опухоли после проведенной НАХТ возможно только при патоморфологическом анализе послеоперационного материала с применением системы оценки остаточной опухолевой нагрузки (Residual Cancer Burden, RCB), включающей исследование ложа опухоли и регионарных лимфатических узлов [15].
Учитывая наличие группы пациентов, у которых стандартная химиотерапия не дает ожидаемого результата, продолжаются разработки новых схем лечения при тройном негативном раке молочной железы, а также поиск молекулярных предикторов ответа на неоадъювантную терапию с целью выделения химиорезистентной подгруппы, так как в настоящее время нет официально одобренного биомаркера – предиктора ответа на терапию [1, 13].
Цель исследования – изучить особенности клеточного состава микроокружения тройного негативного рака молочной железы, ассоциированные с полным патоморфологическим регрессом опухоли на фоне неоадъювантной терапии.
Задачи исследования:
1. Изучить эффективность комбинации пролголимаба, эмпэгфилграстима, бевацизумаба и химиотерапии (исследуемая группа) по сравнению с химиотерапией на фоне поддержки препаратами класса гранулоцитарного-колониестимулирующего фактора (Г-КСФ) (контрольная группа) в НАХТ тройного негативного рака молочной железы.
2. Оценить частоту достижения pCR в зависимости от уровня опухоль-инфильтрирующих лимфоцитов (TILs).
3. Оценить встречаемость экспрессии молекул клеточной адгезии ICAM-1 (CD54), CD15 при тройном негативном раке молочной железы.
4. Определить потенциальную прогностическую роль иммунных маркеров опухолевого микроокружения (соотношение СD4+/СD8+, уровень экспрессии CD8+, НLA-DR+, СD66b+, CD86, CD54, CD15).
Материал и методы исследования
Работа выполнена в рамках Многоцентрового проспективного сравнительного рандомизированного клинического исследования «EMPATHY», в соответствии с которым все пациентки были разделены на две группы: 1) контрольная группа, получающая стандартную химиотерапию с поддержкой препаратами класса Г-КСФ, 2) исследуемая группа, получающая комбинацию пролголимаба, эмпэгфилграстима, бевацизумаба и стандартной химиотерапии.
Проанализированы образцы трепанобиоптатов молочной железы, взятые до начала неоадъювантного химиотерапевтического лечения, от 20 пациенток, которые перенесли хирургическую резекцию после химиотерапии в МКНЦ им. А.С. Логинова ДЗМ с 2024 по 2025 гг. Все образцы трепанобиоптатов были диагностированы как инвазивная неспецифицированная карцинома молочной железы. Далее для каждой пациентки была сформирована пара образцов, включающая трепанобиоптат до начала химиотерапии и резекционный материал после лечения.
Материал ткани молочной железы с опухолью был изучен с применением гистологического, иммуногистохимического методов исследования и световой микроскопии. Материал проходил предобработку в автоматическом гистологическом процессоре Leica ASP6025S (Leica Biosystems, Германия). На ротационном микротоме Leica RM 2125 RTS (Leica Biosystems, Германия) готовили срезы ткани молочной железы толщиной 4,0 мкм для исследования при помощи световой микроскопии с применением гистологического метода (окрашивание гематоксилином Майера и эозином) на аппарате Leica ST5010 AXL (Leica Biosystems, Германия), иммуногистохимического метода на иммуностейнере Ventana BenchMark XT (Ventana Medical Systems, США) с использованием системы детекции ultraView Universal DAB Detection Kit и антител к Her2/neu, Estrogen Receptor, Progesterone Receptor, Ki-67, PD-L1 CD4, CD8, CD15, CD86, CD101, CD66b. Просмотр, микрофотосъемку с последующей морфометрией готовых гистологических препаратов произвели на светооптическом микроскопе Nikon Eclipse Ci (Nikon Corporation, Япония).
В трепанобиоптате оценивали степень злокачественности по Ноттингемской системе, степень инфильтрации TILs. Ноттингемская система градации рака молочной железы включает оценку: 1) структурообразования (1 балл – более 75% тубулярно-железистого компонента, 2 балла – 10–75%, 3 балла – менее 10%), 2) ядерного плеоморфизма (1 балл – минимально выраженные вариации формы и размера ядер, небольшие ядра, 2 балла – умеренно выраженные вариации, укрупнение ядер, 3 балла – выраженный плеоморфизм, крупные ядра), 3) митотической активности (1 балл – низкая митотическая активность: 0–5 митозов/диаметр поля зрения 0,44, 2 балла – умеренная: 6–11 митозов/диаметр поля зрения 0,44, 3 балла – высокая: более 11 митозов/диаметр поля зрения 0,44). На основании данных параметров рассчитывается общий балл, отражающий степень злокачественности опухоли: 3–5 баллов – низкая (1), 6–7 – умеренная (2), 8–9 – высокая (3).
Степень инфильтрации стромальными TILs оценивалась в среднем на трех случайно выбранных полях зрения с высоким увеличением (HPF) в случаях однородной инфильтрации; при неоднородной инфильтрации поля зрения с наибольшей и наименьшей инфильтрацией исключались. Инфильтрация TILs классифицировалась как низкая (≤ 10%), средняя (>10–49%) или высокая (≥ 50%). Иммуногистохимическим методом оценивались уровни экспрессии рецепторов эстрогена и прогестерона по Allred Score, Her2/neu-статус по ASCO/CAP'23, уровень пролиферативной активности Ki-67, PD-L1 статус (клон 22С3) по шкале CPS, наличие экспрессии молекулы клеточной адгезии ICAM-1 (CD54) на опухолевых клетках, а также субпопуляции TILs. Количество субпопуляций TILs определялось с помощью подсчета клеток в среднем на HPF. Рассчитывалось среднее количество CD4+, CD8+, CD15+, CD86+, CD101+, CD66b+, а также соотношение CD8+/CD4+.
В материале после резекции молочной железы оценивалась степень патоморфологического регресса опухоли по шкале RCB (Residual Cancer Burden). Выделены две подгруппы: полный патоморфологический ответ (pCR) и неполный патоморфологический ответ (не-pCR: RCB-I, RCB-II, RCB-III).
Статистическая обработка результатов осуществлялась с использованием программы «Statistica 6.0» (StatSoft Inc., США) и онлайн-калькулятора (https://medstatistic.ru/calculators/calcchoice.html). Данные анализировались с помощью критерия хи-квадрата илиU-критерия Манна – Уитни.Различия между исследуемыми группами считали достоверными при уровне статистической значимости (р) менее 0,05 (р<0,05).
Результаты исследования и их обсуждение
Во всех исследуемых образцах трепанобиоптата молочной железы опухоль была представлена инвазивной неспецифицированной карциномой со 2–3 степенью злокачественности по Ноттингемской системе. Во всех образцах опухоли экспрессия рецепторов эстрогена была негативной (0–2 балла по Allred Score), прогестерона – негативной или слабо позитивной (0–3 по Allred Score). Her2/neu-статус опухолей варьировал от 0 до 2+ по ASCO/CAP'23 (при негативном результате гибридизации in situ). Индекс пролиферативной активности Ki-67 варьировал от 20 до 98%, с медианой – 75%. При оценке PD-L1 статуса (клон 22С3) по шкале CPS составлял в 86,6% случаев менее 1, в двух случаях – более 1. В подгруппах pCR и не-pCR не выявлено статистически значимых различий (р>0,05, U-критерийМанна – Уитни) между показателями экспрессии рецепторов стероидных гормонов, Her2/neu-статусом, уровнем пролиферативной активности, CPS и степенью дифференцировки опухоли, что соотносится с данными литературы [6].
В 47,1% анализируемых случаев отмечен pCR после НАХТ. При этом полный ответ встречался достоверно чаще (р<0,05, p=0,017, критерий хи-квадрата) в группе, получавшей комбинацию пролголимаба, эмпэгфилграстима, бевацизумаба и химиотерапии. Так, в исследуемой группе pCR достигнут в 57,0%, не-pCR – 43,0%, из которых 14,4% – RCB-I и 28,6% – RCB-II. В контрольной группе pCR достигнут в 40,0%, не-pCR – 60,0%, из которых все случаи составляли RCB-II.

Высокая степень TILs выявлена в 12,5% случаев pCR, средняя – в 12,5% и низкая – в 75,0% (рис.1). В случаях не-pCR не было выявлено высокой степени инфильтрации TILs, средняя и низкая степени были отмечены у 44,4 и 55,6% соответственно. Однако не выявлено статистически значимых различий (р>0,05, U-критерийМанна – Уитни) между уровнем инфильтрации TILs в группах pCR и не-pCR.
Рис.1. Морфологическое исследование биоптатов рака молочной железы. Окраска гем.-эозин. Общ. ув. х 200. Степени инфильтрации TILs: А) высокая, B) средняя, С) низкая. Примечание: составлен авторами по результатам данного исследования
Во всех исследуемых образцах выявлена экспрессия молекулы клеточной адгезии ICAM-1(CD54) на опухолевых клетках, что соотносится с литературными данными о сверхэкспрессии этого белка на поверхности клеток тройного негативного рака молочной железы и представляет интерес в плане изучения в качестве возможной терапевтической мишени [13]. Экспрессия носила очаговый или диффузный характер разной степени выраженности: варьировала от слабой до умеренной и выраженной мембранной (рис.2). Экспрессия CD15 выявлена во всех случаях pCR, и в 89,0% случаев не-pCR, демонстрируя очаговое умеренно выраженное мембранное окрашивание опухолевых клеток. Не выявлено статистически значимых различий (р>0,05, U-критерийМанна – Уитни) между степенью выраженности экспрессии CD54 и CD15 на опухолевых клетках и частотой достижения pCR.
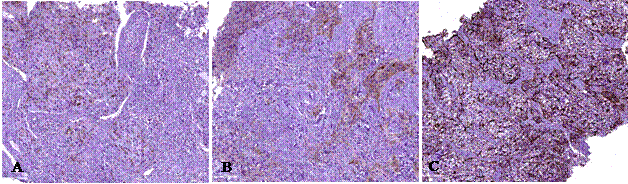 |
Рис.2. Морфологическое исследование биоптатов рака молочной железы. Иммуногистохимическое исследование с антителами к ICAM-1(CD54). Общ. ув. х 200. Характер экспрессии CD54 в опухолевых клетках: А) слабая очаговая, B) умеренная диффузная, С) выраженная диффузная.
Примечание: составлен авторами по результатам данного исследования.
Для оценки связи между субпопуляциями TILs и pCR сравнивали количество TILs CD4+, CD8+, CD15+, CD86+, CD101+, CD66b+ в случаях pCR и не-pCR. Данные субпопуляций TILs в контрольной и исследуемой группах pCR и не-pCR представлены на рис.3.
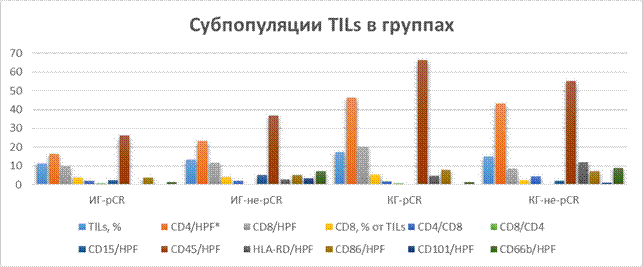
Рис.3. Распределение субпопуляций TILs в исследуемой и контрольной группах.
ИГ-pCR – исследуемая группа с pCR, ИГ-не-pCR – исследуемая группа без достижения pCR, КГ-pCR – контрольная группа с pCR, КГ-не-pCR – контрольная группа без достижения pCR. Примечание: составлен авторами по результатам данного исследования
При достижении pCR инфильтрация CD8+ была выше, чем в случаях не-pCR (р<0,05, U-критерийМанна – Уитни). Также группа pCR показала более высокое соотношение CD8+/CD4+, чем группа не-pCR (р<0,05, U-критерийМанна – Уитни). Полученные результаты соотносятся с данными ряда исследований [5, 6, 8]. Напротив, более высокие уровни инфильтрации CD15+, CD101+ и CD66b+ отмечены в группе не-pCR. Однако лишь в отношении CD15 эти различия статистически значимы. Не выявлена взаимосвязь между уровнем инфильтрации CD86 и pCR (p>0,05, U-критерийМанна – Уитни).
Выводы
1. При применении комбинации пролголимаба, эмпэгфилграстима, бевацизумаба и химиотерапии (исследуемая группа) отмечается увеличение частоты достижения pCR по сравнению с химиотерапией на фоне поддержки препаратами класса Г-КСФ (контрольная группа) в НАХТ тройного негативного рака молочной железы.
2. Не выявлено статистически значимых различий в частоте достижения pCR в зависимости от уровня TILs, что ограничивает использование данного параметра в качестве предиктора ответа на НАХТ тройного негативного рака молочной железы.
3. Во всех исследованных случаях тройного негативного рака молочной железы выявлена экспрессия молекул клеточной адгезии ICAM-1 (CD54), CD15, что может быть использовано в качестве потенциальных мишеней при таргетной терапии тройного негативного рака молочной железы. Не выявлено различий в частоте достижения pCR в зависимости от уровня экспрессии данных биомаркеров.
4. В исследовании выявлено, что высокое соотношение CD8+/CD4+, а также более высокие уровни TILs CD8+ ассоциированы с pCR при НАХТ тройного негативного рака молочной железы, что свидетельствует о функциональности данных параметров в качестве предикторных.
Заключение
Таким образом, в результате проведенного исследования доказана эффективность комбинации пролголимаба, эмпэгфилграстима, бевацизумаба и химиотерапии по сравнению с химиотерапией на фоне поддержки препаратами класса Г-КСФ в НАХТ тройного негативного рака молочной железы. Определены предикторные биомаркеры микроокружения опухоли, ассоциированные с pCR при НАХТ тройного негативного рака молочной железы: высокий уровень инфильтрации TILs CD8+ и высокое соотношение CD8+/CD4+.
Conflict of interest
Financing
Библиографическая ссылка
Шурыгина Е.И., Карнаухов Н.С., Сухова М.В., Пасечнюк О.С., Филоненко Д.А., Жукова Л.Г. РОЛЬ МИКРООКРУЖЕНИЯ ПРИ НЕОАДЪЮВАНТНОЙ ТЕРАПИИ ТРОЙНОГО НЕГАТИВНОГО РАКА МОЛОЧНОЙ ЖЕЛЕЗЫ // Современные проблемы науки и образования. 2026. № 3. ;URL: https://science-education.ru/en/article/view?id=34512 (дата обращения: 10.06.2026).
DOI: https://doi.org/10.17513/spno.34512



