Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
FACTORS DETERMINING THE DEVELOPMENT OF POSTEMBOLIZATION SYNDROME IN PATIENTS WITH PRIMARY AND METASTATIC LIVER CANCER AFTER TRANSARTERIAL CHEMOEMBOLIZATION
Введение
Гепатоцеллюлярная карцинома (ГЦК) – пятое по распространенности злокачественное новообразование в мире, ежегодно выявляется у 500 тыс. – 1 млн чел., преимущественно в регионах с высокой распространенностью хронических вирусных гепатитов и афлатоксиновой нагрузки [1]. Смертность от ГЦК достигает 500 тыс. – 600 тыс. случаев в год, что делает ее второй по частоте причиной онкологической смертности [2]. Печень является основной мишенью для метастазов колоректального рака (мКРР): у 20–25% пациентов метастазы в печени выявляются при постановке диагноза, а у 30–50% – развиваются в течение болезни. Таким образом, как первичные, так и вторичные опухоли печени представляют серьезную проблему онкологии [3, 4].
Транскатетерная артериальная химиоэмболизация (ТАХЭ) является стандартом локально-регионарной терапии нерезектабельных опухолей печени. Методика основана на селективной доставке химиотерапевтических агентов (доксорубицин, цисплатин, иринотекан и др.) с последующей эмболизацией артерий, кровоснабжающих опухоль, что потенцирует ишемическое и цитотоксическое воздействие [5]. Эффективность ТАХЭ подтверждена при лечении как ГЦК, так и мКРР, однако ее роль в неоадъювантном режиме при резектабельной ГЦК остается предметом дискуссий [6–8].
Наиболее частым осложнением ТАХЭ является постэмболизационный синдром (ПЭС), регистрируемый у 80–90% пациентов. Клиническая манифестация ПЭС наблюдается в течение 1–3 суток и включает лихорадку [9, 10], абдоминальный болевой синдром, тошноту и повышение активности печеночных ферментов. Несмотря на тенденцию к спонтанному разрешению, ПЭС пролонгирует сроки госпитализации и может нарушать планируемый лечебный алгоритм [11]. Патогенез ПЭС связывают с развитием системного воспалительного ответа на опухолевый некроз, однако предикторы его развития и особенности течения при различных нозологиях изучены недостаточно [12].
Цель исследования – выявить факторы, влияющие на развитие ПЭС после ТАХЭ, установить причинно-следственные связи между ними и определить возможные факторы риска или профилактики этого осложнения у пациентов, проходящих лечение методом ТАХЭ.
Материал и методы исследования
Проведен ретроспективный анализ 333 пациентов (181 мужчина и 152 женщины), проходивших лечение в ФГБУ «НМИЦ онкологии» Минздрава РФ (г. Ростов-на-Дону) в течение двух лет – с 2023 по 2024 г. В исследование вошли 93 случая гепатоцеллюлярной карциномы (C22.0 по МКБ-10) и 240 случаев метастатического поражения печени при колоректальном раке (C78.7 по МКБ-10). Возрастной диапазон пациентов – от 19 до 83 лет, со средним возрастом 60,1±0,55 года. Всем участникам исследования была выполнена ТАХЭ. Более подробная клиническая характеристика пациентов представлена в таблице.
Распределение пациентов по клиническим параметрам
|
Стадии заболевания |
Общее число пациентов (n=333) |
|
|
Гепатоцеллюлярная карцинома (n=93) |
Метастатический очаг КРР в печени (n=240) |
|
|
II стадия |
n=8 (8,6%) |
n=37 (15,4%) |
|
III стадия |
n=64 (68,8%) |
n=61 (25,4%) |
|
IV стадия |
n=21 (22,6%) |
n=142 (59,2%) |
|
Число пациентов в зависимости от размера опухоли |
||
|
Т2 |
n=13 (14%) |
n=9 (3,8%) |
|
Т3 |
n=80 (86%) |
n=152 (63,3%) |
|
Т4 |
– |
n=79 (32,9%) |
|
Число пациентов с поражением в региональных лимфатических узлах |
||
|
Не выявлены |
n=64 (68,8%) |
n=183 (76,2%) |
|
Выявлены |
n=29 (31,2%) |
n=57 (23,8%) |
|
Число пациентов с обнаруженными метастазами в отдаленные органы |
||
|
Не выявлены |
n=72 (77,4%) |
n=0 (0%) |
|
Выявлены |
n=21 (22,6%) |
n=240 (100%) |
|
Число пациентов с проведенной таргетной терапией |
||
|
n=81 (87,1%) |
n=82 (34,2%) |
|
Примечание: составлена авторами на основе полученных данных в ходе исследования
Критерии включения пациентов в исследование следующие:
- гистологически верифицированные опухоли;
- невозможность выполнения радикальных оперативных вмешательств;
- пациенты с прогрессированием процесса (ГЦК и КРР с метастазами в печень) на фоне проведенных курсов системной ПХТ;
- подписанное информированное согласие.
Критерии исключения пациентов из исследования следующие:
- неотложные состояния (острый инфаркт миокарда, острое нарушение мозгового кровообращения, тромбоэмболия легочной артерии);
- острая печеночная недостаточность;
- наличие декомпенсированного цирроза печени;
- тромбоз воротной вены;
- нарушение свертывающей функции крови;
- экстрапеченочное метастазирование;
- желтуха любого генеза;
- напряженный асцит;
- гиповаскулярность опухоли по данным инструментальных методов исследования;
- возраст младше 18 лет;
- отказ от участия в исследовании.
Лабораторные исследования выполнены на автоматизированных анализаторах. Концентрация воспалительных маркеров, включая интерлейкин-6 (ИЛ-6) и прокальцитонин, определялась на иммунохимическом анализаторе Cobas Е411 (Япония). Биохимические показатели, а именно: уровень альбумина, активность аланинаминотрансферазы (АЛТ), аспартатаминотрансферазы (АСТ) и щелочной фосфатазы (ЩФ), измерялись на анализаторе Vitros 5600 (США).
Для статистического анализа результатов исследования использовалась программа STATISTICA 10 (StatSoft Inc., США), данные представлены в виде среднего ± ошибка среднего.
Проведенное исследование соответствует стандартам Хельсинкской декларации, одобрено независимым этическим комитетом Национального медицинского исследовательского центра онкологии (Россия, 344037, Ростов-на-Дону, ул. 14-линия, 63), протокол № 32 от 14 сентября 2023 г.
Все пациенты подписали письменное информированное согласие на публикацию данных в медицинском журнале, включая его электронную версию.
Результаты исследования и их обсуждение
На предоперационном этапе оценивалась прогностическая значимость биохимических параметров. У всех пациентов регистрировались признаки хронической печеночной недостаточности I–II степени (класс A–B по Чайлд-Пью). Помимо абсолютных значений АЛТ и АСТ, анализировалось их соотношение (АСТ/АЛТ), как более точный индикатор повреждения гепатоцитов.
Ретроспективный сравнительный анализ пациентов с развившимся ПЭС и без него выявил, что до проведения ТАХЭ в группе с последующим ПЭС исходный уровень альбумина был достоверно ниже (p=0,046), а соотношение АСТ/АЛТ – достоверно выше (p=0,048). Регрессионный анализ Кокса подтвердил ассоциацию низкого исходного уровня альбумина (p=0,049) и высокого соотношения АСТ/АЛТ (p=0,051) с повышенным риском развития ПЭС.
Однако ROC-анализ показал ограниченную прогностическую ценность этих исходных параметров. Для соотношения АСТ/АЛТ пороговое значение составило 2,53. Его превышение до ТАХЭ позволяло предсказать высокий риск ПЭС с чувствительностью 57,3% и специфичностью 82,4%. Площадь под ROC-кривой составила AUC = 0,702 ± 0,132 (p = 0,003) (рис. 1).
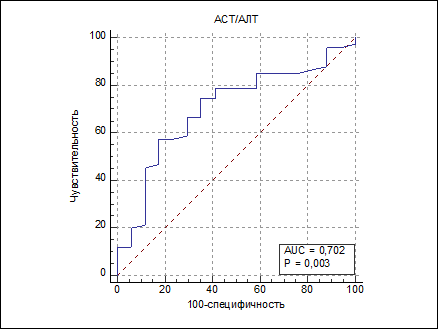
Рис. 1. ROC-кривая прогноза развития ПЭС после ТАХЭ у пациентов по соотношению АСТ/АЛТ
Примечание: составлен авторами по результатам данного исследования
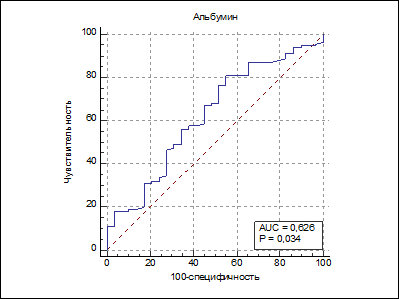
Для альбумина критическое значение составило 34 г/л. Снижение концентрации ниже этого уровня предсказывало риск ПЭС с чувствительностью 81%, но специфичностью всего 44,8%. Площадь под ROC-кривой была AUC = 0,626 ± 0,092 (p = 0,034) (рис. 2). Таким образом, несмотря на статистическую значимость, исходные значения обладают недостаточной диагностической точностью для надежного прогнозирования.
Рис. 2. ROC-кривая прогноза развития постэмболизационного синдрома после трансартериальной химиоэмболизации у пациентов по концентрации альбумина в сыворотке крови
Примечание: составлен авторами по результатам данного исследования
На следующем этапе анализировалась динамика показателей после ТАХЭ. На 1-е и особенно 3-и сутки отмечался резкий рост активности АЛТ, АСТ, ЩФ и соотношения АСТ/АЛТ, а уровень альбумина достоверно снижался (p < 0,001). При сравнении пациентов с ПЭС и без него на 3-и сутки выявлены значимые различия: у пациентов с ПЭС активность всех ферментов была значительно выше (p < 0,001), а альбумин – ниже (p = 0,008).
ROC-анализ на 3-и сутки выявил следующие пороговые значения: АЛТ ≥ 109,2 Е/л (чувствительность 77,4%, специфичность 72,8%), АСТ ≥ 374,4 Е/л (84,5% и 82,1%), АСТ/АЛТ ≥ 2,96 (87,5% и 88,3%), ЩФ ≥ 156,6 Е/л (70,3% и 71,4%), альбумин ≤ 28 г/л (90,5% и 89,4%). Наибольшую прогностическую информативность продемонстрировали альбумин, АСТ/АЛТ и АСТ.
Параллельно оценивалась роль системного воспаления. Исходные уровни ИЛ-6 и прокальцитонина не различались между группами (p > 0,9). Однако уже на 1-е сутки после ТАХЭ наблюдался резкий рост обоих маркеров: ИЛ-6 увеличивался с 7,2 до 9,6 нг/мл, прокальцитонин – с 0,021 до 0,14 нг/мл. К 3-м суткам ИЛ-6 достигал 16,7 нг/мл, а прокальцитонин – 0,30 нг/мл (p < 0,001). Это свидетельствует о выраженной системной воспалительной реакции.
ROC-анализ на 3-и сутки установил пороговые значения: ИЛ-6 ≥ 12,7 нг/л (чувствительность 74,8%, специфичность 79,1%) и прокальцитонин ≥ 0,30 нг/л (71,7% и 74,5%) как предикторы высокого риска ПЭС.
Таким образом, исходные биохимические параметры имеют статистически значимую, но клинически ограниченную прогностическую ценность. В то же время их динамика на 3-и сутки после ТАХЭ – особенно снижение альбумина, рост АСТ/АЛТ и воспалительных маркеров – является высокоинформативной. Упомянутые ROC-кривые (рис. 1 и 2) наглядно подтверждают умеренную прогностическую силу исходных показателей. Мониторинг предложенного комплекса биохимических и воспалительных маркеров в раннем послеоперационном периоде позволяет своевременно идентифицировать пациентов высокого риска и назначать превентивную или симптоматическую терапию.
В ходе исследования получены данные, уточняющие патогенетические механизмы и улучшающие прогнозирование постэмболизационного синдрома – наиболее распространенного осложнения транскатетерной артериальной химиоэмболизации, возникающего у 80–90% пациентов с гепатоцеллюлярной карциномой или метастатическим колоректальным раком [13]. Показано, что исходные значения сывороточного альбумина (<34г/л) и соотношения АСТ/АЛТ (> 2,53) обладают статистически значимой, но клинически ограниченной прогностической способностью вследствие низких чувствительности и специфичности. Наибольшую диагностическую значимость продемонстрировали динамические изменения лабораторных параметров на 3-и сутки после ТАХЭ: снижение альбумина до ≤ 28 г/л (чувствительность 90,5%, специфичность 89,4%), повышение АСТ≥374,4 Е/л и соотношения АСТ/АЛТ ≥ 2,96, что отражает выраженность острого повреждения гепатоцитов и угнетения синтетической функции печени [14]. Кроме того, установлено, что развитие ПЭС сопряжено со значительной активацией системного воспалительного ответа: к 3-м суткам наблюдается достоверный рост уровней интерлейкина-6 (≥ 12,7 нг/л) и прокальцитонина (≥ 0,30 нг/л), подтверждающий асептическую, опухолево-некроз-индуцированную природу воспаления [15]. Отмечена сопоставимость частоты и патофизиологических механизмов ПЭС у пациентов с ГЦК и мКРР, что свидетельствует о доминирующей роли реакции печеночной паренхимы на ишемию и цитотоксическое воздействие, независимо от гистогенеза опухоли [16, 17]. Таким образом, комбинированный мониторинг указанных биохимических и воспалительных маркеров в раннем послеэмболизационном периоде позволяет надежно стратифицировать риск тяжелого ПЭС и своевременно инициировать превентивные меры. Ограничениями работы являются ретроспективный характер исследования и относительно небольшой размер подгруппы пациентов с ГЦК (n=93), что обуславливает необходимость проведения проспективных многоцентровых исследований для валидации предложенных пороговых значений.
Заключение
Проведенное исследование установило, что ключевое значение для прогнозирования постэмболизационного синдрома после ТАХЭ имеет не исходный уровень, а динамика лабораторных маркеров в раннем послеоперационном периоде. Наиболее информативными являются показатели на 3-е сутки: снижение альбумина ≤ 28 г/л, повышение АСТ ≥ 374,4 Е/л и соотношения АСТ/АЛТ≥2,96, обладающие высокой диагностической точностью (чувствительность и специфичность ~85–90%). Значительный прирост воспалительных маркеров (ИЛ-6, прокальцитонин) подтверждает ведущую роль системного воспалительного ответа в патогенезе ПЭС. Частота и характер ПЭС сопоставимы при гепатоцеллюлярной карциноме и метастатическом колоректальном раке, что указывает на общность патогенетических механизмов, связанных с реакцией печеночной паренхимы.
Практической имплементацией результатов работы является обоснование алгоритма раннего послеоперационного мониторинга, основанного на оценке комплекса биохимических и воспалительных маркеров на 3-и сутки после ТАХЭ. Данный подход позволяет осуществлять стратификацию пациентов по риску развития тяжелого ПЭС и своевременно инициировать превентивные или симптоматические лечебные мероприятия, минимизируя негативное влияние синдрома на общие результаты лечения.
Conflict of interest
Financing
Библиографическая ссылка
Солодов И.И., Шатова Ю.С., Фоменко Ю.А., Маслов А.А., Колесников Е.Н., Егоров Г.Ю., Дженкова Е.А., Петров Д.С., Галина А.В., Ступникова Е.С., Целищева И.В., Головинов И.В. ФАКТОРЫ, ОПРЕДЕЛЯЮЩИЕ РАЗВИТИЕ ПОСТЭМБОЛИЗАЦИОННОГО СИНДРОМА У ПАЦИЕНТОВ С ПЕРВИЧНЫМ И МЕТАСТАТИЧЕСКИМ РАКОМ ПЕЧЕНИ ПОСЛЕ ТРАНСАРТЕРИАЛЬНОЙ ХИМИОЭМБОЛИЗАЦИИ // Современные проблемы науки и образования. 2026. № 1. ;URL: https://science-education.ru/en/article/view?id=34453 (дата обращения: 29.04.2026).
DOI: https://doi.org/10.17513/spno.34453