Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
GENES OF CANCER-TESTICULAR ANTIGENS TRANSCRIPTIONAL PROFILE IN PATIENTS WITH LOCALIZED AND LOCALLY ADVANCED COLORECTAL CANCER
Введение
Колоректальный рак (КРР) занимает четвертое место в мире по смертности, с ежегодной регистрацией более 1 млн новых случаев и ~715 000 летальных исходов [1]. В России за последнее десятилетие заболеваемость КРР возросла на 49.5%, а годичная летальность достигает 40%, что во многом обусловлено поздней диагностикой [2]. Частота метастазирования превышает 50%, а 5-летняя выживаемость без лечения не превышает 2% [1]. Эти данные подчеркивают необходимость поиска новых высокоспецифичных молекулярных маркеров для ранней диагностики и прогноза. Раково-тестикулярные антигены (РТА, Cancer-Testis Antigens - CTA) представляют перспективную группу таких маркеров. Их ключевая особенность – ограниченная экспрессия в норме (преимущественно в зародышевых клетках семенников, плаценте и некоторых нейронах) и реактивация в различных типах злокачественных опухолей [3]. Известно 276 CTA, объединенных в 138 семейств, наиболее изученными из которых являются MAGE-A, MAGE-B, BAGE, GAGE, SSX, LAGE и MAGE-C [4]. Пептиды CTA, презентируемые в комплексе с молекулами HLA I или II класса, способны индуцировать специфический противоопухолевый иммунный ответ [5]. Каждый тип опухоли обладает уникальным профилем экспрессии CTA, что требует детального анализа для их использования в качестве диагностических/прогностических маркеров или мишеней иммунотерапии [6; 7].
Экспрессия CTA при КРР, особенно у пациентов российской популяции, изучена фрагментарно [7; 8]. Первые исследования (1996 г.) показали гиперэкспрессию MAGEA1 (30%), MAGEA2 (28%) и MAGEA3 (20%) у 54 пациентов, причем чаще при наличии метастазов [9]. Это позволяет предположить связь экспрессии генов семейства MAGE с агрессивным фенотипом и метастатическим потенциалом КРР. Однако сравнительный анализ экспрессии CTA в первичных опухолях и метастазах (особенно печеночных) остается недостаточным [10]. Существующие данные указывают на значительный диагностический и прогностический потенциал отдельных представителей CTA при КРР [1].
Цель исследования - провести сравнительный анализ транскрипционных профилей расширенной панели генов РТА в опухолевой ткани пациентов с локализованным (T1-3N0M0) и регионарно-метастатическим (T1-3N1-2M0) КРР для выявления ассоциаций с метастатическим потенциалом.
Материалы и методы исследования
Характеристика пациентов. В исследовании использованы парные образцы (опухоль и гистологически нормальная слизистая оболочка толстой кишки, взятая на расстоянии >10 см от опухоли) от 60 пациентов, проходивших лечение в НМИЦ в 2023-2025 гг. Исследование одобрено этическим комитетом ФГБУ «РНИОИ» МЗ РФ; для каждого больного было получено информированное согласие на включение его в данное исследование. Образцы тканей, полученные во время операции, мгновенно замораживали в жидком азоте в криопробирках [6].
Пациенты, вошедшие в исследование, были разделены на 2 группы: группа 1 (n=30): T1-3N1-2M0 (регионарные метастазы), группа 2 (n=30): T1-3N0M0 (без регионарных метастазов).
Выделение РНК и синтез кДНК. Ткани гомогенизировали в буфере с гуанидин тиоцианатом. Тотальную РНК выделяли методом фенол-хлороформной экстракции [11] c использованием станции QIAcube Connect (Qiagen). Контаминацию геномной ДНК удаляли с помощью ДНКазы I [12]. Качество РНК оценивали электрофорезом в 2% агарозном геле (соотношение интенсивностей полос 28S:18S ≈ 2:1). Синтез кДНК проводили с использованием набора Reverta-L («Интерлабсервис») [12].
Анализ экспрессии генов методом RT-qPCR. Анализировали относительную экспрессию 20 РТ-генов (MAGE-A1, -A2, -A3, -A4, -B1, -B2, GAGE-1, -3, -4, MAGE-C1, BAGE, XAGE-3, NY-ESO-1, SSX-2, SCP-1, PRAME-1, CTAG-1B, SPAG-9, PAGE-5, CXorf61) методом RT-qPCR. В качестве референсных генов использовали GAPDH и GUSB. ПЦР проводили в 20 мкл реакционной смеси (11 нг кДНК, 0.2 мМ dNTPs, 2.5 мМ MgCl₂, 1х ПЦР-буфер, 2 ед. SynTaq ДНК-полимеразы, краситель EVA-Green, по 435 нМ каждого праймера) на амплификаторе CFX-96 (Bio-Rad). Условия амплификации: 95 °C - 240 с; 40 циклов: 95 °C - 10 с, 58 °C - 30 с, 72 °C - 30 с. Последовательности праймеров представлены в таблице. Расчет относительной экспрессии (RЕ) проводили по методу 2-ΔΔCt [7; 13]: 1) проводилась нормализация по среднему референсных генов: ΔC(t) = C(t)target – C(t)reference; 2) рассчитывали медианы ΔC(t) по каждому гену для условно-нормальной и опухолевой ткани; 3) проводилась нормализация по условно-нормальной ткани: ΔΔC(t) = ΔC(t)Медиана опухолевой ткани – ΔC(t) Медиана нормальнойткани; 4) окончательный результат (кратное различие (Fold difference)): 2-ΔΔC(t)..
Панель праймеров для определения относительной экспрессии генов
|
№ |
Название гена |
Последовательности праймеров (5'->3') |
|
|
Прямой |
Обратный |
||
|
1 |
GAPDH |
GTCAAGGCTGAGAACGGGA |
TCGCCCCACTTGATTTTGG |
|
2 |
GUSB |
CAGGACCTGCGCACAAGA |
CTAGCGTGTCGACCCCATT |
|
3 |
MAGE-A1 |
GAAGGAACCTGATCCAGG |
GGGAATTCTGTCCTCTGGG |
|
4 |
MAGE-A2 |
CGAAGGCTCCGTGAGG |
TGTATTGACCTGAGTCACC |
|
5 |
MAGE-A3 |
TGAGCAAAGAGCGACG |
TCAGACTGTCCCCTCAGA |
|
6 |
MAGE-B1 |
TTCAGTGTGGTGTCCAGCA |
CGAGTTGTACTCCTGGATGATC |
|
7 |
MAGE-B2 |
AGCCAGGGGTGAATTCTCT |
GCACGGAGCTTACTCTCCT |
|
8 |
GAGE-1 |
CTGATGGGCACGAGATGGA |
CCAGTCTCGGCAACATAGTG |
|
9 |
GAGE-3 |
TCACACAGCTGAGTTGGCG |
TGTGTGAAATATGAGTTGGCGC |
|
10 |
GAGE-4 |
GAGGAGGTGAAAACGCCTG |
CATCATTTCAACGTGCCTTCG |
|
11 |
MAGE-C1 |
ACGAGGATCGTCTCAGGTC |
CAGGTCTTCAACTCCTGCC |
|
12 |
MAGE-A4 |
CTGACCAGCAGCTTGGGAT |
TCCAGGGAATCCTGTCCTC |
|
13 |
BAGE |
GCCGGCTCCTTTCAGGATT |
ACATCTTTCAGGAGCTTGGT |
|
14 |
XAGE-3 |
ACTTGCCCTGAGACTTAGT |
CTTGCCCTGAGACTTAGTTT |
|
15 |
NY-ESO-1 |
GAGTTCACTGTGTCCGGCA |
TGGAGACAGGAGCTGATGG |
|
16 |
SSX-2 |
TACGGTTGGTGCTCAAATAC |
CGAGGCTTTCATCTTTTCCT |
|
17 |
SCP-1 |
AGGTGAAACCTCAGACCC |
AGTCTTTGCAAATGGAAACTCAA |
|
18 |
PRAME-1 |
GCTGAGCCATTGTCTCGTTAC |
GGTCTCAGTCACTTGTTGCC |
|
19 |
CTAG-1B |
GCCAGTGACCCAGAGATGAA |
GCACAGGATGTAGGTGGTGA |
|
20 |
SPAG-9 |
AAGCCCAGACCTTTGATGCT |
TGGTTTCGGCTTCAGGTAGT |
|
21 |
PAGE-5 |
CTGGGACTCCTGGGACTCTA |
GGGACAGGTAGCCATTGTGT |
|
22 |
CXorf61(CT83) |
ATGAACTTCTATTTACTCCTAGCGAG |
CTACAATATTGAGTGTGGGAAATTATTTA |
Примечание: составлено авторами на основе полученных данных в ходе исследования.
Статистический анализ. Сравнение между двумя независимыми группами проводили с использованием непараметрического U-критерия Манна-Уитни в среде R (версия 4.5.2). При выполнении множественных сравнений применяли поправку Бонферрони. Различия считали статистически значимыми при скорректированном уровне значимости p<0.05 (padjust bonferroni) [7].
Результаты исследования и их обсуждение
В объединенной выборке, состоящей из 30 пациентов с наличием (T1-3N1-2M0) и 30 пациентов без (T1-3N0M0) регионарных метастазов, обнаружено статистически значимое (р<0,005) увеличение экспрессии РТ-генов SSX-2, SCP-1 и PAGE-5 в 1,6, 2,2 и 5,5 раза в опухолевой ткани относительно нормальной ткани и снижение экспрессии РТ-генов BAGE, MAGE-A2 в 1,5 раза, MAGEB2 в 2,0 раза в опухолевой ткани относительно нормальной ткани толстой кишки (рис. 1). Экспрессия остальных 11 генов (MAGE-A1, MAGE-A3, MAGE-B1, GAGE-1, GAGE-3, GAGE-4, MAGE-C1, MAGE-A4, XAGE-3, NY-ESO-1, CTAG-1B) значимо не отличалась от нормы (р > 0.05) (рис. 1).
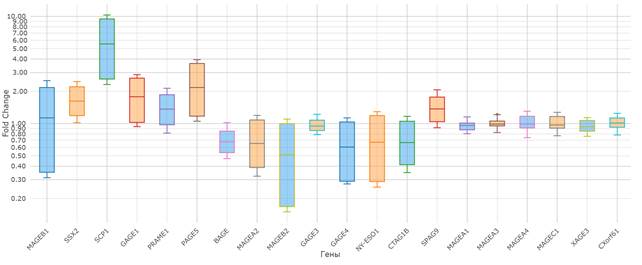
Рис. 1. Соотношение экспрессии РТ-генов в опухолевой ткани толстой кишки относительно нормальной (объединенная выборка, n=60)
Составлено авторами по результатам данного исследования.
У больных КРР без регионарных метастазов (T1-3N0M0) обнаружено статистически значимое (р<0,05) увеличение экспрессии РТ-генов SPAG-9, MAGE-B1, SSX-2 и SCP-1 в 1,8, 2,2, 2,2 и 2,7 раза соответственно в опухолевой ткани толстой кишки относительно нормальной, а также снижение экспрессии гена BAGE в 1,9 раза в опухолевой ткани относительно нормальной ткани толстой кишки (рис. 2).
У пациентов с наличием регионарных метастазов (группа T1-3N1-2M0) обнаружено статистически значимое (р<0,05) увеличение экспрессии генов GAGE-1, SCP-1, PAGE-5 и PRAME-1 в 2,5, 9,1, 3,5 и 1,9 раза соответственно в опухолевой ткани толстой кишки относительно нормальной, а также снижение экспрессии генов MAGE-A2, MAGE-B1, MAGE-B2, GAGE-4, CTAG-1B и NY-ESO-1 в 2,7, 3,0, 5,9, 3,1, 2,5 и 3,3 раза соответственно в опухолевой ткани толстой кишки относительно нормальной ткани (рис. 2). Следует отметить, что в группе пациентов с метастазами (T1-3N1-2M0) в опухолевой ткани экспрессия генов GAGE-1, SCP-1 и PAGE-5 в 2,3, 3,4 и 3.0 раза соответственно выше (р<0,01) уровня экспрессии этих генов в группе пациентов без метастазов (T1-3N0M0). При этом в группе пациентов с метастазами экспрессия таких генов, как MAGE-A2, MAGE-B1, MAGE-B2, GAGE-4, NY-ESO-1, CTAG-1B и SSX-2 в опухолевой ткани статистически значимо (р<0,05) ниже в 2,8, 6,7, 5,6, 3,8, 2,6 и 1,9 раза соответственно, чем в группе пациентов без метастазов (рис. 2).
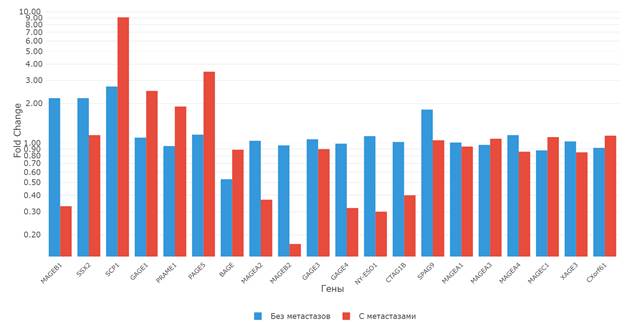
Рис. 2. Уровень транскрипционной активности РТ-генов в опухолевой ткани толстой кишки относительно нормальной у пациентов с регионарными метастазами (n=30) и без (n=30)
Составлено авторами по результатам данного исследования.
Как видно из полученных данных, у пациентов с локализованным и местнораспространенным КРР транскрипционные профили РТА значительно отличаются. На рисунке 3 представлены тепловые карты, отражающие экспрессию РТ-генов индивидуально у каждого пациента в двух сравниваемых группах. Полученные данные позволили выделить несколько кластеров экспрессии РТ-генов: 1) гены ранних стадий и локализованного рака - гиперэкспрессия MAGE-B1, SSX-2, SCP-1, SPAG9 (активны в локализованных опухолях и подавляются при прогрессии, кроме SCP-1); 2) гены, активирующиеся при метастазировании в лимфоузлы - PAGE-5, GAGE-1, PRAME-1 (активируются при метастазировании и участвуют в инвазии и диссеминации); 3) гены, не изменяющие экспрессию при локализованном раке и снижающие её при метастазирования - MAGE-A2, MAGE-B2, GAGE-4, NY-ESO-1 и CTAG-1B.
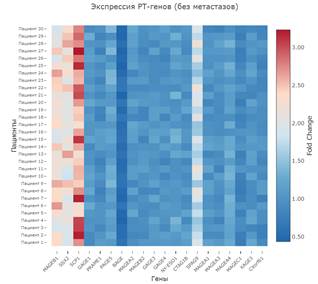
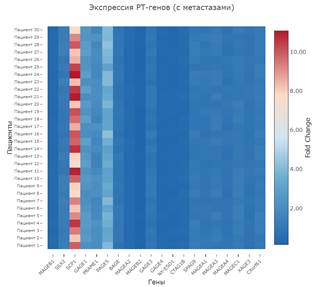
Рис. 3. Тепловые карты экспрессии РТ-генов у пациентов с метастазами (n=30) и без метастазов (n=30)
Составлено авторами по результатам данного исследования.
Ген SCP-1 (Synaptonemal Complex Protein 1) участвует в мейотической рекомбинации, реэкспрессия в опухолях может нарушать репарацию ДНК, а высокая экспрессия коррелирует с геномной нестабильностью. Так, при РЖ его гиперэкспрессия ассоциирована с микросателлитной нестабильностью (MSI) (r=0.62, p=0.01) [14]. Умеренная активация SPAG-9 в группе без метастазов и подавление в группе с метастазами позволяет рассматривать его как ген, чья экспрессия ассоциирована с менее агрессивным фенотипом КРР. Ген PAGE-5 (Prostate-Associated Gene 5) является новым маркером метастазирования при КРР (повышение и в этом исследовании) и ассоциирован с активацией пути Wnt/β-катенин [15].
Продукт гена SSX-2 принадлежит к семейству высокогомологичных белков точек разрыва синовиальной саркомы X (SSX). Эти белки могут функционировать как репрессоры транскрипции. Они также способны вызывать спонтанный гуморальный и клеточный иммунный ответ у онкологических пациентов и являются потенциально полезными мишенями для иммунотерапии на основе противораковых вакцин. Этот ген, а также члены семейств SSX1 и SSX4, участвуют в транслокациях t(X;18) (p11.2;q11.2), характерных для всех синовиальных сарком. Эта транслокация приводит к слиянию гена транслокации синовиальной саркомы на 18-й хромосоме с одним из генов SSX на X-й хромосоме. Кодируемые гибридные белки, вероятно, ответственны за трансформирующую активность. Альтернативный сплайсинг этого гена приводит к образованию множественных вариантов транскриптов. Семейство SSX, включая SSX2, представляет особый интерес как в контексте КРР, так и других злокачественных заболеваний. Повышенная экспрессия SSX2 в неметастатических опухолях КРР согласуется с данными о его детекции при колоректальном раке с частотой 2,5% [16]. Важно отметить, что SSX2 является классическим раково-тестикулярным антигеном, который индуцирует специфический иммунный ответ при различных опухолях, включая меланому, рак легких и рак мочевого пузыря [17].
Гены MAGEB1/B2 – также классические тестикулярно-ограниченные гены, выступающие как супрессоры метастазирования, снижение экспрессии которых может отражать дедифференцировку опухоли. Так, в данном исследовании экспрессия гена MAGE-B1 была повышена в локализованных опухолях КРР. Гиперэкспрессия этого гена ранее была обнаружена в 60% образцов колоректального рака, но экспрессия практически отсутствовала в нормальных тканях, что подтверждает его потенциал в качестве диагностического маркера [18]. Повышение экспрессии гена GAGE-1, а также снижение экспрессии генов SSX-2, MAGE-B1, MAGE-B2, GAGE-4 и NY-ESO-1 согласуется с данными по их экспрессии при местнораспространенном КРР в других исследованиях [9; 10].
При этом полученные данные о дифференциальной экспрессии РТ-генов при локализованном и местнораспространенном КРР также находят подтверждение в исследованиях других онкологических заболеваний. Так, ген GAGE-1, демонстрирующий повышенную экспрессию при местнораспространенном КРР, ранее был обнаружен в различных опухолях, включая гепатоцеллюлярную карциному и опухоли яичников, что подтверждает его роль в прогрессировании опухолевого процесса [19]. Ген PRAME-1, экспрессия которого также возрастает при метастазировании КРР, проявляет схожие паттерны в ряде злокачественных новообразований. Но при немелкоклеточном раке легких экспрессия PRAME часто снижается [20], а при раке молочной железы его высокая экспрессия ассоциирована с плохим прогнозом [21]. Эти различия подчеркивают тканеспецифичность функций РТ-генов.
Для NY-ESO-1/CTAG-1B характерно значимое подавление в опухолях с метастазами, что указывает на возможную роль в качестве супрессора метастазирования или маркера изменения регуляции РTA при прогрессии заболевания. Ген NY-ESO-1 /CTAG-1B, который по полученным данным продемонстрировал снижение экспрессии в метастатических опухолях КРР, в других исследованиях показал противоположную тенденцию. В частности, при раке молочной железы NY-ESO-1 чаще экспрессируется в метастатических очагах по сравнению с первичными опухолями [22], что указывает на различия в регуляции этих антигенов в зависимости от типа опухоли. В отличие от данных литературы [23; 24] для РТ-генов из семейства MAGE-A в проведенном в НМИЦ онкологии исследовании не обнаружено статистически значимого увеличения транскрипционной активности, что коренными образом отличает КРР от опухолей желудка [25]. Эти данные демонстрируют как общие, так и тканеспецифические паттерны экспрессии РТ-генов при различных злокачественных новообразованиях, что имеет важное значение для разработки персонализированных диагностических и терапевтических стратегий.
Заключение
В результате проведенного исследования выявлены значимые различия в транскрипционных профилях раково-тестикулярных антигенов у пациентов с локализованным и местнораспространенным КРР. Установлено, что гены MAGE-B1, SSX2 и SCP1 характеризуются повышенной экспрессией при локализованном КРР, тогда как гены GAGE1, PRAME1 и PAGE5 ассоциированы с метастатическим потенциалом опухоли. Выявленные паттерны экспрессии позволяют выделить три функциональных кластера РТ-генов: гены ранних стадий опухолевого процесса; гены, активирующиеся при метастазировании в лимфоузлы; гены, снижающие экспрессию при метастазировании. Полученные данные имеют важное клиническое значение, поскольку выявленные молекулярные маркеры могут быть использованы для прогнозирования метастатического потенциала колоректального рака и персонализации подходов к лечению. В частности, ген PAGE5, ассоциированный с активацией пути Wnt/β-катенин, представляет особый интерес как потенциальная терапевтическая мишень. Кроме того, обнаруженные различия в экспрессии РТ-генов открывают перспективы для разработки иммунотерапевтических стратегий, направленных на индукцию специфического противоопухолевого иммунного ответа. Дальнейшие исследования должны быть направлены на верификацию выявленных маркеров в проспективных когортах пациентов, а также на изучение функциональной роли этих генов в патогенезе метастазирования КРР.
Conflict of interest
Financing
Библиографическая ссылка
Кутилин Д.С., Худына Ю.Е., Маслов А.А., Колесников Е.Н., Кожушко М.А., Анисимов А.Е., Озеркова Е.А., Камлык Д.В., Легенько Н.Н. ТРАНСКРИПЦИОННЫЙ ПРОФИЛЬ ГЕНОВ РАКОВО-ТЕСТИКУЛЯРНЫХ АНТИГЕНОВ У БОЛЬНЫХ С ЛОКАЛИЗОВАННЫМ И МЕСТНО-РАСПРОСТРАНЕННЫМ КОЛОРЕКТАЛЬНЫМ РАКОМ // Современные проблемы науки и образования. 2026. № 1. ;URL: https://science-education.ru/en/article/view?id=34445 (дата обращения: 29.04.2026).
DOI: https://doi.org/10.17513/spno.34445



