Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
ISSUES IN THE COMPARABILITY OF D-DIMER CONCENTRATION MEASUREMENTS IN ROUTINE CLINICAL PRACTICE
Введение
Определение концентрации D-димера в качестве маркера активации коагуляции и фибринолиза было введено в клиническую практику более 40 лет назад [1]. На сегодняшний день измерение данного маркера стало важным условием диагностики тромбоза глубоких вен (ТГВ) и тромбоэмболии легочной артерии (ТЭЛА) [2–4]. Кроме того, он используется для распознавания ДВС-синдрома и контроля за эффективностью антикоагулянтной терапии [5, 6], получив еще большую актуальность на фоне распространения новой коронавирусной инфекции COVID-19.
Большое значение D-димера как маркера тромбообразования и его широкое применение, в том числе в автоматизированных методах измерения, способствовало появлению большого количества различных коммерческих тест-систем для его определения. Однако в связи с этим появилась проблема сопоставимости получаемых результатов при применении тест-систем различных фирм-производителей. Возникновение данной проблемы обусловлено целым рядом причин. С одной стороны, к этому привело использование фирмами-производителями моноклональных антител с различной чувствительностью и специфичностью к данному производному стабилизированного фибрина, что препятствует получению сопоставимых результатов при исследовании одного и того же образца плазмы крови. С другой стороны, получаемые результаты тестирования зависят от гетерогенности структуры самого аналита, так называемого D-димера. Как известно, последний представляет собой неоднородную смесь продуктов распада фибрина, возникающих в результате многостадийной деградации поперечно-сшитого фибрина плазмином с появлением продуктов широкого диапазона молекулярных масс и структур (рис. 1).
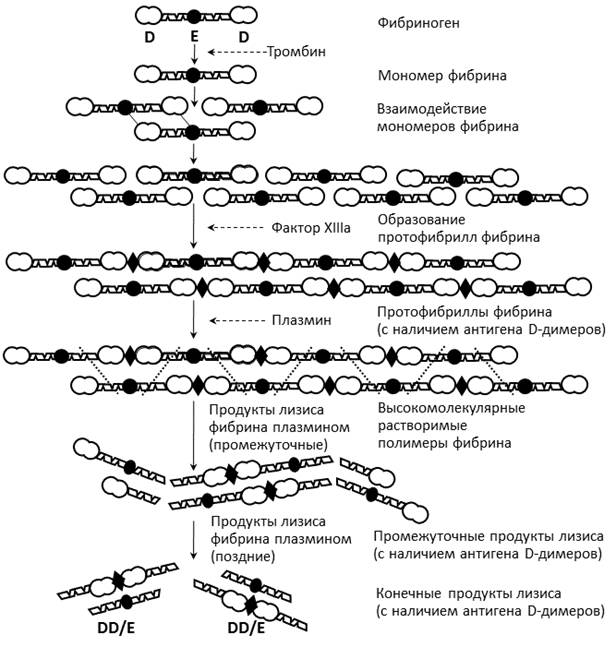
Рис. 1. Последовательность формирования разнообразных производных фибриногена, обладающих неоантигенами D-димера
Примечание: составлен авторами на основе источника [7]
В совокупности с отличающимися характеристиками используемых разными производителями антител (чувствительностью и специфичностью) это вносит дополнительный вклад в несопоставимость результатов [7, 8] (рис. 2).
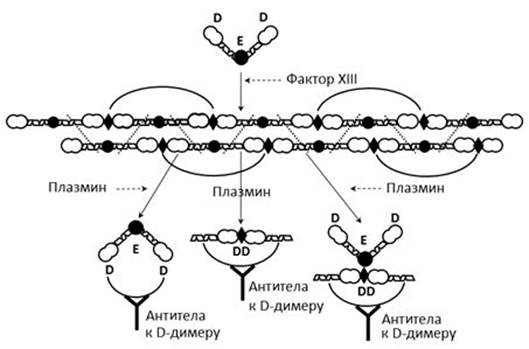
Рис. 2. Разнородность аналита, измеряемого разными коммерческими тест-системами для определения D-димера
Примечание: составлен авторами на основе источника [9]
О проблеме сопоставимости результатов определения D-димера различными тест-системами в образцах плазмы крови пациентов уже было заявлено в ряде зарубежных работ [10, 11]. В России было опубликовано две работы на тему сравнения результатов измерения различными тест-системами [12, 13]. В первой из них было проведено сравнение различных диагностических наборов для определения D-димера в рамках одной лаборатории на образцах плазмы крови женщин с физиологически протекающей беременностью. Авторы второй работы проводили сравнение результатов измерения концентрации этого маркера в контрольных материалах, а также в образцах плазмы крови, полученных от здоровых лиц и пациентов, находившихся на лечении в НИИ акушерства, гинекологии и репродуктологии им. Д.О. Отта, а также в клиниках ПСПбГМУ им. И.П. Павлова.
Цель исследования – изучение принятых подходов в лабораториях РФ к измерению концентрации D-димера и сравнение результатов определения его уровня в стандартных образцах, для улучшения сопоставимости оценки данного маркера в различных лечебных учреждениях.
Материал и методы исследования
1. Приготовление образца плазмы крови с высокой концентрацией D-димера
Плазма крови пациентов с уровнем D-димера более 3000 нг/мл (DDU – D-dimer units) была получена из отделений сосудистой хирургии, кардиологии и пульмонологии клиник г. Барнаула от пациентов с диагнозами ДВС-синдром, ТЭЛА и тромбоз глубоких вен (ТГВ). Концентрация D-димера в каждом из случаев определялась с помощью различных тест-систем: «Auto Red D-dimer» (Helena Biosciences, Великобритания); «Innovance D-dimer» (Siemens Healthineers, Германия). Далее полученные образцы, предварительно исследованные на наличие вирусов СПИД и гепатитов, объединяли в один пул. Уровень D-димера в полученном пуле, измеренный с помощью ИФА-набора ASSERACHROM D-Di (Diagnostica Stago S.A.S., Франция), составил после пересчета из FEU (fibrinogen equivalent units) в DDU 8796 нг/мл [9].
2. Приготовление образцов плазмы доноров
На следующем этапе в работу взяли свежезамороженную плазму от доноров-добровольцев для того, чтобы получить пул нормальной плазмы крови. Мешки с плазмой крови условно здоровых доноров были разморожены при +37 °C и объединены в общий пул. Основные показатели коагулограммы для полученного пула были следующими: протромбиновое время – 13,2 с, АПТВ – 33,0 с, концентрация фибриногена – 2,2 г/л, концентрация D-димера – 48 нг/мл.
3. Приготовление образцов плазмы крови с разной концентрацией D-димера
Используя пул нормальной плазмы крови доноров и плазмы с высокой концентрацией D-димера, последовательными разведениями были приготовлены четыре образца плазм с ориентировочными концентрациями 250, 500, 2000 и 4000 нг/мл.
Для удобства анализа результаты были условно разделены на два диапазона: область низких концентраций (до 1000 нг/мл включительно), включающая диагностически значимое пороговое значение 250 нг/мл, и область высоких концентраций (более 1000 нг/мл), соответствующая заведомо патологическим уровням D-димера 2000 и 4000 нг/мл.
Далее, образцы плазмы крови, соответствующие этим контрольным точкам (КТ), были лиофильно высушены с добавлением общепринятых компонентов для лиофилизации, а также апротинина в конечной концентрации 100 Ед/мл для предотвращения возможных процессов фибринолиза и, как следствие, деградации аналита.
В лиофилизированных КТ, а также исходном пуле с высоким содержанием исследуемого маркера была определена концентрация D-димера, а также основные показатели системы гемостаза: протромбиновое время (ПВ), активированное парциальное тромбопластиновое время (АПТВ), концентрация фибриногена (ФГ) – при помощи наборов «Thromborel S» (Siemens Healthineers, Германия), «APTT Si L Minus» (Helena Biosciences, Великобритания), «Тех-Фибриноген-тест» (Технология-Стандарт, Россия) соответственно. Результаты представлены в табл. 1.
Таблица 1
Результаты измерения лиофильно высушенных образцов с различными значениями D-димера и исходного пула плазм с высоким уровнем D-димера
|
Наименование образца |
ПВ, с |
АПТВ, с |
ФГ, г/л |
D-димер, нг/мл (DDU) |
КВ, с |
МНО |
|
Исходный пул |
14,4 |
34 |
2,9 |
8796 |
78 |
1,1 |
|
КТ 4000 |
13,5 |
32 |
2,8 |
3966 |
91 |
1,0 |
|
КТ 2000 |
13,1 |
32 |
2,7 |
1979 |
98 |
1,0 |
|
КТ 500 |
12,8 |
32 |
2,7 |
522 |
100 |
1,0 |
|
КТ 250 |
12,7 |
33 |
2,6 |
280 |
106 |
1,0 |
|
Контроль |
13,0 |
29 |
3,0 |
60 |
89 |
1,0 |
КВ – каолиновое время; МНО – международное нормализованное отношение. Примечание: составлена авторами на основе полученных данных в ходе исследования
Образцы плазмы крови с измеренной концентрацией D-димера в числе четырех контрольных точек были зашифрованы в случайном порядке (пронумерованы арабскими цифрами: 1, 2, 3 и 4) и переданы участникам исследования для измерения. В исследовании приняла участие 61 лаборатория ЛПУ. Измерения концентрации D-димера участниками исследования проводились в условиях реальной клинической практики.
4. Проведение анкетирования участников исследования
Кроме измерения уровня D-димера в анализируемых образцах участников исследования просили ответить на вопросы анкеты, включающие определение области применения анализа на D-димер, установление факта проведения ежедневного контроля качества (Daily Quality Control – DQC) установление величины и обоснование выбора верхней границы нормы (cut-off) концентрации D-димера.
5. Обработка полученных результатов
Полученные от участников исследования результаты измерения уровня D-димера приводились к единому значению концентрации в DDU (нг/мл). В случае предоставления участниками результатов в формате FEU проводился пересчет – путем деления результата в FEUна 2 [9].
Статистическая обработка данных проводилась с использованием алгоритмов, реализованных в программах Microsoft Office Excel 2007 (Microsoft Corp., США) и Statistica версия 12.0 (StatSoft Inc., США). Результаты представлены в виде медианы и квартилей – Me (Q1; Q3).
Результаты исследования и их обсуждение
Образцы плазм и анкеты были разосланы 80 учреждениям здравоохранения. В итоге результаты были получены от 61 лаборатории из 34 регионов Российской Федерации.
Ниже в табл. 2 приведены данные о комбинациях реагентов и приборов, используемых участниками исследования.
Таблица 2
Варианты комбинаций реагентов и приборов, использованных участниками исследования
|
Наименование прибора |
Число участников и варианты комбинаций (набор/прибор) |
|||||||
|
Auto Red D-dimer 700 |
D-Dimer HS Hemosil |
TS-D-димер |
Innovance D-dimer |
STA Liatest D-Di |
SIEMENS IMMULITE 2000 |
D-димер-ИФА-БЕСТ |
Tina-quant D-Dimer Gen. 2 |
|
|
Thrombolyzer XRM |
1 |
|
|
|||||
|
ACL TOP 500 |
2 |
|
|
|||||
|
ACL TOP 700 |
6 |
|
|
|||||
|
ACL Elite Pro |
2 |
|
|
|||||
|
TS 190 |
8 |
|
|
|||||
|
TS-60 |
6 |
|
|
|||||
|
Sysmex CA-560 |
1 |
|
|
|||||
|
Sysmex CA-600 |
4 |
|
|
|||||
|
Sysmex CA-1500 |
1 |
4 |
|
|
||||
|
Sysmex CS 2100 (2000i) |
1 |
|
12 |
|
|
|||
|
Sysmex CS 5100 |
3 |
|
|
|||||
|
Siemens BCS XP |
1 |
|
|
|||||
|
STA Compact Max |
3 |
|
|
|||||
|
STA Compact |
2 |
|
|
|||||
|
Immulite 2000 Xpi |
2 |
|
||||||
|
Tecan Sunrise RC4 |
|
1 |
||||||
|
Cobas 8000 |
|
|
|
|
|
|
|
1 |
Примечание: составлена авторами на основе полученных данных в ходе исследования
По результатам опроса о проведении ежедневного внутреннего контроля качества (DQC) 43 из 52 (82,7 %) участников, ответивших на этот вопрос, подтвердили его проведение.
Варианты показаний для исследования уровня D-димера представлены в табл. 3. Как показали результаты, основным направлением использования явилась диагностика ТГВ/ТЭЛА/ДВС-синдрома и мониторинг эффективности антитромботической терапии.
Таблица 3
Варианты показаний для измерения уровня D-димера на основе опроса участников исследования
|
Цель определения концентрации D-димера
|
Количество ответов |
Положительные ответы, %* |
|
Диагностика тромбоза глубоких вен нижних конечностей / тромбоэмболии легочной артерии |
44 |
72,1 |
|
Мониторинг эффективности антитромботической терапии |
44 |
72,1 |
|
ДВС-синдром |
32 |
52,5 |
|
Инфекция COVID-19 |
10 |
16,4 |
|
Контроль D-димера при беременности |
3 |
4,9 |
|
В рамках диагностики внутрисосудистого свертывания крови при лейкозах и солидных опухолях |
1 |
1,6 |
* Сумма превышает 100 %, поскольку участники могли выбирать несколько ответов. Примечание: составлена авторами на основе полученных данных в ходе исследования
Большинство участников исследования указывали, что при выборе верхней границы нормы D-димера опирались на данные, приведенные в инструкции производителя (табл. 4). Однако их значения не всегда совпадали с официальными рекомендациями: иногда использовались другие единицы измерения или применялись ошибочные обозначения. Например, для тест-системы «Innovance D-dimer» значение указывалось в нг/мл вместо мкг/мл, а в некоторых случаях применялись единицы FEU там, где должна была использоваться размерность в DDU. И лишь один участник добавил к верхней границе нормы поправку на возраст, что будет рассмотрено подробнее в настоящей статье.
Таблица 4
Варианты определения верхней границы нормы концентрации D-димера на основе результатов опроса участников исследования
|
Вариант ответа |
Количество ответов |
|
Согласно инструкции |
49 (80,3 %) |
|
Данные литературных источников |
6 (9,8 %) |
|
Согласно инструкции + данные литературных источников |
4 (6,6 %) |
|
Локальная валидированная норма + данные литературных источников |
2 (3,3 %) |
Примечание: составлена авторами на основе полученных данных в ходе исследования
В табл. 5 представлены медианы концентраций D-димера (нг/мл) для точек 1–4, указанные для различных методов. Для каждого метода указано общее количество участников (n).
Таблица 5
Концентрации D-димера (Mе (Q1; Q3)), полученные разными методами в DDU (нг/мл)
|
Наименование тест-системы, количество участников |
Кодировка |
Единица измерения |
КТ* 250 |
КТ* 500 |
КТ* 2000 |
КТ* 4000 |
|
Auto Red D-dimer 700 (n = 3) |
A |
в нг/мл DDU |
295 (280; 311) |
521 (484; 538) |
1600 (1581; 1751) |
3205 (2982; 3800) |
|
D-Dimer HS Hemosil (n = 10) |
B |
в нг/мл DDU |
303 (294; 351) |
514 (498; 547) |
1923 (1854; 2083) |
3428 (3347; 3798) |
|
TS-D-димер (n = 15) |
C |
в нг/мл DDU |
254 (224; 310) |
508 (412; 531) |
1767 (1367; 1909) |
3467 (3018; 3905) |
|
D-димер-ИФА-БЕСТ (n = 1) |
D |
в нг/мл DDU |
255 |
489 |
2477 |
3845 |
|
Innovance D-dimer** (n = 24) |
E |
в нг/мл FEU |
974 (906; 1015) |
1706 (1564; 1775) |
5505 (4732; 5904) |
11604 (10207; 12464) |
|
в нг/мл DDU |
487 (453; 507) |
853 (782; 888) |
2752 (2366; 2952) |
5820 (5103; 6232) |
||
|
STA Liatest D-i** (n = 5) |
F |
в нг/мл FEU |
880 (825; 910) |
1580 (1420; 1605) |
4840 (4625; 5009) |
10455 (9730; 11400) |
|
в нг/мл DDU |
440 (413; 455) |
790 (710; 803) |
2420 (2313; 2504) |
5228 (4865; 5700) |
||
|
Tina-quant D-Dimer Gen. 2** (n = 1) |
G |
в нг/мл FEU |
780 |
1510 |
4865 |
8140 |
|
в нг/мл DDU |
390 |
755 |
2433 |
4070 |
||
|
D-Dimer SIEMENS IMMULITE 2000** (n = 2) |
I |
в нг/мл FEU |
777 (616; 939) |
1368 (1101; 1634) |
4976 (3989; 5963) |
10767 (8650; 12883) |
|
в нг/мл DDU |
389 (308; 469 |
684 (551; 817) |
2488 (1994; 2981) |
5383 (4325; 6442) |
* – КТ (контрольная точка) – образец плазмы крови человека с указанным содержанием в ней D-димера в нг/мл; ** – звездочками помечены наборы, где приведены данные после пересчета в единицы DDU.
Примечание: составлена авторами на основе полученных данных в ходе исследования
Результаты оценки уровня D-димера, пересчитанные из FEU (наборы реагентов E, F, G и I), в большинстве случаев были заметно выше и существенно отличались от данных тест-систем, измеряющих концентрацию этого показателя в единицах DDU (наборы A, B, C и D) во всех четырех точках (рис. 3). В частности, для реагентов E и F увеличение оказалось наиболее выраженным – в среднем около 160 % относительно наборов A–D (от 133 % при концентрации 2000 нг/мл (DDU) и до 168 % при концентрации 250 нг/мл (DDU)). Важно подчеркнуть, что именно расхождения в области низких концентраций (168 %) имеют особое значение, так как все исследованные тест-системы трактуют повышение уровня D-димера свыше 250 нг/мл как патологический показатель.
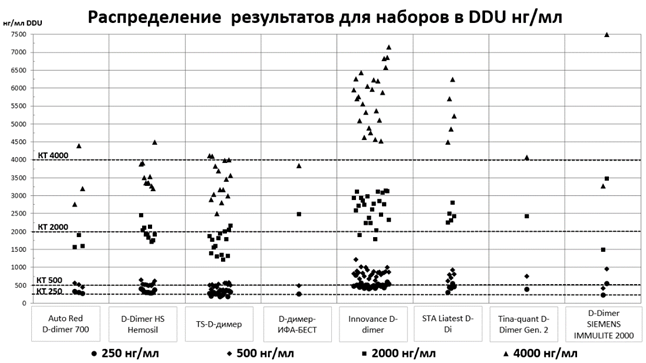
Рис. 3. Распределение результатов оценки уровня D-димера, полученных от участников исследования, полученное при работе с разными тест-системами.
Знаками обозначены: ● – средний результат двух измерений для образца с содержанием
D-димера 250 нг/мл, ♦ – 500 нг/мл, ■ – 2000 нг/мл, ▲– 4000 нг/мл
Примечание: составлен авторами на основе полученных данных в ходе исследования
Учитывая, что каждая контрольная точка была измерена дважды всеми участниками исследования, имелась возможность рассчитать коэффициенты внутрилабораторной вариации (CV) (табл. 6). В данной таблице результаты представлены в виде диапазона значений CV в %, которые были получены при использовании какой-либо тест-системы из приведенных в данной таблице.
Таблица 6
Диапазоны коэффициентов внутрилабораторной вариации, в %
|
Наименование тест-системы, количество лабораторий |
КТ 250 |
КТ 500 |
КТ 2000 |
КТ 4000 |
|
Auto Red D-dimer 700 (n = 3) |
1,3–4,1 |
0,1–3,0 |
0,2–4,9 |
0,2–3,7 |
|
D-Dimer HS Hemosil (n = 10) |
0,2–6,5 |
0,1–3,9 |
0,6–6,9 |
0,5–6,3 |
|
TS-D-димер (n = 15) |
0,6–13,9 |
1,6–16,9 |
0,0–12,3 |
0,3–16,5 |
|
D-димер-ИФА-БЕСТ (n = 1) |
2,8 |
1,2 |
6,3 |
10,9 |
|
Innovance D-dimer (n = 24) |
0,0–6,8 |
0,2–9,0 |
0,1–7,9 |
0,1–23,2 |
|
Tina-quant D-Dimer Gen. 2 (n = 1) |
1,8 |
0,9 |
0,1 |
1,2 |
|
STA Liatest D-i (n = 5) |
0,0–10,5 |
0,0–2,7 |
0,0–6,9 |
0,6–3,9 |
|
D-Dimer SIEMENS IMMULITE 2000 (n = 2) |
0,0–2,3 |
3,0–5,8 |
1,4–6,1 |
0,0–1,1 |
Примечание: составлена авторами на основе полученных данных в ходе исследования
Согласно данным, изложенным в табл. 7, проведение ежедневного контроля качества в большинстве случаев приводило к заметному снижению внутрилабораторной вариации.
Таблица 7
Диапазоны коэффициентов внутрилабораторной вариации для лабораторий, проводящих ежедневный контроль качества, в %
|
Наименование тест-системы, количество лабораторий |
КТ 250 |
КТ 500 |
КТ 2000 |
КТ 4000 |
|
Auto Red D-dimer 700 (n = 2) |
1,3–2,2 |
2,8–3,0 |
0,2–1,0 |
0,2–3,2 |
|
D-Dimer HS Hemosil (n = 10) |
0,2–6,5 |
0,1–3,9 |
0,6–6,9 |
0,5–6,3 |
|
TS-D-димер (n = 11) |
1,2–9,2 |
2,2–5,2 |
0,0–5,9 |
0,3–4,7 |
|
D-димер-ИФА-БЕСТ (n = 1) |
2,8 |
1,2 |
6,3 |
10,9 |
|
Innovance D-dimer (n = 22) |
0,0–3,5 |
0,2–9,0 |
0,1–7,9 |
0,1–16,5 |
|
Tina-quant D-Dimer Gen. 2 (n = 1) |
1,8 |
0,9 |
0,1 |
1,2 |
|
STA Liatest D-i (n = 4) |
0,0–1,6 |
0,0–2,7 |
0,0–0,9 |
0,6–3,9 |
|
D-Dimer SIEMENS IMMULITE 2000 (n = 1) |
0,0 |
3,0 |
1,4 |
0,0 |
Примечание: составлена авторами на основе полученных данных в ходе исследования
Далее были рассчитаны коэффициенты межлабораторной вариации CV (%) для образцов контрольных точек, для тест-систем, результаты по которым были получены от не менее чем трех участников (табл. 8).
Таблица 8
Коэффициенты межлабораторной вариации для образцов контрольных точек
|
Наименование тест-системы, количество измерений |
КТ 250 |
КТ 500 |
КТ 2000 |
КТ 4000 |
|
Auto Red D-dimer 700 (n = 3) |
10,6 % |
10,8 % |
11,0 % |
24,5 % |
|
D-Dimer HS Hemosil (n = 10) |
12,2 % |
10,5 % |
10,9 % |
11,2 % |
|
Innovance D-dimer (n = 24) |
15,4 % |
14,5 % |
15,1 % |
13,3 % |
|
STA Liatest D-i (n = 5) |
19,9 % |
14,4 % |
8,8 % |
12,9 % |
|
TS-D-димер (n = 14) |
21,8 % |
16,1 % |
18,3 % |
15,2 % |
Примечание: составлена авторами на основе полученных данных в ходе исследования
Существуют вопросы, которые нуждаются в дополнительном изучении, так как практически во всех случаях межлабораторная вариация превышала 10 %. Поскольку коэффициент межлабораторной вариации должен составлять не более 10 %, мы видим, что полученные результаты свидетельствуют о недостаточной однородности данных. Основной массив результатов, полученных при использовании тест-системы «D-Dimer HS Hemosil», поступил из сети лабораторий «Инвитро», функционирующих в различных городах России, что может рассматриваться как подтверждение эффективного межлабораторного контроля качества внутри данной сети. Использование данных от лабораторий, осуществляющих ежедневный контроль качества (табл. 9), в целом улучшало показатели.
Таблица 9
Коэффициенты межлабораторной вариации для лабораторий, проводящих и не проводящих ежедневную процедуру контроля качества
|
Межлабораторная вариация |
КТ 250 |
КТ 500 |
КТ 2000 |
КТ 4000 |
|
Для всех лабораторий (n = 61) |
55,2 % |
55,3 % |
50,7 % |
53,9 % |
|
Для лабораторий проводящих DQC (n = 52) |
50,1 % |
52,0 % |
48,5 % |
52,1 % |
|
Для лабораторий не проводящих DQC (n = 9) |
88,4 % |
78,5 % |
63,1 % |
64,8 % |
Примечание: составлена авторами на основе полученных данных в ходе исследования
При сравнении межлабораторной вариации полученных результатов в двух ведущих единицах измерения (DDU нг/мл и FEU нг/мл) было установлено, что для всех контрольных точек (КТ 250, КТ 500, КТ 2000, КТ 4000) значение межлабораторной вариации для результатов, получаемых в DDU, было ниже в 1,2; 1,5; 1,1; 1,4 раза соответственно (табл. 10).
Таблица 10
Коэффициенты межлабораторной вариации для результатов тест-систем, измеряющих уровень D-димера в единицах DDU и FEU
|
Межлабораторная вариация |
КТ 250 |
КТ 500 |
КТ 2000 |
КТ 4000 |
|
DDU |
18,8 % |
14,0 % |
17,7 % |
14,3 % |
|
FEU |
23,2 % |
21,5 % |
20,2 % |
20,1 % |
Примечание: составлена авторами на основе полученных данных в ходе исследования
Полученные и обработанные авторами данные подтверждают наличие проблемы, поднимаемой разными исследователями [1, 8, 14], касающейся расхождения результатов измерения концентрации D-димера тест-системами различных производителей, а также их дальнейшего сопоставления между собой. У данной проблемы несколько причин, и представленная работа подтвердила, что они не устранены.
Отсутствие ежедневного контроля качества
Ежедневный контроль качества призван оценивать правильность получаемых результатов, что, в свою очередь, позволяет уверенно получать сопоставимые данные, тем самым снижая внутрилабораторную вариацию. По данным анкетирования, 9 лабораторий из 61 (14,8 %) не проводили эту процедуру. Между тем проведение ежедневного контроля качества позволяло в разы уменьшить диапазон внутрилабораторной вариации (табл. 7).
Использование различных единиц измерения
Использование той или иной единицы измерения является важным вопросом, который часто вызывает путаницу и ставит под сомнение сопоставимость результатов испытаний между разными лабораториями. Начиная с появления самых ранних количественных методов оценки D-димера, существовали разногласия по поводу выбора правильной единицы измерения его уровня – должны ли это быть единицы в эквиваленте фибриногена (FEU) или D-димера (DDU) [15]. Как известно, единицы FEU сопоставляют массу D-димера с массой фибриногена (молекулярная масса 340 кДа), а калибратор для оценки в этих единицах получают путем деградации плазмином очищенного фибриногена, свернувшегося под действием тромбина в присутствии фактора XIII [15]. В свою очередь, единица DDU соответствует предполагаемой массе D-димера (молекулярная масса 195 кДа), а, соответственно, калибратором в данном случае является очищенный D-димер [15]. Принято, что величина FEU в 2 раза больше чем DDU [9], хотя, по другим данным, принят коэффициент 1,75 [16, 17]. Это означает, что один и тот же образец плазмы крови может дать два разных результата для одного и того же теста. Незнание этого факта врачами КДЛ может привести к возникновению значительных ошибок в интерпретации результатов определения уровня D-димера.
Современные исследования указывают на значительные различия в способах представления результатов анализа D-димера между лабораториями. По данным международных программ внешнего контроля качества, отдельные лаборатории используют различные типы единиц измерения (например, DDU или FEU) и нередко изменяют тип или величину единиц измерения по сравнению с рекомендованными производителем (как правило, это нг/мл или мкг/л). Такая вариабельность в выражении концентрации D-димера (в нг/мл, мкг/л и других единицах) неизбежно приводит к путанице при интерпретации результатов и ограничивает сопоставимость данных, полученных в различных учреждениях [18, 19].
Согласно проведенному авторами данной статьи опросу, у ряда участников исследования также сохраняется неопределенность в используемых единицах измерения, когда для набора, оценивающего уровень D-димера в DDU, указаны единицы FEU. Кроме того, в настоящем исследовании было выявлено 9 случаев несоответствия единиц измерения из общего количества участников (14,8 %). Еще одной наблюдаемой ошибкой было отсутствие указания варианта измерения (DDU или FEU), а также некорректный перевод мкг/мл в мг/л. Результаты веб-опроса, опубликованные в 2015 г. [14], показали, что респондентами используются не менее 28 различных комбинаций единиц измерения для регистрации результатов тестирования D-димера в мировой практике, что еще раз подчеркивает необходимость дополнительных усилий для унификации применяемых единиц измерения.
Отсутствие единых подходов к установлению верхней границы нормы
Традиционное пороговое значение D-димера для исключения венозных тромбоэмболических осложнений (ВТЭО) составляет 500 нг/мл (FEU) или 250 нг/мл DDU, однако могут существовать тест-системы и с другими пороговыми значениями, поэтому пользователи должны быть внимательны в данном вопросе. Авторами работы были отмечены явные ошибки. Так, например, в одной из лабораторий участником опроса, применявшим набор «Auto Red D-dimer 700» (отрицательный прогностический уровень – 200 DDU (нг/мл)), указано, что в лаборатории использовались FEU единицы с порогом 500 нг/мл.
Современные исследования подтверждают, что концентрация D-димера физиологически увеличивается с возрастом, что необходимо учитывать при интерпретации результатов теста. Показано, что использование пороговых значений, скорректированных по возрасту, повышает клиническую информативность анализа и позволяет сократить количество ненужных инструментальных исследований, особенно у пациентов старших возрастных групп [17, 18]. Ряд крупных мультицентровых исследований продемонстрировал, что диапазоны нормальных значений D-димера зависят не только от возраста, но и от пола пациентов, а также от применяемой тест-системы, что подтверждает необходимость индивидуального подхода при интерпретации результатов [20, 21]. Наиболее надежная и широко используемая формула возрастной коррекции, предложенная R.A. Douma et al. [22], сохраняет свое клиническое значение и в современных протоколах: Скорректированное по возрасту значение cut-off, мкг/л FEU = (возраст, годы) × 10 [23]. Внедрение отчетности с учетом возрастного порога доказало эффективность в снижении избыточного применения визуализирующих методов при сохранении высокой чувствительности теста у пациентов с подозрением на венозную тромбоэмболию [23].
К применению валидированных порогов отсечения для конкретной лаборатории с поправкой на возраст пациента призывают в своей работе группа по изучению биомаркеров Европейского общества кардиологов (ESC) и ассоциация неотложной помощи при сердечно-сосудистых заболеваниях (ACCA) [24], а также отечественные специалисты в области лабораторной диагностики [25, 26].
По данным полученных анкет, преобладающее большинство пользователей (85,2 %) в своей практике используют cut-off для D-димера, согласно инструкции. В проведенном опросе лишь два участника отметили применение собственной валидированной нормы, при этом лишь один из респондентов заявил об использовании поправки на возраст, что может говорить о возможной неосведомленности сотрудников КДЛ об этом аспекте.
Вариабельность результатов между разными тест-системами
Авторы исследования FACT, опубликованного в 2001 г., сравнивали результаты, полученные при применении 23 различных тест-систем для оценки уровня D-димера [10]. Было установлено, что средние значения, полученные в 39 образцах, варьировали от 630 до 13 350 мкг/л (с 21-кратной разницей), причем две тест-системы показывали высокую чувствительность по отношению к продуктам распада фибриногена. Также было обнаружено, что некоторые тест-системы на основе ELISA оказались прежде всего более чувствительны к D фрагментам поперечно не сшитого фибрина, а часть иммунотурбидиметрических методов с латексным усилением – к высокомолекулярным продуктам деградации фибрина (ПДФ) [10]. В анализе, представленном P. Meijer et al., на основании данных, полученных из 357 лабораторий, использующих 7 наиболее часто употребляемых диагностических наборов для определения D-димера, показано, что ряд тест-систем давал 20-кратное превышение концентрации данного маркера по сравнению с другими [27]. Еще одно исследование, сравнивающее значения D-димера, полученные из 423 лабораторий, также показало высокую вариабельность результатов [11]. В 2014 г. в исследовании, в котором участвовало 3800 лабораторий, было обнаружено, что коэффициент вариации между методами достигал 42 % [19], что согласуется с полученными данными, представленными в настоящей работе. Еще одна публикация, основанная на анализе четырех отчетов UKNEQAS, показала, что CV между методами (после исключения выбросов) колебались в диапазоне от 30,9 до 41,8 %, для результатов, представленных в DDU, и в диапазоне от 17,7 до 19,3 %, – для FEU единиц [1]. Однако в представляемой работе авторы получили обратный результат (табл. 10).
Авторами настоящего исследования также было установлено, что диагностические наборы, измеряющие уровень D-димера в FEU (мкг/л), после приведения значений к размерности DDU (нг/мл), на всех определяемых точках (КТ 250–4000) дают более высокие значения, чем тест-системы, изначально измеряющие уровень D-димера в DDU. При этом в области низких значений данная закономерность становится особенно актуальной, так как для диагностических наборов, измеряющих уровень D-димера в DDU (нг/мл), значение КТ 250 является значением, при котором делается вывод о наличии патологических значений у пациента. В частности, в приведенном исследовании диагностические наборы, измеряющие уровень D-димера в DDU (нг/мл), показали в этой области сопоставимые результаты (медиана – 295 нг/мл). Однако результаты, измеренные тест-системами в единицах FEU, для КТ 250 (после пересчета) были в 1,62 раза выше данных, полученных на диагностических наборах, измеряющих уровень D-димера в единицах DDU (478 нг/мл против 295 нг/мл соответственно).
Заключение
Определение уровня D-димера на сегодняшний день считается очень важным критерием диагностики/исключения ВТЭО, а также все чаще применяется для оценки риска рецидива ВТЭО в различных медицинских учреждениях. Значение и частота использования этого показателя сегодня многократно возросли из-за связи тромбоза с новой коронавирусной инфекцией COVID-19, что повысило требования к правильности проведения теста и интерпретации результатов, в том числе полученных из разных лабораторий и с применением тест-систем тех или иных производителей. Для лабораторий, проводящих измерение концентрации D-димера у пациентов, весьма важно обращать внимание на то, в каких единицах измерения получен результат (например, в FEU – в мкг/л или DDU – в нг/мл), а также на осознанный выбор применяемой верхней границы нормы, которая в лучшем случае должна быть скорректирована с учетом возраста пациента. Кроме того, ежедневный контроль качества значительно снижает внутрилабораторную вариацию, что свидетельствует о настоятельной необходимости его проведения.
Что касается высокой вариабельности значений уровня D-димера, полученных при применении различных тест-систем, то перспективное использование методов гармонизации, основанных на математическом сопоставлении данных с применением коэффициентов пересчета, призвано снизить зафиксированные различия в его уровне между различными диагностическими наборами. Данное обстоятельство, вероятно, позволит выполнять адекватный пересчет показателей, полученных при использовании всей линейки тест-систем для определения D-димера, используемых в России.
Conflict of interest
Библиографическая ссылка
Момот Д.А., Кудинов А.В., Мамаев А.Н., Терехов С.С., Шахматов И.И., Момот А.П. ПРОБЛЕМЫ СОПОСТАВИМОСТИ РЕЗУЛЬТАТОВ ИЗМЕРЕНИЯ КОНЦЕНТРАЦИИ D-ДИМЕРА В РЕАЛЬНОЙ КЛИНИЧЕСКОЙ ПРАКТИКЕ // Современные проблемы науки и образования. 2025. № 6. ;URL: https://science-education.ru/en/article/view?id=34355 (дата обращения: 21.05.2026).
DOI: https://doi.org/10.17513/spno.34355



