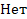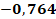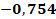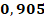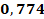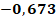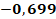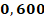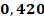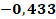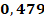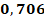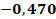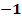Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
ANALYSIS OF RISK FACTORS FOR RETINOPATHY OF PREMATURITY DEVELOPMENT DURING NEONATAL INTENSIVE CARE IN EXTREMELY LOW BIRTH WEIGHT INFANTS
Васкулогенез сетчатки начинается на 16-й неделе внутриутробного развития и завершается к моменту рождения ребенка. При преждевременных родах у недоношенных детей всегда выявляются аваскулярные зоны, размер которых зависит от гестационного возраста. Наличие таких аваскулярных зон сетчатки является предрасположенностью к развитию серьезного заболевания глаз – ретинопатии новорожденных [1]. По мере того как совершенствуются методы выхаживания младенцев с низкой и экстремально низкой массой тела, растет и частота встречаемости ретинопатии. Это ставит перед неонатологами-реаниматологами новые задачи, направленные не только на спасение жизни пациентов, но и на снижение риска развития инвалидизации и улучшение качества жизни недоношенных детей. При решении этих задач принципиально важно оценивать вклад факторов риска в развитие заболевания, чтобы минимизировать их во время интенсивной терапии новорожденных. Исследования последних лет подтверждают, что гестационный возраст (ГВ) и вес пациентов являются ведущими факторами риска развития ретинопатии новорожденных [2-4]. К другим значимым факторам относятся длительная кислородотерапия [5] и тяжелая асфиксия в родах [6]. Обнаружено, что количество гемотрансфузий (ГТС) коррелирует со степенью выраженности ретинопатии недоношенных [7; 8].
Ранее в исследовании, проведенном в отделении интенсивной терапии и реанимации новорожденных (ОРИТН) «Детского городского многопрофильного клинического специализированного центра высоких медицинских технологий» г. Санкт-Петербурга, анализировали связь между осуществляемой интенсивной терапией и риском развития ретинопатии новорожденных у 40 недоношенных пациентов с ГВ 29 [24;35] недель [9]. Основное внимание уделяли изучению роли предполагаемых ведущих факторов риска: кислородозависимости (FiO2), количества ГТС, ГВ и применения инотропной поддержки в ходе лечения. Дополнительно анализировали критерии: продолжительность искусственной вентиляции легких (ИВЛ) в часах, вес при рождении, инфекционный статус, присутствие внутриутробных фетальных коммуникаций и показатели венозной сатурации. Обнаружено, что более низкий ГВ (недоношенность) является одним из ведущих факторов риска развития и тяжести ретинопатии новорожденных, о чем свидетельствует сильная отрицательная корреляция (r= -0.75, p<0.001). Выявлен критический порог оксигенации (40-45%), начиная с которого риск неблагоприятного исхода (развития тяжелой ретинопатии новорожденных) возрастает. Корреляции в группе пациентов с ретинопатией 1-й и 2-й стадии (FiO2 с ИВЛ и ГТС) также подчеркивают роль кислородотерапии и связанных с ней вмешательств в патогенезе заболевания. Не выявлено достоверных различий в количестве ГТС между группами А, В и С. Однако корреляционный анализ в группе В показал, что у более незрелых детей внутри этой группы ГТС было больше. Это позволяет предположить, что роль ГТС может быть более значимой именно у глубоко недоношенных с ретинопатией 1-2-й степени, но не является универсальным маркером тяжести заболевания на уровне сравнения групп. Наличие инотропной поддержки также является значимым фактором риска тяжести ретинопатии, о чем говорит выявленная положительная корреляция (r=0.61, p<0.001) [9].
Таким образом, было выявлено, что основными факторами риска развития и тяжести ретинопатии новорожденных являются глубокая недоношенность (низкий ГВ) и связанные с интенсивной терапией недоношенных вмешательства: высокодозовая кислородотерапия (особенно FiO2 >40-45%), длительная ИВЛ, необходимость инотропной и вазопрессорной поддержки и количество ГТС. Выявленные сильные корреляции между этими факторами (особенно в группе В) с тяжестью ретинопатии, а также специфические взаимосвязи внутри разных групп пациентов подчеркивают сложный многофакторный патогенез заболевания и важность тщательного мониторинга и оптимизации респираторной, гемодинамической и трансфузионной терапии у глубоко недоношенных детей для профилактики тяжелых форм ретинопатии.
Целью данной работы был анализ зависимости прогрессирования ретинопатии новорожденных в группе младенцев с экстремально низкой массой тела от влияния проводимой интенсивной терапии недоношенных.
Материалы и методы исследования
Исследование включило 40 новорожденных младенцев с экстремально низкой массой тела и ГВ менее 32 недель. Пациенты находились на лечении в ОРИТН № 39А «Детский городской многопрофильный клинический специализированный центр высоких медицинских технологий» (Детская городская больница № 1) в 2021-2023 гг. Проведено клинико-диагностическое обследование пациентов по общепринятому протоколу (Приказ МЗ РФ №909н от 12.11.2012). Исследование одобрено локальным этическим комитетом Детской городской больницы № 1.
Дети поделены на 3 группы:
- Группа А - 11 человек. Прооперированные пациенты с диагнозом «ретинопатия 3-й стадии».
- Группа B - 26 человек. Пациенты с диагнозом «ретинопатия 1-й и 2-й стадии».
- Группа C - 3 человека. Пациенты с диагнозом «сетчатка в стадии васкуляризации».
Межгрупповые и внутригрупповые различия оценивали по следующим критериям: FiO2, количество ГТС, ГВ, вес пациентов, количество часов ИВЛ, наличие инотропной поддержки препаратами группы биогенных аминов в ходе лечения. Для оценки кислородозависимости пациентов рассчитали количество кислорода, которое пациент получал в ходе лечения по данным «Медицинской информационной системы qMS». Обработка данных средствами Statistica 10.0 включала применение критерия Краскела - Уоллиса с целью обнаружения различий по параметрам между группами. Для апостериорных сравнений между группами использовали критерий Манна - Уитни. Рассчитали коэффициенты ранговой корреляции Спирмена между факторами риска в каждой группе. Результаты представлены как Мe[Q1;Q2].
Результаты исследования и их обсуждение
В исследовании участвовали новорожденные с гестационным возрастом 26 [20;32] недель. Статистический анализ выявил пять ведущих факторов риска развития заболевания. Результаты сравнения групп представлены в таблице 1: отсутствие различий маркировано как A=B, наличие – как А˂С.
Таблица 1
Межгрупповые различия по исследуемым параметрам
|
|
Группы |
||||
|
Параметр FiO2 |
|
А |
В |
С |
|
|
Группы |
А |
* |
= |
= |
|
|
В |
|
* |
= |
||
|
Параметр Вес |
Группы |
А |
* |
= |
= |
|
В |
|
* |
= |
||
|
Параметр ИВЛ |
Группы |
A |
* |
˃ |
˃ |
|
B |
|
* |
˃ |
||
|
Параметр ГТС |
Группы |
A |
* |
= |
˃ |
|
B |
|
* |
˃ |
||
|
Параметр ГВ |
Группы |
A |
* |
= |
˂ |
|
B |
|
* |
˂ |
||
Примечание: составлено авторами на основе полученных данных в ходе исследования. FiO2 - степень оксигенации, ИВЛ - продолжительность искусственной вентиляции легких, ГТС – гемотрансфузии, ГВ - гестационный возраст.
Анализ параметра кислородозависимости показал, что разницы между пациентами группы А (0,30%[0.21-0.50]), В (0,32%[0.21-0.45]) и С (0,3%[0.21-0.30]) нет. Количество часов ИВЛ пациентов, вошедших в группу А (393[135;2400]), достоверно больше, чем в группах В и С. Пациенты группы В (190[9;1313]) также провели больше часов с применением ИВЛ, чем пациенты группы С (21[20;96]). Количество ГТС в группе А (4[2;12]) и В (3,5[1;10]) больше, чем в группе С (1[1;2]). Анализ массы тела пациентов не показал статистически значимых отличий группы А (850 [600;1000]) от группы В (870 [700;1000]) или группы С (940 [830;1000]). ГВ в группах А (25 [20;28]) и В (26 [24;32]) также не различался достоверно. В то же время группа С (31 [28;32]) имела значимо больший ГВ по сравнению как с группой А, так и с группой В. Статистический анализ выявил ряд значимых взаимосвязей между ключевыми параметрами в группе А, представленными коэффициентами ранговой корреляции Спирмена с уровнем значимости p<0.05 (табл. 2). Данные демонстрируют выраженную обратную зависимость массы тела пациентов от продолжительности ИВЛ (r = -0.764), а также от количества ГТС (r = -0.754). В то же время вес ожидаемо достоверно положительно коррелировал с ГВ новорожденных, показывая высокий коэффициент связи (r = 0.905). Параметры ИВЛ и ГТС обнаружили тесную прямую взаимосвязь (r = 0.774), тогда как между длительностью вентиляции и ГВ наблюдалась умеренная обратная корреляция (r = -0.673). Анализ пары ГТС-ГВ выявил статистически значимую умеренную обратную связь (r = -0.699), однако регрессионное моделирование не подтвердило наличия значимой линейной зависимости между этими переменными.
Таблица 2
Результаты корреляционного анализа исследуемых показателей в группе А
|
Группа А |
FiO2 |
Вес |
ИВЛ |
ГТС |
ГВ |
|
FiO2 |
|
|
|
|
|
|
Вес |
|
|
|
|
|
|
ИВЛ |
|
|
|
|
|
|
ГТС |
|
|
|
|
|
|
ГВ |
|
|
|
|
|
Примечание: составлено авторами на основе полученных данных в ходе исследования. FiO2 - степень оксигенации, ИВЛ - продолжительность искусственной вентиляции легких, ГТС – гемотрансфузии, ГВ - гестационный возраст.
Корреляционный анализ данных по группе В выявил статистически значимую положительную взаимосвязь между продолжительностью ИВЛ и объемом проведенных ГТС, выражающуюся коэффициентом корреляции Спирмена r = 0,706, что согласуется с аналогичной закономерностью, обнаруженной в группе А (табл. 2 и 3). Помимо этой выраженной связи, анализ позволил обнаружить более слабые, но также статистически значимые положительные корреляции: между количеством ГТС и FiO2 (r = 0,420), а также между массой тела пациентов и их ГВ (r = 0,479).
Таблица 3
Результаты корреляционного анализа исследуемых показателей в группе В
|
Группа B |
FiO2 |
Вес |
ИВЛ |
ГТС |
ГВ |
|
FiO2 |
|
|
|
|
|
|
Вес |
|
|
|
|
|
|
ИВЛ |
|
|
|
|
|
|
ГТС |
|
|
|
|
|
|
ГВ |
|
|
|
|
|
Примечание: составлено авторами на основе полученных данных в ходе исследования. FiO2 - степень оксигенации, ИВЛ - продолжительность искусственной вентиляции легких, ГТС – гемотрансфузии, ГВ - гестационный возраст.
Результаты корреляционного анализа группы С продемонстрировали идеальную обратную взаимосвязь между уровнем FiO2 и объемом гемотрансфузий ГТС (r = -1.0). Данный результат согласуется с данными, полученными в группе А (табл. 2 и 4).
Таблица 4
Результаты корреляционного анализа исследуемых показателей в группе С
|
Группа C |
FiO2 |
Вес |
ИВЛ |
ГТС |
ГВ |
|
FiO2 |
|
|
|
|
|
|
Вес |
|
|
|
|
|
|
ИВЛ |
|
|
|
|
|
|
ГТС |
|
|
|
|
|
|
ГВ |
|
|
|
|
|
Примечание: составлено авторами на основе полученных данных в ходе исследования. FiO2 - степень оксигенации, ИВЛ - продолжительность искусственной вентиляции легких, ГТС – гемотрансфузии, ГВ - гестационный возраст.
Основная часть пациентов с ретинопатией получала инотропные и вазопрессорные препараты группы тирозиновых биогенных аминов (табл. 5). Результаты корреляционного анализа демонстрируют умеренную отрицательную корреляцию ГВ со степенью заболевания (r= -0,59, р<0,001) и умеренную положительную корреляцию между применением инотропной поддержки и выраженностью ретинопатии новорожденных (r= 0,5, р<0,001).
Таблица 5
Применение инотропной и вазопрессорной поддержки при проведении интенсивной терапии у детей с экстремально низкой массой тела
|
Поддержка |
Группа А |
Группа Б |
Группа В |
|
Адреналин, добутамин |
6 |
5 |
0 |
|
Норадреналин, адреналин и добутамин |
3 |
5 |
0 |
|
Дофамин и/или добутамин |
1 |
13 |
1 |
|
Без инотропной поддержки |
1 |
3 |
2 |
Примечание: составлено авторами на основе полученных данных в ходе исследования.
Таким образом, ГВ остается ключевым фактором риска развития заболевания, но его роль меняется в группе младенцев с экстремально низкой массой тела. Хотя корреляционный анализ по всем детям подтвердил умеренную отрицательную связь между ГВ и тяжестью ретинопатии новорожденных (r= -0.59), среди самых незрелых детей (ГВ <32 недель, особенно <28 недель) другие факторы (ИВЛ, ГТС) становятся более важными предикторами тяжести заболевания (стадия 3 vs 1-2), чем минимальные различия в ГВ.
По результатам анализа длительность искусственной вентиляции легких является одним из самых значимых факторов для развития заболевания (В/А vs С) и его тяжести (А vs В) у детей с экстремально низкой массой тела. Сильная отрицательная связь с весом и ГВ (в группе А) отражает общую незрелость всех систем организма, а сильная положительная связь с количеством ГТС (в группах А и В) подчеркивает важность данного фактора. В исследовании Сайдашевой Э.И с соавт. наблюдается схожая картина: средняя продолжительность нахождения детей со сроком гестации менее 27 недель на ИВЛ имела статистически значимые различия (р < 0,05) в группах пациентов с ретинопатией 1-й и 3-й стадий [10].
Ранее получены доказательства отсутствия связи между количеством гемотрансфузии и степенью прогрессирования ретинопатии [9]. Однако у детей с экстремально низкой массой тела множественные гемотрансфузии являются значимым фактором прогрессирования ретинопатии новорожденных (группы А/В vs С). Тем не менее среди детей, у которых развилась ретинопатия, количество ГТС не является основным фактором, отличающим тяжелую (группа А) от средней/легкой (группа В) степени. Сильная связь с низким весом и ГВ в группе А указывает на уязвимость самых незрелых младенцев.
Результаты предыдущего исследования показали, что прогрессирование ретинопатии было пропорционально кислородозависимости. Дети, получающие газовоздушную смесь с содержанием кислорода 40% и выше, были прооперированы или имели худший прогноз по прогрессированию данного заболевания [9]. Сходный результат описан в работе ряда исследователей [11-13]. В группе детей с экстремально низкой массой тела по усредненному показателю FiO2 различий не было. Однако его связь с продолжительностью ИВЛ в группе В и общая патофизиология ретинопатии предполагают, что длительность воздействия или вариабельность сатурации (а не только средний FiO2) могут играть важную роль.
Параметр «вес» теряет прогностическую ценность для анализа риска развития или тяжести ретинопатии между группами у детей с экстремально низкой массой тела, но остается важным внутри группы самых тяжелых пациентов (А).
Проведенные исследования показали, что среди детей с экстремально низкой массой тела наличие инотропной и вазопрессорной поддержки также является значимым фактором риска тяжести ретинопатии (r=0.50, p<0.001), как было обнаружено ранее и у детей с низкой массой тела (Лопатин и др., 2023). Экспериментальные исследования подтверждают вовлеченность адренорецепторов в ретинальный ангиогенез [14; 15] и регуляцию роста сетчатки в эмбриогенезе [16].
Заключение
Проведенное исследование подтверждает, что гестационный возраст сохраняет роль ключевого фактора риска ретинопатии новорожденных, однако его прогностическая значимость снижается в группе младенцев с экстремально низкой массой тела, где ведущими предикторами тяжести заболевания выступают длительность искусственной вентиляции легких, множественные гемотрансфузии и необходимость инотропной и вазопрессорной поддержки. При этом вес теряет дифференцирующую ценность между подгруппами, но остается значимым внутри подгруппы тяжелых пациентов. Влияние кислородотерапии определяется не только средним FiO₂, но и длительностью воздействия или вариабельностью сатурации, что подчеркивает комплексный характер патогенеза ретинопатии новорожденных, объединяющий общую незрелость систем организма и ятрогенные воздействия.
Conflict of interest
Библиографическая ссылка
Лопатин А.И., Пасатецкая Н.А., Лопатина Е.В., Андреев В.В. АНАЛИЗ ФАКТОРОВ РИСКА РАЗВИТИЯ РЕТИНОПАТИИ В ХОДЕ ИНТЕНСИВНОЙ ТЕРАПИИ И РЕАНИМАЦИИ НЕДОНОШЕННЫХ МЛАДЕНЦЕВ С ЭКСТРЕМАЛЬНО НИЗКОЙ МАССОЙ ТЕЛА // Современные проблемы науки и образования. 2025. № 5. ;URL: https://science-education.ru/en/article/view?id=34279 (дата обращения: 31.05.2026).
DOI: https://doi.org/10.17513/spno.34279