Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
COMPARATIVE ANALYSIS OF EXTRAPLEURAL AND TRANSPLEURAL THORACOPLASTY OF ASYMMETRIC PECTUS EXCAVATUM IN CHILDREN
Введение
Воронкообразная деформация грудной клетки (ВДГК) – это врожденный порок развития, проявляющийся различными по глубине и форме деформациями хрящевых участков ребер и западением грудины. Согласно данным различных авторов, в структуре всех деформаций грудной клетки ВДГК составляет от 75 до 91%, а среди населения встречается от 0,06 до 2,3% [1; 2, с. 7]. Распространенность случаев порока у мальчиков от 2 до 9 раз чаще по сравнению с девочками [2, с. 20; 3, с. 4]. Этиология данной патологии остается неясной, но, по литературным данным, предполагается, что она связана с нарушением роста реберных хрящей [4].
Клинически ВДГК может проявляться от легкой до тяжелой степеней. Легкие случаи определяются как эстетическая проблема, в то время как деформации средней и тяжелой степеней могут приводить к сердечно-легочным нарушениям, включая снижение объема легких и компрессию сердца [5]. Для диагностики ВДГК и формирования показаний к коррекции деформации, помимо клинических данных, используют множество индексов на основе лучевых методов исследований, самым распространенным из которых является индекс Галлера [6]. Варианты лечения варьируются в зависимости от тяжести деформации и симптомов. В легких случаях может быть достаточно динамического наблюдения, а при средней и тяжелой степенях – от консервативных методов до хирургического вмешательства.
Коррекция ВДГК в случаях средней и тяжелой степеней наиболее эффективна хирургическими методами - применяются радикальные и малоинвазивные, а также их сочетание. В последние десятилетия малоинвазивные методы получили достаточно широкое распространение, а в основе их развития лежала методика D. Nuss. Методика D. Nuss - малоинвазивная методика, включающая проведение металлических пластин трансплеврально и ретростернально с целью коррекции деформации [7].
На сегодняшний день торакопластика по D. Nuss имеет различные модификации, направленные на снижение количества и типов осложнений, характерных для оригинальной методики автора [8]. В настоящее время данная группа вмешательств обозначается аббревиатурой MIRPE (minimally invasive repair of pectus excavatum – малоинвазивная коррекция воронкообразной деформации грудной клетки) [9]. Говоря об эффективноcти MIRPE, D. Nuss в результате 10-летнего лечения ВДГК приводит данные о 8% неудовлетворительных результатов [8]. А.Ю. Разумовский и А.А. Павлов получили 21% неудовлетворительных результатов при использовании данной методики [10]. Другие исследователи утверждали, что такие осложнения, как гемоторакс, пневмоторакс и кровотечения, могут достигать величины в 10,6%, а миграция пластины возникает в 4 раза чаще у пациентов с асимметричной деформацией грудной клетки (АВДГК) и в 3 раза чаще у детей с генетической патологией [11].
Несмотря на продолжающееся совершенствование MIRPE, сохраняется достаточное количество нерешенных вопросов, требующих дальнейшего осуществления поиска и разработки новых, более приемлемых методов коррекции ВДГК при минимальной инвазивности [12].
Одним из современных вариантов MIRPE является экстраплевральная малоинвазивная торакопластика, описание которой в литературе является весьма ограниченным. Данный метод, согласно мнению ряда авторов, обладает рядом объективных преимуществ [13; 14].
Цель исследования. Провести ретроспективный сравнительный анализ результатов хирургической коррекции АВДГК у детей с использованием экстраплевральной и трансплевральной малоинвазивных торакопластик.
Материалы и методы исследования. Исследование основано на предварительном комплексном обследовании и лечении 112 детей в возрасте от 6 до 17 лет с АВДГК. Хирургическое лечение детей проведено в период с 2021 по 2023 г. в отделении костной патологии. Всем пациентам выполняли коррекцию с применением малоинвазивной торакопластики. Исследование выполнено в соответствии с этическими стандартами Хельсинкской декларации Всемирной медицинской ассоциации, одобрено локальным этическим комитетом ФГБУ «НМИЦ ДТО им. Г.И. Турнера» Минздрава России (протокол № 22-5 от 15.09.2022). Пациенты (их представители) дали согласие на обработку и публикацию персональных данных.
Пациенты были разделены на две группы в зависимости от варианта хирургического вмешательства. Первой группе, которую составили 54 пациента (основная группа), была выполнена малоинвазивная экстраплевральная торакопластика, второй группе (58 пациентов – группа сравнения) осуществили торакопластику трансплевральным способом.
Группы были сопоставимы по полу и возрасту. В обеих группах преобладали мальчики: 45 (83%) пациентов в первой и 50 (86%) детей во второй (табл. 1).
Таблица 1
Распределение пациентов по полу
|
Группа |
Пол |
Всего |
p (χ2-тест) |
|
|
мужской |
женский |
|||
|
n (%) |
n (%) |
n (%) |
0,673 |
|
|
Первая |
45 (83) |
9 (17) |
54 (100) |
|
|
Вторая |
50 (86) |
8 (14) |
58 (100) |
|
Возраст абсолютного большинства пациентов в двух группах исследования находился в диапазоне 10-17 лет, что составило свыше 97% (табл. 2).
Таблица 2
Распределение пациентов по возрасту
|
Группа |
Возраст, лет |
Всего |
Med [Q1; Q3] |
p, тест Манна-Уитни |
|
|
5-9 |
10-17 |
||||
|
n (%) |
n (%) |
n (%) |
|||
|
Первая |
1 (2) |
53 (98) |
54 (100) |
15[14;16] |
0,005 |
|
Вторая |
2 (3) |
56 (97) |
58 (100) |
14 [13; 16] |
|
У более чем 4/5 пациентов каждой из групп была определена 3-я степень деформации: в первой – 43 (80%) ребенка, во второй – 51 (88%) пациент (табл. 3).
Таблица 3
Распределение пациентов по степени деформации
|
Группа |
Степень деформации |
Всего |
p (χ2-тест) |
|
|
2-я |
3-я |
|||
|
n (%) |
n (%) |
n (%) |
0,232 |
|
|
Первая |
11 (20) |
43 (80) |
54 (100) |
|
|
Вторая |
7 (12) |
51 (88) |
58 (100) |
|
В обеих группах преобладала правосторонняя деформация грудной клетки: 34 (63%) пациента в первой и 37 (64%) детей – во второй. По типам деформаций распределение было следующим: в группе экстраплевральных торакопластик превалировал локальный тип – 37 (69%) пациентов, в группе трансплевральных торакопластик также преимущественно встречался локальный тип деформации – 46 (79%) пациентов (табл. 4).
Таблица 4
Распределение пациентов по типу и стороне деформации
|
Группа |
Тип деформации |
Сторона деформации |
Всего в каждой группе |
|||
|
локальный |
протяженный |
плоско-вороночный |
лево- сторонняя |
право- сторонняя |
||
|
n (%) |
n (%) |
n (%) |
n (%) |
n (%) |
n (%) |
|
|
Первая |
37 (69) |
15 (28) |
2 (3) |
20 (37) |
34 (63) |
54 (100) |
|
Вторая |
46 (79) |
9 (16) |
3 (5) |
21 (36) |
37 (64) |
58 (100) |
Предоперационные индексы деформаций отображены в таблице 5, значимые отличия, причем близкие к критическому уровню значимости, были выявлены только по индексу компрессии.
Таблица 5
Индексы деформации (предоперационные данные)
|
Индексы (нормальные значения) |
Первая группа Med [Q1;Q3] |
Вторая группа Med [Q1;Q3] |
p, тест Манна-Уитни |
|
ИГ (≤ 2) |
3,855 [3,45; 4,766] |
4,371 [3,48; 5,12] |
0,233 |
|
ИК (≥ 0,89) |
0,6 [0,52; 0,68] |
0,565 [0,5; 0,619] |
0,039 |
|
УНГРК (≤ 5°) |
16 [11; 21] |
15 [11; 21] |
0,793 |
Примечание. ИГ – индекс Галлера; ИК – индекс компрессии; УНГРК – угол наклона грудинореберного комплекса.
Кроме клинического осмотра с целью определения степени, типа, симметричности деформации, проводили рентгенографию в переднезадней проекции и компьютерную томографию (КТ) грудной клетки. На основе полученных данных рентгенограмм определяли смещение органов средостения, состояние плевральных синусов с целью последующего сравнения с послеоперационными данными. По результатам КТ оценивали особенности расположения органов грудной клетки, их смещение деформированным грудинореберным комплексом, а также ряд индексов (индекс Галлера, индекс компрессии, угол наклона грудинореберного комплекса). После оперативного лечения оценивали восстановление ретростернального пространства и косметический результат по симметричности передней грудной стенки, исходя из разницы высоты гемитораксов. Отсутствие асимметрии трактовали как отличный результат, разницу до 10 мм – хороший, от 10 до 20 мм относили к удовлетворительным результатам, разницу более чем 20 мм – к неудовлетворительным косметическим результатам коррекции. Данные пациентов являлись архивным материалом.
Хирургическое вмешательство в 1-й группе проводили согласно методу, описанному Han Y. с соавторами в 2010 г. [13].
В положении пациента лежа на спине, с отведенными верхними конечностями до 90 градусов и сгибанием в локтевых суставах. Из двух контралатеральных доступов длиной до 30 мм в проекции передней подмышечной линии на уровне вершины деформации формировали каналы до парастернальной линии субфасциально. Создание ретростернального канала выполняли при помощи изогнутого зажима (длиной 450 мм) с фиксированной в нем лентой Мерсилен 5 мм, с точкой входа в 1,5-2 см от края грудины с постоянным мануальным контролем контакта дорсальной поверхности грудины и конца зажима, с аналогичной (парастернальной) точкой выхода на противоположной стороне вне плевральных полостей всегда слева направо. Асимметричную пластину проводили по ленте-проводнику. Первоначально пластину моделировали и проводили по контурам деформации передней грудной стенки с последующим ее поворотом на 180 градусов вокруг продольной оси. Фиксацию пластины осуществляли лентой Мерсилен 5 мм, при помощи иглы Дешана (Deschamps), проведенной вокруг ближайшего ребра и через отверстия в пластине в двух точках с каждой стороны. Дренирование обеих плевральных полостей выполняли из дополнительных проколов на период получения экссудата.
У пациентов 2-й группы хирургическое вмешательство проводили в идентичном положении пациента на операционном столе. Выполняли два контралатеральных доступа длиной до 30 мм по передней подмышечной линии на уровне, соответствующем вершине деформации. Медиальнее границы западения грудины осуществляли вход в плевральную полость по верхнему краю ребра на протяжении 20-25 мм, через который интродьюсером формировали ретростернальный канал. По созданному каналу проводили асимметричную пластину, с учетом характера деформации, с последующим ее поворотом на 180 градусов вокруг продольной оси. Дальнейшую фиксацию пластины и дренирование плевральных полостей осуществляли идентично, как у пациентов первой группы.
Все осложнения были разделены на две категории: интраоперационные и ранние послеоперационные ввиду ограниченного срока наблюдения.
Статистическую обработку материала проводили c использованием программы IBMSPSS26. Большинство выборочных распределений показателей были далеки от нормальных и представлены в виде медианы [Q1; Q3] (нижний и верхний квартили). Для сравнения бинарных показателей первой и второй групп применялись тест хи-квадрат и точный тест Фишера, а для сравнения упорядоченных признаков: возраст, индексы и прочее – тест Манна-Уитни. Для сравнений групп по неупорядоченным категориям применен тест хи-квадрат. За критический уровень значимости выбран p=0,05.
Результаты исследования и их обсуждение
Всем детям была осуществлена хирургическая коррекция воронкообразной деформации грудной клетки в объеме малоинвазивной торакопластики с восстановлением ретростернального пространства и синтезом грудинореберного комплекса пластиной. При использовании экстраплевральной и трансплевральной малоинвазивных торакопластик была достигнута планируемая коррекция ретростернального пространства в 100% наблюдений. Косметический результат торакопластик в группах был различным. Частота отличных результатов в 1-й группе была на 17% больше по сравнению со второй группой, хороших в 1,5 раза меньше, удовлетворительных вдвое меньше. Неудовлетворительных результатов не было отмечено ни в одной группе исследования (табл. 6).
Таблица 6
Результаты лечения в группах исследования
|
Группа |
Отличные результаты, % (n) |
Хорошие результаты, % (n) |
Удовлетворительные результаты, % (n) |
p (χ2-тест) |
|
Первая |
76 (41) |
15 (8) |
9 (5) |
0,138 |
|
Вторая |
59 (34) |
22 (13) |
19 (11) |
В группе трансплевральных торакопластик осложнения наблюдались в 5 раз чаще, чем в группе экстраплевральных торакопластик. Пневмотораксы, некупированные в первые сутки от момента оперативного лечения и требовавшие более продолжительного срока дренирования плевральных полостей, были разрешены без дополнительных инвазивных методов лечения. Во второй группе, по сравнению с первой, наблюдали: в 7 раз больше пневмотораксов, в 2 раза больше миграций пластин, в 2 и 5 раз больше плекситов плечевого сплетения и плевритов, соответственно. Один случай гемоторакса в группе 2 был купирован с применением дренирования, медикаментозной терапии и ортопедического режима.
Интенсивность болевого синдрома у детей обеих групп оценивали по предикторам боли: по вербальной рейтинговой шкале, маркерам стресс-ответа (кортизол и лактат). В ходе исследования установлено, что в группах сравнения существенной разницы в выраженности болевого синдрома не отмечалось. Интенсивность боли была связана с антропометрическими данными пациента, а также тяжестью и ригидностью деформации грудной клетки. Продолжительность операции в среднем составила: в 1-й группе исследования 33,7 мин. (от 25 до 44 мин.), во 2-й группе – 41,1 мин. (от 36 до 51 мин.) (p<0,01). Интраоперационная кровопотеря была минимальной в обеих группах – в пределах 20 мл. Удовлетворенность послеоперационным эстетическим результатом в группах исследования у пациентов составила 100%. Пациенты после хирургического вмешательства находились под наблюдением в стационаре в среднем в течение 8 суток. Ни у одного из них не возникло интраоперационных осложнений. В раннем послеоперационном периоде были купированы все осложнения, значительная часть из которых проявлялась в виде пневмотораксов (верхушечных и малых), что не потребовало дополнительных инвазивных манипуляций, не повлияло на продолжительность лечения и конечный результат на стационарном этапе (табл. 7).
Несмотря на это, пациенты основной группы имеют меньше ранних послеоперационных осложнений по каждому пункту в таблице 7, что в итоге сказалось на статистически значимом, меньшем количестве этих осложнений даже с учетом множественности сравнений.
Таблица 7
Варианты и количество осложнений в группах исследования
|
Осложнение |
Первая группа n (%) |
Вторая группа n (%) |
p, Точный тест Фишера |
|
Интраоперационные |
|||
|
Повреждение сердца |
0 |
0 |
- |
|
Повреждение крупных сосудов средостения |
0 |
0 |
- |
|
Повреждение органов брюшной полости |
0 |
0 |
- |
|
Ранние послеоперационные |
|||
|
Пневмоторакс |
2 (4) |
14 (24) |
0,006 |
|
Гемоторакс |
0 |
1 (2) |
0,999 |
|
Миграция металлоконструкции |
1 (2) |
2 (3) |
0,999 |
|
Кровотечение |
0 |
0 |
- |
|
Нагноение послеоперационной раны |
0 |
0 |
- |
|
Плексит плечевого сплетения |
1 (2) |
2 (3) |
0,999 |
|
Плеврит |
1 (2) |
5 (9) |
0,208 |
|
Итого |
5 (10) |
24 (41) |
0,0001 |
Клинический пример пациента из 1-й группы иллюстрируют рис. 1, 2, из 2-й группы – рис. 3, 4.
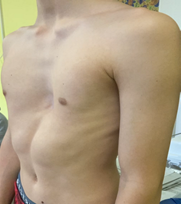
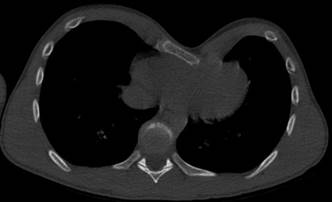
Рис. 1. Пациент 16 лет с ВДГК 3 ст., локальный тип, левосторонняя, до лечения. ИГ 4,83, ИК 0,526, УНГРК 23 влево
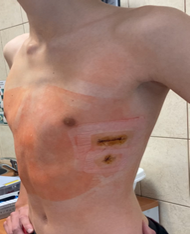
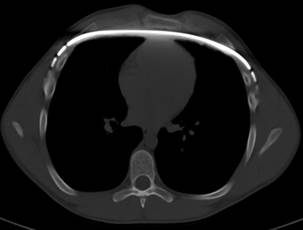
Рис. 2. Пациент 16 лет с ВДГК 3 ст., локальный тип, левосторонняя, ранний послеоперационный период. Выполнена малоинвазивная трансплевральная торакопластика. ИГ 1,84, ИК 0,82, УНГРК 5 влево
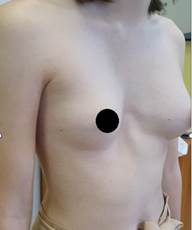
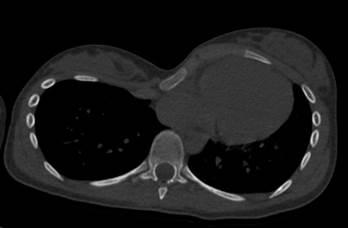
Рис. 3. Пациентка 15 лет с ВДГК 3 ст., локальный тип, правосторонняя, до лечения. ИГ 7,49, ИК 0,5176, УНГРК 26 вправо
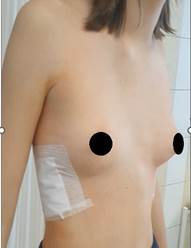
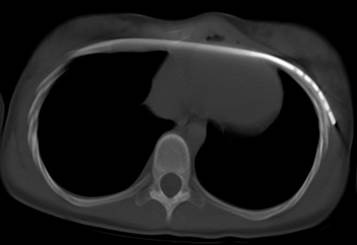
Рис. 4. Пациентка 15 лет с ВДГК 3 ст., локальный тип, правосторонняя, ранний послеоперационный период. Выполнена малоинвазивная экстраплевральная торакопластика. ИГ 3, ИК 0,80, УНГРК 7 вправо
MIRPE является первоочередной при выборе методики коррекции ВДГК. Технология обладает рядом преимуществ: минимальной инвазивностью, стабильной фиксацией грудинореберного комплекса в положении коррекции, отличным или хорошим косметическим результатом в случаях симметричной деформации или эластичной асимметричной деформации грудной клетки. Одновременно с этим необходимо подчеркнуть, что данная методика имеет некоторые недостатки, из которых к числу наиболее распространенных относятся повреждения органов грудной клетки, пневмотораксы, недостаточная коррекция рельефа передней грудной стенки при ригидных асимметричных деформациях. Вышеизложенные осложнения, как правило, связаны с техническими особенностями реализации методики [3, с. 104]. При трансплевральном проведении пластины нарушается целостность плевральной полости, что приводит к ее разгерметизации, а эта ситуация, в свою очередь, приводит к ряду других проблем. Помимо широко известных рисков, сопровождающих практически все виды малоинвазивных торакопластик, хирурги неизбежно сталкиваются с пневмотораксом в раннем послеоперационном периоде и с миграцией пластины в поздних периодах наблюдения.
Металлоконструкция, которая фактически является инородным телом, в плевральной полости увеличивает площадь для адгезии микроорганизмов, что повышает риск возникновения инфекционного плеврита. Кроме того, интраплевральная пластина на начальных этапах дополнительно ограничивает дыхательный акт, создавая механическое препятствие полноценному контакту плевральных листков, что в результате давления на париетальную плевру и ее раздражения может вызывать более значимые и длительные болевые ощущения [14].
Говоря об экстраплевральной торакопластике, что подразумевает проведение пластины за пределами плевральной полости, можно выделить ряд потенциальных преимуществ в сравнении с вышеизложенным классическим методом:
- уменьшение операционной травмы и снижение интенсивности болей в раннем послеоперационном периоде благодаря технике выполнения операции;
- снижение риска возникновения плеврита и практически исключение пневмоторакса за счет сохранения целостности плевральной полости;
- более высокие корригирующий эффект после проведенной операции и стабильность металлоконструкции за счет изменения точек перфорации грудной клетки, увеличения площади контакта передней поверхности ребер и пластины, а также противоположных векторов давления на нее.
В результате использования такой методики хирургического вмешательства и вышеперечисленных преимуществ достигается более ранняя активизация пациентов, сокращается период восстановительного лечения, значительно снижается количество осложнений в раннем послеоперационном периоде и отдаленных периодах наблюдения. Однако, согласно проведенному исследованию, длительность нахождения детей в стационаре и интенсивность болевого синдрома в группах исследования остается сопоставимой.
Стопроцентная удовлетворенность пациентов эстетическим результатом в обеих группах, несмотря на наличие до 19% удовлетворительных результатов, объясняется следующим: возраст детей в 97-98% случаев находился в диапазоне 10-17 лет, а наличие показаний к хирургической коррекции деформации говорило о ее выраженности, что, в свою очередь, указывало на длительность существования осознанной патологии и наличия у пациентов психоэмоционального «утомления» от визуальной картины. Поэтому даже остаточная асимметрия грудной клетки в послеоперационном периоде, имеющая значительно лучшую эстетику по сравнению с изначальной ситуацией, формировала у пациентов исключительно позитивный эффект от конечной визуальной формы передней грудной стенки.
Определение асимметрии грудной клетки в послеоперационном периоде наблюдения по высоте гемитораксов в проекции передней грудной стенки выполняли ввиду исключения КТ как метода оценки коррекции на данном этапе. Это было обусловлено двумя причинами: во-первых, снижением лучевой нагрузки на пациента, во-вторых, планируемым выполнением КТ на заключительном этапе лечения (удаление пластины), что будет являться более информативным.
Меньшая продолжительность операций в 1-й группе (34 [29; 39] – для первой группы, 39,5 [38; 44] – для второй; p<0,0001, тест Манна-Уитни) связана с тем, что протяженность безопасного канала (для использования диссектора, а затем пластины) была значительно больше, что снижало длительность формирования канала, а применение ленты-проводника увеличивало скорость проведения пластины по нему.
Несмотря на явные преимущества метода, следует сказать и о его особенностях. Во-первых, при экстраплевральном проведении пластины через средостение без визуального контроля риски повреждения сосудов и сердца сопоставимы с прочими методиками [14]. Во-вторых, возможность возникновения пневмоторакса за счет попадания воздуха в плевральную полость во время фиксации металлоконструкции к ребрам лентой и (или) установки плевральных дренажей. Вероятность возникновения вышеизложенных осложнений обратно пропорциональна опыту хирурга, что делает этот метод зависимым от навыков и умений специалиста и требует более длительной практической подготовки. Вероятность интраоперационных потенциальных осложнений и рисков при выполнении экстраплевральной торакопластики, особенно при тяжелой ригидной деформации грудной клетки, может быть снижена посредством применения УЗИ-контроля, что подразумевает использование предварительной интраоперационной элевации грудины через субмечевидный доступ [15]. Вышеупомянутый технический прием, за счет увеличения объема ретростернального пространства и контроля его прохождения, снижает риски травматизации анатомических образований, а также повышает безопасность манипуляции.
Выводы
Применение экстраплевральной малоинвазивной торакопластики при коррекции АВДГК у детей имеет более высокий корригирующий эффект, статистически и клинически значимо сопровождается меньшей частотой осложнений, сокращает продолжительность хирургического вмешательства. В процессе исследования не установлено значительного изменения выраженности болевого синдрома в раннем послеоперационном периоде в обеих группах исследования.
Заключение
Экстраплевральная малоинвазивная торакопластика обладает рядом преимуществ, которые значимо улучшают качество лечения, однако требовательна к опыту хирурга, что усложняет ее реализацию. Необходимы дополнительные исследования в отдаленном периоде наблюдения для объективизации информации о данной методике.
Источник финансирования. Исследование не имело финансового обеспечения или спонсорской поддержки.
Конфликт интересов. Авторы декларируют отсутствие явных и потенциальных конфликтов интересов, связанных с публикацией настоящей статьи.
Библиографическая ссылка
Долгиев Б.Х., Рыжиков Д.В., Виссарионов С.В. СРАВНИТЕЛЬНЫЙ АНАЛИЗ ЭКСТРАПЛЕВРАЛЬНОЙ И ТРАНСПЛЕВРАЛЬНОЙ ТОРАКОПЛАСТИК АСИММЕТРИЧНЫХ ВОРОНКООБРАЗНЫХ ДЕФОРМАЦИЙ ГРУДНОЙ КЛЕТКИ У ДЕТЕЙ // Современные проблемы науки и образования. 2024. № 5. ;URL: https://science-education.ru/en/article/view?id=33659 (дата обращения: 31.05.2026).
DOI: https://doi.org/10.17513/spno.33659



