Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
OPTICAL COHERENCE TOMOGRAPHY IN PREVENTIVE SURGERY OF MACULAR HOLES
Витреоретинальный интерфейс представляет собой плотно упакованные коллагеновые фибриллы заднего гиалоида стекловидного тела, прикрепляющиеся адгезивными молекулами, такими как ламинин, фибронектин и протеогликаны геперансульфата, к внутренней пограничной мембране сетчатки. Прогрессирующий синерезис стекловидного тела с выходом жидкости через дефекты в задней гиалоидной мембране после 40 лет приводит к развитию заполненных жидкостью карманов премакулярно [1]. Со временем разрушение коллагеново-гиалуронатной сети ослабляет адгезию стекловидного тела и сетчатки, что приводит к локализованному отделению стекловидного тела от перифовеальной области с усилением тракционного воздействия на фовеолу. Прогрессирование тракций разделяет слои сетчатки, приводя к формированию дефекта на всю толщину фовеолярной зоны [1–3]. Современные приборы для спектральной оптической томографии (ОКТ) сетчатки за счет высокого разрешения позволяют диагностировать все стадии витреомакулярной адгезии (ВМА) и ее перехода в витреомакулярную тракцию (ВМТ) с формированием макулярного разрыва [4, 5]. Динамическое наблюдение на сканах оптической когерентной томографии дает возможность своевременно запланировать хирургическое лечение патологии витреоретинального интерфейса [6, 7].
Наиболее распространенная хирургия патологии витреомакулярного интерфейса – это витрэктомия, пилинг внутренней пограничной мембраны (ВПМ) с возможной аутологичной трансплантацией остатков ВПМ и тампонадой витреальной полости [8–10]. Однако данная технология имеет ряд интраоперационных рисков: токсическое воздействие витальных красителей на структуры глазного яблока; механическая травма, деформирующая внутренние слои поверхности сетчатки, вплоть до формирования ятрогенного разрыва в макулярной зоне [10–12].
Цель исследования – проанализировать на горизонтальных снимках и картах толщины сетчатки сканов ОКТ анатомические результаты хирургии пациентов с витреомакулярной адгезией начальных стадий, прооперированных методом щадящей витрэктомии с сохранением фиксированного фрагмента гиалоида и внутренней пограничной мембраны; оценить функциональные результаты примененной хирургии у пациентов с исходно высокой остротой зрения.
Материалы и методы исследования
Авторами проведен анализ функциональных и анатомических результатов хирургического лечения 15 пациентов с витреомакулярными адгезиями в фовеолярной зоне. У обследуемых пациентов визуализировались различные стадии анатомического воздействия ВМА на сетчатку. Стадии ВМА выставлялись по данным горизонтальных ОКТ-сканов. У всех пациентов регистрировался сквозной макулярный разрыв на парном глазу. Наличие сквозного разрыва обуславливало резкое снижение остроты зрения.
Стадии ВМА выставлялись по морфологическим изменениям, визуализированным на первичных снимках ОКТ. Исследования проводились на приборах Cirrus HD-OCT 5000 C.ZEISS протокол Macular cube 512 × 128 и RTVue 100 Optovue протокол Retina Map. Оценивались центральная толщина сетчатки (ЦТС) на горизонтальных снимках и ретинальная поверхность на картах толщины сетчатки. Первичная томография выполнялась за день до хирургии и в сроки 3 дня, 1 месяц и 6 месяцев после операции. Пациенты разделены на три группы в зависимости от выявленной стадии ВМА. Пациенты из первой группы, включающей 7 глаз, имели первую стадию витреомакулярной адгезии, определяющуюся на томограммах как увеличение фовеолярной толщины сетчатки под воздействием витреомакулярного натяжения. Вторая группа прооперированных пациентов включала 6 глаз со второй стадией ВМА. На томографических изображениях этих пациентов визуализировались подъем и внутрифовеолярное расслоение внутренних слоев сетчатки с формированием псевдокисты. Третья стадия ВМА определялась в двух глазах третьей группы исследуемых пациентов. На снимках ОКТ пациентов третьей группы к псевдокистозному расслоению внутренних слоев фовеолы присоединялось разделение наружных слоев фовеолярной сетчатки с дефектом в эллипсоидной зоне и наружной пограничной мембране. На снимках ОКТ парного глаза пациентов всех трех групп визуализировался сквозной макулярный разрыв с дефектом всех слоев сетчатки и диастазом краев разрыва. У всех исследуемых пациентов регистрировалась высокая максимальная корригированная острота зрения (МКОЗ) и отсутствие жалоб на остроту и качество центрального зрения глаза с витреомакулярной адгезией.
Пациенты всех трех групп прооперированы технологией 27G методом субтотальной закрытой витрэктомии с сохранением фиксированного к фовеоле фрагмента задней гиалоидной мембраны и внутренней пограничной мембраны. В ходе хирургии с целью ликвидации тракционного натяжения с деформацией ретинальных слоев в макулярной зоне иссекалась задняя гиалоидная мембрана за исключением фрагмента с плотной фовеолярной фиксацией к поверхности сетчатки (рис. 1).
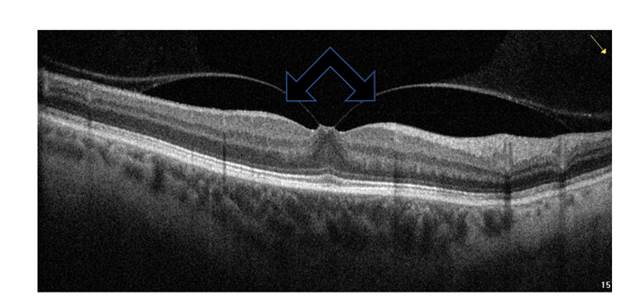
Рис. 1. Горизонтальное ОКТ изображение ВМА 1 стадии. Стрелками указаны зоны планируемого иссечения задней гиалоидной мембраны с сохранением фрагмента с фовеолярной тракцией
Внутренняя пограничная мембрана макулярной зоны в ходе хирургии сохранялась интактной с целью исключения ятрогенных дефектов поверхности сетчатки, формирования скотом в центральном зрении и снижения зрительных функций. Витальные красители в ходе хирургии не применялись, что позволило исключить их возможное токсическое воздействие на сетчатку.
Результаты исследования и их обсуждение
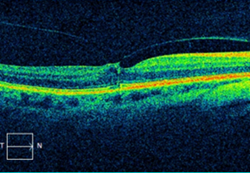
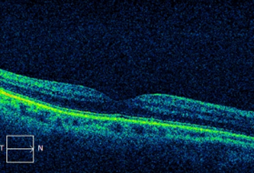
По данным оптической когерентной томографии у всех пациентов с витреомакулярной адгезией в трех группах (рис. 2, а, б), после субтотальной закрытой витрэктомии с сохранением фиксированного к фовеоле фрагмента гиалоида и ВПМ, определялось отсутствие витреофовеолярной тракции и деформаций фовеолы как в ранних, так и в отдаленных сроках послеоперационного наблюдения (рис. 3, а). На карте толщины сетчатки пациентов с сохраненной внутренней пограничной мембраной визуализировалось отсутствие деформаций и ятрогенных дефектов внутренних ретинальных слоев (рис. 3, б). Наличие ятрогенных дефектов ретинальной поверхности с очаговыми истончениями сетчатки часто визуализируется на картах толщины послеоперационных томограмм у пациентов перенесших витрэктомию с пилингом внутренней пограничной мембраны (рис. 4, а, б). Присутствие дефектов внутренних слоев сетчатки может сопровождаться появлением скотом в центральном зрении, метаморфопсий и стойким снижением центрального зрения.
 а
а 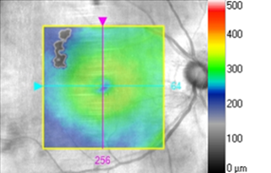 б
б
Рис. 2. а) горизонтальный снимок ОКТ пациента Б. с ВМА 3 стадии: тракционное утолщение сетчатки в фовеолярной зоне с формированием псевдокисты во внутренних слоях и дефекта в слое фоторецепторов; б) карта толщины макулярной зоны сетчатки с ВМА 3 стадии: Увеличение толщины сетчатки в фовеоле
 а
а  б
б
Рис. 3. а) горизонтальный снимок ОКТ пациента Б. через 1 месяц после витрэктомии с сохранением фиксированного гиалоида и ВПМ: восстановление в фовеолярной зоне архитектоники ретинальных слоев и профиля фовеа; б) карта толщины макулярной зоны сетчатки пациента Б. через 1 месяц после витрэктомии с сохранением фиксированного гиалоида и ВПМ: нормализация толщины сетчатки в фовеоле
 а .
а .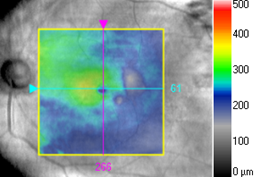 б
б
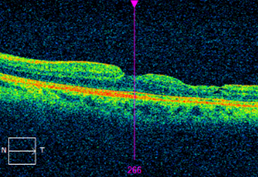
Рис. 4. а) горизонтальный снимок ОКТ пациента Ф. через 1 месяц после витрэктомии с пилингом ВПМ: асимметрия поверхности сетчатки за счет ятрогенных дефектов во внутренних слоях; б) карта толщины макулярной зоны сетчатки пациента Ф. через 1 месяц после витрэктомии с пилингом ВПМ: грубая асимметрия в толщине сетчатки макулярной зоны с фокальными истончениями в зонах ятрогенных дефектов внутренних слоев
Анализ горизонтальных сканов оптической когерентной томографии продемонстрировал незначительное увеличение центральной толщины сетчатки в фовеолярной зоне в первые дни послеоперационного периода во всех группах. К шестому месяцу после операции центральная толщина сетчатки в фовеальной зоне полностью достигала значений нормы (табл. 1). Статистическая значимость различий в ЦТС до и через 6 месяцев после хирургии наблюдалась в первой и третьей группах – р < 0,05.
Таблица 1
Динамика центральной толщины фовеальной зоны сетчатки пациентов с ВМА, перенесших субтотальную закрытую витрэктомию с сохранением фрагмента фиксированного в фовеоле гиалоида и внутренней пограничной мембраны
|
|
ЦТС до операции (мкм) |
ЦТС через 3 дня после операции (мкм) |
ЦТС через 1 месяц после операции (мкм) |
ЦТС через 6 месяцев после операции (мкм) |
|
Группа 1 |
279,8±11,8* M ± m |
298,7±10,8 M ± m |
248,6±9,7 M ± m |
231,2±9,5* M ± m |
|
Группа 2 |
288,±8,7 M ± m |
302,8±12,7 M ± m |
276,5±10,4 M ± m |
226,5±11,3 M ± m |
|
Группа 3 |
318±4,0** M ± m |
320,8±14,3 M ± m |
251,3±11,2 M ± m |
228,2±10,2** M ± m |
Примечание. Статистическая значимость различий в ЦТС: * – р < 0,05 (в 1 группе до и после хирургии); ** – р < 0,05 (в 3 группе до и после хирургии).
Применение технологии витрэктомии с сохранением внутренней пограничной мембраны и отсутствием механического воздействия хирургических инструментов на поверхность сетчатки позволило избежать повреждений внутренних слоев и появления центральных и парацентральных скотом в поле зрения со снижением остроты зрения. Изначальная высокая корригированная острота зрения у пациентов с витреомакулярной адгезией во всех трех группах сохранялась на всех этапах послеоперационного периода (табл. 2). Статистически значимых различий в данных визометрии во всех группах до и через 6 месяцев после хирургии не выявлялось – р > 0,05. Что подтверждает сохранение исходно высокого зрения у исследуемых пациентов. Жалоб на появление скотом и метаморфопсий в послеоперационном периоде не регистрировалось ни у одного из наблюдаемых пациентов.
Таблица 2
Динамика максимальной корригированной остроты зрения пациентов с ВМА, прооперированных с сохранением фрагмента фиксированного гиалоида
|
|
МКОЗ до хирургии |
МКОЗ через 3 дня после хирургии |
МКОЗ через 1 месяц после хирургии |
МКОЗ через 6 месяцев после хирургии |
|
Группа 1 |
0,91±0,21 M ± m |
0,82±0,19 M ± m |
0,95±0,22 M ± m |
0,98±0,25 M ± m |
|
Группа 2 |
0,92±0,11 M ± m |
0,72±0,2 M ± m |
0,82±0,18 M ± m |
0,95±0,16 M ± m |
|
Группа 3 |
0,75±0,1 M ± m |
0,7±0,17 M ± m |
0,81±0,14 M ± m |
0,88±0,19 M ± m |
Примечание. Статистической значимости различий в остроте зрении исследуемых пациентов всех групп до и после хирургии не определяется: р > 0,05.
Диагностика с применением оптической когерентной томографии сетчатки позволяет визуализировать даже минимальные патологические изменения в витреоретинальном интерфейсе [4–6]. В том числе в случаях с витреомакулярной адгезией различных стадий [7]. На сегодняшний день витрэктомия – общепринятый максимально эффективный способ хирургии патологий витреомакулярного интерфейса [8–10]. Пилинг ВПМ может негативно сказываться на интерфейсе макулярной зоны и зрительных функциях за счет ятрогенных повреждений внутренних слоев сетчатки [11, 12]. При наличии витреомакулярной адгезии 1–3 стадии на сканах ОКТ у пациентов с высокой остротой зрения и сквозным макулярным разрывом на парном глазу предпочтительна хирургия, устраняющая витреомакулярную тракцию с сохранением фиксированного фрагмента гиалоида и внутренней пограничной мембраны.
Заключение
Высокое разрешение и точность метода спектральной оптической томографии сетчатки позволяет диагностировать даже самые начальные стадии витреомакулярной адгезии, а также наблюдать динамику прогрессирования и послеоперационной реабилитации пациентов с патологией витреоретинального интерфейса. В случаях регистрации на ОКТ ВМА 1–3 стадий у пациентов с высоким зрением и сквозным макулярным разрывом на парном глазу оптимальной хирургической тактикой является витрэктомия с сохранением фиксированного фрагмента гиалоида и ВПМ. Данная хирургия является щадящей альтернативой пилингу ВПМ для сохранения центрального зрения и анатомии фовеальной зоны, что подтверждает анализ горизонтальных сканов и карт толщины сетчатки на послеоперационных ОКТ снимках. Данную хирургию ВМА можно считать превентивным лечением сквозного макулярного разрыва.
Библиографическая ссылка
Козина Е.В., Бронская А.Н., Быкова Е.В., Курская Т.Е. ОПТИЧЕСКАЯ КОГЕРЕНТНАЯ ТОМОГРАФИЯ В ПРЕВЕНТИВНОЙ ХИРУРГИИ МАКУЛЯРНЫХ РАЗРЫВОВ // Современные проблемы науки и образования. 2023. № 5. ;URL: https://science-education.ru/en/article/view?id=32988 (дата обращения: 24.05.2026).
DOI: https://doi.org/10.17513/spno.32988



