Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
CARDIAC ARRHYTHMIA IN A NEWBORN WITH CONGENITAL MYOCARDITIS. A CLINICAL CASE.
Нарушения ритма сердца (НРС) — достаточно частая патология у детей периода новорожденности, которая начинает проявлять себя, как правило, с первых дней до 6 месяцев жизни [1, 2]. Она занимает второе, после врожденных пороков сердца, место в структуре сердечно-сосудистых нарушений детского возраста [3]. Нарушения функции синусового узла встречаются у 9% новорожденных и 45% здоровых подростков, предсердная экстрасистолия – у 0,8% новорожденных и 2,2% подростков, а при суточном мониторировании – у 18% новорожденных и 50% подростков без признаков органического заболевания сердца [3]. НРС может быть отражением как сердечных, так и внекардиальных патологических процессов, таких как: сахарный диабет, гипотиреоз, гипертиреоз, опухоли головного и спинного мозга, черепно-мозговая травма, сепсис [3, 4, 5]. Факторами риска развития НРС могут быть отягощенный акушерско-гинекологический анамнез, экстрагенитальная патология у матери, гипоксия плода, перенесенные инфекционные заболевания матери и плода [1, 4, 6]. Среди предрасполагающих факторов следует выделить наличие анатомического субстрата аритмии в виде малых аномалий развития сердца: дополнительных хорд, пролапсов митрального и трикуспидального клапанов и врожденной патологии проводящей системы сердца [3]. Различные патологические факторы через систему вторичных посредников способствуют нарушению метаболизма в миокарде, что приводит к функционированию ионных каналов и вызывает электрофизиологическую неоднородность миокарда [3, 6]. Установлено, что независимо от электрофизиологического варианта одним из ведущих патофизиологических механизмов аритмий у детей является снижение адаптационно-трофических влияний симпатического отдела вегетативной нервной системы на сердце [3, 6]. При нормальном внутриутробном развитии в середине пренатального периода происходит дифференцировка адренергического аппарата сердца, а патология беременности и родов может оказывать существенное влияние на становление иннервации сердца [3]. Согласно классификации М.А. Школьниковой, выделяют шесть клинически значимых и наиболее распространенных НРС: суправентрикулярные и желудочковые экстрасистолии (ЭКС), суправентрикулярные и желудочковые тахиаритмии, синдром слабости синусового узла и автриовентрикульные (АВ) блокады [3]. В настоящее время также выделяют молекулярно-генетические варианты первичных электрических заболеваний сердца (врожденные каналопатии): наследственный синдром удлиненного интервала QT (Джервела–Ланге–Нильсена, Романо–Уорда, Андерсена–Тавила, Тимоти), синдром короткого интервала QT, синдром Бругада, катехоламин-зависимую полиморфную желудочковую тахикардию [3]. Основным методом диагностики аритмий является электрокардиограмма (ЭКГ), в том числе и ЭКГ плода, регистрируемая с живота матери [1, 2, 4]. При этом качество записи достаточно низкое, чтобы оценить зубец Р [2]. С этой же целью может проводиться магнитокардиография плода, позволяющая улучшить качество отведения, но это весьма дорогостоящий метод [2]. Помимо этого, для диагностики аритмий используются суточное мониторирование ЭКГ по Холтеру, чреспищеводное электрофизиологическое исследование [1, 2, 5]. Более пролонгированным методом длительной регистрации сердечного ритма является ревил – имплантируемый регистратор, который может фиксировать ЭКГ до нескольких лет (до развития эпизода аритмии) [2]. Вспомогательное значение имеют ультразвуковые методы обследования новорожденного ребенка [2]. В большинстве случаев НРС имеют благоприятный прогноз и купируются самостоятельно либо с помощью консервативной терапии [1, 2, 6], в остальных – могут приводить к формированию стойкого патологического процесса с развитием сердечной недостаточности, а в некоторых случаях, при отсутствии адекватной терапии – к летальному исходу [2, 4].
Цель исследования: описание клинического случая НРС у новорожденного с врожденным миокардитом.
Клинический случай
Ребенок от 3-й беременности и 3-йх родов на 40-й неделе гестации, рожден естественным путем. Состояние при рождении удовлетворительное, закричал сразу. Вес при рождении 2970 г, рост 50 см. Оценка по шкале APGAR 8/8 баллов. При осмотре кожные покровы и видимые слизистые чистые, нормальной окраски и влажности. Аускультативно дыхание пуэрильное, проводится по всем полям, хрипов нет, ЧД 44 в минуту. Sat O2 98%. Тоны сердца достаточной громкости, ритм правильный, ЧСС 144 уд/мин. Живот мягкий, не вздут. При пальпации печень и селезенка не увеличены. Рефлексы новорожденного вызываются. Физиологические отправления не нарушены. На 3-и сутки жизни отмечается отрицательная динамика в состоянии ребенка в виде быстрого угасания рефлексов новорожденного, снижения мышечного тонуса, возникновения тремора рук и подбородка при плаче, появления акроцианоза. При аускультации сердца выслушиваются неправильный ритм, приглушенность тонов, систолический шум по левому краю грудины средней интенсивности. Ребенок переведен в отделение патологии новорожденных и недоношенных детей (ОПННД) на обследование с предварительным диагнозом: Врожденный миокардит? Нарушение ритма сердца. В отделении ребенку экстренно проведено ЭХОКГ, где визуализированы: множественные мышечные трабекулярные дефекты межжелудочковой перегородки (ДМЖП) 2,2 мм, открытый артериальный проток (ОАП) 2,1 мм, открытое овальное окно (ООО) 1,7 мм, дилатация полости левого желудочка (ЛЖ) 20,3 мм (норма 14–18 мм), множественные дополнительные хорды диагонального направления в полости (ДХЛЖ). Фракция выброса составила 70% (норма 60–80%). На ЭКГ зарегистрированы: синусовый ритм с ЧСС 150 уд/мин, который прерывается частыми одиночными АВ ЭКС с эпизодами аллоритмии по типу бигеминии, тригеминии. Электрическая ось сердца (ЭОС) отклонена вправо (рис. 1).
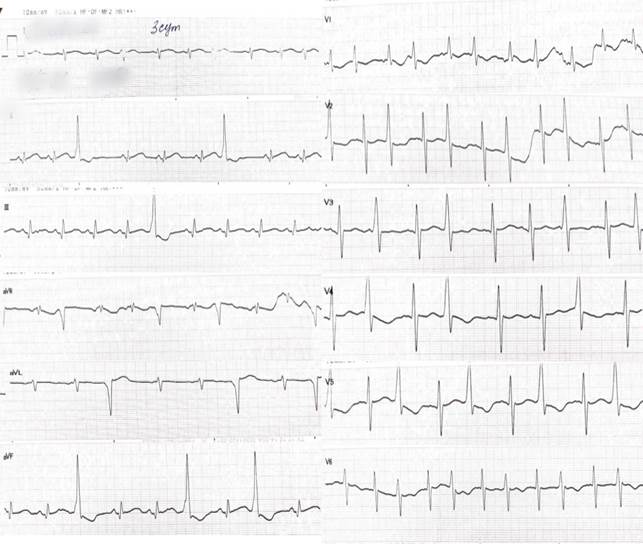
Рис. 1. ЭКГ: синусовый ритм с ЧСС 150 уд/мин. Одиночные атриовентрикулярные экстрасистолы с эпизодами аллоритмии по типу бигеминии, тригеминии. Электрическая ось сердца отклонена вправо
В динамике, на 5-й день жизни, на ЭКГ прослеживаются частые одиночные АВ-узловые ЭКС. Эпизод атриовентрикулярной тахикардии с ЧСС 171–176 уд/мин. Зафиксированы комплексы с нарушением проведения по дополнительным проводящим путям (транзиторный синдром WPW?) (рис. 2).
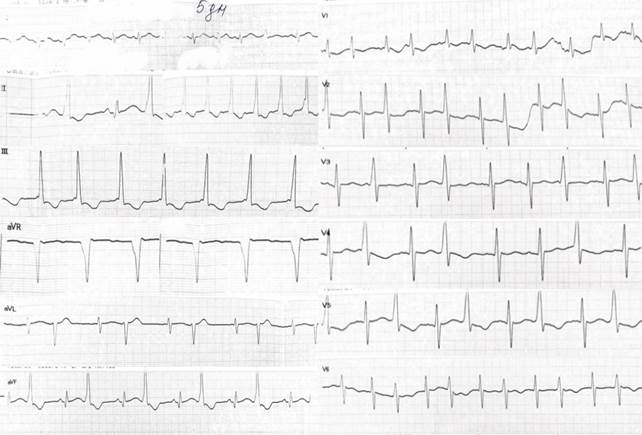
Рис. 2. ЭКГ: частые одиночные атриовентрикулярные узловые экстрасистолы. Эпизод атриовентрикулярной тахикардии с ЧСС 171–176 уд/мин. Комплексы с нарушением проведения по дополнительным проводящим путям (транзиторный синдром WPW?)
При анализе суточного холтеровского мониторирования (ХМ) обнаружено 67575 штук АВ ЭКС, из них 43491 одиночные, 1863 парные, 20357 групповые, по типу бигеминии 23417 (рис. 3), по типу тригеминии 10573 (рис. 4), квадригеминии 633 (рис. 5).
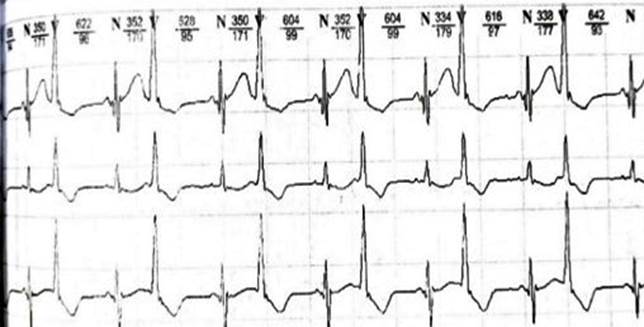
Рис. 3. Суточное холтеровское мониторирование: атриовентрикулярная экстрасистола по типу бигеминии
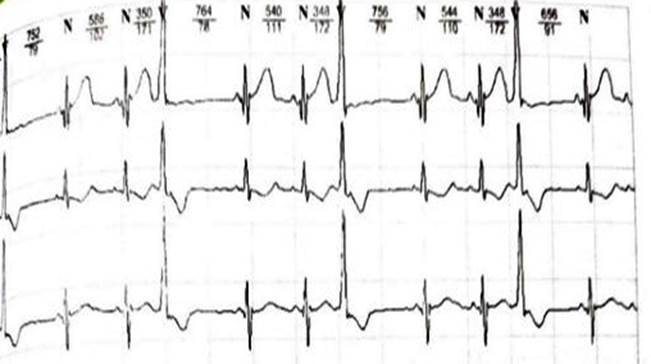
Рис. 4. Суточное холтеровское мониторирование: атриовентрикулярная экстрасистола по типу тригеминии
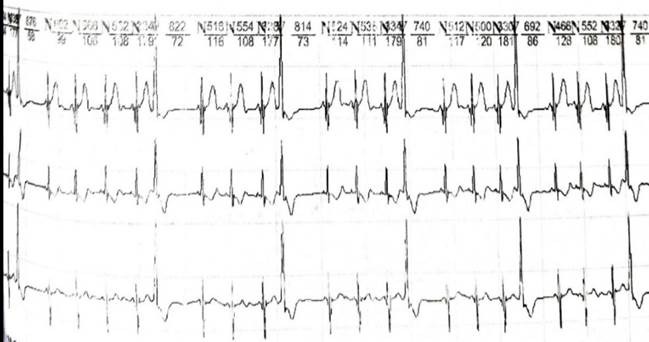
Рис. 5. Суточное холтеровское мониторирование: атриовентрикулярная экстрасистола по типу квадригеминии
В биохимическом анализе крови обнаружена гипопротеинемия – 45 г/л (норма 66–88 г/л), гипербилирубинемия – 172,2 мкмоль/л (норма 20,5 мкмоль/л), нарастание уровня лактатдегидрогеназы (ЛДГ) в динамике от 932 до 1023 ед/л (норма 225–450 ед/л) и тропонина I от 0,46 до 0,60 нг/мл (норма до 0,020 нг/мл). В иммунограмме выявлены антитела к Micoplasma hominis класса G в титре 1:20, IgG к Toxoplasma gondii 200 МЕ/мл со 100% авидностью, также IgG к вирусам простого герпеса 1-го, 2-го типов 1:3200 с 95%-ной авидностью и IgG к цитомегаловирусу 21 с авидностью 84%. Заключение по результатам рентгенологического исследования грудной клетки и брюшной полости: признаков инфильтрации в легких не выявлено. Кардиоторакальный индекс (КТИ) 46%. Согласно федеральным клиническим рекомендациям 2021 года «Миокардиты у детей», лабораторные исследования (клинический и биохимический анализы крови и мочи) в диагностике кардитов недостаточно информативны, изменения при обследованиях неспецифичны и имеют диагностическое значение только в сочетании с клиническими данными и данными функциональных исследований [7, 8]. На основании проведенного обследования выставлен диагноз: основной: Врожденный миокардит вирусной этиологии, с поражением проводящей системы сердца, АВ узловая ЭКС – одиночная, парная, групповая, эпизоды аллоритмии – бигеминия, тригеминия, квадригеминия, АВ узловая тахикардия. Непароксизмальная АВ тахикардия возвратная форма. Желудочковая тахикардия с ретроградным зубцом Р. Сопутствующий: Транзиторный WPW-синдром. Группа риска по аритмогенной кардиомиопатии. Врожденный порок сердца: множественные мышечные дефекты межжелудочковой перегородки без нарушения внутрисердечной гемодинамики. Функционирование фетальных коммуникаций: ООО. ДХЛЖ. Было назначено лечение согласно клиническим рекомендациям по миокардиту. В питании смесь NAN-1 в объеме 600 мл/сут. Этиотропная терапия в стандартных дозировках, так как причиной миокардита может быть вирусно-бактериальная ассоциация: ампицилин сульбактам 75мг/кг/сутки и ацикловир 60 мг/кг/сут в/в капельно. Инфузионная терапия 10%-ным раствором глюкозы, 10%-ным раствором кальция глюконата в/в капельно. Несмотря на проведенную терапию, к 10-му дню сохраняются стойкое нарушение ритма и угроза перехода в хроническое течение. Учитывая увеличение количества ЭКС, показателей тропонина и ЛДГ, решено подключить внутривенный человеческий иммуноглобулин в дозе 1 г/кг и преднизолон в дозе 2 мг/кг/сут per os. Также произведена смена антибиотиков на ванкомицин 40 мг/кг/сут в/в капельно и цефаперазон 100 мг/кг/сут в/в капельно в 2 раза в сутки. На фоне данного лечения отмечается положительная клиническая динамика в виде улучшения общего состояния. При осмотре кожные покровы и видимые слизистые нормальной окраски и влажности. В легких дыхание пуэрильное, проводится по всем полям, хрипов нет, ЧД 38 в минуту. Sat O2 98%. Тоны сердца достаточной громкости, ритм правильный, ЧСС 140 уд/мин. Живот мягкий, не вздут. При пальпации печень и селезенка не увеличены. Рефлексы новорожденного вызываются. Физиологические отправления не нарушены. Прибавка в весе до 3300 г. По данным ХМ регистрируется уменьшение количества экстрасистол до 566, из них 277 с аберрантным проведением. В биохимическом анализе крови уровень тропонина I снизился до 0,04 нг/мл, ЛДГ – до 660 ед/л.
Заключение
Несмотря на то что неонатальные НРС в большинстве случаев носят транзиторный характер и отражают функциональное состояние периода адаптации, нельзя не думать о клиническом проявлении врожденного миокардита с нарушением ритма. Своевременное комплексное лечение миокардита с использованием внутривенного иммуноглобулина, антибиотиков, глюкокортикоидов позволило значительно уменьшить выраженность аритмии без применения антиаритмических препаратов.
Библиографическая ссылка
Науменко Е.И., Гришуткина И.А., Акашкина Е.Ю., Тягушева Е.Н., Тишкова О.Е., Косарева Т.В. НАРУШЕНИЕ РИТМА СЕРДЦА У НОВОРОЖДЕННОГО С ВРОЖДЕННЫМ МИОКАРДИТОМ. КЛИНИЧЕСКИЙ СЛУЧАЙ. // Современные проблемы науки и образования. 2023. № 1. ;URL: https://science-education.ru/en/article/view?id=32415 (дата обращения: 22.05.2026).
DOI: https://doi.org/10.17513/spno.32415



